Klopidogreeli põhjustatud neutropeenia 80--aastasel kroonilise neeruhaigusega patsiendil, kellele tehti perkutaanne koronaarsekkumine: juhtumiaruanne ja kirjanduse ülevaade
Jul 27, 2023
Abstraktne
1. Taust
Klopidogreel on laialdaselt kasutatav trombotsüütidevastane aine ja toimib adenosiindifosfaadi retseptori inhibiitorina. Neutropeenia on klopidogreeli harvaesinev, kuid tõsine kõrvaltoime. Ei ole teada, kas sellel kõrvaltoimel on seos neerufunktsiooni kahjustusega.
2. Juhtumi esitlus
Kroonilise neeruhaigusega {{0}}-aastasel mehel diagnoositi ST elevatsioonita müokardiinfarkt ja talle tehti perkutaanne koronaarne sekkumine. Haiglaravi ajal diagnoositi patsiendil kontrastainest põhjustatud nefropaatia, teda raviti sümptomaatiliselt ja ta lasti koju tagasi algtaseme kreatiniinitasemega. Kaks nädalat hiljem pöördus patsient palaviku ja külmavärinatega erakorralise meditsiini osakonda. Täielik vereanalüüs näitas leukopeeniat (0,84 × 103 /mm3) ja rasket neutropeeniat (0,13 × 103 /mm3). Verekultuurid olid Pseudomonas aeruginosa suhtes positiivsed. Klopidogreeli kasutamine lõpetati kohe ja viidi üle tikagreloorile. Patsiendile manustati imipeneemi ja granulotsüütide kolooniaid stimuleerivaid faktoreid. Patsiendi valgete vereliblede ja absoluutsete neutrofiilide arv olid pärast neljapäevast ravi normi piires. Patsient vabastati pärast 10-päevast haiglaravi ja tema täielik vereanalüüs oli edasiste jälgimiste ajal normaalne.
3. Järeldused
Klopidogreel oli meie puhul kõige tõenäolisem neutropeenia peamine põhjus. Klopidogreeli põhjustatud neutropeenia esinemissagedus on väike ja täpset mehhanismi ei ole täielikult selgitatud. Pakume soovitusi klopidogreeli kasutamisega seotud neutropeenia ravi kohta ja võtame kokku kõik viis klopidogreeli põhjustatud neutropeenia juhtumit neerufunktsiooni kahjustusega patsientidel.

Klõpsake siin, et teada saada, mis on Cistanche, ja osta Cistanche tooteid
Märksõnad
Klopidogreel, neutropeenia, krooniline neeruhaigus, PCI.
Taust
Klopidogreeli kasutatakse sageli osana duaalsest trombotsüütide agregatsioonivastasest ravist (DAPT) ägeda koronaarsündroomi või perkutaanse koronaarse sekkumise (PCI) patsientidel. Klopidogreel on trombotsüütide vastane aine, mis inhibeerib adenosiindifosfaadi (ADP) seondumist P2Y12 retseptoriga [1]. Klopidogreel võib põhjustada võimalikke hematoloogilisi kõrvaltoimeid ja neutropeenia on haruldane, kuid tõsine kõrvaltoime, mille esinemissagedus CAPRIE uuringu kohaselt on 0,10 protsenti [2]. Siin kirjeldame klopidogreelist põhjustatud neutropeenia juhtumit kroonilise neeruhaigusega (CKD) patsiendil, kellele tehti PCI, ja võtame kokku kõik viis klopidogreeli põhjustatud neutropeenia juhtumit neerufunktsiooni kahjustusega patsientidel.
Juhtumi esitlus
80--aastane mees kaebas kolm nädalat vahelduva valu rinnus. Sel perioodil oli tal diagnoositud mitte-ST elevatsiooniga müokardiinfarkt (NSTEMI). Patsiendil oli anamneesis hüpertensioon (ravitud amlodipiini ja ramipriiliga), II tüüpi suhkurtõbi (ravitud glargiini, asparti ja vogliboosiga) ja kaheaastane krooniline neeruhaigus (4. staadium). Seoses murega neerufunktsiooni halvenemise pärast anti talle enne meie haiglasse üleviimist arstiabi. Teda raviti kolm nädalat enne vastuvõtmist aspiriini (100 mg päevas), klopidogreeli (75 mg päevas) ja isosorbiidmononitraadiga (20 mg päevas).
Vastuvõtmisel näitasid hematoloogilised leiud normaalset hemoglobiini (12,3 g/dl), leukotsüütide arvu (7,85 × 103/mm3), neutrofiilide arvu (5,13 × 103 /mm3) ja trombotsüütide arvu (183 × 103 /mm3). Tema kreatiniini algtase oli 3,35 mg/dl ja tema hinnanguline glomerulaarfiltratsiooni kiirus (eGFR) oli 16,42 ml/min/1,73 m2. Enne plaanilist PCI-d manustati küllastusannus 300 mg klopidogreeli ja 300 mg aspiriini. Protseduuri ajal paigaldati kaks stenti vasakusse eesmisse laskuvasse arterisse ja kaks stenti paremasse koronaararterisse. Patsient sai pärast protseduuri säilitusannusena klopidogreeli 75 mg päevas ja aspiriini 100 mg päevas. Arvestades tema madalat glomerulaarfiltratsiooni kiirust (GFR), manustati intravenoosselt isotoonilist normaalset soolalahust vastavalt 24 tundi enne protseduuri ja pärast protseduuri ning kontrastaine annus PCI jaoks oli 150 ml. Madala uriinierituse ja kõrgenenud kreatiniini (3,35–4,81 mg/dl) tõttu tehti patsiendile perioodiline venovenoosne hemofiltratsioon (IVVHF) kokku kuus korda (joonis 1). Tema hemoglobiin langes 12,3-lt 6,5 g/dl-le, mis oli tõenäoliselt tingitud neerupõhjustest ja verekaotusest IVVHF-i ajal, ning talle tehti kolmeühikuline punaste vereliblede ülekanne. Vahepeal olid tema valgete vereliblede ja neutrofiilide arv normis. 10. päeval pärast PCI protseduuri tõusis tema uriinieritus 1590 ml-ni ja kreatiniini tase langes 3,16 mg/dL-ni (joonis 1) ning selleks ajaks lõpetasime hemofiltratsiooni. Seejärel vabastati ta algtaseme kreatiniini tasemega 3,37 mg/dl ja normaalse leukotsüütide arvuga 7,5 × 103/mm3. Tema väljaheiteravimite nimekirjas olid klopidogreel (75 mg päevas), aspiriin (100 mg päevas), isosorbiidmononitraat (30 mg päevas), atorvastatiin (20 mg päevas), karvedilool (6,25 mg kaks korda päevas), furosemiid (20). mg päevas) ja erütropoetiini (10,000 RÜ kolm korda nädalas subkutaanselt).

Klopidogreelravi 51. päeval läks patsient kliinikusse järelkontrolli ilma muude sümptomitega peale anoreksia ning tema täielik vereanalüüs näitas leukotsüütide arvu 2,5 × 103 /mm3 ja neutrofiilide arvu. 1.0× 1{{20}}3 /mm3. Patsiendil paluti tulla kliinikusse täieliku verepildi täpseks jälgimiseks. Klopidogreelravi 55. päeval tuli ta erakorralise meditsiini osakonda, kurtes palaviku ja külmavärinate üle 39,0 kraadise temperatuuriga. Ta oli unine, kuid ärrituv. Elulised näitajad näitasid, et pulss oli 110, hingamissagedus 22, vererõhk 99/58 mmHg ja O2 küllastus 100 protsenti. Täielik vereanalüüs näitas leukopeeniat (0,84 × 103 /mm3) ja rasket neutropeeniat (0,13 × 103 /mm3). Kuna neutropeeniline palavik on potentsiaalselt eluohtlik seisund, oli meie prioriteediks febriilse neutropeenia esialgne hindamine ja kiire ravi. Manustati intravenoosselt tavalist soolalahust ja täiendavat hapnikku. Enne intravenoosset empiirilist laia toimespektriga antibiootikume (imipeneem/tsilastatiin) võeti kaks komplekti verekultuure. Selle patsiendi kriitilise seisundi tõttu manustati subkutaanset granulotsüütide kolooniaid stimuleerivat faktorit (G-CSF). Arvestades ravimist põhjustatud neutropeenia võimalust, klopidogreeli enam ei kasutatud ja see asendati tikagrelooriga (90 mg kaks korda päevas). Edasised vereanalüüsid näitasid normaalseid elektrolüütide ja maksafunktsiooni teste, kreatiniini taset 3,96 mg/dl ja kõrgenenud C-reaktiivse valgu taset 18 ng/dl. Tegime mitmeid laboriuuringuid ja pildiuuringuid, et tuvastada võimalikke patogeene ja nakkusallikaid. Kaks verekultuuride komplekti osutusid Pseudomonas aeruginosa suhtes positiivseks ja antibakteriaalse tundlikkuse testid näitasid, et patogeen oli imipeneemile vastuvõtlik. Tavalised viirusuuringud olid negatiivsed (CMV, EBV, gripp, HIV, hepatiidiviirus). Mis puutub nakkuse allikasse, siis patsiendil ei olnud püsikateetreid, nahakahjustusi, orofarüngeaalsete ja perirektaalsete uuringute ajal kõrvalekaldeid ning ta kaebas kõhuvalu või kõhulahtisuse puudumise üle. Uriinianalüüs oli valgete vereliblede suhtes negatiivne. Auskultatsioonil oli kuulda kraaksumist ning rindkere röntgeni- ja rindkere CT-skaneeringud näitasid paremas alumises labas lihvklaasi läbipaistmatust. Seega oli esmane nakkusallikas suure tõenäosusega põhjustatud kopsuinfektsioonist, mis hiljem arenes sepsiseks.

Cistanche toidulisand
Tegime põhjaliku diferentsiaaldiagnoosi neutropeenia võimalike põhjuste kohta. Täiendavad laboratoorsed hinnangud, sealhulgas B12-vitamiini ja foolhappe tase, autoimmuunsed antikehad, perifeerse vere määrded ja kõhuõõne ultraheli (splenomegaalia välistamiseks) ja kõik need ei näidanud kõrvalekaldeid. Eakate neutropeenia levinumad etioloogiad on infektsioon, ravimid, toitumisvaegused, hematoloogilised pahaloomulised kasvajad ja autoimmuunhaigused [3]. Toitumisalased põhjused olid välistatud, kuna B12-vitamiini ja foolhappe tase oli normi piires. Autoimmuunhäired olid negatiivsete autoimmuunantikehade tõttu ebatõenäolised. Mis puutub hematoloogilistesse põhjustesse, siis selle patsiendi kiire ravivastus ja normaalsed perifeerse vere määrded vähendasid hematoloogiliste pahaloomuliste kasvajate tõenäosust ning kõhu ultraheliuuring näitas normaalse suurusega põrna, mis välistas hüpersplenismi. Infektsioonide osas olid viiruslikud seroloogiad (CMV, EBV, gripp, HIV, hepatiidiviirus) negatiivsed, kuid positiivsed verekultuurid näitasid, et Pseudomonas sepsis võib olla neutropeenia potentsiaalne põhjus. Teisest küljest oli ravimist põhjustatud neutropeenia veel üks usutav seletus. Kõigist tema kasutatud ravimitest võivad klopidogreel, aspiriin ja furosemiid põhjustada neutropeeniat. Siiski oli klopidogreel ainus ravim, mida hakati kasutama esimest korda viimase kolme kuu jooksul, mistõttu ei saanud teised ravimid tõenäoliselt neutropeeniat põhjustada. Nende kahe võimaliku põhjuse hulgas ei olnud patsiendil palavikku ega infektsioonisümptomeid, kui neutropeeniat avastati esmakordselt klopidogreelravi 51. päeval. Seetõttu oli tõenäolisem, et neutropeenia tekkis enne sepsist, mitte vastupidi. Veelgi enam, monotsentrilise kohortuuringu kohaselt esines 34 protsendil ravimitest põhjustatud agranulotsütoosiga patsientidest peamiselt septitseemia või septiline šokk [4] ja eakatel patsientidel tõusis see protsent 64 protsendini [5], mis näitab, et septitseemia ei olnud patsientide puhul haruldane. ravimist põhjustatud neutropeeniaga. Rakendades sellele patsiendile Naranjo ADR-i (ravimi kõrvaltoime) tõenäosuse skaalat, saavutasime tulemuseks 5, mis näitas, et klopidogreel oli tõenäoline põhjus [6]. See muutis klopidogreeli selle patsiendi neutropeenia kõige tõenäolisemaks peamiseks süüdlaseks ja ebapiisava luuüdi reservi põhjustatud äge sepsis võib neutropeenia progresseerumist veelgi süvendada.

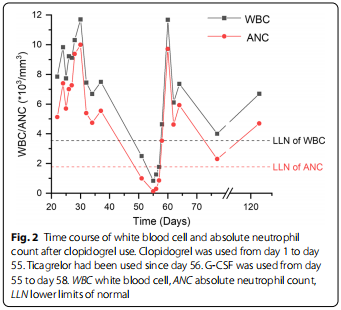
Haiglaravi ajal jätkasime tema elutähtsate näitajate, täieliku verepildi, põletikumarkerite ja südame biomarkerite jälgimist (tabel 1). Valgevereliblede ja absoluutse neutrofiilide arvu muutus on näidatud joonisel 2. Pärast neljapäevast ravi G-CSF-i ja imipeneemi/tsilastatiiniga oli ta kliiniliselt stabiilne normaalse temperatuuri ja valgete vereliblede arvuga ning tema absoluutne neutrofiilide arv oli taastatud kuni 3,53 × 103 /mm3. Seetõttu lõpetati G-CSF ja imipeneem/tsilastatiini kasutamine ning antibiootikumid viidi üle suukaudsele moksifloksatsiinile, mida kasutati veel neli päeva. Patsiendi kliiniline seisund, temperatuur, neutrofiilide arv ja põletikulised markerid olid sellest ajast alates normaalsed. Ta vabastati pärast 10-päevast haiglaravi ja talle tehti ülesandeks perioodiliselt jälgida oma täielikku verepilti. Ta tuli järelkontrollile pärast tikagreloori kasutamist vastavalt 23 ja 68 päeva ning tema täielik vereanalüüs oli normi piires. Patsient ei teatanud tikagreloori kasutamisega seotud kõrvaltoimetest.
Arutelu ja järeldused
Kahekordne trombotsüütidevastane ravi (DAPT) sisaldab aspiriini ja klopidogreeli. Euroopa Kardioloogide Seltsi juhised soovitavad kasutada kahekordset trombotsüütidevastast ravi (DAPT) patsientidel, kellel on diagnoositud äge koronaarsündroom või patsientidel, kellele tehakse perkutaanset koronaarset sekkumist [7]. Klopidogreel võib põhjustada võimalikke hematoloogilisi kõrvaltoimeid ja veritsus on kõige levinum. Muud hematoloogilised kõrvaltoimed on neutropeenia, trombotsütopeenia, pantsütopeenia, trombootiline trombotsütopeeniline purpur ja hemolüütiline ureemiline sündroom [8]. CAPRIE (Clopidogrel Versus Aspirin in Patients at Risk of Ischemic Events) [2] ja CURE (Clopidogrel in Unstable Angina to Prevent Recurrent Events) uuringute [9] kohaselt on neutropeenia esinemissagedus klopidogreeliga ravitud patsientidel madal. CAPRIE uuringus oli neutropeenia esinemissagedus pärast klopidogreeli kasutamist 0,10 protsenti ja raske neutropeenia (<450/mm3 ) was 0.05%. In the CURE studies, eight patients were reported with neutropenia in the clopidogrel group, which had 6259 patients in total, and the estimated incidence of neutropenia was 0.12%. Even though neutropenia is a rare adverse event, the actual incidence could be underestimated until further investigation in large multi-center clinical trials [8].

Cistanche tubulosa
Klopidogreeli põhjustatud neutropeenia täpset mehhanismi ei selgitatud täielikult. Varasemad luuüdi biopsiad näitasid, et klopidogreel võib müeloidsete kolooniate kasvu pärssimise kaudu põhjustada neutropeeniat [10]. Teised uuringud viitasid kahele võimalikule mehhanismile, sealhulgas kumulatiivne toksilisus ja idiosünkraatiline reaktsioon [11]. Tiklopidiinist põhjustatud neutropeenia võimalike mehhanismide kohta tehti rohkem uuringuid. Tiklopidiin ja klopidogreel on vastavalt esimese ja teise põlvkonna tienopüridiinid. Neil on sarnane struktuur, kuid tiklopidiinil on palju suurem neutropeenia esinemissagedus (2,1 protsenti) [12]. Tusal, tiklopidiinil ja klopidogreelil võivad olla sarnased mehhanismid, mis põhjustavad neutropeeniat. Ono et al. [13] viitas, et tiklopidiinil oli otsene ja annusest sõltuv inhibeeriv toime kolooniaid moodustavale ühikule kultuuris (CFU-C). Selle põhjuseks võib olla tiklopidiini poolt toodetud prostaglandiini E1 lokaalne suurenemine või immunoloogilise mehhanismi tagajärg [14]. Maseneni jt. [15] näitasid, et müeloperoksidaasi poolt moodustatud tienopüridiinide metaboliidid põhjustasid neutrofiilide granulotsüütide toksilisust. Need metaboliidid põhjustasid reaktiivsete hapnikuliikide akumulatsiooni ja raku apoptoosi.
According to Wu et al. [10], who summarized 12 cases from 2000 to 2014, the median age of clopidogrel-associated neutropenia patients was 65 years old. On average, neutropenia was detected after using clopidogrel for 22 days (ranging from 7 to 48 days), and the median neutrophil count at the time of onset was 479/mm3 (ranging from 0 to 1600/mm3 ). The recovery time was four days in those treated with G-CSF, while the recovery time was six days in those who were not treated with G-CSF. In our case, neutropenia was detected on the 51st day of clopidogrel therapy with a neutrophil count of 1000/ mm3, and the nadir of the neutrophil count was 130/mm3. We stopped clopidogrel therapy, switched to ticagrelor, and used empiric broad-spectrum antibiotics to treat sepsis. Several factors are correlated with poor prognosis in patients with drug-induced neutropenia, including age>65-aastane, olemasolevad kaasuvad haigused (eriti neerupuudulikkus), septitseemia ja absoluutne neutrofiilide arv<100/mm3 [16–18]. Due to multiple poor prognostic factors, we used G-CSF treatment in this patient. The patient's neutrophil count recovered in four days. Even though neutropenia is an infrequent adverse effect of clopidogrel, clinicians should always keep its possibility in mind and check complete blood count during patient follow-ups. In summary of the reported cases, the presenting symptoms range widely from normal being with no chief complaints to moderate tiredness to critical neutropenic fever. As for management, clopidogrel should be discontinued, and G-CSF could be used in patients with poor prognostic factors to speed the recovery time. Prevention of secondary infections and timely treatment of sepsis is a critical part of management as well. If neutropenic fever occurred, possible pathogens and sources of infection should be identified, and temperature, complete blood count, and inflammatory markers should be followed up to decide treatment duration.
Kirjanduse ülevaated viitavad mitmete teiste trombotsüütide vastaste ravimite, sealhulgas prasugreeli, tsilostasool ja tikagreloor, kasutamist, kui tekkis klopidogreeliga seotud neutropeenia [19–21]. Prasugreel kuulub tienopüridiini trombotsüütidevastaste ainete hulka ja sellel on sarnased tsüklistruktuurid, mida on täheldatud klopidogreelil ja tiklopidiinil [19]. TRITON-TIMI 38 uuringus oli neutropeenia esinemissagedus prasugreeli rühmas alla 0,1 protsendi, samas kui klopidogreeli rühmas oli esinemissagedus 0,2 protsenti [22]. Teisest küljest on tikagreloor mittetienopüridiini trombotsüütidevastane toime ja tsilostasool on selektiivne fosfodiesteraas-III inhibiitor. Nende struktuursed erinevused klopidogreelist võivad toetada nende kasutamist klopidogreeliga seotud neutropeenia korral. Meie puhul valisime tikagreloori, kuna ei olnud teateid tikagreloori põhjustatud neutropeenia kohta. Meie patsiendi valgete vereliblede ja absoluutsete neutrofiilide arv on pärast tikagreloorile üleminekut olnud normi piires. Siiski puudub konsensus selles, milline ravim on parem klopidogreeli põhjustatud neutropeenia ilmnemisel, ja veel on vaja rohkem tõendeid.

Cistanche kapslid
Meie patsiendi teeb eriliseks see, et tal oli krooniline neeruhaigus (4. staadium) ja ta põdes kontrastainest põhjustatud nefropaatiat. Pärast kõigi Pubmedi klopidogreeliga seotud neutropeenia juhtumite aruannete läbivaatamist leidsime kokku neli kroonilise neeruhaigusega patsientide juhtumit. Järgmine tabel (tabel 2) võtab kokku need neli juhtumit lisaks meie patsiendile. Neutropeenia keskmine algusaeg kroonilise neeruhaigusega patsientidel oli 36 päeva. Klopidogreel metaboliseerub maksas aktiivseteks metaboliitideks ja eritub neerude kaudu [23]. Kuigi tienopüridiinid võivad annusest sõltuval viisil põhjustada neutropeeniat, ei ole veel teada, kas sellel kõrvaltoimel on seos neerufunktsiooni kahjustusega. Klopidogreeliga ravitavate patsientide puhul on kriitilise tähtsusega hoolikas kliiniline ja hematoloogiline jälgimine, eriti kroonilise neeruhaigusega patsientide puhul esimese ühe kuni kahe kuu jooksul [24]. Lisaks on seerumi kreatiniini tase > 1,36 mg/dl üks ravimitest põhjustatud neutropeenia halbu prognostilisi tegureid [17] ning kroonilise neeruhaigusega patsiente tuleb hoolikalt jälgida ja kohe ravida.

Kokkuvõtteks võib öelda, et klopidogreel oli sellel patsiendil kõige tõenäolisem neutropeenia peamine põhjus. Klopidogreeli põhjustatud neutropeenia esinemissagedus on väike ja täpset mehhanismi ei ole täielikult selgitatud. Ei ole teada, kas sellel kõrvaltoimel on seos neerufunktsiooni kahjustusega. Me võtame kokku kõik viis klopidogreeli põhjustatud neutropeenia juhtumit neerufunktsiooni kahjustusega patsientidel. Soovitatav on klopidogreeliga ravitavate patsientide hoolikas kliiniline ja hematoloogiline jälgimine.
Cistanchise mõju neerude toitumisele
Neerud on elutähtis organ, mis vastutab vedeliku tasakaalu säilitamise, jääkainete filtreerimise ja vererõhu reguleerimise eest. Neerude tervis ja toitumine on üldise heaolu jaoks üliolulised. Cistanchis, tuntud ka kui Cistanche või Rou Cong Rong, on traditsioonilises hiina meditsiinis tavaliselt kasutatav taim neerude toitmiseks ja neerude tervise edendamiseks. Viimastel aastatel on kasvanud huvi Cistanchise võimalike eeliste vastu neerude toitumisele.
Cistanchis on rikas bioaktiivsete ühendite, nagu fenüületanoidglükosiidide, polüsahhariidide ja alkaloidide poolest, mis arvatakse soodustavat selle ravitoimet. Uuringud on näidanud, et Cistanchisel on antioksüdantsed omadused, mis aitavad kaitsta neere oksüdatiivse stressi ja kahjulike vabade radikaalide põhjustatud kahjustuste eest. Oksüdatiivne stress on erinevate neeruhaiguste peamine soodustav tegur.
Lisaks on leitud, et Cistanchisel on põletikuvastane toime. Krooniline neerupõletik võib põhjustada progresseeruvaid kahjustusi ja neerufunktsiooni häireid. Põletikku vähendades võib Cistanchis aidata ära hoida või aeglustada neeruhaiguste progresseerumist.
Teine viis, kuidas Cistanchis võib soodustada neerude toitumist, on vereringe parandamine ja neerude toitainetega varustatuse suurendamine. Tervislik verevool on oluline neerude tõhusaks toimimiseks ja elutähtsate toitainete tarnimiseks.
Lisaks on teatatud, et Cistanchis suurendab teatud ensüümide ja valkude aktiivsust, mis on seotud neerude regenereerimise ja parandamisega, toetades seeläbi neerukoe taastumist ja aidates kaasa neerukahjustustest taastumisele.
Kuigi olemasolevad uuringud viitavad Cistanchise paljulubavatele eelistele neerude toitumisele, on oluline märkida, et nende leidude kinnitamiseks ning optimaalse annuse ja pikaajaliste mõjude kindlaksmääramiseks on vaja täiendavaid uuringuid, sealhulgas kliinilisi uuringuid. Lisaks peaksid neeruhäiretega või ravimeid võtvad isikud enne Cistanchise lisamist oma raviskeemi konsulteerima oma tervishoiuteenuse osutajaga.
Kokkuvõtteks võib öelda, et Cistanchis on oma antioksüdantsete, põletikuvastaste ja regenereerivate omaduste kaudu näidanud potentsiaali neerude toitumise edendamisel. Selle toimemehhanismide täielikuks mõistmiseks ning selle tõhususe ja ohutusprofiili kindlakstegemiseks on siiski vaja rohkem uurida.
Viited
1. Sharis PJ, Cannon CP, Loscalzo J. Tiklopidiini ja klopidogreeli trombotsüütide vastane toime. Ann Intern Med. 1998;129(5):394–405.
2. CAPRIE juhtkomitee. Randomiseeritud, pimendatud uuring klopidogreeli ja aspiriini kohta isheemiliste sündmuste riskiga patsientidel (CAPRIE). Lancet. 1996;348(9038):1329–39.
3. Poksija LA. Kuidas neutropeeniale läheneda. Hematol Am Soc Hematol Educ Progr. 2012;2012:174–82.
4. Andrès E, Maloisel F, Kurtz JE, Kaltenbach G, Alt M, Weber JC, Sibilia J, Schlienger JL, Blicklé JF, Brogard JM jt. Mittekemoteraapiast põhjustatud agranulotsütoosi kaasaegne juhtimine: 90 juhtumi monotsentriline kohortuuring ja kirjanduse ülevaade. Eur J Intern Med. 2002;13(5):324–8.
5. Andrès E, Noel E, Kurtz JE, Henoun Loukili N, Kaltenbach G, Maloisel F. Eluohtlik idiosünkraatiline ravimite põhjustatud agranulotsütoos eakatel patsientidel. Narkootikumid Vananemine. 2004;21(7):427–35.
6. Naranjo CA, Busto U, Sellers EM, Sandor P, Ruiz I, Roberts EA, Janecek E, Domecq C, Greenblatt DJ. Meetod ravimi kõrvaltoimete tõenäosuse hindamiseks. Clin Pharmacol Ther. 1981;30(2):239–45.
7. Windecker S, Kolh P, Alfonso F, Collet JP, Cremer J, Falk V, Filippatos G, Hamm C, Head SJ, Jüni P jt. 2014. aasta ESC/EACTS-i juhised müokardi revaskularisatsiooni kohta: Euroopa Kardioloogide Seltsi (ESC) ja Euroopa Kardio-Torakaalkirurgia Assotsiatsiooni (EACTS) müokardi revaskularisatsiooni töörühm, mis on välja töötatud Euroopa Perkutaansete Kardiovaskulaarsete Interventsioonide Assotsiatsiooni erilise panusega. EAPCI). Eur Heart J. 2014;35(37):2541–619.
8. Almsherqi ZA, McLachlan CS, Sharef SM. Klopidogreeli mitte-verejooksu kõrvaltoimed: kas suured mitmekeskuselised kliinilised uuringud on nende esinemissagedust alahinnanud? Int J Cardiol. 2007;117(3):415–7.
9. Yusuf S, Zhao F, Mehta SR, Chrolavicius S, Tognoni G, Fox KK. Klopidogreeli toime lisaks aspiriinile ägeda koronaarsündroomiga patsientidel ilma ST-segmendi elevatsioonita. N Engl J Med. 2001;345(7):494–502.
10. Wu CW, Wu YJ, Wu CC. Klopidogreeliga seotud neutropeenia: juhtumiaruanne ja kirjanduse ülevaade. Olen J Ther. 2016;23(5):e1197-1201.
11. Andres E, Perrin AE, Alt M, Goichot B, Schlienger JL. Klopidogreeli kasutamisega seotud febriilne pantsütopeenia. Arch Intern Med. 2001; 161(1):125.
12. Quinn MJ, Fitzgerald DJ. Tiklopidiin ja klopidogreel. Tiraaž. 1999;100(15):1667–72.
13. Ono K, Kurohara K, Yoshihara M, Shimamoto Y, Yamaguchi M. Tiklopidiinist põhjustatud agranulotsütoos ja selle mehhanism. Olen J Hematol. 1991;37(4):239–42.
14. Taher A, Ammash Z, Dabajah B, Nasrallah A, Mourad FH. Tiklopidiinist põhjustatud aplastiline aneemia ja kiire taastumine G-CSF-iga: juhtumiaruanne ja kirjanduse ülevaade. Olen J Hematol. 2000;63(2):90–3.
15. Maseneni S, Donzelli M, Brecht K, Krähenbühl S. Tienopüridiinide toksilisus inimese neutrofiilide granulotsüütidel ja lümfotsüütidel. Toksikoloogia. 2013;308:11–9.
16. Juliá A, Olona M, Bueno J, Revilla E, Rosselló J, Petit J, Morey M, Flores A, Font L, Maciá J. Narkootikumide põhjustatud agranulotsütoos: prognostilised tegurid 168 episoodist koosnevas seerias. Br J Haematol. 1991;79(3):366–71.
17. Andrès E, Maloisel F. Idiosünkraatiline ravimitest põhjustatud agranulotsütoos või äge neutropeenia. Curr Opin Hematol. 2008;15(1):15–21.
18. Maloisel F, Andrès E, Kaltenbach G, Noel E, Martin-Hunyadi C, Dufour P. Hematoloogilise taastumise prognostilised tegurid eluohtlikus nonchemotherapy drug-induced agranulocytosis. Uuring, milles osales 91 patsienti ühest keskusest. Vajutage Med. 2004;33(17):1164–8.
19. Shah R, Keough LA, Belalcazar-Portacio A, Ramanathan KB. Tikagreloor alternatiivina klopidogreeliga seotud neutropeenia korral. Trombotsüüdid. 2015;26(1):80–2.
20. Khangura S, Gordon WL. Prasugreel alternatiivina klopidogreeliga seotud neutropeenia korral. Kas J Cardiol. 2011;27(6):869.e869-811.
21. Montalto M, Porto I, Gallo A, Camaioni C, Della Bona R, Grieco A, Crea F, Landolf R. Klopidogreeli põhjustatud neutropeenia pärast koronaarstentimist: kas tsilostasool on hea alternatiiv? Int J Vasc Med. 2011;2011:867964.
22. Wiviott SD, Braunwald E, McCabe CH, Montalescot G, Ruzyllo W, Gottlieb S, Neumann FJ, Ardissino D, De Servi S, Murphy SA jt. Prasugreel versus klopidogreel ägedate koronaarsündroomidega patsientidel. N Engl J Med. 2007;357(20):2001–15.
23. Balamuthusamy S, Arora R. Klopidogreeli hematoloogilised kahjulikud mõjud. Olen J Ther. 2007;14(1):106–12.
24. Suh SY, Rha SW, Kim JW, Park CG, Seo HS, Oh DJ, Ro YM. Klopidogreeli kasutamisega seotud neutropeenia kroonilise neerupuudulikkusega patsiendil, kellele tehti perkutaanne koronaarne ja perifeerne sekkumine. Int J Cardiol. 2006;112(3):383–5.
25. Chemnitz J, Söhngen D, Schulz A, Diehl V, Scheid C. Klopidogreeliga seotud surmaga lõppenud toksiline luuüdipuudulikkus. Eur J Haematol. 2003;71(6):473–4.
26. Akcay A, Kanbay M, Agca E, Sezer S, Ozdemir FN. Klopidogreeli põhjustatud neutropeenia lõppstaadiumis neeruhaigusega patsiendil. Ann Pharmacother. 2004;38(9):1538–9.
Yannan Pan 1, Bing Liu 2, Junmeng Liu 2, Wei Zhuang 3, Qing He 2 ja Ming Lan 2
1 Meditsiinikool, Pekingi ülikooli terviseteaduste keskus, Peking, Hiina.
2 Pekingi haigla kardioloogia osakond, riiklik gerontoloogia keskus, Peking, Hiina.
3 Riikliku Vähikeskuse meditsiinilise onkoloogia osakond / riiklik vähiuuringute keskus / vähihaigla, Hiina meditsiiniteaduste akadeemia ja Peking Unioni meditsiinikolledž, Peking, Hiina.






