SMFM Loote anomaaliad Konsulteerige seeria nr 4: Urogenitaalsüsteemi anomaaliad
Mar 23, 2023
Sissejuhatus
Loote urogenitaalsüsteem hõlmab loote neere, kusejuhasid, põit ning sise- ja välissuguelundeid. Loote urogenitaalsüsteemi standardne ultraheliuuring pärast raseduse esimest trimestrit hõlmab loote neerude ja põie visualiseerimist (joonised 1, A ja B ning 2). Neeruvaagna laienemist tuleks hinnata raseduse teisel ja kolmandal trimestril anteroposterioorse diameetri telgvaates (joonis 1, C). Loote suguelundeid tuleks uurida mitme raseduse ajal, kuna see võib aidata määrata koorionilisust või kui see on meditsiiniliselt näidustatud, näiteks kui patsiendil on X-seotud geneetilise häire oht (joonis 3). Lisaks tuleks mõõta lootevee mahtu (joonis 4), kuna see annab funktsionaalse hinnangu loote neerudele, mis toodavad lootevett pärast 16–17 rasedusnädalat. Neerupatoloogia võib seetõttu põhjustada nii lootevee mahu suurenemist kui ka vähenemist.
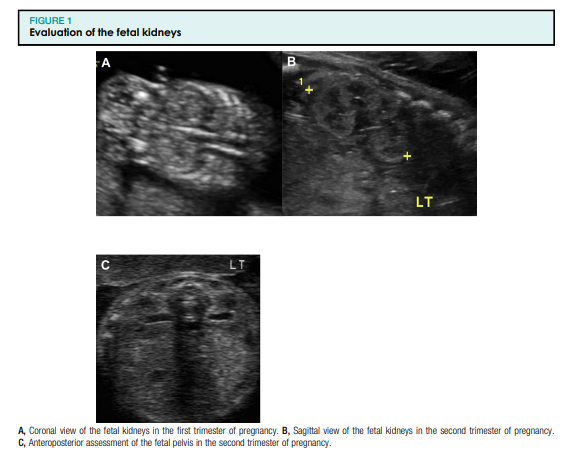
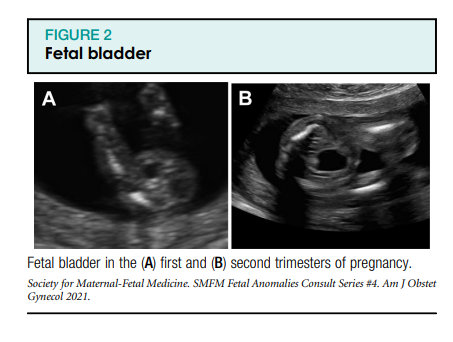
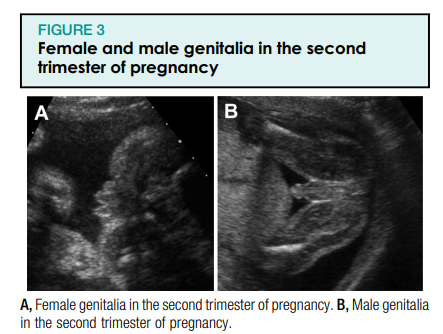


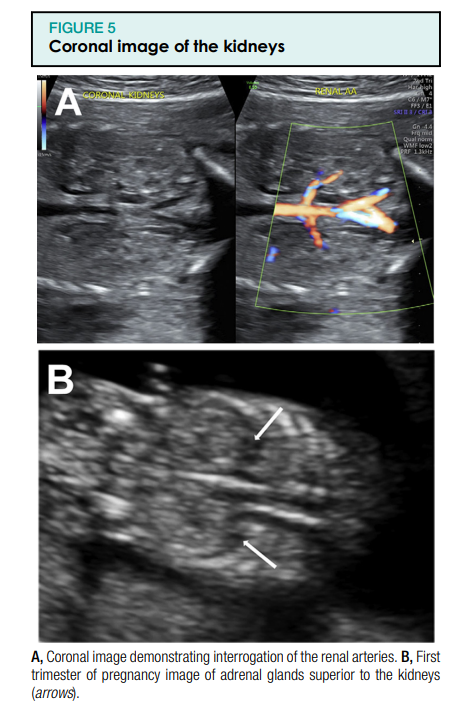
Kui see on näidustatud, võib üksikasjalik ultraheliuuring (76811) hõlmata neerupealiste uurimist ja neeruarterite ülekuulamist (joonis 5). Siia kuulub ka loote suguelundite uurimine.1
Urogenitaalsüsteemi kõrvalekalded on üks levinumaid loote struktuurilisi väärarenguid. Sellised kõrvalekalded ulatuvad kergest (nt kerge kuseteede laienemine) kuni raskete eluohtlike kõrvalekalleteni (nt kahepoolne neeruagenees).
Kuna neerud vastutavad amnionivedeliku tootmise eest, võivad tõsised neerukahjustused, mis kahjustavad uriini tootmist või eritumist (nt kuseteede obstruktsioon), põhjustada rasket oligohüdramnioni, mis võib põhjustada kopsu hüpoplaasiat ja olla eluohtlik. Loote põis ja neeruvaagen on suhteliselt kergesti visualiseeritavad ning seetõttu on neerude kõrvalekalded tavaliselt kergesti tuvastatavad. Need kõrvalekalded, mida on raskem tuvastada, nagu ühepoolne neeru-agenees või vaagnaneer, on vähem tõenäoliselt eluohtlikud või lootele kahjulikud.
Enamik neeruanomaaliaid on isoleeritud ja reeglina on aneuploidsuse või geneetiliste sündroomide risk madal. Erandiks on polütsüstilised neerud, mida võib seostada autosoomsete retsessiivsete või domineerivate häiretega. Teisi geneetilisi sündroome võivad iseloomustada mitmesugused multitsüstiliste või polütsüstiliste neerude vormid. Seetõttu peaks tsüstiline neeruhaigus nõudma hoolikat hindamist, et otsida muid kõrvalekaldeid ja pärilikke haigusi.
See konsultand annab ülevaate järgmiste urogenitaalsüsteemi kõrvalekallete ultrahelidiagnoosist, geneetilisest hindamisest ning võimalikust ravist ja tulemustest:
1 Neerupealiste neuroblastoom
2 Autosoomne retsessiivne polütsüstiline neeruhaigus
3 Kusepõie väljalaskeava takistus
4 Dubleeritud kogumissüsteem
5 Emakaväline ureterotseel
6 Hüdroureter
7 hüpospadiaat
8 Multitsüstiline düsplastiline neer
9 Munasarja tsüst
10 Vaagna neer
11 Neerude agenees
12 Neeruvaagna laienemine
13 Urinoom
Neeru- ja kuseteede haigustega vastsündinutel on sellega seoses palju probleeme ka täiskasvanutel. Täiskasvanute puhul peame ennetama neeruhaigusi. Enamik neeruhaigusi on põhjustatud ebanormaalsest neerufunktsioonist, mis põhjustab neerude võimetuse metaboliite ja toksiine organismist normaalselt väljutada. Siiski leidsime, et Cistanche'il on neeruhaigusi ennetav toime. Cistanche võib reguleerida neerupealiste funktsiooni, kaitsta maksa ja vähendada kusihapet. See võib aidata kehal vähendada neerude liigset koormust ja vähendada neeruhaiguste esinemissagedust.
Klõpsake Cistanche'i kasulikkust tervisele
Kodeerimine
Loote urogenitaalsüsteemi anomaaliate kodeerimisel soovitab Ema-Loote Meditsiini Kodeerimiskomitee kasutada rahvusvahelist haiguste klassifikatsiooni kümnendat redaktsiooni koodisarja O35.8XX.
TUNNUSTUS
Autorid soovivad tunnustada Mary E. Nortonit, MD; Jeffrey A. Kuller, MD; ja Angie C. Jelin, MD, andis ülevaate geneetika sisust ja Joseph Wax, MD, andnud üldise ülevaate selle konsultatsiooni kohta.
VIIDE
1. AIUM praktika parameeter üksikasjalike teise ja kolmanda trimestri diagnostiliste sünnitusabi ultraheliuuringute läbiviimiseks. J Ultrasound Med 2019;38:3093–100.
Neerupealiste neuroblastoom
Emade-Lootemeditsiini Ühing (SMFM); Jeffrey Sperling, MD
Sissejuhatus
Loote neerupealisi saab ultraheliuuringuga näha raseduse esimese trimestri lõpuks.1 Need on püramiidsed hüpoehoilised struktuurid, mis on kõrgemad kui hüperkaja neerud. Raseduse teisel trimestril võib kortikomedullaarset diferentseerumist täheldada hüpoehhoilise ajukoore ja hüperhehoilise medullaga. Nääre suurus suureneb kogu raseduse ajal, kuid jääb neerust väiksemaks. Raseduse kolmandal trimestril on loote neerupealiste välimus sarnane vastsündinu neerupealiste omaga.1
Neuroblastoomid moodustavad 50 protsenti loote neerupealiste massist.2,3 Neid esineb sagedamini valgetel imikutel ja veidi sagedamini meestel kui naistel.2 Neuroblastoomid pärinevad sümpaatilise närvisüsteemi neuraalharja rakkudest. Kuigi enamik juhtudest tulenevad neerupealistest, võivad need esineda ka tagumises mediastiinumis.2
Definitsioon
Termin neuroblastoom viitab neuroblastiliste kasvajate (nt neuroblastoomid, ganglioneuroblastoomid ja ganglioneuroomid) spektrile, mis tekivad sümpaatilistest ganglionrakkudest.2 Kuigi neuroblastoomid on pahaloomulised kasvajad ja mõned võivad metastaaseeruda, on prognoos suurepärane ja paljudel juhtudel taandub spontaanselt. 4
Ultraheli leiud
Neerupealiste neuroblastoom näib üldiselt hästi kapseldunud tsüstilise või tahke massina, mis asub neeru ja muude retroperitoneaalsete struktuuride kõrval, kuid on neist eraldi (joonis).3 Soovitatav on hinnata kontralateraalset neerupealist, et välistada normaalsed, kuid silmapaistvad neerupealised. Värvi-Doppleri uuringu tulemused on esitatud erinevalt ja hõlmavad perifeerset voolu, voolu puudumist või massi hüperehhogeensete aspektide sisemist vaskularisatsiooni.3,5 Tavaliselt ei esine üksikut toitumisarterit ja see viitab levinumale subdiafragmaatilisele bronhopulmonaalsele sekvestratsioonile (BPS). .6

Seotud kõrvalekalded
Postnataalselt on neuroblastoomi seostatud LiFraumeni sündroomi, Hirschsprungi tõve ja 1. tüüpi neurofibromatoosiga, kuid sünnieelsetel juhtudel ei ole neid seoseid kirjeldatud. Kui neuroblastoom oluliselt suurendab ja surub seedetrakti kokku, võib tekkida polühüdramnion.7 Teatatud on katehhoolamiinide taseme tõusust, mis võib põhjustada ema sümptomeid, nagu tahhükardia, hüpertensioon, iiveldus ja oksendamine.8 Lisaks on katehhoolamiinide vabanemist seostatud loote kardiomüopaatiaga. , tahhükardia ja vesitõbi.9 Harva võivad loote neuroblastoomid anda metastaase maksa.10

Diferentsiaaldiagnoos
Selle piirkonna massi diferentsiaaldiagnoos hõlmab neerupealiste tsüste11 (isoleeritud või seotud multitsüstiliste düsplastiliste neerude või Beckwith-Wiedemanni sündroomiga), neerupealiste hemorraagiat, 12 subdiafragmaatilist BPS-i, 13 maksakasvajaid ja adrenogenitaalset sündroomi (sekundaarne kaasasündinud hüperplaasiale14). On teatatud Beckwith-Wiedemanni sündroomiga seotud neerupealiste tsüstide hemorraagiast, mille puhul on tegemist kompleksse massiga.15
Geneetiline hindamine
Loote neuroblastoom on tavaliselt juhuslik leid. Kui ultraheliuuringus ei täheldata täiendavaid kõrvalekaldeid ja perekonna ajalugu ei ole märkimisväärne, ei soovitata tavaliselt geneetilist hindamist peale standardse aneuploidsuse sõeluuringu.
Raseduse ja sünnituse juhtimine
Lootevesi, polühüdramnion või mõlemad võivad tekkida harvadel juhtudel, tavaliselt suurte kahjustustega või metastaatilise haiguse taustal; seetõttu tuleks teha seeria ultraheliuuringud. Ultraheli seeriaanalüüs võib aidata välistada neerupealiste hemorraagiat, mis võib areneda.4,16 Sünnieelse ja postnataalse ravi planeerimiseks ja koordineerimiseks tuleks konsulteerida laste onkoloogia, neonatoloogia ja kirurgiaga. Üldiselt on raseduse katkestamine võimalus, mida tuleks patsientidele pakkuda, kui avastatakse suur looteanomaalia.
Enamikul neuroblastoomi juhtudest on prognoos siiski soodne ja tulemus on hea. Patsientide jagatud otsuste tegemine nõuab põhjalikku hindamist ja multidistsiplinaarset prognoosiga seotud nõustamist. Kui soovitakse rasedust katkestada, võib histoloogiline hindamine diagnoosi kinnitada.
Enamikul juhtudel on vaginaalne sünnitus sobiv ja keisrilõige tuleks reserveerida tavapäraste sünnitusnäidustuste jaoks. Keisrilõiget soovitatakse potentsiaalselt eelistada väga suurte neerupealiste tsüstiliste masside korral, et vältida rebenemist või pehmete kudede düstookiat. Neerupealiste tsüsti aspiratsioon enne sünnitust on vastuoluline, kuna see võib põhjustada verejooksu, pahaloomuliste kasvajate külvamist, enneaegset sünnitust või infektsiooni. Kui on tõendeid loote kahjustamise kohta, on soovitatav sünnitus kolmanda taseme hooldekeskuses, võttes arvesse varajase sünnituse võimalust. Soovitatav on postnataalne uuring, sealhulgas ultraheli, magnetresonantstomograafia või muud pildistamisviisid. Ülaltoodud kujutise, lõpliku diagnoosi ja vastsündinu seisundi tulemuste põhjal võib osutuda vajalikuks oodatav ravi, nõelbiopsia või kirurgiline uurimine.
Prognoos
Üldiselt on prognoos hea ja neuroblastoomid võivad isegi taanduda emakas või vahetult pärast sündi.3,13 Madala staadiumiga haigusega imikute elulemus on suurepärane, isegi nende puhul, kellel on metastaatiline haigus.17 On esinenud spontaanse involutsiooni juhtumeid. 18. Selle kahjustuse kordumise risk on teadmata, kuid tõenäoliselt väike.
Kokkuvõte
Loote neerupealiste neuroblastoomid, mis on saadud neuraalharja rakkudest, on lapsepõlves kõige sagedamini diagnoositud ekstrakraniaalne tahke kasvaja. Need haruldased kasvajad on seotud suurepärase postnataalse prognoosiga. Soovitatav on hoolikas jälgimine ja seeria ultraheliuuringud, mille käigus hinnatakse loote hüdropsi ja polühüdramnioni sümptomeid. Soovitatav on sünnituseelne konsultatsioon laste onkoloogia, neonatoloogia ja kirurgiaga.

VIITED
1. Norton ME. Calleni ultraheli sünnitusabi ja günekoloogia e-raamat. Elsevier Health Sciences; 2016. aasta.
2. Goodman MT, Gurney J, Smith M, Olshan A. Sümpaatilise närvisüsteemi kasvajad. Laste ja noorukite vähi esinemissagedus ja ellujäämine: Ameerika Ühendriikide SEER programm. 1975;1995:65–72.
3. Sauvat F, Sarnacki S, Brisse H jt. Perinataalsel perioodil diagnoositud suprarenaalsete lokaliseeritud masside tulemus: retrospektiivne mitmekeskuseline uuring. Vähk: Ameerika Vähiliidu interdistsiplinaarne rahvusvaheline ajakiri. 2002;94(9):2474–80.
4. Fisher JPH, Tweddle DA. Vastsündinu neuroblastoom. Seminarid loote- ja vastsündinute meditsiinis 2012 Aug;17(4):207–15.
5. Schwärzler P, Bernard JP, Senat MV, Ville Y. Loote neerupealiste masside sünnieelne diagnoos: hemorraagia ja soliidtuumori eristamine värvilise Doppleri sonograafia abil. Ultraheli sünnitusabis ja günekoloogias: Rahvusvahelise sünnitusabi ja günekoloogia ultraheliühingu ametlik väljaanne. 1999;13(5):351–5.
6. Curtis MR, Mooney DP, Vaccaro TJ jt. Suprarenaalse massi sünnieelne ultraheliuuring: neuroblastoomi ja subdiafragmaatilise ekstralobaarse kopsu sekvestratsiooni erinevus. Journal of Ultrasound in Medicine 1997;16(2):75–83.
7. Cho JY, Lee YH. Loote kasvajad: sünnieelsed ultraheliuuringud ja kliinilised omadused. Ultrasonograafia 2014;33(4):240.
8. Jennings RW, LaQuaglia MP, Leong K, Hendren WH, Adzick NS. Loote neuroblastoom: sünnieelne diagnoos ja looduslugu. Journal of Pediatric Surgery 1993;28(9):1168–74.
9. Inoue T, Ito Y, Nakamura T, Matsuoka K, Sago H. Catecholamine-secreting neuroblastoma leads to hydrops fetalis. Journal of Perinatology 2014;34:405–7.
10. Desai G, Filly RA, Rand L. Neerupealisevälise neuroblastoomi sünnieelne tuvastamine maksa metastaasidega. J Ultrasound Med 2009; 28(8): 1085–90.
11. Patti G, Fiocca G, Latini T, Celli E, Bellussi A, Nazzicone P. Kahepoolsete neerupealiste tsüstide sünnieelne diagnoos. The Journal of Urology 1993; 150 (4): 1189–91.
12. Strouse P, Bowerman RA, Schlesinger AE. Antenataalsed sonograafilised leiud loote neerupealiste hemorraagia kohta. Journal of Clinical Ultrasound 1995;23(7):442–6.
13. Rubenstein S, Benacerraf B, Retik A, Mandell J. Loote suprarenaalsed massid: sonograafiline välimus ja diferentsiaaldiagnostika. Ultrasound in Obstetrics & Gynecology 1995;5(3):164–7.
14. Maki E, Oh K, Rogers S, Sohaey R. Loote suprarenaalsete masside kuvamine ja diferentsiaaldiagnostika. J Ultrasound Med 2014;33(5):895–904.
15. Gocmen R, Basaran C, Karcaaltincaba M jt. Kahepoolsed hemorraagilised neerupealiste tsüstid Beckwith-Wiedemanni sündroomi mittetäielikus vormis: MRI ja sünnieelsed USA leiud. Abdominal Imaging 2005;30(6):786–9.
16. Birkemeier KL. Tahkete kaasasündinud kõhumasside kuvamine: kirjanduse ülevaade ja praktiline lähenemine kujutise tõlgendamisele. Pediatr Radiol 2020 detsember;50(13):1907–20.
17. London W, Castleberry R, Matthay K jt. Tõendid vanusepiiri üle 365 päeva kohta neuroblastoomi riskirühma kihistumise kohta laste onkoloogiarühmas. Journal of Clinical Oncology 2005; 23(27): 6459–65.
18. Holgersen LO, Subramanian S, Kirpekar M, Mootabar H, Marcus JR. Antenataalselt diagnoositud neerupealiste masside spontaanne lahenemine. Journal of Pediatric Surgery 1996;31(1):153–5.
Autosoomne retsessiivne polütsüstiline neeruhaigus
Emade-Lootemeditsiini Ühing (SMFM); Kate Swanson, MD
Sissejuhatus
Autosoomne retsessiivne polütsüstiline neeruhaigus (ARPKD) on haruldane geneetiline haigus, mille esinemissagedus on hinnanguliselt 1/20, 000 elussündi kohta.1 Kuigi esinemine on erinev ja uued edusammud, mis muudavad haigete inimeste eeldatavat eluiga, on see siiski endiselt olemas. kõrge haigestumuse ja suremusega haigus, eriti kui seda diagnoositakse sünnieelselt.
Definitsioon
ARPKD-ga haigetel inimestel on tavaliselt kromosoomi 6p21 PKHD1 geenis bialleelsed patogeensed variandid. Need variandid mõjutavad fibrotsüstiini tootmist – valku, mida leidub neerutuubulite ja maksa sapiteede epiteelirakkude primaarses tsiliumis või basaalkehakompleksis.2 Need variatsioonid põhjustavad kogumiskanalite pikenemist ja laienemist, mikrotsüstiinide moodustumist ja neerude difuusne suurenemine.3 Selle tulemusena arenevad haigetel inimestel välja lõppstaadiumis neeruhaigus ja hepatobiliaarne haigus.
Ultraheli leiud
There is wide variability in the prenatal presentation of ARPKD. In some cases, enlarged hyperechoic kidneys with poor corticomedullary differentiation can be identified in the second trimester of pregnancy. Frequently, the kidneys are quite enlarged, ranging from 4 to 15 standard deviations above normal in size. In addition, oligohydramnios or hydramnios are frequently present in ARPKD. In more subtle cases, mild enlargement and a hyperechoic cortical rim may be the only findings. In the third trimester of pregnancy, larger cysts >Võib tekkida 3 mm suurune. Need tsüstid võivad olla kahepoolsed või ühepoolsed. Mõningatel juhtudel sünnieelselt kõrvalekaldeid ei tuvastata (joonis).4
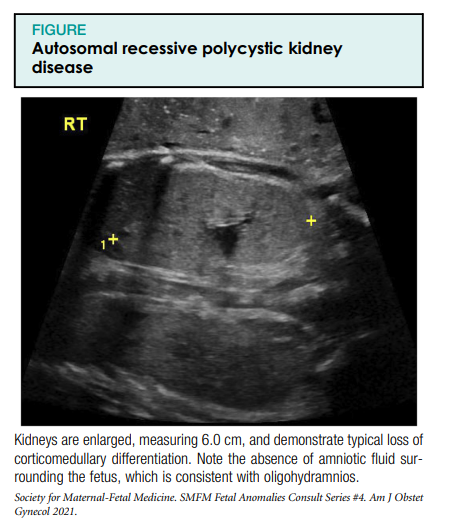
Seotud kõrvalekalded
Lisaks oligohüdramnionile või hüdramnionile ja sellest tulenevale kopsu hüpoplaasiale, mida võib mõnikord ultraheliuuringuga kahtlustada, on täiendavad ultrahelianomaaliad harvad. Kuigi maksafibroos ja sapiteede düsgenees on haigetel patsientidel tavalised, tuvastatakse neid leide prenataalselt harva.4,5
Diferentsiaaldiagnoos
Bardet-Biedli sündroom on veel üks tsiliopaatia, mis võib esineda sünnieelselt koos tsüstiliste neerude suurenemisega. Postaksiaalne polüdaktüülia on tavaline Bardet-Biedli sündroomiga inimestel ja võib aidata seda eristada ARPKD-st. Lisaks on Bardet-Biedli sündroomiga inimestel neeruparenhüüm tavaliselt homogeensem.6 Meckel-Gruberi sündroom on veel üks haruldane autosoomne retsessiivne seisund, mis võib avalduda tsüstiliste neerude suurenemisega; tsüstid ilmuvad sageli varem kui ARPKD korral. Postaksiaalne polüdaktüülia ja kesknärvisüsteemi väärarengud on Meckel-Gruberi sündroomi korral tavalised.
Geneetiline hindamine
ARPKD kahtluse korral tuleks pakkuda sünnieelset diagnostilist testi. Lisaks võib sünnieelse diagnoosi tegemisel pakkuda kromosomaalset mikrokiibi analüüsi, eriti täiendavate ultraheli leidude korral, kuigi see ei tuvasta ühe geeni häireid, sealhulgas ARPKD-d. PKHD1 geeni patogeensete variantide tuvastamiseks saab kasutada koorionivilluse proovide võtmise või amniotsenteesi teel saadud kudede molekulaargeneetilist testimist. Kahe patogeense variandi olemasolu selles geenis kinnitab ARPKD diagnoosi. Kuid isegi juhtudel, kui diagnoosimisel on tugev histopatoloogiline ja kliiniline tugi, on variantide tuvastamise määr vahemikus 80–85 protsenti.7,8 Kui esineb täiendavaid kõrvalekaldeid, suguluskuuluvust või perekonnas on esinenud konkreetset haigusseisundit, tehakse geenipaneeli testimine või eksoomide järjestamine on mõnikord kasulik.
Raseduse ja sünnituse juhtimine
Arvestades sünnieelselt tuvastatud ARPKD-ga isikute halba prognoosi, eriti varajase oligohüdramnioni või hüdramnioni korral, tuleks kahjustatud lootega patsientidele pakkuda raseduse katkestamist. Vanematele, kes otsustavad rasedust jätkata, tuleks pakkuda vastsündinule sünnituse ajal mugavust. Raseduse ajal võivad seeria ultraheliuuringud olla kasulikud neerude suuruse ja lootevee mahu hindamiseks.9 Vanemad, kes soovivad täielikku elustamist, peaksid toimetama IV taseme vastsündinute intensiivravi osakonnas. Kuna neerude ulatuslik suurenemine võib põhjustada kõhu ümbermõõtu, mis võib välistada vaginaalse sünnituse õigeaegselt, võib vajalik olla keisrilõige.10

Prognoos
ARPKD esitus ja prognoos on märgatavalt varieeruvad. Sünnieelselt diagnoositud ARPKD on seotud kehvemate tulemustega kui vastsündinu perioodil või lapsepõlves tuvastatud ARPKD. Neil, kellel on sünnieelse ultraheliuuringuga tuvastatud oligohüdramnion või hüdramnion, on märkimisväärne kopsuhüpoplaasia risk ja nende suremus esimesel eluaastal on ligikaudu 30%.11 Lisaks on teatatud, et genotüübil võib olla teatav seos fenotüübiga ja et isikud kärbivate variantidega on suurema tõenäosusega kehvad tulemused kui missense variantidega.3
Inimestel, kes jäävad ellu pärast esimest elukuud, on parem prognoos – teatatud 10-aastase elulemuse määr on koguni 82 protsenti. Kuid need patsiendid vajavad tavaliselt dialüüsi ja neerusiirdamist ning neil tekib sageli hüpertensioon, maksafibroos ja portaalhüpertensioon.12
Kokkuvõte
ARPKD-d diagnoositakse sünnieelse ultraheliga harva. Kuid kui see tuvastatakse, seostatakse seda märkimisväärse haigestumuse ja suremusega. Autosomaalse retsessiivse haigusena, millel on varieeruv väljendusvõime, tuleks mõjutatud rasedusega patsientide vanemaid ja õdesid-vendi hinnata ja nõustada nende riskide osas, et neil on ka mõjutatud rasedus.
VIITED
1. Wilson PD. Polütsüstiline neeruhaigus. N Ingl J Med 2004;350:151–64.
2. Ward CJ, Yuan D, Masyuk TV jt. ARPKD valgu rakuline ja subtsellulaarne lokaliseerimine; fibrotsüstiin ekspresseerub primaarsetel ripsmetel. Hum Mol Genet 2003;12:2703–10.
3. Denamur E, Delezoide AL, Alberti C jt. Genotüübi-fenotüübi korrelatsioonid autosomaalse retsessiivse polütsüstilise neeruhaigusega loodetel ja vastsündinutel. Kidney Int 2010;77:350–8.
4. Avni FE, Garel L, Cassart M jt. Pärilike tsüstiliste neeruhaiguste perinataalne hindamine: sonograafia panus. Pediatr Radiol 2006;36:405–14.
5. Erger F, Brüchle NO, Gembruch U, Zerres K. Sünnieelne ultraheliuuring, genotüüp ja tulemus suurel prenataalselt mõjutatud patsientide rühmal, kellel on autosoom-retsessiivne polütsüstiline neeruhaigus ja muud pärilikud tsüstilised neeruhaigused. Arch Gynecol Obstet 2017; 295:897–906.
6. Mary L, Chennen K, Stoetzel C jt. Bardet-Biedli sündroom: teadaolevates Bardet-Biedli sündroomi geenides bialleelsete patogeensete variantidega neljakümne viie loote sünnieelne esitlus. Clin Genet 2019;95:384–97.
7. Bergmann C, Senderek J, Schneider F jt. PKHD1 mutatsioonid perekondades, kes taotlevad autosoomse retsessiivse polütsüstilise neeruhaiguse (ARPKD) sünnieelset diagnoosi. Hum Mutat 2004;23:487–95.
8. Guay-Woodford LM, Desmond RA. Autosoomne retsessiivne polütsüstiline neeruhaigus: kliiniline kogemus Põhja-Ameerikas. Pediaatria 2003;111:1072–80.
9. Guay-Woodford LM, Bissler JJ, Braun MC jt. Ekspertide konsensuse soovitused autosomaalse retsessiivse polütsüstilise neeruhaiguse diagnoosimiseks ja raviks: rahvusvahelise konverentsi aruanne. J Pediatr 2014;165:611–7.
10. Dukic L, Schaffelder R, Schaible T, Sütterlin M, Siemer J. [Loote kõhu ümbermõõdu massiline suurenemine päriliku polütsüstilise neeruhaiguse tõttu]. Z Geburtshilfe Neonatol 2010;214:119–22.
11. Sweeney WE, Avner ED. Polütsüstiline neeruhaigus, autosoomne retsessiivne. Seattle, WA: Washingtoni Ülikool; 2021. aasta.
12. Bergmann C, Senderek J, Windelen E jt. PKHD1 mutatsioonide kliinilised tagajärjed 164 autosoom-retsessiivse polütsüstilise neeruhaigusega (ARPKD) patsiendil. Kidney Int 2005;67:829–48.
Kusepõie väljalaskeava takistus
Emade-Lootemeditsiini Ühing (SMFM); Anne Mardy, MD
Sissejuhatus
Loote põie väljavoolu obstruktsioon (või alumiste kuseteede obstruktsioon [LUTO]) on kõige sagedamini põhjustatud ureetra tagumisest ventiilist ja kusiti atreesiast ning see võib põhjustada neerude ebanormaalset arengut ja kopsu hüpoplaasiat. Seda seostatakse kõrge perinataalse haigestumuse ja suremusega.
Definitsioon
Sünnieelselt tuvastatud LUTO tekib areneva loote alumiste kuseteede (põie väljalaskeava) ummistumise tõttu ja põhjustab megatsüsti, paksenenud põieseina ja kahepoolset hüdroonefroosi koos neeruparenhüümi tsüstilise düsplaasiaga või ilma.
Ultraheli leiud
In the first trimester of pregnancy, megacystis, or an enlarged bladder, is commonly defined as a sagittal length >7 mm.1e3 After the first trimester of pregnancy, there is no single definition of megacystis, with many different definitions found in the literature.4 One study defined the normal sagittal length as the gestational age in weeks minus 5 mm (95% upper or lower confidence interval [CI]¼7); megacystis was defined as greater than the upper limit of the 95% CI for the gestational age.5 A thickened bladder wall is defined as one that measures >3 mm. Hüdronefroos on defineeritud kui neeruvaagna laienemine, mõõdetuna anteroposterioorses läbimõõdus, 4 mm raseduse teisel trimestril ja 7 mm raseduse kolmandal trimestril (joonis 1). Laienenud tagumine ureetra, tuntud ka kui "võtmeaugu" märk, on tavaliselt seotud tagumiste kusiti klappidega (joonis 2). Lisaks võib kõrgest põierõhust tingitud tagasivoolu tõttu täheldada kusejuha laienemist. Neerud võivad välja arendada tsüstilise düsplaasia või muutuda ehhogeenseks ja atrofeeruda.
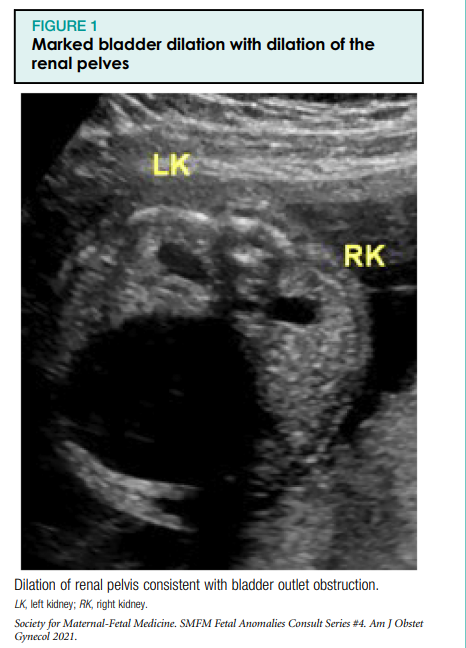

Seotud kõrvalekalded
Enamik LUTO juhtumeid (78 protsenti) on isoleeritud.6 LUTO-d seostatakse sageli oligohüdramnioniga, mis võib põhjustada jalgade lonkamist või kopsu hüpoplaasiat. Kusepõie või neeru rebenemise tagajärjel võivad tekkida kuseteede astsiit ja perinefrilised urinoomid.
Diferentsiaaldiagnoos
LUTO kõige levinum etioloogia on ureetra tagumised klapid (63 protsenti), mis on kaasasündinud membraanid tagumises ureetras, mis toimivad urineerimist blokeerivate ventiilidena. Klassikaliste tunnuste hulka kuuluvad megatsüstiit, paksenenud põie sein, laienenud tagumine kusiti ("võtmeaugu" märk), kahepoolne hüdronefroos või kortikaalsed tsüstid ja oligohüdramnion. Ureetra atresia on LUTO levinuim etioloogia teine (10 protsenti) ja sellel võib olla sama välimus kui oluliselt laienenud põiel, kuigi ilma laienenud ureetra või võtmeauguta. Erinevalt tagumistest ureetra klappidest, mis esinevad ainult meestel, võib kusiti atreesia esineda nii mees- kui ka naislootel.6
Laienenud põie diferentsiaaldiagnostika muud seisundid hõlmavad Prune-Belly sündroomi (kõhu lõtva või puuduva lihaskonna kolmik, õhukese seinaga laienenud põis ja krüptorhidism), aneuploidsust (kõige sagedamini trisoomia 13, 18 või 21), megatsüstiidi-megaureteri sündroom (raske vesikoureteraalne refluks) ja megatsüstiidi-mikrokoloonia sündroom (õhukese seinaga põis ilma laienenud tagumise ureetrata; normaalne või suurenenud amnionivedelik).6,7 Naislootel võib vaheseinaanomaaliast põhjustatud laienenud tupp jäljendada. laienenud põis. Arvestada tuleks ka püsiva kloaagiga (põie, pärasoole ja tupe lähenemine ühe perineaalse avaga). Suur juhtumite seeria näitas, et 26,9 protsenti LUTO sünnieelsetest diagnoosidest olid valepositiivsed. Nendel juhtudel olid kõige levinumad lõplikud postnataalsed diagnoosid vesikoureteraalne refluks (24,5 protsenti), kloaagi düstroofia (18,9 protsenti) ja hüdronefroos (11,3 protsenti). 5 juhul lahenes obstruktsioon raseduse ajal.6

Geneetiline hindamine
Kui tuvastatakse põie väljalaskeava obstruktsioon, tuleks pakkuda diagnostilist testimist amniotsenteesi või koorioni villuse proovide võtmisega ja kromosomaalse mikrokiibi analüüsiga (CMA). Kui laienenud põis ja raske oligohüdramnion muudavad amniotsenteesi võimatuks, võib testida platsenta biopsiaga või vesikotsenteesiga saadud vedelikuga. Kui ultraheli leiud või sõeluuringu tulemused viitavad tavalisele aneuploidsusele, on mõistlik esialgu läbi viia karüotüübi analüüs või fluorestsentsi in situ hübridisatsioon, peegeldades CMA-le, kui neid testitulemusi oodatakse. Kui esineb täiendavaid kõrvalekaldeid, sugulushaigust või perekonna ajalugu, on geenipaneeli testimine või eksoomide järjestamine mõnikord kasulik, kuna CMA ei tuvasta ühe geeni (Mendeli) häireid. Kui teostatakse eksoomide sekveneerimist, soovitatakse asjakohast eel- ja testijärgset geneetilist nõustamist genoomse sekveneerimise keerukuse alal kogenud pakkujalt. Pärast nõuetekohast nõustamist on rakuvaba DNA skriinimine võimalus patsientidele, kes keelduvad diagnostilisest hindamisest, eriti kui kahtlustatakse tavalist aneuploidiat.
Raseduse ja sünnituse juhtimine
Arvestades LUTO-ga seotud halba prognoosi, tuleks pakkuda raseduse katkestamist. Patsientide jagatud otsuste tegemine nõuab põhjalikku hindamist ja multidistsiplinaarset prognoosiga seotud nõustamist. Patsientidel, kes jätkavad rasedust, on soovitatud kasutada seeriavesikotsenteesid, et hinnata loote neerufunktsiooni, et aidata kindlaks teha, kas loote sekkumist tuleks jätkata, kuigi on vaidlusi nende kasulikkuse kohta prognostiliste markeritena.7 Vedelik põiest eemaldatakse täielikult kaks või kolm korda. järjestikuselt uriini elektrolüütide taseme ja põie täitumise määra mõõtmiseks. Loote uriini normaalväärtused on järgmised: naatrium<100 mg/dL, chloride<90 mg/ dL, osmolarity<200 mOsm/L, calcium<8 mg/dL, total protein<20 mg/dL, and beta-2-microglobulin<4 mg/dL.8 After the first vesicocentesis, a subsequent ultrasound examination can determine whether the bladder refills. The absence of a bladder refill usually indicates severe renal dysfunction, and no further vesicocenteses are recommended.7
Loodud on LUTO staadiumisüsteem koos soovitatavate looteravidega.7 Võimalike loote sekkumiste hulka kuuluvad tsüstoskoopia, vesikoamniootiline šunt või amnioinfusioon. Tsüstoskoopia võib võimaldada nii diagnoosimist kui ka ravi läbi ureetra juhttraadi või tagumiste ureetra klappide laserablatsiooni. PLUTO (perkutaanne vesikoamniootiline šunteerimine loote alumiste kuseteede obstruktsiooni korral) uuringus ei suurendanud vesikoamniootiline šunt ravikavatsusanalüüsis võrreldes konservatiivse raviga elulemust 28 päevani, kuid suurendas tegeliku ravi põhjal elulemust. Haigestumus ja suremus olid mõlemas rühmas väga kõrged ning šundi tüsistuste esinemissagedus oli kõrge.9 On pakutud välja, et amnioonfusioonide sari on üks võimalus, mis võimaldab rasketel juhtudel ellujäämist, vähendades kopsu hüpoplaasia riski, kuigi andmed on piiratud. selle sekkumise sobiva rolli kindlaksmääramiseks on vaja uuringuid.10
Vanemad, kes soovivad täielikku elustamist, peaksid toimetama IV taseme vastsündinute intensiivravi osakonnas (NICU). Üldiselt peaks sünnitusviis põhinema tavapärastel sünnitusabi näidustustel ja vanemate eelistustel elustamist rasketel juhtudel. Ei ole tõestatud, et kavandatud enneaegne sünnitus põie šunteerimiseks oleks kasulik.
Prognoos
LUTO on seotud kõrge loote ja perinataalse haigestumuse ja suremusega. Halvimat prognoosi nähakse varajase, raske, pikaajalise oligohüdramnioni koos kaasneva kopsuhüpoplaasiaga.11,12 Muud halvad prognostilised tunnused hõlmavad neeruparenhüümi kõrvalekaldeid ja ebanormaalset loote uriinianalüüsi. Märkimisväärsel protsendil tagumiste kusitiklappidega patsientidest tekib lõppstaadiumis neeruhaigus ning nad vajavad dialüüsi ja siirdamist.13 Need patsiendid vajavad pikemat NICU-s viibimist, sageli mitu aastat kestvat gastrotoomiasondi kasutamist ning neil on kalduvus infektsioonidele ja mehaanilise dialüüsi ebaõnnestumisele. Lisaks võivad ureetra tagumised klapid kahjustada põit ja laps võib vajada puhast vahelduvat kateteriseerimist või põieoperatsioone, et saavutada kontinents pärast sündi ja kogu elu jooksul.
Kokkuvõte
Loote LUTO-le on iseloomulik suurenenud põis, paksenenud põieseinad ja hüdroonefroos. Seda põhjustavad kõige sagedamini tagumised ureetra ventiilid. Loote LUTO võib põhjustada ebanormaalset neerude arengut ja kopsu hüpoplaasiat ning seda seostatakse kõrge perinataalse haigestumuse ja suremusega. Loote sekkumise võimaluse hindamiseks tuleks pakkuda vesikotsenteesi ja geneetilist testimist, kuigi optimaalne sekkumine ja tulemused on ebaselged. Teatatud sekkumiste hulka kuuluvad tsüstoskoopia koos klapi ablatsiooniga või ilma, vesikoamniootiline šunteerimine või amnioinfusioon. Hoolimata sekkumisest on prognoos sageli halb, kõrge kopsuhüpoplaasia, lõppstaadiumis neeruhaiguse ja põie düsfunktsiooniga.
VIITED
1. Sebire NJ, Von Kaisenberg C, Rubio C, Snijders RJ, Nicolaides KH. Loote megatsüstiit 10-14 rasedusnädalal. Ultrasound Obstet Gynecol 1996;8:387–90.
2. Liao AW, Sebire NJ, Geerts L, Cicero S, Nicolaides KH. Megatsüstiit 10-14 rasedusnädalal: kromosoomidefektid ja tulemus vastavalt põie pikkusele. Ultraheli Obstet Gynecol 2003;21:338–41.
3. Kagan KO, Staboulidou I, Syngelaki A, Cruz J, Nicolaides KH. 11- 13-Nädala skaneerimine: holoprosentsefaalia, eksomfalose ja megatsüstiidi diagnoos ja tulemus. Ultraheli obstet Gynecol 2010;36:10–4.
4. Taghavi K, Sharpe C, Stringer MD. Loote megatsüstis: süstemaatiline ülevaade. J Pediatr Urol 2017;13:7–15.
5. Maizels M, Alpert SA, Houston JT, Sabbagha RE, Parilla BV, MacGregor SN. Loote põie sagitaalne pikkus: lihtne monitor loote normaalse ja suurenenud põie suuruse ning kliinilise tulemuse prognoosimiseks. J Urol 2004;172:1995–9.
6. Malin G, Tonks AM, Morris RK, Gardosi J, Kilby MD. Kaasasündinud alumiste kuseteede obstruktsioon: populatsioonipõhine epidemioloogiline uuring. BJOG 2012;119:1455–64.
7. Ruano R, Dunn T, Braun MC, Angelo JR, Safdar A. Alumiste kuseteede obstruktsioon: loote sekkumine sünnieelsel etapil. Pediatr Nephrol 2017;32:1871–8.
8. Abdennadher W, Chalouhi G, Dreux S jt. Loote uriini biokeemia 13-23 rasedusnädalal alumiste kuseteede obstruktsiooni korral: inuteroravi kriteeriumid. Ultrasound Obstet Gynecol 2015;46:306–11.
9. Morris RK, Malin GL, Quinlan-Jones E jt. Perkutaanne vesikoamniootiline šunteerimine versus loote alumiste kuseteede obstruktsiooni (PLUTO) konservatiivne ravi: randomiseeritud uuring. Lancet 2013;382: 1496–506.
10. Haeri S, Simon DH, Pillutla K. Serial amnioinfusions for fetal pulmonary palliation in fetes with neerupuudulikkus. J Matern Fetal Neonatal Med 2017;30:174–6.
11. Kilbride HW, Yeast J, Thibeault DW. Elulemuse piirid: surmav kopsu hüpoplaasia pärast trimestri keskpaiga enneaegset membraanide purunemist. Am J Obstet Gynecol 1996;175:675–81.
12. Nakayama DK, Harrison MR, de Lorimier AA. Sünnil esinevate ureetra tagumiste klappide prognoos. J Pediatr Surg 1986;21:43–5.
13. Morris RK, Kilby MD. Pikaajaline neeru- ja närvisüsteemi arengu tulemus LUTO-ga imikutel koos loote sekkumisega ja ilma. Early Hum Dev 2011;87:607–10.
For more information:1950477648nn@gmail.com
