Kroonilise neeruhaiguse erinevad tüübid, mida peate teadma
Mar 22, 2022
ali.ma@wecistanche.com
Ⅱ osa: uriinivalgu ja peptiidi markerid kroonilise neeruhaiguse korral
Natalia Chebotareva, Anatoli Vinogradov jt.
Abstraktne
Krooniline neeruhaigus (CKD)on mittespetsiifiline tüüpneeruhaigusmis põhjustab neerufunktsiooni järkjärgulist langust (kuudest aastateni). CKD(Krooniline neeruhaigus)on oluline surma, südame-veresoonkonna haiguste ja lõppstaadiumis neeruhaiguse riskitegur. CKD(Krooniline neeruhaigus) erineva päritoluga kliinilised ja laboratoorsed ilmingud võivad olla samad, kuid erinevad progresseerumise määrad, mille kindlakstegemiseks on vaja varajast diagnoosimist. See ülevaade keskendub kroonilise neeruhaiguse peamiste põhjuste valgu/peptiidi biomarkeritele(Krooniline neeruhaigus): diabeetiline nefropaatia, IgA nefropaatia, luupusnefriit, fokaalne segmentaalne glomeruloskleroos ja membraanne nefropaatia. Massispektromeetria (MS) lähenemisviisid andsid kõige rohkem teavet uriini peptiidide ja valkude sisalduse kohta erinevates nefropaatiates. Uued analüütilised lähenemisviisid võimaldavad kasutada uriini proteoomiliste peptiidide profiile varajase mitteinvasiivse diagnostikavahendina spetsiifiliste morfoloogiliste vormide jaoks.neeruhaigusja võib saada ohutuks alternatiiviks neerubiopsiale. MS uuringud neeruhaiguse progresseerumise peamiste patogeneetiliste mehhanismide kohta võivad samuti aidata kaasa uute lähenemisviiside väljatöötamisele suunatud ravi jaoks.

Klõpsake, et näha cistanche tubulosa eeliseid ja kõrvaltoimeid ning neeruhaiguste korral
OSAKS KLIKI SIIAⅠ & Ⅲ
4. Membraanne nefropaatia
Membraanne nefropaatia(MN) on nefrootilise sündroomi (NS) peamine põhjus täiskasvanutel. Sellel haigusel on autoimmuunne iseloom, mida kinnitas podotsüütide antigeenide, sealhulgas fosfolipaasi A2 retseptorite (aPLA2R) ja trombospondiin 1 domeeni sisaldava 7A (THSD7A) vastaste autoantikehade olemasolu[97,98]. MN sekundaarsed põhjusedMembraanne nefropaatia) hõlmavad uimastitarbimist, infektsioone, autoimmuunhaigusi ja vähki [99]. MN esmane mehhanism(Membraanne nefropaatia)on podotsüütide autoimmuunne kahjustus fosfolipaasi A2 retseptori antikehade poolt, mis põhjustab massilist proteinuuriat. Selle haiguse diagnoosimine ja ravi põhineb praegu aPLA2R antikeha tiitri määramisel. Täiendavate markerite otsimine tundub paljutõotav aPLA2R-negatiivset tüüpi idiopaatilise MN puhul(Membraanne nefropaatia). MN(Membraanne nefropaatia)patsiendiuuringud pakuvad MN-i proteoomi võrdlevaid ristlõike analüüse(Membraanne nefropaatia)võrreldes teiste nefrootiliste nefriidi tüüpidega ja tervete kontrollidega. Spetsiifiliste uriinivalgu markerite paneel, mis eristab MN-i(Membraanne nefropaatia)teistest nefropaatiatest põhjustatud tsingi sõrmevalgu ZFPM2, E1A-d siduva valgu ja mikrotuubulitega seotud valgu tauAP-3 kompleksi subühiku delta-1 [54] taseme langus, samuti türoksiini siduva globuliini taseme tõus. (SERPINA7)[50], lüsosoomi membraanivalk-2(LIMP-2)[56], plasminogeen [54], LDB3, PDLI5 [100] ja afamiin [55,57]. APLA2R-positiivse MN-i ja APLA2R-negatiivse MN-ga patsientide ning tervete isikute proovide võrdlemine näitas, et positiivse MN-i rühmas on A1AT ja näljahäda oluliselt kõrgemad [101]. Uriini retinooli siduva valgu 4 ja SH3 domeeni siduva glutamiinhappe rikka valgu 3 kombinatsioon võib eristada MCD-d DN-st. Samamoodi võib uriini afamiini ja komplemendi C3 uriini/plasma suhte kombinatsioon MN-i eristada DN-st[55].

Üldiselt MN-st leitud markerid(Membraanne nefropaatia)mängivad rolli komplemendi aktiveerimise ja immuunvastuste, rakkude adhesiooni, retseptori vahendatud endotsütoosi, trombotsüütide degranulatsiooni ja hüübimiskaskaadi klassikalises rajas [57]. LIMP-2 mängib keskset rolli põletikulise immuunvastuse regulatsioonis neerukoes [56] ja peegeldab immuunrakkude infiltratsiooni kudedesse. LMP-2 võib samuti aidata määrata haiguse aktiivsust. LDB3 ja PDL5 valgud mängivad rolli podotsüütide tsütoskeleti modifikatsioonis, mis võib viia proteinuuria tekkeni. Afamin, mille tõus on seotud idiopaatilise MN-ga(Membraanne nefropaatia), on kõige lootustandvam spetsiifiline MN(Membraanne nefropaatia)marker, kuna selle olulisust kinnitasid mitmed uuringud (tabel 2).
Tabel 2. Potentsiaalsed uriini proteoomimarkerid erinevate nefropaatiate korral.
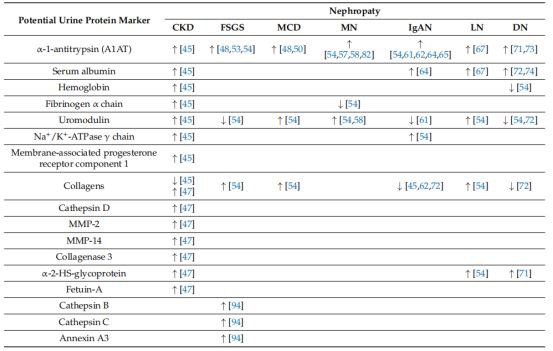
5. IgA nefropaatia
IgA nefropaatia(IgAN) on kroonilise glomerulaarhaiguse kõige levinum vorm täiskasvanutel. Euroopas on IgAN(IgA nefropaatia) ulatub 19–51 protsendini glomerulaarhaiguste korral tehtud neerubiopsiatest [102-104]. LgAN-iga patsientidel on sageli suurenenud IgA1 tase koos galaktoosipuudulike O-glükaanidega liigendpiirkonnas. Aberrantselt glükosüülitud IgA1 tase veres on kõrgem IgAN-is(IgA nefropaatia)kui tervetel kontrollidel või patsientidel, kellel on muudneeruhaigused. Näidati, et galaktoosipuudulike IgA1 antikehade tootmine, immuunkomplekside moodustumine ja nende komplekside kuhjumine mesangiumis põhjustavad neerukahjustusi [105]. Lisaks võimendas alternatiivsete komplemendi radade aktiveerimine koekahjustusi [106]. Transferriini retseptor (CD71) inimese mesangiaalrakkudel võib siduda immuunkomplekse, mis sisaldavad galaktoosipuudulikku IgA-d [107].
Umbes 40 uriinivalgu markerit, mis eristavad IgANIgA nefropaatia) have been described, >20 neist on spetsiifilised ainult lgAN jaoks (tabel 2). Komplemendi C9, Ig kappa ahela C piirkonna ja kolme tsütoskeleti keratiini (tüüp I (10) ja tüüp I (1 ja 5)) tasemed muutusid lgAN patsientide glomerulites (biopsiaproovis) sünkroonselt võrreldes terve neerukoega. kasvajatega patsientide alad [59]. IgAN-is tuvastati 30 uriinivalgu ja nelja potentsiaalse markeri (rakkudevaheline adhesioonimolekul 1 (ICAMl), metalloproteinaasi inhibiitor 1, antitrombiin IIl ja adiponektiin) muutunud tasemed.IgA nefropaatia) madala proteinuuriaga (<1 g/l)="" and="" stable="" renal="" function="" (glomerular="" filtration="" rate:57.3="" (23-106)ml/min).="" a="" larger="" multicenter="" study="" suggested="" that="" a="" decreased="" number="" of="" collagen="" fragments="" in="" the="" urine="" (specifically="" type="" i="" collagen)="" might="" be="" most="" informative="" in="" progressive="">IgA nefropaatia), mis on tingitud kollageeni vähenenud lagunemisest ja kollagenaasi inhibeerimisest neerufibroosi korral [62].

Teised potentsiaalsed lgAN-spetsiifilised markerid hõlmavad adiponektiini 60], 2-makroglobuliini, komplemendi C4a, protrombiini [63], antitrombiin II [60,63], -1B-glükoproteiini [64], glükoproteiini suurenenud taset. 2, epidermaalne kasvufaktor, CMRF35-sarnane molekul, protokadheriin, uteroglobiin, dipeptidüülpeptidaas IV, NHL-i kordusi sisaldav valk 3 ja CD84 [36] ning vähenenud fibuliini tase-5, YIP1 perekonnaliige 3 , pakkudes välja [108], aminopeptidaasi N [65] ja Pellini LG3 fragmenti [64]. Viimane oli ainus vähenenud valk raskemas IgAN-is(IgA nefropaatia)aeglasema glomerulaarfiltratsiooni kiirusega [64]. Samal ajal võivad kõrged LG3 tasemed pärssida angiogeneesi ja olla vastutavad neerufunktsiooni kaotuse eest mõnes teises IgAN-is(IgA nefropaatia)patsiendid [64]. Kuigi andmed vasoriini taseme muutuste kohta on vastuolulised [36,65], võib seda pidada ka spetsiifiliseks IgAN-iks(IgA nefropaatia)marker. Antitrombiin I on eriti tähelepanuväärne kui ainuke spetsiifiline IsAN-marker, mida kinnitati kahes sõltumatus uuringus [60,63].

6. Diabeetiline nefropaatia
Diabeetiline nefropaatia(DN) mõjutab umbes 30-40 protsenti suhkurtõvega (DM) patsientidest ja on kroonilise neeruhaiguse peamine põhjus.(Krooniline neeruhaigus)ja lõppstaadiumis neeruhaigus (ESRD) kogu maailmas, eriti kõrge ja keskmise sissetulekuga riikides. DN(Diabeetiline nefropaatia)viib glomerulaarse mesangiaalse laienemiseni; basaalmembraani paksenemine; ja iseloomulikult nodulaarse glomeruloskleroosi progresseerumine glomerulaarse hüperfiltratsiooni tõttu [109.
Potentsiaalse spetsiifilise DN(Diabeetiline nefropaatia) markers in the urine includes >10 valku (tabel 2), D-vitamiini siduva valgu suurenenud tasemega, kalgranuliin B, hemopeksiini [71l, tsink- 2-glükoproteiin [71,74], 408 N-seotud glükoproteiinid [73], tsüstatiin C, ubikvitiin, -1-happeline glükoproteiin 1, pigmendiepiteelist tuletatud faktor [74], Clara raku valk CC16 [76] ja fi-bronektiin [110], samuti transtüretiini [71,74] taseme langus ja erinevalt muutuv tase -1 mikroglobuliini/bikuniini prekursorist (AMBP) [71,74,75].
B-glükoproteiini (7- korda), tsinki sisaldava 2-glükoproteiini (59- korda), 2-HS-glükoproteiini (4{{) sisalduse märkimisväärne tõus uriinis 8}} korda), D-vitamiini siduvat valku (48- korda), kalgranuliin B(39- korda), A1AT(29- korda) ja hemopeksiin ( 2.4-kord) usaldusväärselt eristatav DN(Diabeetiline nefropaatia)DM makroalbuminuuriaga ilma albuminuuriata[71]. Seevastu transtüretiini (43- korda), apolipoproteiini A1 (32- korda), AMBP (16- korda) ja retinooli siduva plasmavalgu ( 1.{10}}korda) täheldati DN-is(Diabeetiline nefropaatia)makroalbuminuuriaga [71]. Valitud valkudega tehtud mudeluuring viitas katepsiin A, mutsiini 1, GM2 gangliosiidi aktivaatori, SPARC-sarnase valgu 1 ja lüsosomaalse happefosfataasi olulisusele DN varajase arengu halvas prognoosis.(Diabeetiline nefropaatia), samuti neerufibroosi korral [111]. Näidati, et 408 N-seotud glükoproteiini, A1AT ja tseruloplasmiini kombinatsioon suudab DN-is eristada mikroalbuminuuriat ja normoalbuminuuriat(Diabeetiline nefropaatia)patsiendid [73]. Uriini haptoglobiin ja AMBP võivad eristada diabeediga patsiente DN-ga ja ilma(Diabeetiline nefropaatia)[75]. Leiti, et 15,8 kDa Clara raku valgu CC16 suurenenud eritumine on seotud mikro- või makroalbuminuuriaga DM-i patsientidel proksimaalsete tuubulite düsfunktsiooniga võrreldes albuminuuriata ja tervete kontrollidega DM-i patsientidega [76]. Osteopontiini ja fibronektiini tase oli samuti kõrgem DN-is(Diabeetiline nefropaatia)võrreldes DM patsientidega ning pärast losartaanravi täheldati neerude neprilüsiini ja VCAM-i tõusu uriinis-1(Diabeetiline nefropaatia) [110].
2. tüüpi DM pikisuunaline uuring näitas transtüretiini/prealbumiini ja lg kappa C ahela piirkonna suurenemist uriinis 0-5 aasta jooksul alates DM algusest; tsüstatiin C ja ubikvitiini ilmumine 5-10 aasta pärast; ja -1-happe glükoproteiin 1, apolipoproteiin A1, AMBP, pigmendiepiteelist pärineva faktori ja tsingi -2-glükoproteiini tuvastamine 10-20 aasta pärast [74]. Nende valkude ja nende peptiidide mitteensümaatiline glükeerimine häirib normaalset tubulaarset reabsorptsiooni ja võib põhjustada proksimaalsete tuubulite kahjustusi ja valkude otsest eritumist uriiniga.
Üldiselt eelnimetatud DN(Diabeetiline nefropaatia)markerid võivad kajastada tubulaarse atroofia ja tubulointerstitsiaalse fibroosi protsesse, millest paljud on DN jaoks olulised(Diabeetiline nefropaatia)prognoos. Erilist tähelepanu tuleks pöörata tsingi- 2-glükoproteiinile, transtüretiinile ja AMBP-le, kuna nende prognostilist tähtsust kinnitati vähemalt kahes sõltumatus uuringus [71,74,75].
7. Luupusnefriit
Lupus nefriit(LN) on süsteemse erütematoosluupuse üks levinumaid ja raskemaid tüsistusi ning ilmneb tavaliselt vähemalt 3-5 aastat pärast haiguse algust. Neeru glomeruli kahjustuse mehhanisme võib leida immuunkomplekside või autoantikehade ladestumisest koos järgneva komplemendi aktivatsiooniga [112].LN(Lupus nefriit) põhjustab tõsist neerukahjustust, mis adekvaatse ravi puudumisel areneb lõppstaadiumis neeruhaiguseks. LN jaoks kõige olulisem eesmärk(Lupus nefriit)Ravi eesmärk on neerukahjustuse aktiivsuse dünaamiline hindamine, kuna olemasolevad aktiivsuse markerid (igapäevane proteinuuria, erütrotsütuuria, komplement ja tuumavastased antikehad) ei ole informatiivsed. LN(Lupus nefriit)patsiendid peavad praegu läbima mitu neerubiopsiat, et jälgida LN-i(Lupus nefriit)aktiivsus immunosupressiivse ravi ajal, et teha kindlaks, kus LN(Lupus nefriit)ravi tuleb jätkata või katkestada. Sel juhul on vaja ülitundlikku ja spetsiifilist LN-i(Lupus nefriit)markerid, mis suudavad ennustada haiguse ägenemist või näitavad ravi ebapiisavat efektiivsust.
Ainult mõned potentsiaalsed uriinivalgu markerid, mis on spetsiifilised LN-le(Lupus nefriit)võib märkida (tabel 2). Peptiidide paar "3340" ja "3980" (m/z) on võimaldanud eristada ägedat LN(Lupus nefriit)seisukord LN-st(Lupus nefriit)remissioon 92-protsendilise tundlikkusega ja 92-protsendilise spetsiifilisusega enne mis tahes muutusi kliinilistes parameetrites (uriini valgu/kreatiniini suhe, DNA-vastased antikehad, hematuuria, seerumi kreatiniinisisaldus jne). Lisaks suutsid need peptiidid ennustada varajast retsidiivi ja remissiooni [66].
Leiti, et teatud heptsidiini fragmendid koos A1AT ja albumiini fragmentidega on olulisemad kui süsteemse erütematoosluupuse neerude ägenemise tsükkel LN(Lupus nefriit)dünaamilises uuringus uriini proteoomi kohta [67l. Heptsidiin 20 muutunud ekspressioon võib olla neerude ägenemise marker, samas kui heptsidiin 25 suurenemist ravi ajal saab kasutada ravi efektiivsuse hindamiseks [67].
172 peptiidil põhinev klassifikaator eristas usaldusväärselt 92 LN(Lupus nefriit)üldisest kroonilise neeruhaiguse juhtudest(Krooniline neeruhaigus)rühma (1180 patsienti) ja tuvastas valgu S100-A9 teise spetsiifilise LN-na(Lupus nefriit)marker, mille suurenenud tase leiti olevat LN jaoks hädavajalik(Lupus nefriit)diferentseerumine kombinatsioonis kollageenpeptiidide ja uromoduliini suurenenud tasemega, samuti klastri, -2-mikroglobuliini ja -2-HS-glükoproteiini taseme langusega [54].
-1-Antihümotrüpsiin (SERPINA3) on veel üks potentsiaalne spetsiifiline LN(Lupus nefriit)marker uriinis ja ainus LN(Lupus nefriit)marker, mille olulisust kinnitati kahes sõltumatus uuringus [68,69]. Koos haptoglobiini ja retinooli siduva valguga suurenes SEPINA3 aktiivses LN-s märkimisväärselt(Lupus nefriit)võrreldes mitteaktiivse LN-ga(Lupus nefriit)[68]. Lisaks näitas SERPINA3 mõõdukalt positiivset korrelatsiooni LN-ga(Lupus nefriit)histoloogiline aktiivsus, mida kinnitati immunohistokeemia abil [69].
Üldiselt on kirjeldatud LN(Lupus nefriit)markerid võimaldavad hinnata haiguse aktiivsust ja fibroosi kuhjumist neerudesse, mis on kliinilises praktikas patsientide ravimisel väga olulised. Mõnede valkude suurenenud tase võib viidata tubulaarsele düsfunktsioonile haiguse ägeda vormi ajal [68].
8. Mittespetsiifilised uriinivalgu markerid
Uromoduliin, kollageenid, AlAT ja nende fragmendid on peamised mittespetsiifilised uriinivalgu markerid, mis tuvastati kõigi eelnimetatud nefropaatiate (tabel 2), aga ka paljude teiste neerufunktsiooni häire või proteinuuriaga seotud häirete korral [17-39] . Uromoduliin on neeruspetsiifiline glükosüülfosfatidüülinositooli (GPI) ankurdatud glükoproteiin, mida toodavad eranditult Henle ahela jämedat tõusvat haru vooderdavad epiteelirakud ja see on uriini normaalne komponent. Kollageeni peptiidid esinevad tavaliselt ka uriinis ja peegeldavad rakuvälise maatriksi käivet neerukudedes. Sellest hoolimata võivad mõlemad tavalised uriinikomponendid viidata patoloogilistele muutustele. Uromoduliin võib olla ka potentsiaalne biomarker, mis on oluline tubulaarse funktsiooni ja kroonilise neeruhaiguse jaoks(Krooniline neeruhaigus)[113]. Kollageeni fragmentide tase on tugevas korrelatsioonis DN initsiatsiooniga(Diabeetiline nefropaatia)[13,17,19,45,72]; kvantitatiivseid muutusi nendes fragmentides uriinis täheldati 3-5 aastat enne makroalbuminuuria tekkimist [19]. Üldiselt võib kollageenifragmentide kvalitatiivne koostis erinevate nefropaatiate korral erineda [45, 47, 54, 72].
Erinevalt uromoduliinist ja kollageenpeptiididest on AlAT ilmumine uriinis alati seotud teatud tüüpi patoloogiaga ja võib peegeldada podotsüütide stressi [53]. Eelkõige täheldati kõigi käesolevas uuringus vaadeldud nefropaatiate korral uriini AlAT suurenemist (tabel 2).
Üldiselt parandas mittespetsiifiliste markerite hindamine kombinatsioonis spetsiifiliste markeritega oluliselt nefropaatiate diferentseerumist. Eelkõige eristasid kuue UMOD ja A1AT peptiidi tasemed proliferatiivset ja mitteproliferatiivset (sealhulgas MCD, MN, FSGS ja IgAN(IgA nefropaatia)) glomerulaarsed vormidneeruhaigused[58]. Lisaks näitas uromoduliini üleekspressioon eelsoodumust krooniliste neeruhaiguste tekkeks(Krooniline neeruhaigus)nagu hüpertensiivne nefropaatia ja DN(Diabeetiline nefropaatia)[114]. Kollageeni fragmentide tuvastamine koos endorepelliini LG3 fragmendiga on IgAN diagnoosimisel ülioluline(IgA nefropaatia), kuna kollageen võib viidata raskemale haiguse kulgu, millega kaasneb angiogeneesi kahjustus ja neerufibroosi kiire areng [64]. A1AT, uromoduliini, transferriini, seerumi albumiini ja -1- -glükoproteiini taseme hindamine on samuti oluline lgAN-is, kuna sellised tasemed peegeldavad tavalisi patoloogilisi protsesse, sealhulgas suurenenud apoptoosi, põletikku, koagulatsiooni ja komplemendi aktivatsiooni [45,54, 61,62,64,65,72].
9. Järeldused
Uuringutulemused näitavad proteoomianalüüsi suurt potentsiaali mitteinvasiivse diagnoosimise jaoksneeruhaigused, haiguse progresseerumise juhtivate patogeneetiliste mehhanismide selgitamine ja haiguse progresseerumise pärssimise toime sihtmärkide kindlaksmääramine. Erinevalt neeru biopsiast on uriini proteoomiline analüüs ohutu ja usaldusväärne ning seda saab haiguse jälgimiseks mitu korda korrata. Proteoomiline uriiniprofiil annab väärtuslikku teavet juhtivate patoloogiliste protsesside kohta, mis esinevad neerukudedes uurimise ajal.
Proteoomianalüüsi põhijooneks on see, et paljusid uriinis tuvastatud markereid täheldatakse valgu tungimise tulemusena verest (albumiin, retinooli siduv valk jne) või tavaliste patoloogiliste protsesside, näiteks rakuvälise maatriksi akumulatsiooni peegeldusena. (kollageenid ja A1AT), immunoglobuliinikomplekside ladestumine, komplemendi aktivatsioon, apoptoos, lipiidide oksüdatsioon ja tubulaarne düsfunktsioon (-2-mikroglobuliin, uromoduliin jne) koos kõrge proteinuuriaga. Sel juhul on ülioluline hinnata nende näitajate kvantitatiivseid muutusi, et kajastada täpselt töötlemistegevust ja kahju tõsidust.
Uriini proteoomilise analüüsi üks olulisemaid eesmärke kroonilise neeruhaigusega patsientidel(Krooniline neeruhaigus)on haigusspetsiifiliste biomarkerite või nende kombinatsioonide määramine. Esmakordselt ekstraheeritud valgud nõuavad kõige rohkem tähelepanu, kuna need võivad kajastada haiguse arengu kõige olulisemaid patogeneetilisi etappe. Näiteks CD44, aktiveeritud parietaalsete epiteelirakkude marker, võib peegeldada glomeruloskleroosi protsesse MN[50] või IgAN-is.(IgA nefropaatia)[38], kuid samal ajal võib see olla ka oluline tunnus FSGS-i eristamisel MCD-st [52]. Arvatakse, et peamiselt FSGS-is tuvastatud DPEP1 peegeldab TRPC6 aktivatsiooni podotsüütides [52]; ubikvitiini -60S ribosomaalne valk L40 (UBA52), mis on rakulise stressi marker; või podotsüütide tsütoskeleti komponendid, mis on kahjustatud antikehade poolt [49,115]. Apolipoproteiinid, mis võivad mängida potentsiaalset rolli FSGS patogeneesis kui "läbilaskvusfaktorid"]116l, samuti valgud, mille rollid pole veel täielikult teada, nagu lüsosoomi membraanivalk{11}} ja afamiin MN-s[56,57] ja laminiin G-sarnane 3(LG3) fragment toetab Pellinit IgAN-is(IgA nefropaatia)[64], võivad kajastada patoloogilisi protsesse ja võivad olla immunosupressiivse või nefroprotektiivse ravi uute lähenemisviiside sihtmärgid. Lisaks võivad proteoomilise profiili positiivsed dünaamilised muutused pärast määratud ravi aidata kinnitada, kas määratud ravimid valiti õigesti ja kas need aitavad saavutada soovitud tulemusi. Vaatamata CKD valideerimisele(Krooniline neeruhaigus)273 klassifikaatorit mitmes uuringus, on vaja edasi arendada uusi paneele, mis on spetsiifiliste nefropaatiate suhtes spetsiifilisemad. See näib olevat edasiste proteoomikauuringute kõige olulisem eesmärk.
Viited
1. NeeruhaigusGlobaalsete tulemuste parandamine (KDIGO).KDIGO kliinilise praktika juhis glomerulonefriidi korral;NeerRahvusvahelised toidulisandid; Nature Publishing Group: New York, NY, USA, 2012.
2. National Kidney Foundation.K/DOQI kliinilise praktika juhisedkrooniline neeruhaigus: hindamine, klassifitseerimine ja kihistamine. Olen. J. Kidney Dis.2002, 39, 1-266.
3.Sarnak, MJ;Levey, AS;Schoolwerth, AC;Coresh, J;Culleton,B.; Hamm, LL; McCullough, PA; Kasiske, BL; Kelepouris, E.; Kag, MJ; et al.Neeruhaiguskui südame-veresoonkonna haiguste arengu riskitegur. Tiraaž 2003, 108, 2154-2169. [CrossRef] [PubMed]
4. Alani, H: Tamimi, A.; Tamimi, N.Kardiovaskulaarne kaashaigestumine inkrooniline neeruhaigus: Praegused teadmised ja tulevased uurimisvajadused. World J. Nephrol.2014, 3, 156-168. [CrossRef] [PubMed]
5. Hsu, C; Ordonez, J: Chertow, G.; Fan, D.; McCulloch, C.; Go, A. Ägeda neerupuudulikkuse risk patsientidelkrooniline neeruhaigus. Kidney Int.2008, 74, 101-107. [CrossRef] [PubMed]
6. Tonelli, M.; Wiebe, N.; Culleton, B.; House, A.; Rabbat, C.; Fok, M.; McAlister, F; Garg, AXKrooniline neeruhaigusja suremusrisk: süstemaatiline ülevaade. J. Am. Soc. Nephrol.2006, 17, 2034-2047. [CrossRef]
7. Hsu. C.-Y: Iribarren, C; McCulloch, CE; Darbinian, J.; Mine, ASRisk Factors for End-StageNeerudHaigus: 25-aasta järelkontroll. Arch. Intern. Med. 2009, 169, 342-350. [CrossRef]
8. Hill, NR; Fatoba, ST; Okei, JL; Hirst, J.; O'Callaghan, CA; Lasserson, D.; Hobbs, R. Ülemaailmne levimusKrooniline neeruhaigus— Süstemaatiline ülevaade ja metaanalüüs. PLoS ONE 2016, 11, e0158765. [CrossRef]
9, Schieppati, A.; Remuzzi, G. Kroonilised neeruhaigused kui rahvatervise probleem: epidemioloogia, sotsiaalsed ja majanduslikud tagajärjed. Kidney Int.2005, 68, S7-S10. [CrossRef]
10. Bommer, J. Levimus ja sotsiaal-majanduslikud aspektidkrooniline neeruhaigus. Nephrol.Vali. Transplant.2002, 17,8-12.[CrossRef]
11. Vos, T.; Allen, C.; Arora, M; Juuksur, RM; Bhutta, ZA; Brown, A.; Carter, A.; Casey, DC; Charlson, FJ.; Chen, AZ; et al. Ülemaailmne, piirkondlik ja riiklik esinemissagedus, levimus ja puudega elatud aastad 310 haiguse ja vigastuse korral, 1990-2015: A systematic analysis for the Global Burden of Disease Study 2015.Lancet 2015, 388, 1545-1602. [CrossRef]
12. Dhaun, N.; Bellamy, CO; Cattran, DC; Kluth, DCU Neerubiopsia kasutatavus kliinilises juhtimisesneeruhaigus. NeerInt. 2014, 85, 1039-1048. [CrossRef] [PubMed]
