Uuring tõhusa loodusliku aine valmistamise kohta, mis põhineb Schisandra Chinensis ekstraheeritud fermentatsioonil
Apr 14, 2023
Eesmärk:Selles uuringus kasutati kosmeetikatoodete valmistamisel antioksüdantmaterjalina tõhusate mikroorganismide (EM) kääritamisel toodetud kõrge efektiivsusega Schisandra chinensise ekstrakti (SCE).
Asjakohaste uuringute kohaseltcistancheon tavaline ravimtaim, mida tuntakse kui "imerohi, mis pikendab eluiga". Selle põhikomponent ontsistanosiid, millel on erinevad mõjud naguantioksüdant, põletikuvastane,jaimmuunfunktsiooni edendamine. Tsistanche ja naha valgendamise vaheline mehhanism seisneb selle antioksüdantses toimescistancheglükosiidid. Inimese nahas sisalduv melaniini toodetakse türosiini oksüdeerumisel, mida katalüüsibtürosinaas, ja oksüdatsioonireaktsioon nõuab hapniku osalemist, seega muutuvad keha hapnikuvabad radikaalid oluliseks melaniini tootmist mõjutavaks teguriks. Tistanche sisaldab tsistanosiidi, mis on antioksüdant ja võib vähendada vabade radikaalide teket organismis, seegamelaniini tootmise pärssimine.

Klõpsake valikul Kust saab Cistanche'i osta
Lisateabe saamiseks:
david.deng@wecistanche.com WhatApp:86 13632399501

Sissejuhatus
Viimastel aastatel on paranemine ja kõrge elatustaseme poole püüdlemine tekitanud palju inimeste tervist mõjutavaid probleeme. Nende hulgas on kosmeetikatooted eriline näide, mida tuleb hoolikalt uurida. Sünteetiliste kemikaalide kasutamine kosmeetikatoodete peamise koostisosana toob kaasa palju negatiivseid tulemusi, nagu toksilisus ja kõrge hind. See on põhjus, miks kosmeetikatoodetes kasutatavate looduslike toodete uurimine on äratanud paljude teadlaste suurt huvi. Schisandra chinensis (SC) on ravim- ja söödav taim, millel on viis maitset (magus, hapu, mõru, soolane ja terav)1,2 ning mida kasutatakse laialdaselt paljudes toiduainetes, jookides ja ürditööstuses jne.3,4 SC sisaldab palju bioaktiivseid ühendeid, nagu domeen, õunhape ja sidrunhape, ning seda saab tõhusalt kasutada köha ja astma raviks.5 Lisaks saab seda kasutada toiduaine- ja kosmeetikatööstuses tänu oma tuntud antibakteriaalsetele ja sidrunhapetele. antioksüdantsed võimed. Lisaks on sellel suurepärane kuumusstabiilsus ning seda saab kasutada kosmeetikatoodetes ja toiduainetes, mis ei mõjuta inimeste tervist.6 Käärimine viitab orgaanilise materjali lagunemisprotsessile mikroorganismide ensüümide abil ja on tuletatud ladinakeelsest sõnast fervent. 7 Seda on kasutatud mitmel viisil ja erinevates valdkondades, nagu toit, ravimid ja kosmeetika.7 Toidu fermentatsiooni mikroorganismide ensümaatilise toime kaudu kasutatakse traditsiooniliselt tootmisprotsessides maitse parandamiseks ja toksiinide hävitamiseks ning sellel on ka soodustav toime. biomolekulid.8,9 Efektiivsed mikroorganismid (EM) on kasulikud mikroorganismid, mis töötati välja 1982. aastal.10 EM töötati algselt välja kasutamiseks looduslikus ja mahepõllumajanduses. Hiljem on selle kohaldamisala järk-järgult laienenud ja seda kasutatakse laialdaselt Aasia riikides, Venemaal ja USA-s.11 Esialgu töötati EM-i lahendus välja 80 liigist 10 perekonnast 5 perekonnas; see oli aga väga keeruline protsess. Seetõttu arendasid EM-i lihtsalt mõned peamised organismid, nagu fotosünteesivad bakterid, piimhappebakterid, seened, pärm ja aktinomütseedid.12 Mis puutub fermentatsioonirakendusse, siis seda fermenteeritakse fakultatiivsetes anaeroobsetes tingimustes, seega on selle sünteesiproduktid, nagu vitamiin. ja karoteen pigmendid võimsate antioksüdantidena, et vältida orgaanilise materjali lagunemist.13 Saadud aminohapped ja orgaanilised happed muudetakse vastavateks valkudeks ja suhkruteks ning imenduvad seejärel kohe taime poolt. See parandab oluliselt nii taimse toidu sünteesi kui ka kasutamise efektiivsust. EM töötati algselt välja kasutamiseks looduslikus mahepõllumajanduses, kuid tänapäeval kasutatakse seda paljudes valdkondades, nagu ehitus-, meditsiini- ja kosmeetikatööstus.14–16

Materjalid ja meetodid
Materjalid
SC ekstraheerimine
Erinevate ekstraktikontsentratsioonide valmistamine
Mikroelementide analüüs
Toidukoodeksi meetodil lahustati {{0}},0 g proovi 100 ml lämmastikhappes 100 kraadise DI veega. Seejärel mõõdeti proovis olevate mikroelementide kogused ja analüüsiti neid elementanalüsaatoriga (Vario EL, Saksamaa).

Polüfenoolisisalduse mõõtmine
Polüfenoolide sisaldust proovi grammi kohta mõõdeti Folin-Denise meetodil.18 Nii segati EP katseklaasis 100 µl ekstrakti ja 2 massiprotsenti Na2CO3. EP-toru hoiti reaktsiooni jaoks 2 minutit toatemperatuuril. Pärast seda lisati tuubi 50 protsenti Folin-Ciocalteu fenoolreaktiivi. Proov pandi 30 minutiks toatemperatuuril keerismikserisse ja seejärel analüüsiti UV-Vis spektrofotomeetriga 750 nm juures.
Flavonoidide mõõtmine
Flavonoidide kogusisaldust ühe grammi ekstrakti kohta mõõdeti dietüleenglükooli kolorimeetria abil.19 Seega lisati EP katseklaasi 100 μL ekstrakti ja 100 μL 1,0 N NaOH-d ning segati vortex mikser. Pärast segamist hoiti lahust reaktsiooni ajaks 30 kraadi juures 1,0 tundi. Reaktsiooni saagist analüüsiti UV-Vis spektrofotomeetriga 420 nm juures.
Vabade radikaalide eemaldamise mõõtmine
Vabade radikaalide eemaldamist 1,1-difenüül-2-pikrüülhüdrasüüli (DPPH) abil mõõdeti modifitseeritud Bloisi meetodil.20 Selles kontekstis kasutati 0,1 M Trizma alus-HCl puhvrit (Tris). puhver, pH 7,4) ja 500 mM DPPH valmistati algselt metanooliga. Kontrollkatse standarditeks valiti butüülitud hüdroksütolueen (BHT) ja butüülitud hüdroksüanisool (BHA). Seejärel segati EP katseklaasis 100 μL ekstraktiproove ja 400 μL Tris puhvrit, millele järgnes 500 μL DPPH lahuse lisamine. Segu hoiti 20 minutit pimedas ruumis, seejärel analüüsiti UV-Vis spektrofotomeetriga 517 nm juures. Kontrollkatses lisati ekstraktiproovide asemel 100 µl BHT-d ja BHA-d. Lisanditeta rühmas lisati EP katseklaasi ekstraktiproovide asemel 100 μl Tris puhvrit. Elektronide loovutamise võime mõõtmine on näidatud järgmiselt:21

Nitritite eemaldamise aktiivsuse mõõtmine
Nitritite eemaldamise aktiivsust mõõdeti Kim jt poolt välja töötatud modifitseeritud meetodil.22,23 Täpsemalt 0,3 ml ekstraheeritud proovi ja 0,1 ml 1.0 mM NaNO2 lahus, 0,2 M tsitraatpuhver-HCl pH 2,5 juures segati, et saada lõppmahuks 1.0 ml. Seejärel lasti segul reageerida 37 kraadi juures 1.0 h. Seejärel segati see 0,4 ml Griessi reagendiga (30% CH3COOH lahus, mis sisaldas sulfaniilhapet (1 0 massiprotsenti): naftüülamiin (1 massiprotsent)) ja 3 0 ml CH3COOH lahust (2,0 massiprotsenti). Seejärel toimus reaktsioon toatemperatuuril 15 minutit.
![]()
Superoksiidi dismutaasitaolise aktiivsuse (SODA) mõõtmine

Türosinaasi inhibeeriva aktiivsuse mõõtmine
Türosinaasi inhibeerivat aktiivsust mõõdeti Masamoto jt esitatud meetodi modifitseeritud versiooniga.25 Seene türosinaasi deaktiveerivate omaduste mõõtmiseks in vitro tingimustes 0,3 ml 2,5 mM 3,4 dihüdroksüfenüülalaniini (L-DOPA) ), {{10}}.{{20}}5 ml ekstraheeritud proovi ja 0,1 M fosfaatpuhverlahust (pH 6,8, kogumaht 1,5 ml) segati keerise abil mikseris ja seejärel eelinkubeeriti 25 kraadi juures. Seejärel lisati 0,05 ml seene türosinaasi 1380 ühikut · ml-1 (Sigma Co., USA) ja segati keerismikseri abil. Seejärel viidi reaktsioon läbi 25 kraadi juures 2,0 minutit.

kus A on reaktsioonilahuse neeldumisväärtus vahemikus {{0}},5 kuni 1 min ilma proovita, mõõdetuna lainepikkusel 475 nm UV-Vis spektrofotomeetriga; ja B on prooviga reaktsioonilahuse neeldumisväärtus vahemikus 0,5 kuni 1,0 min, mõõdetuna lainepikkusel 475 nm UV-Vis spektrofotomeetriga.
Kreemi materjali ettevalmistamine
Destilleeritud vee, ekstraheeritud õli ja lisandite baasil valmistatud koorevalemid valmistati vastavalt tabelis 1 toodud loetelule. Vesi, lisandid ja õli kaaluti ja kuumutati seejärel 80 kraadini veevannis. Lisati aeglaselt vesi ja segati minimikseris (DS-1800; Korea) jõuliselt õliga. Kreem A valmistati ilma ekstraheeritud õlita. Kreemid B, C, D, E ja F sisaldasid vastavalt 1, 5, 10, 20 ja 40 mg·mL−1 SC ekstrakti (SCE). Kreemid G, H, I, J ja K sisaldasid 1, 5, 10, 20 ja 40 mg·mL-1 SCE fermentatsiooni (SCEF).

Ohutuse hindamine
Stabiilsuse hindamine


Tulemused ja arutlus
Mikroelementide analüüs
SCE induktiivsidestatud plasma massispektromeetria (ICP) analüüsi tulemused on toodud tabelis 2, mis näitab, et 1.0 mg·mL−1 SCE-st sisaldab 23,71, 0,42 ja 0.03 mg·kg−1 K, Fe ja Se vastavalt. Kui SCE kogus suurenes, suurenes nende mikroelementide sisaldus. Sellega seoses oli K suurenemine domineeriv ning Mn, Fe, Cu ja Zn suurenemine ei olnud märkimisväärne. Se sisaldus jäi samaks, sõltumata SCE kontsentratsioonist. Need mikroelemendid aitavad kaasa paljude füsioloogiliselt aktiivsete ainete toimele nii inimkeha sees kui ka väljaspool ning täidavad olulisi rolle, sealhulgas antioksüdeerivaid ja immuunsust tugevdavaid ülesandeid.
Ekstrakti ja selle flavonoidide ja polüfenoolide sisalduse mõõtmine
SCE sisaldus oli 27,91 massiprotsenti 100 g SC-s. Ekstraheerimine andis sama saagise, kui protseduur viidi läbi vees ja etanoolis. Ekstrakti saagis oli aga väiksem kui varasemates töödes.26,27 Selle põhjuseks on erinevused nii SC kasvukohtades kui ka kultiveerimistingimustes ja ekstraheerimismeetodis.26 Polüfenoolide sisaldus on on näidatud tabelis 3. Tavalise SCE ekstrakt 1.0 mg·mL−1 andis 1,53±0.02 mg·g−1 polüfenooli, samas koguses sama palju EM SCEF andis kõrgema polüfenoolisisalduse (20,84±0,04 mg·g−1) kui fermenteerimata ekstrakt. EM SCEF ekstraheerimise tulemused 5, 10, 20 ja 40 mg·mL-1 olid vastavalt 25,82±0,04, 29,13±0,05, 42,07±0,05 ja 59,22±0,09 mg·g-1.

Vabade radikaalide eemaldamise mõõtmine
Vabad radikaalid kehas võivad soodustada bioloogilist vananemist, reageerides lipiidide ja valkudega. Selle nähtuse kõrvaldamiseks on paljudes uuringutes uuritud looduslikke tooteid.31 DPPH radikaali püüdmise katsemeetodit kasutatakse paljudes looduslikes toodetes antioksüdantide mõõtmiseks, kasutades antioksüdantide elektrondoonorvõimet.32–34 Antioksüdantsete mõjude tulemused SCE-s ja EM SCEF rühmad on näidatud joonisel 1. SCE DPPH radikaali püüdmise võime puhul, kuna kontsentratsioon varieerus vahemikus 1.0, 10 kuni 40 mg·mL-1, antioksüdantide võime suurenes 37 protsendilt 72 protsendilt 74 protsendile. EM SCEF rühm näitas 63 protsenti, 67 protsenti ja 79 protsenti antioksüdantset võimet vastavatel kontsentratsioonidel 1,0, 10 ja 40 mg·mL-1. EM SCEF-i rühmas näib väike muutus antioksüdantide võimes koos kontsentratsiooniga olevat tingitud EM SCEF-i ja mikroobide vahelisest reaktsioonist antioksüdantsete ainete tootmiseks. SC antioksüdantset võimet võrreldi mõnede tuntud antioksüdantidega, nagu BHT (89 protsenti) ja BHA (88 protsenti). Leiti, et SC vabade radikaalide eemaldamise võime ei erinenud palju nende omast. Lisaks on SCEF-il suurem radikaalide eemaldamise võime kui SCE-l isegi madalate kontsentratsioonide korral. See tähendab, et kui SC ja EM aktiivlahused reageerisid üksteisega, tekitasid mikroobid füsioloogiliselt aktiivseid materjale, millel on antioksüdantne võime. Seetõttu on võimalik toota materjale, mis sisaldavad kõrgemaid antioksüdante ja mille EM SCEF on väiksem kui SCE. Jõudsime järeldusele, et see võib lahendada doseerimisprobleemi kosmeetikatoodete valmistamisel ja samal ajal parandada taimedest saadud looduslikke aineid sisaldavate kosmeetikatoodete funktsionaalseid aspekte.

Nitritite eemaldamise aktiivsuse mõõtmine
Nitrit reageerib sekundaarse amiiniga (keemiline ühend, milles kaks ammoniaagi vesinikuaatomit on asendatud süsivesiniku funktsionaalrühmaga R), tekitades kurikuulsa kantserogeeni nitrosamiini; teisisõnu toimib nitrit nitrosamiini eelkäijana. Seetõttu saab nitrosamiini moodustumist tõhusalt pärssida nitraadi eemaldamisega.35 Kui analüüsitava proovi ja nitriti vaheline reaktsioonivõime on kõrge, eemaldatakse nitrit, kuna see reageerib ioniseeritud olekus, mis põhjustab nitrosamiini moodustumise pärssimist. See kehtib võrdselt ka muude ioonide või elektronidena esinevate ainete kohta ning proovi kõrge reaktsioonivõime on samaväärne nitritite sidumise ja antioksüdatsiooni kõrge aktiivsusega või seda hinnatakse kui kõrget aktiivsust. Mida suurem on kogu fenoolühendite kogus proovis, seda võimsam on nitritite sidumise reaktsioon madalamas pH vahemikus ja negatiivselt langeb eemaldav toime ülemises pH vahemikus.36 Tabelist 5 on näha, et nitritite eemaldamise aktiivsus. SCE oli 15 protsenti 1 mg·mL-1, 40 protsenti 10 mg·mL-1 ja 89 protsenti 40 mg·mL-1 juures. Teisest küljest näitas SCEF nitritite eemaldamise aktiivsust 1 mg·mL-1 juures 51 protsenti, 10 mg·mL-1 juures 69 protsenti ja 40 mg·mL-1 juures 98 protsenti. Sellest testist ilmnes, et kui mõlema rühma kontsentratsioon suurenes, suurenes ka eemaldamisaktiivsus. Lisaks oli SCEF oma nitritite eemaldamise aktiivsuse poolest SC-st parem, mis on sarnane muude katsetulemustega. Kontsentratsioonil 1,0 mg·mL-1 oli eemaldamisaktiivsuse erinevus 40 mg·mL-1, mis on erinevate kontsentratsioonide seas suurim, ja vahe vähenes kontsentratsiooni kasvades. Sellest võrdlevast katsest paranes EM-kääritamisprotsessi kaudu SC nitritit eemaldav toime, mis hinnati üsna heaks. Seda nähtust võib seostada käärimisprotsessiga, mille käigus tekib rohkem bioloogiliselt aktiivseid aineid, mis omakorda tõi kaasa nitrosamiinide moodustumise pärssimise suurenemise, aga ka paljude fenoolide kui toortaimsete koostisosade tekke, aidates kaasa ka tõhusale nitritite eemaldamise reaktsioonile. .


SODA mõõtmine
SOD on ensümaatiline antioksüdant, mis võib detoksifitseerida ja pärssida O2, H2O2, peroksiidi, OH radikaalide jne toksilisust.37,38 SODA on näidatud tabelis 6 SCE (või SCEF) kontsentratsiooni 1 korral.0, 1 0 ja 40 mg·mL-1. SCE rühmas oli SODA 6 protsenti, 18 protsenti ja 41 protsenti, samas kui EM SCEF rühmas oli SODA 28 protsenti, 32 protsenti ja 43 protsenti, kui kontsentratsioon tõusis 1-lt 40 mg·mL-1-le. Kahe rühma aktiivsuse erinevuse analüüsimiseks oli SODA väärtuse erinevus suurem SCE ja SCEF madala kontsentratsiooni korral (1,0 mg · ml–1) ja väiksem kõrge kontsentratsiooni korral (40 mg · ml–1). Selles testis oli mõlemal rühmal silmapaistev SODA tase.26,39 Seetõttu võib järeldada, et nii SCE-l kui ka SCEF-il on kõrge looduslikult pärinev antioksüdantne võime.
Türosinaasi inhibeeriva aktiivsuse mõõtmine
Türosinaasi inhibeeriva toime mehhanism on kosmeetikatööstuses väga oluline ja seda saab kasutada nahka valgendava toime mõõtmiseks.40 SCE rühmas suurenes türosinaasi inhibeeriv aktiivsus 35 protsendilt 36 protsendile, 37 protsendile, 38 protsendile ja 39 protsenti, kuna ekstrakti kontsentratsioon suurenes (tabel 7). EM SCEF rühmas suurenes türosinaasi inhibeeriv aktiivsus kontsentratsiooni suurenemisel 38 protsendilt 39 protsendile, 40 protsendile, 41 protsendile ja 42 protsendile. EM SCEF-il oli tõhusam türosinaasi inhibeeriv toime kui tavalisel ekstraktil, kuid erinevusi ei olnud palju. Siiski arvatakse, et mõlemal ekstraktil on kosmeetikatoodete valmistamisel nahka valgendav toime.41


Ohutuse hindamine
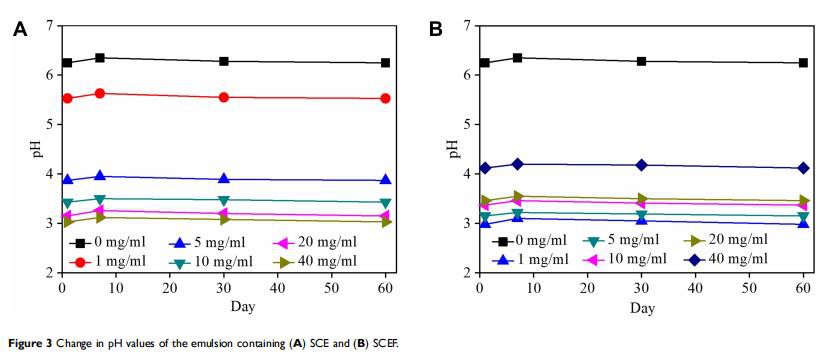
Erinevate SCE ja EM SCEF-i kontsentratsioonidega kosmeetikatoodete valemid, st {{0}}.0, 1.0, 5.0, 1{{ 25}}, 20 ja 40 mg·mL−1, on näidatud joonisel 2. Valmistatud kosmeetika valmistati W/O annustamisvormina, lisades õlifaasile vesifaasi . Inimese naha pinna pH on üldiselt vahemikus 4,5–6,5, mis on kas kergelt happeline või neutraalne.42 Kui pH muutub aluseliseks, siis naha vastupanuvõime nõrgeneb, mis viib mikroobide levikuni ja lõpuks nahahaigusteni. Seetõttu on väga soovitatav kasutada neutraalseid või kergelt happelisi kosmeetikatooteid. PH väärtuse muutus koos säilitusajaga on näidatud joonisel 3. Ilma SCEta kreemi kasutamisel tõusis pH 60 päeva pärast veidi 6,23-ni võrreldes algväärtusega 6,25. Kreemitoodetel, mille SCE kontsentratsioonid olid 1,0, 5,0, 10, 20 ja 40 mg·mL−1, olid esialgsed pH väärtused vastavalt 5,53, 3,87, 3,43, 3,15 ja 3,03. Need pH väärtused ei muutunud 60 päeva pärast. EM SCEF-põhistel kreemidel, mille EM SCEF kontsentratsioonid olid 1,0, 5,0, 10, 20 ja 40 mg·mL−1, olid esialgsed pH väärtused vastavalt 4,12, 3,46, 3,37, 3,15 ja 2,98. Sarnaseid pH väärtusi täheldati 60 päeva pärast. Need tulemused tähendavad, et kummaski rühmas ei olnud olulist erinevust pH muutuses ja kui ekstrakti kontsentratsioon tõusis, pH väärtus langes. Need tulemused viitavad sellele, et nende kosmeetikatoodete kasutamisel ei esinenud ohutusprobleeme.
Temperatuuri mõju kosmeetilisele stabiilsusele

Järeldus

Tunnustus
Avalikustamine
Viited
1. Choi BR, Kim HK, Park JK. Schisandra chinensise puuviljaekstrakti ja domeeni A mõju peenise corpus cavernosumi silelihaste kontraktiilsusele: potentsiaalne mehhanism lämmastikoksiidi - tsüklilise guanosiinmonofosfaadi raja kaudu. Nutr Res Pract. 2018;12 (4): 291–297. doi:10.4162/nrp.2018.12.4.291
2. He JL, Zhou ZW, Yin JJ, He CQ, Zhou SF, Yu Y. Schisandra chinensis reguleerib ravimeid metaboliseerivaid ensüüme ja ravimitransportereid, aktiveerides Nrf{6}} vahendatud signaaliraja. Drug Des Devel Ther. 2015;9:127–146.
3. Nowak A, Szyda MZ, Błasiak J, Nowak A, Zhang Z, Zhang B. Schisandra chinensis (Turcz.) Bailli potentsiaal. Inimese tervises ja toitumises: ülevaade praegustest teadmistest ja terapeutilistest perspektiividest. Toitained. 2019;11(2):333. doi:10.3390/nu1102 0333
4. Ramanathan L, Das NP. Uuringud põhjakala lipiidide oksüdatsiooni kontrollimise kohta mõnede polüfenoolsete looduslike saaduste abil. J Agric Food Chem. 1992;40(1):17–21. doi:10.1021/jf00013a004
5. Yang S, Yuan C. Schisandra chinensis: selle fütokemikaalide ja bioloogilise tegevuse põhjalik ülevaade. Arab J Chem. 2021;14 (9):103310. doi:10.1016/j.arabjc.2021.103310
6. Cho EG, Cho HI, Choi YJ. Kääritatud Omija (Schizandra chinensis Baillon.) joogil on antioksüdantne ja antibakteriaalne toime ning türosinaasi ja elastaasi pärssiv toime. J Appl Biol Chem. 2010;53(4):212–221. doi:10.3839/jabc.2010.038
7. Park SJ, Seong DH, Park DS jt. Kääritatud Codonopsis lanceolata keemilised koostised. J Korea Soc Food Sci Nutr. 2009;38(3):396–400. doi:10.3746/jkfn.2009.38.3.396
8. Dimidi E, Cox SR, Rossi M, Whelan K. Fermenteeritud toidud: määratlused ja omadused, mõju soolestiku mikrobiootale ning mõju seedetrakti tervisele ja haigustele. Toitained. 2019;11(8):1806. doi:10.3390/nu11081806
9. Kuu SH, Chang HC. Riisikliide kääritamine, kasutades starterina Lactiplantibacillus plantarum EM-i ja kääritatud riisikliide potentsiaali funktsionaalse toiduna. Toiduained. 2021;10(5):978. doi:10.3390/foods10050978
10. Katina K, Liukkonen KH, Kaukovirta A, Adlercreutz H, Heinonen SM, Lampi AM. Fermentatsioonist tingitud muutused idandatud rukki toiteväärtuses. J Cereal Sci. 2007;46 (3):348–355. doi:10.1016/j.jcs.2007.07.006
11. Foolad N, Brezinski EA, Chase EP, Armstrong AW. Toitainete lisamise mõju atoopilisele dermatiidile lastel. Arch Dermatol. 2012;17:E1–E6.
12. Olle M, Williams IH. Tõhusad mikroorganismid ja nende mõju köögiviljakasvatusele – ülevaade. J Hortic Sci Biotechnol. 2031;88 (4):380–386. doi:10.1080/14620316.2013.11512979
13. Uma MN, Abirami R. Ülevaade tõhusatest mikroorganismidest ja nende rakendustest. AJMR. 2019;8(4):121–129. doi:10.5958/2278-4853.20 19.00142.3
14. Bzdyk RM, Olchowik J, Studnicki M jt. Efektiivsete mikroorganismide (EM) ning orgaaniliste ja mineraalväetiste mõju Fagus sylvatica ja Quercus robur seemikute kasvule ja mükoriisa koloniseerimisele paljasjuurelise puukooli katses. Metsad. 2018;9(10):597. doi: 10.3390/f9100597
15. Chui CH, Cheng GYM. Efektiivse mikroorganismi fermentatsiooniekstrakti (EM-X) kasvu inhibeeriv potentsiaal vähirakkudel. Int J Mol Med. 2004;14:925–929.
16. Chui CH, Hau DKP. Kontsentreeritud tõhusa mikroorganismide fermentatsiooniekstrakti apoptootiline potentsiaal inimese vähirakkudel. Int J Mol Med. 2006;17:279–284.
17. Vajutage minu oma. Viige läbi laboratoorsed testid vastavalt toidukoodeksi spetsifikatsioonidele ja katsemeetoditele. Toit ja haldus; 2003:887–892.
18. Latimer GW. AOAC Internationali ametlikud analüüsimeetodid. 21. väljaanne Kõva köide; 2019
19. Kim JH. Astragaluse membraansete ekstraktide bioloogilise aktiivsuse uuringud. Biomed Sci Lett. 2012;18(1):35–41.
20. Blois MS. Antioksüdantide määramine stabiilse vaba radikaali abil. Loodus. 1958;26(4617):1199–1200. doi: 10.1038/1811199a0
21. Ahn YH, Yoo JS, Kim SH. Antioksüdandi võimekuse test, kasutades polüvinüülalkoholipõhist DPPH pelletit. Bull Korean Chem Soc. 2010;31(9):2557–2560. doi:10.5012/bkcs.2010.31.9.2557
22. Kim BJ, Park YK, Kang BS. Rubifructuse mõju munasarjadele ja rottide munasarjadele. Korea J Herb. 2001;16:139–152.
23. Grey JI, Dugan JRL. N-nitrosamiini moodustumise pärssimine mudeltoidusüsteemis. J Food Sci. 1975;40(5):981–985. doi:10.1111/j.{9}}.1975.tb02248.x
24. Marklund S, Marklund G. Superoksiidi kui aminoradikaali kaasamine pürogallooli oksüdatsiooni ja mugav test superoksiidi dismutaasile. Eur J Biochem. 1975;47:468–474.
25. Masamoto YH, Ando Y, Murata Y, Shiraishi M, Tada K, Takahata K. Euphorbia lathyris L. seemnetest eraldatud esculetiini seente türosinaasi inhibeeriv aktiivsus. Biosci Biotechnol Biochem. 2003;67(3):631–634. doi: 10.1271/bbb.67.631
26. Kwon HJ, Park CS. Omija ekstraktide bioloogiline aktiivsus. Korea J toidukonserv. 2008;15:587–592.
27. Shin HO. Puhastatud polüfenooli füsioloogilise toime ja mitmekordse emulgeerimise arengu uuringud. Gyeongbuk, Korea: Cosmeceutical Science Graduate School, Daegu Haany Ülikool; 2009.
28. Markris DP, Rossiter JT. Kvertsetiini ja mitte-orto-hüdroksüflavonooli kui antioksüdantide võrdlus konkureerivate in vitro oksüdatsioonireaktsioonide abil. J Agric Food Chem. 2001;49(7):3370–3377. doi:10.1021/jf010107l
29. An BJ, Park TS, Lee JY jt. Kiiritatud rohelise tee polüfenooli lisamisel kosmeetilisele koostisele antimikroobne toime. J Korean Soc Appl Biol Chem. 2007;50:210–216.
30. Hong JY, Nam HS, Yoon KY, Shin SR. Kääritatud musta jujuubi ekstraktide antioksüdantne toime. Korea J toidukonserv. 2012;19(6):901–908. doi:10.11002/kjfp.2012.19.6.901
31. Youn JS, Shin SY, Wu Y jt. Aruncus dioicus var. antioksüdant ja kortsudevastane toime. kamtschaticuse ekstrakt. Korea J toidukonserv. 2012;19(3):393–399. doi:10.11002/kjfp.2012.19.3.393
32. Chan YY, Kim KH, Cheah SH. Sargassumi polütsüstiini inhibeeriv toime türosinaasi aktiivsusele ja melaniini moodustumisele hiire B16F10 melanoomirakkudes. J Etnopharmacol. 2011;137(3):1183–1188. doi:10.1016/j.jep.2011.07.050
33. Huang HC, Hsieh WT, Niu YL, Chang TM. Magnolia grandiflora L. lilleekstrakti melanogeneesi ja antioksüdantsete omaduste pärssimine. BMC Complement Altern Med. 2012; 6:12–72.
34. Jang MJM, Woo H, Kim YH, Jun DY, Rhee WJ. Sancho (Zanthoxylum schinifolium) ekstrakti antioksüdatiivse, DPPH-radikaale püüdva toime ja trombivastase toimega toime. Korea J Nutr 2005;38:386–394.
35. Fiddler W, Piotrowski EG, Pensabean JW, Doerr RC, Wassermann AE. Naatriumnitriti kontsentratsiooni mõju N-nitroso-dimetüülamiini moodustumisele frankfurterites. J Food Sci. 1972;37(5):668–673. doi:10.1111/j.{9}}.1972.tb02721.x
36. Lee SJ, Chung MJ, Shin JH, Sung NJ. Looduslike taimsete komponentide mõju nitritite eemaldamisele. J Food Hyg Safety. 2000;15 (2):88–94.
37. Kang BR, SOD-like tegevuste ja nitritite eemaldamise võime muutused pruuni riisi idanemise teel Souli riikliku tehnikaülikooli magistritöö (2003).
38. Yang YW, Hsu PYJ. Polüelektrolüüdist isekoostatud mitmekihiliste pindadega polü (D, L-laktiid-ko-glükoliid) mikroosakeste mõju eksogeensete antigeenide ristesitlusele. Biomaterjalid. 2008;29(16):2516. doi:10.1016/j.biomaterials.2008.02.015
39. Serrano MC, Pagani R, Manzano M, Comas JV, Portoles MT. Polü-(epsilon-kaprolaktoon) kiledel kultiveeritud endoteeli- ja silelihasrakkude mitokondriaalse membraani potentsiaal ja reaktiivsete hapnikuliikide sisaldus. Biomaterjalid. 2006; 27(27):4706. doi:10.1016/j.biomaterials.2006.05.007
40. Pawelek JM. Pärast dopakroomi. Pigm Cell Res. 1991;4(2):53–62. doi:10.1111/j.{8}}.1991.tb00315.x
41. Invergar R, McEvily AJ. Crataegi Fructuse ekstrakti bioloogilise aktiivsuse uuringud. Korea J Herbol. 1992;17(1):29–38.
42. Wilkinson JB, Moore RJ. Harry kosmetoloogia. New York: Chemical Publishing Co., Inc; 1982:749.
Lisateabe saamiseks: david.deng@wecistanche.com WhatApp:86 13632399501






