SARS-CoV{1}} haavatavus tekitab laialdaselt kaitsva antikeha antigeenselt eristatavate Omikroni alamvariantide vastu
Nov 30, 2023
Raske ägeda respiratoorse sündroomi koroonaviiruse 2 (SARS-CoV-2) Omicroni variantide kiire areng on rõhutanud vajadust tuvastada laia neutraliseerimisvõimega antikehad, et anda teavet tulevaste monoklonaalsete ravimeetodite ja vaktsineerimisstrateegiate kohta. Siin tuvastasime S728-1157, laialdaselt neutraliseeriva antikeha (bnAb), mis sihib retseptorit siduvat saiti (RBS), mis pärines indiviidist, kes oli varem nakatunud WT SARS-CoV-ga -2 enne haiguse levikut. probleemsed variandid (LOÜ). S728-1157 näitas kõigi domineerivate variantide, sealhulgas D614G, Beta, Delta, Kappa, Mu ja Omicron (BA.1/BA.2/BA.2.75/BA.4/BA.5/) laialdast ristneutraliseerimist. BL.1/XBB). Lisaks kaitses S728-1157 hamstreid WT, Delta ja BA.1 viirustega in vivo põhjustatud väljakutsete eest. Struktuurianalüüs näitas, et lisaks CDR-H1/ tavalistele motiividele sihib see antikeha retseptori sidumisdomeenis klassi 1/RBS-A epitoobi mitmete hüdrofoobsete ja polaarsete interaktsioonide kaudu selle raske ahela komplementaarsust määrava piirkonnaga 3 (CDR-H3). klassi 1/RBS-A antikehade CDR-H2. Oluline on see, et see epitoop oli diproliini (2P) konstruktidega võrreldes hõlpsamini juurdepääsetav avatud ja eelfusiooni olekus või heksaproliiniga (6P) stabiliseeritud spike-konstruktsioonides. Üldiselt näitab S728-1157 laia terapeutilist potentsiaali ja võib anda teavet sihtmärgipõhise vaktsiini väljatöötamise kohta SARS-CoV-2 tulevaste variantide vastu.

cistanche tubulosa - parandab immuunsüsteemi
Sissejuhatus
Alates pandeemia algusest 2019. aasta detsembris on raske ägeda respiratoorse sündroomi koroonaviirus 2 (SARS-CoV-2) viirus 2019. aastal kaasa toonud üle 660 miljoni koroonaviirushaiguse (COVID-19) juhtu ja üle 6,5 miljonit surmajuhtumit kogu maailmas. Kuigi vaktsiinide ja ravimite kiire väljatöötamine ja levitamine on COVID-i-19 mõju suurel määral pidurdanud, kujutab tsirkuleerivate probleemsete variantide (LOÜ) esilekerkimine jätkuvalt suurt ohtu, kuna on võimalik edasist immuunvastust kõrvalehoidmist. ja suurenenud patogeensus. Variant D614G oli varaseim ilmunud variant ja sai seejärel üldlevinud. Võrreldes WT-ga näitas D614G variant pigem suuremat ülekanduvust kui suurenenud patogeensust ja seetõttu ei vähendanud see tõenäoliselt kliinilistes uuringutes vaktsiinide efektiivsust (1). Ajavahemikul D614G ilmumisest 2021. aasta oktoobrini arenes kogu maailmas välja veel neli olulist lenduvat orgaanilist ühendit, sealhulgas alfa, beeta, gamma ja delta. Nende variantide hulgas sai Delta tõsiseks ülemaailmseks ohuks selle edasikanduvuse, suurenenud haiguse tõsiduse ja osalise immuunsuse vältimise tõttu, mida näitab polüklonaalse seerumi ja mAb-de vähenenud võime seda tüve neutraliseerida (2–6). Varsti pärast seda, 2021. aasta novembris, tuvastati Omicroni variant ja kuulutati see uudseks LOÜks. Sellel variandil oli seni suurim arv mutatsioone ja see levis kiiremini kui varasemad tüved (7, 8). Praegu on suur hulk Omicroni alamliine, mis viivad uute COVID{21}} juhtudeni, kusjuures BQ.1, BQ.1.1 ja XBB.1.5 on muutunud BA.5 ees domineerivaks ja moodustasid sel ajal enamiku uute juhtumite kogu maailmas kirjutamisest. Omicroni variandid võivad COVID-19 vaktsiiniga seotud immuunsuse poolt erineval määral ära tunda, vähendades seeläbi oluliselt taastuvate, täielikult mRNA-ga vaktsineeritud ja uue kahevalentse WT/BA.5-ga võimendatud isikute seerumi antikehade neutraliseerivat toimet. mRNA vaktsiin (9, 10). Samamoodi suutsid Omicroni variandid pääseda mitme hädaolukorras kasutusloaga (EUA) terapeutilise monoklonaalse antikeha sidumisest, kuigi need olid varem osutunud tõhusaks varasemate lenduvate orgaaniliste ühendite vastu (10–12). Omicroni vastase neutraliseerimise vähenemise ja tulevaste lenduvate orgaaniliste ühendite jätkuva ohu tõttu on tungiv vajadus tuvastada laialdased ja tõhusad neutraliseerivad antikehad, mis suudavad kaitsta erinevate arenevate SARS-CoV-2 liinide eest. Selles uuringus tuvastasime SARS-CoV-2-konvalestseeruva indiviidi perifeersest verest tugeva retseptoriga seonduva domeenireaktiivse (RBD-reaktiivse) mAb, mis neutraliseeris tõhusalt alfa, beeta, kappa, delta, mu, ja Omicroni variandid (BA.1, BA.2, BA.2.75, BA.4, BA.5, BL.1 ja XBB). See mAb, S728-1157, vähendas märkimisväärselt BA.1 Omicron, Delta ja WT viiruskoormust kopsudes ja nina limaskestas pärast in vivo nakatamist hamstritel. S728-1157 seob retseptori sidumissaidi (RBS), mis on täielikult paljastatud, kui naelal olev RBD on ülemises konformatsioonis. mAb kasutab CDR-H1 ja CDR-H2 leitud motiive, mis on ühised IGHV3-53/3-66 klassi 1/RBS-A antikehadele (13, 14), aga ka ulatuslike ainulaadsete kontaktide kaudu CDR-iga. -H3, et vältida mutatsioone lenduvate orgaaniliste ühendite naelu. See viitab sellele, et tulevaste Omicroni variante hõlmavate vaktsiinivõimenduste ratsionaalset ülesehitust tuleks muuta nii, et see kujutaks endast stabiliseeritud tippu enamasti üles konfiguratsioonis, et optimaalselt indutseerida klassi 1/RBS-A mAb-sid, millel on sarnased CDR-H3 omadused.

cistanche on kasulikud - tugevdab immuunsüsteemi
Tulemused
RBD-reaktiivsete mAb-de eraldamine, millel on erinevad neutraliseerimis- ja tugevusmustrid. Enne Omicroni liinide levikut iseloomustasime varem 43 mAb-d, mis olid suunatud spike-valgu erinevatele epitoopidele, sealhulgas N-terminaalsele domeenile (NTD), RBD-le ja subühikule 2 (S2). Ükski neist antikehadest ei suutnud neutraliseerida sel ajal ringlevaid SARS-CoV-2 variante (15). Selles uuringus ekspresseeriti RBD-reaktiivsete mAb-de täiendav paneel kolmelt kõrge reageerimisvõimega isikult, kes saavutasid tugevad anti-spike IgG vastused, nagu eelnevalt määratletud (16) (täiendavad tabelid 1 ja 3; lisamaterjal on veebis saadaval selle artikliga; https://doi.org/10.1172/JCI166844DS1). Kuigi teravate RBD-siduvate B-rakkude osakaal oli kõrge reageerimisvõimega patsientide seas sarnane keskmise ja madala reaktsioonivõimega patsientidega (joonis 1, A–C), oli raske ahela somaatilise hüpermutatsiooni määr kõrge reageerimisvõimega rühmas oluliselt suurem (joonis 1). , D ja E), mis viitab sellele, et neil isikutel võib olla suurim potentsiaal luua tugevaid ristreaktiivseid mAb-sid (16). Neid antikehi uuriti täiendavalt RBD mutantide vastu, et teha kindlaks nende epitoopide klassifikatsioon (17). 14 RBD-reaktiivse mAb hulgast tuvastasime 4 klassi 2 mAb-d, 2 klassi 3 mAb-d ja 8 klassifitseerimata mAb-d, mis näitasid vähest või üldse mitte vähenenud seondumist ühegi testitud võtmetähtsusega RBD mutandiga (joonis 1F). Tuleb märkida, et klassi 2, klassi 3 ja klassi 4 antikehad vastavad ligikaudu varasemates uuringutes määratletud RBS BD, S309 ja CR3022 epitoopidele (13, 18). Klassi 2 ja 3 RBD mAb-d ei tundnud ära K417N/E484K/L452R/N501Y asendusi sisaldavat mitmevariandilist RBD mutanti, kunstlikult kavandatud RBD-d, mis sisaldasid võtmemutatsioone viiruse põgenemiseks (17, 18), samuti ei näidanud nad mingit ristreaktiivsust SARS-CoV{54}} ja Lähis-Ida respiratoorse sündroomi (MERS)-CoV RBD (joonis 1F). Funktsionaalselt neutraliseerisid 2. ja 3. klassi RBD mAb-d tõhusalt D614G ja Delta variante, kuid neutraliseeriv aktiivsus oli beeta-, kappa- ja mu-vastasem piiratum (joonis 1G). Ükski testitud klassi 2 või 3 antikehadest ei neutraliseerinud ühtegi testitud Omicroni varianti.
Seevastu suurem osa klassifitseerimata mAb-dest seondus RBD multivariandiga ja ristreageeris SARS-CoV-1 RBD-ga (joonis 1F). Nende hulgas tuvastasime 3 monoklonaalset antikeha S451-1140, S626-161 ja S728-1157, millel oli kõrge neutraliseerimisvõime D614G ning ristneutraliseeritud beeta-, delta-, kappa-, mu- ja Omicron BA.1 99% inhibeeriva kontsentratsiooniga (IC99) vahemikus 20–2500 ng/ml (joonis 1G). Arvestades nende 3 mAb laialdast neutraliseerimisvõimet, teostasime lisaks naastude analüüsi platvormile neutraliseerimistegevuse ka autentsete BA.2.75, BL.1 (BA.2.75+R346T), BA.4, BA.5 ja XBB viirused, kasutades fookuse vähendamise neutraliseerimise testi (FRNT) (joonis 1G). Neist S728-1157 oli Omicroni variantide, sealhulgas BA.1, BA.2, BA.4 ja BA.5 paneeli suhtes kõrge neutraliseeriva toimega, IC99-ga kuni 100 ng/ml, mõõdetuna naastude analüüs. Sarnast stsenaariumi täheldati ka FRNT kasutamisel, kus S728-1157 säilitas kõrge neutraliseerimisaktiivsuse BA.2.75, BL.1, BA.4, BA.5 ja XBB suhtes IC50-ga vahemikus 8–300 ng /mL (joonis 1G). S451-1140 neutraliseeris tugevalt BA.1, BA.2, BA.2.75 ja BL.1, kuid mitte BA.4 ja BA.5, nagu täheldati mõlemal neutraliseerimisanalüüsi platvormil. Teisest küljest ei näidanud S626-161 neutraliseerivat toimet Omicroni variantide suhtes peale BA.1 variandi (joonis 1G). Kuigi S626-161-l oli testitud lenduvate orgaaniliste ühendite suhtes madalam neutraliseerimisvõime kui kahel teisel antikehal, oli see ainus mAb, mis ei näidanud ristreaktiivsust mitte ainult SARS CoV-1 RBD suhtes, vaid suutis ka nahkhiirt neutraliseerida. koroonaviirused WIV{59}} ja RsSHC014 (joonis 1, F ja G). Need andmed viitavad sellele, et S626-161 tunneb ära konserveerunud epitoobi, mis on jagatud nende arboviiruse liinide vahel, kuid mis puudub BA.2 ja hilisemates tüvedes. Lisaks on S626-161 võrreldes S728-1157 ja S451-1140-ga pikem CDR-H3, mis võib pakkuda paremat võimet tuvastada väga konserveerunud jääkide plaastrit, mis on jagatud arboviiruste vahel, nagu kirjeldatud. eelmises uuringus (19) (täiendav joonis 1). Võrreldes nende kolme mAb immunoglobuliini raske (IGHV) ja kerge ahela (IGLV või IGKV) varieeruvaid geene SARS-CoV-2 neutraliseerivate mAb-de andmebaasiga (13, 15, 20–27), leidsime, et raske ahel varieeruvatel geenidel, mida kasutavad S728-1157 (IGHV3-66), S451-1140 (IGHV3-23) ja S626-161 (IGHV4-39), on Varem on teatatud, et need kodeerivad mitmeid tugevalt neutraliseerivaid SARS-CoV{85}} antikehi, mis on suunatud RBD-le (21, 22, 28, 29). Kuid ainult S728-1157-l olid ainulaadsed raske ja kerge ahela varieeruvate geenide paarid, millest andmebaasis ei ole teatatud (täiendav tabel 3), mis näitab, et tegemist ei ole avaliku klonotüübiga.

Joonis 1. COVID-19-ravimitest eraldatud RBD-reaktiivsete mAb-de iseloomustus
Neid 3 mAb-d (S451-1140, S626-161 ja S728-1157) iseloomustati täiendavalt, et määrata nende seostumisaste SARSCoV-2 lenduvate orgaaniliste ühenditega (joonis 2, A ja B) . Prefusiooniga stabiliseeritud piisk, mis sisaldab 2-proliini asendusi S2-subühikus (2P; diproliin), on osutunud WT-spikega võrreldes paremaks immunogeeniks ja on mitme praeguse SARS-CoV{11}} aluseks. vaktsiinid, sealhulgas mRNA-põhised vaktsiinid (30, 31). Hiljuti teatati, et 6 proliiniga stabiliseeritud piigivalk (6P; heksaproliin) võimendab ekspressiooni ja on veelgi stabiilsem kui algne diproliinikonstrukt; Selle tulemusena on tehtud ettepanek kasutada seda COVID{17}} järgmise põlvkonna vaktsiinides (32, 33). Et teha kindlaks, kas diproliini ja heksaproliini spikekonstruktsioonide vahel on antigeensuse erinevusi, lisati meie testpaneeli mõlemad immunogeenid. ELISA-ga mõõdetuna avastasime, et 3 mAb-d sidusid 6P-WT antigeeni suuremal määral kui WT-2P spike (joonis 2, A ja B). Kõik kolm monokloonset antikeha näitasid võrreldavat seondumist alfa-, beeta-, gamma- ja deltaviiruste tippudega võrreldes WT-2P omaga (joonis 2, A ja B). Kuid nende 3 mAb seondumisreaktiivsus vähenes oluliselt Omicroni perekonna antigeenide paneeli suhtes (joonis 2, B ja C). Seondumine S451-1140 oli tundlik mutatsioonides BA.1 ja BA.2 leitud mutatsioonide suhtes, mille tulemuseks oli seondumise suur vähenemine ja nende variantide neutraliseerimise 31-kordne vähenemine võrreldes WT-ga-2 P antigeen ja D614G viirus vastavalt (joonis 2B). Sarbekoviiruse ristneutraliseeriv mAb S626-161 näitas samuti 1.2- kuni 3.5-korda vähenenud seondumine BA.1 antigeeniga, mis võib põhjustada {{45} } korda vähenenud neutraliseerimisaktiivsus BA.1 vastu (joonis 1G ja joonis 2, B ja C). Kõige tugevama laialt neutraliseeriva antikeha (bnAb) S728-1157 puhul vähenes seondumine Omicroni antigeenidega vähemal määral (vahemikus 11- kuni 44-} korda) võrreldes antikehaga. WT-2P tõusis ja seda ei mõjutanud neutraliseeriv aktiivsus (joonis 1G ja joonis 2, B ja C). Omicronit neutraliseeriva mAb seondumise märkimisväärne vähenemine BA.1 tipuga võib olla tingitud muutustest selle liikuvuses ja seotud Omicroni 3-RBD-alla struktuuride tiheda pakkimisega ja 1- eelistamisega. üles RBD, mis aitavad vältida antikehade teket, nagu on kirjeldatud eelmises uuringus (34). 2P ja 6P stabiliseerivatel mutatsioonidel on erinev toime ka Omicroni variantides, kus kõik 3 mAb-d näitasid rohkem kui 28- korda suuremat seondumist BA-ga.1-6P võrreldes BA-ga.1-2P versioon, kuid ainult vähesel määral suurendas seondumist BA.2 ja BA.4/5 6P versioonidega võrreldes nende 2P versioonidega 1,2 × 1,4 ×, mis viitab Omicronit neutraliseerivate mAb-de pisut paremale ligipääsetavusele heksaapoli versioonidele, eriti spike BA.1 konstruktsiooni jaoks. Lisaks ELISA-le kasutati biokihi interferomeetriat (BLI) nende 3 mAb seondumiskiiruse ja tasakaalukonstantide (kon, koff ja KD) kvantifitseerimiseks spike-antigeenide paneeliga (täiendav joonis 2). Fragmendi antigeeni seondumise (Fab) heksaproliini tippudega tuvastamise kon määr oli 15- kuni 33- korda kiirem võrreldes diproliini naastudega (täiendav joonis 2, B ja C), mis näitab, et antikehad seondusid 6P konstruktiga kiiremini kui 2P konstruktiga. Seda oleks võinud oodata, kui epitoobid oleksid RBD-s paremini ligipääsetavad avatud olekus heksaproliini tipul. Välja arvatud S626- 161, dissotsieerusid Fabs heksaproliini piigist aeglasemalt (oma koff oli madalam) kui diproliini piigil, nii et üldine KD näitas, et S728-1157 ja S451-1140 seondusid heksaproliini piisk suurema afiinsusega (täiendav joonis 2, B ja C). Heksaproliini naelaga seondumise suurenemine oli 1:2 interaktsioonimudeliga võrreldes puutumatu IgG puhul veelgi märgatavam, nagu näitasid S728-1157 ja S451- 1140 mAb-d, mis on kooskõlas mitme epitoobi eksponeerimisega 6P stabiliseerimisega, mis võimaldas. paranenud aviidsus (täiendav joonis 2, A ja C). Kokkuvõttes näitavad need tulemused, et sihitud epitoobid võivad olla 6P-stabiliseeritud naelal suhteliselt paremini ligipääsetavad, kui RBD on avatud olekus. Järgmisena viidi selle oletuse kontrollimiseks läbi struktuurianalüüsid.

Joonis 2. Omicronit neutraliseerivate mAb-de seondumislaius
Laias laastus neutraliseerivate mAb-de struktuurianalüüs. Seondunud epitoopide esimese ligikaudsusena kasutati ELISA konkurentsianalüüsi, et teha kindlaks, kas need 3 laialdaselt neutraliseerivat mAb-d kattuvad meie praeguse monoklonaalsete antikehade paneeliga, mis on varasematest uuringutest teadaolevate epitoobi spetsiifiliste mAb-de kogum (15, 25, 35). ja veel 2 praegu kliinilises kasutuses olevat mAb-d, LY-CoV555 (Eli Lilly) (36) ja REGN10933 (Regeneron) (37). S451-1140 ja S728-1157 seondumissaidid kattusid osaliselt CC12.3 (23, 25), 1. klassi neutraliseeriva antikehaga ja enamiku klassi 2 antikehadega, sealhulgas LY-CoV555 ja REGN10933, kuid mitte klassi 3 ja klassi 4 antikehadega (joonis 3A). S626-161 jagas märkimisväärset kattumist seondumispiirkonnas klassi 1 CC12.3, mitme klassi 4 antikehaga, sealhulgas CR3022, ja teiste klassifitseerimata antikehadega, samas kattudes osaliselt mitme klassi 2 ja ühe klassi 3 antikehaga (joonis 3A). Analoogiliselt näitas konkureeriv BLI test, et S451-1140 ja S728-1157 konkureerisid tugevalt üksteisega seondumise pärast naelu WT-6P-ga, samas kui S626-161 mitte (täiendav joonis 3). Üldiselt näitavad need andmed, et S451-1140 ja S728-1157 tunnevad ära sarnased epitoobid, mis erinevad S626-161-st.

Joonis 3. S728-1157 laia neutraliseerimise mehhanism
Antikeha S728-1157 kodeeris IGHV3-66 ja sellel oli lühike komplementaarsust määrav piirkond 3 (CDR-H3). Eelkõige on mAb-d, mis seovad RBS-i sidumisrežiimis 1 (st RBS-A või klassi 1 sait), mida iseloomustavad CC12.1, CC12.3, B38 ja C105 (13, 18, 23, 29, 38, 39), kipuvad kasutama IGHV3-53 või 3-66 ja on tundlikud lenduvate orgaaniliste ühendite mutatsioonide suhtes (40). Kuid S728-1157 CDR-H3 piirkond erineb teistest selle klassi antikehadest tugevalt, mis võib olla tingitud selle laiemast aktiivsusest. Et mõista S728-1157 laialdase neutraliseerimise struktuurset alust sellel epitoobil, lahendasime IgG S728-1157 krüoelektronmikroskoopia (krüo-EM) struktuuri (joonis 3B) kompleksis terava WT{ga. {31}}P-Mut7, tipu WT-6P versioon, millel on C705 ja C883 juures protomeeridevaheline disulfiidside, globaalse eraldusvõimega ligikaudu 3,3 Å (täiendav joonis 4E). Kasutades sümmeetria laiendamist, fokusseeritud klassifitseerimist ja täpsustamise meetodeid, saavutasime RBD-Fv liideses kohaliku eraldusvõime ligikaudu 4 Å (täiendav joonis 4E ja täiendav tabel 8). S728-1157 Fab kristallstruktuur määrati eraldusvõimega 3,1 Å ja seda kasutati aatomimudeli koostamiseks RBD-Fv liideses. Meie struktuurid kinnitavad, et S728-1157 sidus RBS-A (või klassi 1) epitoobi RBD-üles konformatsioonis (joonis 3B ja täiendav joonis 4E), sarnaselt teiste IGHV-ga3-53/{{55} } antikehad (joonis 3C). Angiotensiini konverteeriva ensüümi 2 (ACE2) sidumissaidi steeriline blokeerimine S728-1157 poolt seletab selle suurt neutraliseerimisvõimet SARS-CoV-2 vastu. Motiiv 32NY33 ja motiiv 53SGGS56 (23) S728-1157 CDR-H1 ja -H2 interakteeruvad veekogudega peaaegu samal viisil kui CC12.3 (täiendav joonis 4, B ja C). Võrreldes VH 98DF99-ga CC12.3-s, moodustab VH 98DY99 S728-1157 CDR-H3-s RBD-ga ulatuslikumaid interaktsioone, sealhulgas nii hüdrofoobseid kui ka polaarseid interaktsioone, mis võib põhjustada lenduvate orgaaniliste ühendite ulatuslikku neutraliseerimist (joonis). 3D ja täiendavad tabelid 6 ja 7). Diglütsiin VH 100GG101 S728- 1157 CDR-H3-s võib samuti hõlbustada ulatuslikumat seondumist võrreldes VH Y100-ga CC12.3-s, mis on tõenäoliselt tingitud glütsiinijääkide paindlikkusest, mis põhjustab CDR-i tipu erineva konformatsiooni. -H3 silmus ja jääkide suhteline nihe 98DY99 juures.

cistanche tubulosa - parandab immuunsüsteemi
Cistanche Enhance Immunity toodete vaatamiseks klõpsake siin
【Küsi lisa】 E-post:cindy.xue@wecistanche.com / Whats App: 0086 18599088692 / Wechat: 18599088692
Kuigi Omicroni lenduvate orgaaniliste ühendite RBD-s on ulatuslikud mutatsioonid, ei interakteeru enamik neist jääkidest S728-1157-ga, kuna seondumist täheldatakse endiselt (täiendav joonis 4A). Meie mudelist WT-6P-Mut7 + Fab S728-1157 eeldatakse, et Y505 kuni VL Q31 ja E484 kuni VH Y99 moodustavad vesiniksidemeid (täiendav joonis 4D ja täiendav tabel 6 ), mida võivad Omicroni mutatsioonid Y505H ja E484A häirida. Y505H mutatsioon võimaldaks siiski vesiniksidemeid VL Q31-ga ja E484A mutatsioon lisaks hüdrofoobsete jääkide VL Y99, F456 ja Y489 lähedale veel ühe hüdrofoobse kõrvalahela. Need kontaktid võivad osaliselt seletada mehhanismi, mis võimaldab S728-1157-l säilitada neutraliseerivat aktiivsust, kuigi vähenenud, antigeeni BA.1 vastu (joonis 1G ja joonis 2B). BA.1 antigeen omakorda on tõenäoliselt seotud Omicroni mutatsioonidega, mis muudavad teravikvalgu konformatsioonilist maastikku (34). Kuid mitmed somaatiliselt muteerunud jäägid, st VH L27, L28, R31, F58 ja VL V28 ja Q31, S728-1157-s on seotud interaktsiooniga SARS-CoV-2 RBD-ga (täiendav joonis 1 ja Täiendav tabel 7), mis võib samuti kaasa aidata selle laialdasele reaktsioonivõimele võrreldes CC12.3-ga. Üldiselt näitasid meie struktuuriuuringud S728-1157 laialdase neutraliseerimise alust, mis suudab vastu võtta enamiku SARS-CoV-2 lenduvate orgaaniliste ühendite mutatsioone.
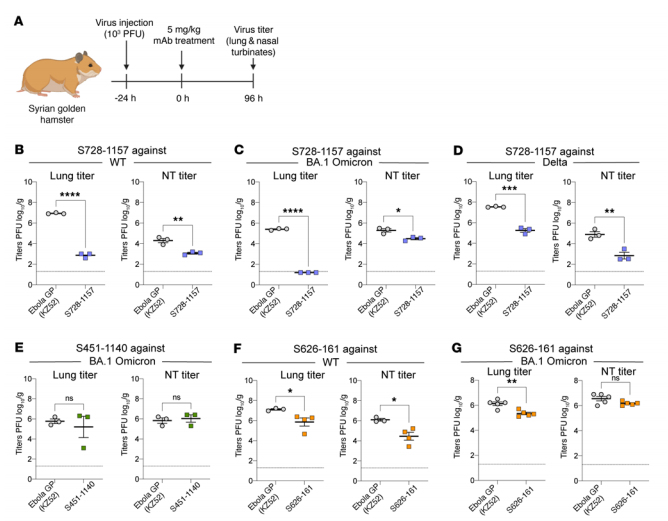
Joonis 4. BnAb-de kaitsetõhusus SARS-CoV-2 nakkuse vastu hamstritel.
S728-1157 vähendab SARS-CoV-2 BA.1 Omicron, Delta ja WT SARS-CoV-2 replikatsiooni Süüria hamstrites. Meie laialdaselt neutraliseerivate mAb-de kaitsetõhususe hindamiseks kasutasime kuldse Süüria hamstri nakkuse mudelit, mida on laialdaselt kasutatud SARS-CoV{7}} puhul. Hamstrid said 5 mg/kg meie testitavaid mAb-sid või isotüübikontrolli, mis oli suunatud ebaolulisele antigeenile (ebolaviiruse glükoproteiin), intraperitoneaalse süstina 1 päev pärast nakatumist SARS CoV{10}} viirustega. Kopsu- ja ninakoed koguti 4 päeva pärast nakatumist (joonis 4A). S728-1157 terapeutiline manustamine vähendas WT, BA.1 Omicron ja Delta variantide tiitreid nii nakatunud hamstrite ninaõõnes kui ka kopsudes (joonis 4, B–D). Huvitaval kombel oli S728-1157 mõju kopsudes dramaatiline, vähendades WT ja BA.1 Omicroni viiruskoormust ligikaudu 104 PFU võrra, kusjuures BA.1 Omicroni variandi viiruse tiitrid kaotati täielikult (joonis 4C). Vastupidiselt in vitro neutraliseerimisele (joonis 1G) ei vähendanud S451-1140 BA.1 Omicroni viiruse replikatsiooni kopsu- ja ninaturbinaatides, mis viitab selle klooni in vitro neutraliseerimise ja in vivo kaitse vahelisele katkemisele (joonis 4E) . Võrdluseks, S626-161 manustamine põhjustas pärast WT ja BA.1 nakatamist kopsuviiruse tiitrite vähesel määral olulist vähenemist (joonis 4, F ja G). Need andmed rõhutavad, et laialdaselt kaitsvate mAb-de täpseks määratlemiseks on vaja hinnata kaitsetõhusust paralleelselt neutraliseerimisaktiivsusega. Edaspidi on huvitav uurida, mil määral on S728-1157 kaitsevõime Fc-st sõltuv. Üldiselt on S728-1157 paljulubav monokloonne antikeha, millel on laialdane neutraliseerimistõhusus SARS CoV-2 variantide vastu, mis on võimelised järsult vähendama WT, Delta ja BA.1 replikatsiooni in vivo.
SARS-CoV-2 infektsioon kutsub harva esile tugevatoimelisi S728-1157-sarnaseid ristneutraliseerivaid mAb-sid. Arvestades S728-1157 ristneutraliseerimist ja profülaktilist potentsiaali, püüdsime hinnata, kas SARS-CoV-2 patsientidel tekivad polüklonaalsete reaktsioonide hulgas sageli S728–1157-sarnased antikehad. Selle hindamiseks viisime läbi konkureeriva ELISA, kasutades taastusseerumit, et tuvastada RBD-vastaste antikehade tiitrid, mis võiksid konkureerida S728-1157-ga seondumise pärast (joonis 5A). Katsealused jagati 3 rühma, lähtudes eelnevalt määratletud antikehavastuste suurusest (15, 16). Kuigi kõrge ja mõõduka ravivastusega inimestel olid S728-1157-konkureerivate seerumi antikehade tiitrid madalad (joonis 5B), olid tiitrid kõikides rühmades üsna madalad, mis viitab sellele, et S{{ kõrge taseme saavutamine on aeg-ajalt. 18}}-sarnased antikehad polüklonaalses seerumis pärast WT SARS-CoV{20}} nakatumist. Lisaks S728-1157-le testisime taastuva seerumi konkurentsi teiste mAb-dega, sealhulgas S451- 1140, S626-161, LY-CoV555, REGN10933, CR3022 ja CC12.3. Sarnaselt S728-1157-ga täheldasime S451-1140-ga, S626-161-ga, LY-CoV555-ga, REGN10933-ga ja CC12.3-ga konkureerivate antikehade suhteliselt madalaid tiitreid enamiku taastumisperioodi polüklonaalses seerumis. üksikisikud (joonis 5, C–F ja H). Sellegipoolest olid kõrge ravireaktsiooniga patsientide tiitrid neutraliseerivate mAb-de suhtes märkimisväärselt kõrgemad kui madala reageerimisega inimestel (joonis 5, B–F ja H). Seevastu CR3022 epitoobi saidile suunatud antikehad olid taastuvatel inimestel rohkem väljendunud, mis viitab klassi 4 RBD antikehade rikastumisele polüklonaalses seerumis (joonis 5G). Märkimisväärselt ei olnud CR3022 tiitrites kolmes ravile reageerinud rühmas olulisi erinevusi, mis viitab sellele, et enamikul isikutel indutseeriti WT SARS-CoV-2 infektsiooni ajal järjekindlalt CR{45}}saidi antikehi. Huvitav on see, et võrreldes CC12.3-ga tuvastati S728-1157 kõrge ravireaktsiooniga inimeste seerumis 4- korda madalamal tasemel. Seega, vaatamata klassi 1 antikehadele, mida sageli indutseerivad looduslikud infektsioonid ja vaktsineerimine (14, 20, 28, 29, 41–43), näitavad meie andmed, et selle klassi alamhulka esindavad S728–1157-sarnased antikehad on suhteliselt haruldased.
Lisaks uurisime meie taastumiskohorti seerumite reaktiivsuse erinevust 2P suhtes ja 6P-stabiliseeritud hüppeid (joonis 5, I–K). Leidsime, et kõik 3 reageerijate rühma paigaldasid 6- kuni 11-kordselt 6- kuni 11-kordselt 6- kuni 11-kordselt 6P-stabiliseeritud terava WT-vastase anti-spike-reaktiivsed antikehad. peamised antigeensed epitoobid olid paremini eksponeeritud või stabiliseerunud 6P-stabiliseeritud antigeenil. Kasutades samu proove, olid kõrge ja mõõduka ravivastuse korral ka BA-vastaste antikehade tiitrid madalam.{17}}P kui BA.{18}}P, 4–5 korda (joonis 5K). Märkimisväärne on see, et madala ravivastuse korral oli seostumisreaktiivsuse muutus BA.1 Omicron-2P ja 6P suhtes väiksem kordi (2-kordne vähenemine) võrreldes WT-2P ja 6P naeluga ({ {28}}-kordne vähenemine) (joonis 5, J ja K), mis viitab sellele, et BA.1 Omikron-reaktiivsete epitoopide vastased seerumi antikehad võivad vähese ravivastuse korral olla piiratud. Üldiselt viitavad need andmed sellele, et nii WT kui ka Omicron viiruste puhul on paranenud polüklonaalne seondumine, mis on põhjustatud looduslikust infektsioonist 6P-stabiliseeritud piigiga.
S728–1157-sarnased antikehad indutseeritakse optimaalselt hübriidimmuunsuse kontekstis. Primaarne SARS-CoV-2 infektsioon ilma vaktsineerimiseta on praeguses globaalses keskkonnas muutunud haruldaseks ja mitmed uuringud on teatanud, et SARS-CoV-2 immuunsus erineb konkreetse vaktsineerimise/infektsiooni ajalooga inimestel. Selle tulemusena püüdsime järgmisena uurida, millised tavalised kokkupuuted, välja arvatud WT-nakkus ainult esivanemate SARS-CoV-2-ga, indutseerivad tõhusalt S728–1157-sarnaseid antikehi monovalentse mRNA-l põhinevate vaktsiinide plasmas nii eelnevaga kui ka ilma. infektsioon. Saime vajaliku bioproovi SARS-CoV-2 (PARIS) kiirimmuunsusega seotud kaitsega seotud uuringurühmast, mis on pandeemia algusest saati jälginud tervishoiutöötajaid pikisuunas (44). Valisime plasmaproovid täielikult immuniseeritud (2 × vaktsineeritud) uuringus osalejatelt, kellel oli ja ilma, samuti võimendatud osalejatelt (3 × vaktsineeritud) infektsiooniga ja ilma. Lisaks kaasasime ka proovid uuringus osalejatelt, kes olid saanud kahevalentset mRNA vaktsiini (esivanemate WA1/2020 pluss Omicron BA.5) (joonis 6A ja täiendav tabel 2). Revaktsineerimise saanud osalejate läbimurdelised infektsioonid toimusid ajal, mil Omicroni suguvõsad olid New Yorgi suurlinnapiirkonnas välja tõrjunud kõik teised SARS-CoV{22}} suguvõsad. Leidsime, et topeltvaktsineeritud isikutel olid S728-1157 konkureerivate seerumi antikehade tiitrid 5 testitud proovirühma hulgas madalaimad (joonis 6B). Nimelt olid need tasemed sarnased meie vaktsineerimata kohordis täheldatuga (kõik reageerijad; joonis 5B). Võrdluseks, inimestel, kellel on anamneesis loomulik infektsioon, sealhulgas taastuvad isikud, kes said 2 3-st vaktsiiniannusest, ja isikud, kellel oli läbimurdeline infektsioon ja kes said kahevalentset revaktsineerimist, näitasid oluliselt kõrgemat S{31}} esilekutsumist võrreldes nakatumata isikutega. kuid vaktsineeritud isikud (joonis 6B). Kuigi nakatumata 3-annuserühmas oli 2-annuserühmaga võrreldes ainult mitteoluline tõus, näitas vaktsiinitüüpide jaotus, et BNT162b2 ja mRNA-1273 homoloogsed kolmandad annused suurendasid oluliselt S{{ 38}} nagu neutraliseerivate antikehade tiitrid vastavalt 2,72 × ja 2,85 × (joonis 6, C ja D). Tuleb märkida, et nende osalejate seas, kellel oli kokku 3 kontakti järsu tõusuga, olid S728-1157-sarnaste antikehade tiitrid taastuvatel topeltvaktsineeritutel 3 korda kõrgemad kui varem nakatumata kolmikvaktsiiniga vaktsineeritutel, mis viitab sellele, et SARS-CoV{{ 51}} infektsioon indutseerib seda klonotüüpi optimaalsemalt. Hübriidimmuunsuse rühmade hulgas märkisime, et enamikul kahevalentse revaktsineeritud vaktsiini annuse saanud võimendatud isikutel oli S728-1157 antikehade tiiter vaid veidi kõrgem võrreldes enne omikronit taastunud vaktsineeritud rühmadega, mis viitab sellele, et S{{53} }} tiiter lähenes tõenäoliselt platoole pärast 3 säritust. Uurisime ka polüklonaalsete antikehade tiitreid, mis konkureerisid lisaks S728-1157-le ka CC12.3 ja CR3022-ga. Kõikidel isikutel esinesid suhteliselt kõrged CC12.3- ja CR3022-sarnaste antikehade tiitrid, sõltumata kokkupuute arvust ja tüübist (täiendav joonis 5), vastupidiselt sellele, mida me täheldasime S728-1157- puhul. nagu antikehad. Üldiselt näitavad need andmed, et SARS-CoV-2-nakkus ja mRNA-ga vaktsineerimine aitavad kaasa S728-1157-sarnaste antikehade indutseerimisele, kusjuures infektsioonil on vaktsineeritud isikutel domineerivam roll.

cistanche tubulosa - parandab immuunsüsteemi
Lõpuks, kui võrrelda vastuseid 2P- ja 6P-stabiliseeritud piigi vastu mRNA-ga vaktsineerimise kohordis, leidsime, et enamik rühmi kutsus esile mõlema konstruktsiooni vastaste antikehade sarnase taseme. Erandiks oli nakatamata kolmikvaktsineeritud rühm, kes näitas statistiliselt kõrgemat, kuigi ainult veidi suurenenud reaktiivsust 2P suhtes, võrreldes 6P-ga stabiliseeritud piigiga (joonis 6E). Need andmed viitavad sellele, et erinevalt loomulikust infektsioonist (joonis 5, J ja K) tekitab ainuüksi vaktsineerimine polüklonaalse vastuse, mis on kooskõlas Spike{11}}P konstrukti epitoopidega rohkem piiratud. }}Praeguste vaktsiinide koostis. Lõppkokkuvõttes toetavad need leiud ideed, et tulevaste SARS-CoV-2 vaktsiinide 6P-stabiliseerimine võib olla suureks kasuks laialdaselt kaitsvate antikehaklonotüüpide, nagu S728-1157 esilekutsumisel.
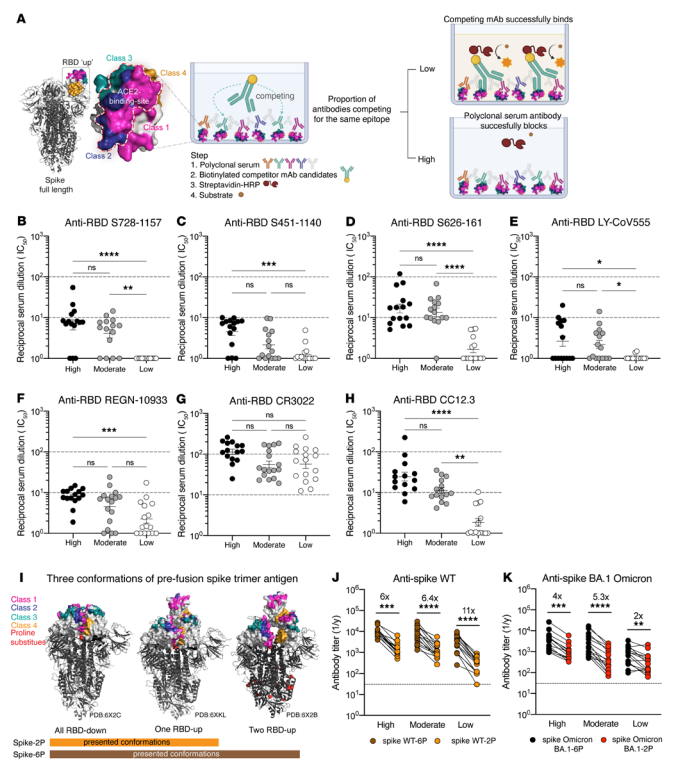
Joonis 5. Taastuvate seerumi antikehade konkurents laias laastus neutraliseerivate RBD-reaktiivsete mAb-dega ja seerumi antikehavastuse võrdlus 6P- ja 2P-stabiliseeritud naelu vastu
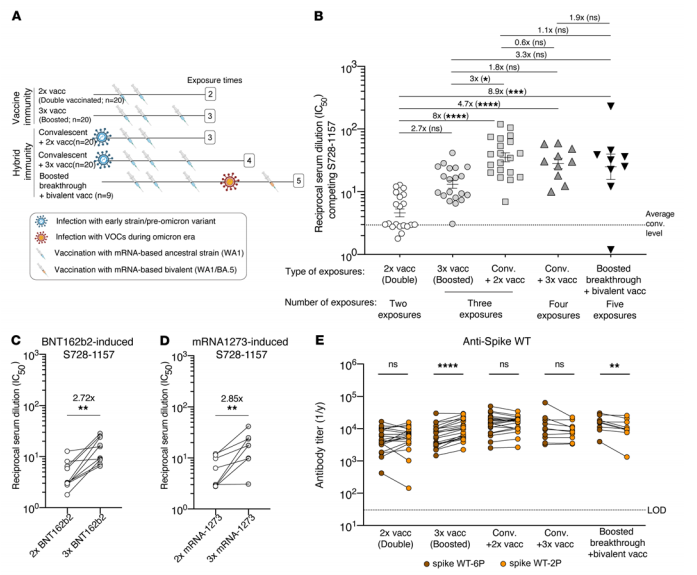
Joonis 6. mRNA-ga vaktsineeritud seerumi antikehade konkurents S728-1157 neutraliseerivate RBD-reaktiivsete mAb-dega ja seerumi antikehavastuse võrdlus 6P- ja 2P-stabiliseeritud naastudega.
Arutelu
Selles uuringus tuvastame COVID-19 pandeemia esialgse laine ajal SARS-CoV-2 infektsioonist paranenud inimese mälu B-rakust eraldatud tugeva bnAb. See bnAb, S728- 1157, säilitas olulise seondumisreaktiivsuse ja sellel oli püsiv neutraliseeriv toime kõigi testitud SARS-CoV-2 lenduvate orgaaniliste ühendite, sealhulgas Omicron BA.1, BA.2, BA.2.75, BL.1 suhtes ( BA.2.75+R346T), BA.4, BA.5 ja XBB ning suutis oluliselt vähendada nakkavate viiruste tiitreid pärast Delta ja BA.1 nakatumist hamstritel.
Leidsime, et meie kohorti taastuv seerum sisaldas madalas kontsentratsioonis antikehi, mis konkureerivad S728-1157 (klassi 1/RBS-A antikeha) ja klassi 2 epitoobi mAb-dega. See viitab sellele, et S728-1157 on mõnevõrra ainulaadne teistest klassi 1 epitoopide sihtmärgiks olevatest antikehadest ja seda indutseeritakse harva RBD-spetsiifilises mälu B-rakkude kogumis. Selle asemel näis meie loomuliku nakkuse kohort indutseerivat CR3022 (klass 4) epitoobile suunatud antikehi; selle spetsiifilisusega antikehad on sageli ristreaktiivsed, kuid vähem tõhusalt neutraliseerivad kui RBS-i sihtivad antikehad (14, 17). Need andmed täiendavad meie varasemaid leide, mis näitavad, et klassi 3/S309 antikehade rohkus taastusravi seerumites võib kaasa aidata neutraliseerivale toimele alfa- ja gammavariantide vastu, samas kui klassi 2 antikehade puudumine võib põhjustada Delta-vastase neutraliseerimisvõime vähenemist (15). . Vaatamata sellele on enamiku nende RBS-i sihtivate antikehade (RBS-A/klass 1, RBS-B, C/klass 2 ja RBS-D, S309/klass 3) Omicroni variantide aktiivsus väga piiratud. (11, 40, 45).
Edasine peamine väljakutse on kindlaks teha, kuidas parandada konserveerunud RBS-epitoopide suhtes laialdaselt ristreaktiivsete antikehade esilekutsumist. Sellega seoses täheldasime siin, et hübriidimmuunsusega indiviididel oli S728-1157-sarnaste antikehade tiitrid oluliselt kõrgemad kui ilma eelneva nakatumiseta vaktsineeritud isikutel. Oluline on see, et seda nähtust täheldati isegi siis, kui ekspositsioonide arvu kontrolliti (st taastuvate topeltvaktsineeritute ja nakatumata kolmikvaktsiini vaktsineeritute puhul), mis viitab sellele, et nakkusega seotud immuunsuse (või vaktsiini koostise, mis võib seda tüüpi immuunsust jäljendada) element on selle klonotüübi esilekutsumiseks oluline. See on kooskõlas eksperimentaalsete tõenditega, mis kinnitavad, et hübriidimmuunsusega isikutel on laiemad antikehade reaktiivsuse profiilid võrreldes nendega, kellel on ainult vaktsineerimisest või primaarsest infektsioonist põhjustatud immuunvastus (9).
Siin toodud struktuurid illustreerivad, et S728-1157 seob RBS-A/klassi 1 epitoobi üleskonformatsiooniga RBD-s. See epitoop näib olevat kergemini ligipääsetav 6P-stabiliseeritud naelu korral, millel on väidetavalt ülemises osariigis 2 RBD-d, võrreldes 2P naeluga, millel on ainult 1 (30, 33, 46, 47) ja mille vastu meie antikehad on spetsiifilised ülesehituse naela suhtes näitavad paremat seondumist. S728-1157 isoleeriti pärast loomulikku nakatumist; sellistes kontekstides on tõenäosus S728-1157-sarnaste kloonide esilekutsumiseks tõenäoliselt suurem, arvestades, et RBD peab suutma kasvõi ajutiselt omaks võtta konformatsiooni ülespoole, et seonduda ACE2-ga, paljastades seeläbi selle epitoobi. Erinevalt enamikust IGHV3-53/3-66 RBS-A/klassi 1 antikehadest, suudab S728-1157 vastu võtta olulisi mutatsioone lenduvate orgaaniliste ühendite hüpetes, kasutades ulatuslikke interaktsioone CDR-H3 ja RBD vahel (29, 48–50). S728-1157 kasutab ka teistsugust kerget ahelat (IGLV3-9) võrreldes teiste vähem laiade antikehadega, nagu CC12.3 (IGKV3-20), mis võib mõjutada üldist seondumisinteraktsiooni; aga meie analüüs näitab, et S728-1157 kerge ahela ja RBD vahel on vähem vesiniksidemeid võrreldes CC12.3-ga (täiendav tabel 7). Kuigi enamus CDR-H3 kontaktjääke, mis on selles interaktsioonis VOC ristreaktiivsuse jaoks kriitilised, on idutee kodeeritud ja neid ei sisesta somaatilised mutatsioonid, on mitmed somaatiliselt muteerunud jäägid raamistiku piirkondades või CDR-H1, CDR-H2 ja CDR-L1. osalenud koostoimes SARS-CoV-2 RBD-ga. Ühest küljest viitab see sellele, et IGHV3-53/66 klassi antikehi kodeerivad mälu-B-rakud võivad edasise afiinsuse küpsemise teel omandada sarnase ristreaktiivsuse taseme. Teisest küljest näitab see ka võimalust kujundada iduliinile suunatud immunogeene, mis on suunatud S{52}}nagu naiivsetele B-rakkudele. Ehkki võib olla keeruline välja töötada vaktsiine, mis võivad esile kutsuda spetsiifiliselt S728-1157-sarnaseid antikehi koos valitud CDR-H3-dega, mis suudavad ületada lenduvate orgaaniliste ühendite mutatsioone, on julgustav, et IGHV geeni piirangut täheldatakse ka teiste tugevate SARS-CoV{ {58}} neutraliseerivate mAb-de uuringud (13, 15, 20–27). Alternatiivina võib see olla teostatav ka iteratiivse immuniseerimise teel optimeeritud RBD immunogeenidega, nagu on varem teatatud teiste patogeenide puhul (51–55).
Kuigi RBS-A/ 1. klassi antigeensaitis (18) on täheldatud palju mutatsioone, on S728-1157 epitoobi osas 13 15-st RBD kontaktjäägist ja 2 CDR-H{{9} 3-st. }seotud RBD kontaktjäägid säilivad Omicronis ja kõigis teistes lenduvates orgaanilistes ühendites. See viitab sellele, et RBD piirkond, kus S728-1157 epitoop leitakse, võib sisaldada selle dünaamilise funktsiooni ja viiruse sobivuse jaoks kriitilisi jääke ning on seetõttu mutatsioonide ja antigeense triivi suhtes vähem tolerantne kui ümbritsevad RBS-A/ klassi 1 saidi jäägid. Kui see nii on, tuleks selle konkreetse epitoobi kadumise tendentsi viirusvariantide arenedes vähendada, muutes S728-1157 ja sarnaste antikehade ja epitoopide iseloomustamise oluliseks variantresistentsete vaktsiinide või mAb terapeutilise väljatöötamise jaoks. Kokkuvõttes tuvastab meie uuring bnAb-d, mis võivad anda teavet järgmise põlvkonna variantikindlate koronaviiruse vaktsiinide immunogeenide kujundamisel või olla SARS CoV{17}} evolutsiooni suhtes resistentsed mAb-ravimid. Eelkõige kombineeritud tugevuse ja laiuse poolest näib S728-1157 olevat oma klassi parim seni eraldatud antikeha. Arvestades, et see antikeha seondub 6P-stabiliseerimisega kergemini, indutseerivad seda eelistatavalt 6P-stabiliseeritud rekombinantsed spike-valgud või terve viirus, mis viitab sellele, et heksaproliini modifikatsioon võib olla kasulik tulevastele vaktsiinikonstruktsioonidele, et kaitsta optimaalselt tulevase SARS-CoV eest. -2 variandid ja muud arboviirused.

cistanche tubulosa - parandab immuunsüsteemi
meetodid
Monoklonaalsete antikehade eraldamine. PBMC-d eraldati leukoreduktsioonifiltritest ja külmutati, nagu eelnevalt kirjeldatud (24). B-rakud rikastati PBMC-dest FACS-i kaudu. Rakud värviti CD19, CD3 ja oligofluorofooriga konjugeeritud antigeenisondidega; huvipakkuvad rakud tuvastati kui CD3–CD19+ antigeen+. Kõik mAb-d genereeriti oligo-märgistatud antigeenide söödaga sorteeritud rakkudest, mis tuvastati üherakulise RNA-Seq abil, nagu eelnevalt kirjeldatud (15, 24). Selles uuringus loodud üksikud B-raku andmed on talletatud Gene Expression Omnibus'i: GSE171703 ja GSM5231088–GSM5231123.
Antigeenispetsiifilised B-rakud valiti monoklonaalsete antikehade genereerimiseks JMP Pro 15 abil analüüsitud antigeenisondi intensiivsuse põhjal. Antikeha raske ja kerge ahela geenid sünteesiti Integrated DNA Technologies (IDT) abil ning klooniti inimese IgG1 ja inimese κ või λ kergesse ahelasse. ekspressioonivektorid Gibsoni kooste abil, nagu eelnevalt kirjeldatud (56). Vastava mAb rasked ja kerged ahelad kotransfekteeriti ajutiselt HEK293T rakkudesse (ATCC). Pärast 18-tunnist transfektsiooni lisati transfekteeritud rakkudele valguvaba hübridoomi söötme supernatant (PFHM-II, Gibco). Sekreteeritud mAb-d sisaldav supernatant koguti 4. päeval ja puhastati, kasutades proteiin-A-agaroosi helmeid (Thermo Fisher Scientific), nagu on kirjeldatud eelnevalt (56). Hästi iseloomustatud antikehade raskete ja kergete ahelate järjestused saadi Protein Data Bankist (PDB), LY-CoV555 (PDB ID: 7KMG), CR3022 (PDB ID: 6W7Y) ja REGN1{{ 125}}933 (PDB ID: 6XDG) ja sünteesiti ülalkirjeldatud viisil. CC12.3 mAb (PDB ID: 6XC4) hankis Meng Yuan Scrippsi uurimisinstituudist (San Diego, California, USA). Rekombinantse piigivalgu ekspressioon. Rekombinantne D614G SARS-CoV-2 täispikk (FL) spike, BA.2-6P, BA.4/5-6P, BQ.1-6P, BQ. 1.1-6P, XBB-6P, WT RBD, üksikud RBD mutandid (R346S, K417N, K417T, G446V, L452R, S477N, F486A, F486Y, N487Q, Y489F, Q493N,5 Y505A ja Y505F), kombineeritud RBD mutant (K417N/E484K/L452R/NN501Y), SARS-CoV-1 RBD ja MERS-CoV RBD loodi ettevõttesiseselt. Lühidalt, rekombinantsed antigeenid ekspresseeriti Expi293F rakkudega (Thermo Fisher Scientific). Huvipakkuv geen klooniti imetaja ekspressioonivektorisse (majasiseselt modifitseeritud AbVec) ja transfekteeriti ExpiFectamin 293 komplektiga (Thermo Fisher Scientific) vastavalt tootja protokollile. Supernatant koguti 4. päeval pärast transfektsiooni ja inkubeeriti Ni-nitrilotriäädikhappe (Ni-NTA) agaroosiga (Qiagen). Puhastamine viidi läbi gravitatsioonivoolu kolonni abil ja elueeriti imidasooli sisaldava puhvriga, nagu eelnevalt kirjeldatud (57, 58). Eluaat puhverdati ja vahetati PBS-iga, kasutades Amiconi tsentrifugaalseadet (Millipore). Variantide B.1.1.7 Alpha, B.1.351 Beta, P.1 Gamma, B.1.617.2 Delta, BA.1, BA.2 ja BA.4 Omicron 2P mutatsioonidega stabiliseeritud rekombinantsed FL piigid olid toodetud Seattle'i lasteuuringute instituudi Satheri laboris. K417V, N439K ja E484K RBD-d ning rekombinantsed FL-i piigid WT-2P ja 6P toodeti Siinai mäel Icahni meditsiinikooli Krammeri laboris. SARS-CoV-2-6P-Mut7 ja spike BA.{91}}P kavandati ja toodeti eelmises uuringus kirjeldatud viisil (59). Iga antigeeni valgujärjestused ja ressursid on loetletud täiendavas tabelis 4. ELISA. Rekombinantsed SARS-CoV-2 spike/RBD valgud kaeti kõrge valkudega seonduvatele mikrotiitrimisplaatidele (Costar) kontsentratsioonis 2 ug/ml PBS-is 50 µl süvendi kohta ja hoiti öö läbi 4 kraadi juures. Plaate pesti PBS-ga, mis sisaldas 0,05% Tween 20 (PBS-T), ja blokeeriti 150 µl PBS-ga, mis sisaldas 20% FBS-i, 1 tund temperatuuril 37 °C. Monoklonaalseid antikehi lahjendati seeriaviisiliselt 3-korda alates 10 ug/ml PBS-is ja inkubeeriti süvendites 1 tund 37 kraadi juures. Seejärel plaate pesti ja inkubeeriti HRP-konjugeeritud kitse inimese IgG-vastase antikehaga (Jackson ImmunoResearch; 109- 035-098), 1:1, 000) 1 tund 37 kraadi juures. Pärast pesemist lisati süvendi kohta 100 μl Super AquaBlue ELISA substraati (eBioscience). Neeldumist mõõdeti 405 nm juures mikroplaadi spektrofotomeetril (Bio-Rad). Analüüsid standardiseeriti, kasutades kontrollantikeha S144-509 (15), mille seondumisomadused olid igal plaadil teada, ja plaate arendati seni, kuni kontrolli neeldumine saavutas OD väärtuseni 3,0. Kõiki mAb-sid testiti kahes eksemplaris ja iga katse viidi läbi kaks korda.
Seerumi ELISA. Kõrge valkudega seonduvad mikrotiiterplaadid kaeti rekombinantsete SARS-CoV-2 spike-antigeenidega kontsentratsioonis 2 ug/ml PBS-is üleöö temperatuuril 4 °C. Plaate pesti PBS-ga 0.05% Tweeniga ja blokeeriti 200 μL PBS-ga 0,1% Tween + 3% lõssipulbrit 1 tund toatemperatuuril (RT). Plasmaproovid inaktiveeriti kuumusega 1 tund temperatuuril 56 kraadi enne seroloogilise katse läbiviimist. Plasma lahjendati seeriaviisiliselt 2-korda PBS 0,1% Tween + 1% lõssipulbriga. Plaate inkubeeriti seerumi lahjendustega 2 tundi toatemperatuuril. Antikehade seondumise tuvastamiseks kasutati HRP-ga konjugeeritud kitse inimese Ig-vastast sekundaarset antikeha, mis oli lahjendatud suhtega 1:3, 000 PBS-iga 0,1% Tween + 1% lõssipulbriga. Pärast 1-tunnist inkubeerimist töötati plaadid välja 100 µl SigmaFast OPD lahusega (Sigma-Aldrich) 10 minutit. Seejärel kasutati arengureaktsiooni peatamiseks 50 μL 3M HCl. Neeldumist mõõdeti 490 nm juures mikroplaadi spektrofotomeetril (Bio-Rad). Lõpp-punkti tiitrid ekstrapoleeriti iga proovi sigmoidse 4PL (kus x on logaritmiline kontsentratsioon) standardkõveralt. Avastamise piir (LOD) on määratletud kui SARS-CoV-eelsete isikute plasmaga salvestatud OD-signaali keskmine + 3 SD. Kõik arvutused viidi läbi GraphPad Prism tarkvaras (versioon 9.0).
Võistlus-ELISA. RBD-reaktiivsete mAb-de sihtepitoopide klassifikatsiooni määramiseks viidi läbi konkureerivad ELISA-d, kasutades konkureerivate mAb-dena teisi teadaolevate epitoobi sidumisomadustega mAb-sid. Konkureerivad mAb-d biotinüüliti, kasutades EZ-Link sulfo-NHS-biotiini (Thermo Fisher Scientific) 2 tundi toatemperatuuril. Biotinüülitud mAb-de liigne biotiin eemaldati 7k molekulmassi piirväärtusega (MWCO) Zeba spin-soolastamiskolonnidega (Thermo Fisher Scientific). Plaadid kaeti öö läbi temperatuuril 4 °C 2 ug/ml RBD antigeeniga. Plaadid blokeeriti PBS-20% FBS-iga 2 tunniks toatemperatuuril ja lisati määramata klassi või seerumi mAb-de 2-kordne lahjendus, alates 20 ug/mL mAb-sid ja seerumi lahjendus 1:10. Pärast antikeha 2-tunnist inkubeerimist toatemperatuuril lisati biotinüülitud konkureeriv mAb kontsentratsioonis, mis ületas kaks korda selle dissotsiatsioonikonstandi (KD) ja inkubeeriti veel 2 tundi toatemperatuuril koos eelnevalt lisatud mAb või seerumiga. Plaate pesti ja inkubeeriti 100 µl HRP-ga konjugeeritud streptavidiiniga (Southern Biotech) lahjenduses 1:1, 000 1 tund 37 kraadi juures. Plaadid töötati välja Super AquaBlue ELISA substraadiga (eBioscience). Analüüside normaliseerimiseks lisati süvendisse konkureeriv biotinüülitud mAb ilma konkureerivate mAb-de või seerumita kontrollina. Andmed registreeriti, kui kontrollkaevu neeldumine saavutas OD 1, 0–1, 5. Seejärel arvutati mAb-de vahelise konkurentsi protsent, jagades proovi vaadeldud OD positiivse kontrolli saavutatud OD-ga, lahutades selle väärtuse 1-st ja korrutades 100-ga. Seerumi puhul transformeeriti OD-d log10 ja analüüsiti mittelineaarse regressiooniga, et määrata 50 Inhibeerimiskontsentratsiooni (IC50) % väärtused, kasutades GraphPad Prism tarkvara (versioon 9.0). Andmed teisendati Log1P-ks ja kanti graafikule, mis esindab seerumi lahjenduse IC50 vastastikust seerumi lahjendust, mis võib saavutada 50% konkurentsi huvipakkuva konkureeriva mAb-ga. Kõiki mAb-sid testiti kahes eksemplaris, iga katse viidi läbi 2 korda sõltumatult ja kahe sõltumatu katse väärtused keskmistati.
Naastude analüüsid. Naastude testid viidi läbi SARS-CoV-2 varianti viirustega Vero E6/TMPRSS2 rakkudel (Jaapani Research Bioresources (JCRB)) (täiendav tabel 5). Rakke kultiveeriti 90% konfluentsuse saavutamiseks enne trüpsiinimist ja külvati 96-süvendiplaatidele tihedusega 3 × 104 rakku süvendi kohta. Järgmisel päeval inkubeeriti 102 PFU SARS-CoV{11}} varianti 2-korda lahjendatud mAb-dega 1 tund. Antikeha-viiruse segu inkubeeriti Vero E6/TMPRSS2 rakkudega 3 päeva temperatuuril 37 °C. Plaadid fikseeriti 20% metanooliga ja värviti seejärel kristallvioletse lahusega. Täielikud inhibeerivad kontsentratsioonid (IC99) arvutati GraphPad Prismi (versioon 9.0) abil, kasutades logaritmi (inhibiitori) versus normaliseeritud reaktsiooni (muutuv kalle). Kõiki mAb-sid testiti kahes eksemplaris ja iga katse viidi läbi kaks korda. Fookuse vähendamise neutraliseerimise test. Fookuse vähendamise neutraliseerimise teste (FRNT) kasutati neutraliseerimistegevuse määramiseks täiendava platvormina naastude analüüsi kõrval. Seerumi seerialahjendused, alustades lõppkontsentratsioonist 1:20, segati 103 fookust moodustava viiruse ühikuga süvendi kohta ja inkubeeriti 1 tund 37 kraadi juures. Pandeemiaeelse seerumi proov toimis kontrollina. Antikeha-viiruse segu inokuleeriti Vero E6/TMPRSS2 rakkudele (JCRB) 96-süvendiga plaatidel ja inkubeeriti 1 tund 37 kraadi juures. Igasse süvendisse lisati võrdne kogus metüültselluloosi lahust. Rakke inkubeeriti 16 tundi 37 kraadi juures ja seejärel fikseeriti formaliiniga. Pärast formaliini eemaldamist värviti rakud hiire mAb-ga SARS-CoV-1/2 nukleoproteiini [kloon 1C7C7 (Sigma-Aldrich)] vastu, millele järgnes HRP-märgistatud kitse hiirevastane immunoglobuliini (Sigma-). Aldrich; A8924). Nakatunud rakud värviti TrueBlue Substraadiga (SeraCare Life Sciences) ja pesti seejärel destilleeritud veega. Pärast kuivatamist kvantifitseeriti fookuse numbrid, kasutades ImmunoSpot S6 Analyzerit, ImmunoCapture tarkvara ja BioSpot tarkvara (Cellular Technology). IC50 arvutati logaritmi (inhibiitori) ja normaliseeritud vastuse interpoleeritud väärtuse põhjal, kasutades muutuva kaldega (4 parameetrit) mittelineaarset regressiooni, mis viidi läbi programmis GraphPad Prism (versioon 9.0).
Viited
1. Hou YJ et al. SARS-CoV-2 D614G variandil on tõhus ex vivo replikatsioon ja in vivo ülekanne. Teadus. 2020;370(6523):1464–1468.
2. Garcia-Beltran WF, et al. Mitu SARS CoV-2 varianti pääseb vaktsiinist põhjustatud humoraalse immuunsuse neutraliseerimisest. Kamber. 2021; 184 (9): 2523.
3. Wall EC et al. SARS-CoV-2 lenduvate orgaaniliste ühendite B.1.617.2 ja B.1.351 vastaste antikehade aktiivsuse neutraliseerimine BNT162b2 vaktsineerimisega. Lancet. 2021;397(10292):2331–2333.
4. Edara VV jt. Infektsioon ja vaktsiinist põhjustatud neutraliseerivate antikehade vastused SARS-CoV-2 B.1.617 variantidele. N Engl J Med. 2021;385(7):664–666.
5. Zhou D, et al. Tõendid SARS-CoV-2 variandi B.1.351 pääsemise kohta looduslikest ja vaktsiinidest põhjustatud seerumitest. Kamber. 2021;184(9):2348–2361.
6. Weisblum Y et al. Põgenege SARS-CoV-2 spike-valgu variantide neutraliseerivate antikehade eest. Elife. 2020;9:e61312.
7. Graham F. Igapäevane infotund: Omicroni koroonaviiruse variant paneb teadlased valvsaks. Loodus. 2021;.
8. Karim SSA, Karim QA. Omicron SARS-CoV-2 variant: uus peatükk COVID-19 pandeemias. Lancet. 2021;398(10317):2126–2128.
9. Carreño JM, et al. Taastusravi ja vaktsiiniseerumi aktiivsus SARS-CoV-2 Omicroni vastu. Loodus. 2021;602(7898):682–688.
10. Wang Q et al. SARS-CoV-2 BQ ja XBB alamvariantide murettekitavad antikehadest kõrvalehoidmise omadused. Kamber. 2022;186(2):279–286.
11. VanBlargan LA et al. Nakkuslik SARS-CoV-2 B.1.1.529 Omicron viirus pääseb neutraliseerimisest terapeutiliste monoklonaalsete antikehadega. Nat Med. 2022;28(3):490–495.
12. Takashita E et al. Antikehade ja viirusevastaste ravimite efektiivsus Covid-19 Omicroni variandi vastu. N Engl J Med. 2022;386(10):995–998.
13. Yuan M, et al. SARS-CoV-2 retseptorit siduva domeeni äratundmine antikehade neutraliseerimise teel. Biochem Biophys Res Commun. 2021;538:192–203.
14. Barnes CO, et al. SARS-CoV-2 neutraliseerivad antikehastruktuurid annavad teavet ravistrateegiate kohta. Loodus. 2020;588(7839):682–687.
15. Changrob S et al. Tekkivate SARS-CoV-2 murettekitavate variantide ristneutraliseerimine antikehadega, mis on suunatud erinevatele epitoopidele. Mbio. 2021;12(6):e0297521.
16. Guthmiller JJ et al. SARS-CoV-2 nakkuse raskusaste on seotud parema humoraalse immuunsusega naelu vastu. Mbio. 2021;12(1):e02940–20.
17. Greaney AJ et al. Mutatsioonide kaardistamine SARS-CoV-2 RBD-ga, mis väldivad erinevate antikehade klasside seondumist. Nat Commun. 2021;12(1):4196.
18. Liu H, Wilson IA. Kaitsvad neutraliseerivad epitoobid SARS-CoV-s-2. Immunol Rev. 2022;310(1):76–92.
19. Jette CA, et al. Laialdane ristreaktiivsus arboviiruste vahel, mida näitab COVID{2}} doonorilt saadud neutraliseerivate antikehade alamhulk. Cell Rep. 2021;36(13):109760.
20. Brouwer PJM et al. COVID{1}} patsientide tugevad neutraliseerivad antikehad määravad haavatavuse mitu sihtmärki. Teadus. 2020;369(6504):643–650.
21. Pinto D et al. SARS CoV-2 ristneutraliseerimine inimese monoklonaalse SARS-CoV antikehaga. Loodus. 2020;583(7815):290–295.
22. Robbiani DF et al. Konvergentsed antikehavastused SARS-CoV-2-le taastuvatel inimestel. Loodus. 2020;584(7821):437–442.
23. Yuan M, et al. SARS-CoV-le jagatud antikehavastuse struktuurne alus-2. Teadus. 2020;369(6507):1119–1123.
24. Dugan HL et al. B-rakkude immunodominantsi profileerimine pärast SARS-CoV-2 nakatumist näitab antikehade evolutsiooni mitteneutraliseerivate viiruse sihtmärkide suhtes. Immuunsus. 2021;54(6):1290–1303.
25. Rogers TF et al. Tugevate SARS CoV{1}} neutraliseerivate antikehade eraldamine ja haiguste eest kaitsmine väikeloommudelil. Teadus. 2020;369(6506):956–963.
26. Schmitz AJ et al. Vaktsiini poolt indutseeritud avalik antikeha kaitseb SARS-CoV-2 ja tekkivate variantide eest. Immuunsus. 2021;54(9):2159–2166.e6.
27. Shi R, et al. Inimese neutraliseeriv antikeha on suunatud SARS-CoV-2 retseptoriga seondumiskohale. Loodus. 2020;584(7819):120–124.
28. Cao Y et al. Tugevad neutraliseerivad antikehad SARS-CoV-2 vastu, mis tuvastati taastuvate patsientide B-rakkude suure läbilaskevõimega üherakulise sekveneerimisega. Kamber. 2020;182(1):73–84.
29. Barnes CO, et al. SARS-CoV-2 tipuga seotud inimese antikehade struktuurid toovad esile antikehade ühised epitoobid ja korduvad tunnused. Kamber. 2020;182(4):828–842.
30. Corbett KS, et al. SARS-CoV-2 mRNA vaktsiini disain, mis on võimaldatud patogeeni prototüübi valmisolekuga. Loodus. 2020;586(7830):567–571.
31. Amanat F et al. Kahe proliini kasutuselevõtt ja mitmealuselise lõhustumiskoha eemaldamine tõi hiiremudelis kaasa rekombinantse piigipõhise SARS-CoV-2 vaktsiini suurema efektiivsuse. mBio. 2021;12(2):e02648–20.
32. Sun W et al. Newcastle'i haiguse viirus, mis ekspresseerib SARS-CoV-2 stabiliseeritud piigivalku, kutsub esile kaitsva immuunvastuse. Nat Commun. 2021;12(1):6197.
33. Hsieh CL et al. Eelfusiooniga stabiliseeritud SARS-CoV-2 tippude struktuuripõhine disain. Teadus. 2020;369(6510):1501–1505.
34. Gobeil SM, et al. SARS-CoV-2 Omicroni tipu struktuurne mitmekesisus. Mol Cell. 2022;82(11):2050–2068.
35. Yuan M, et al. Väga konserveerunud krüptiline epitoop SARS-CoV-2 ja SARS-CoV retseptoriga seonduvates domeenides. Teadus. 2020;368(6491):630–633.
36. Starr TN, et al. Täielik kaart SARS-CoV-2 RBD mutatsioonidest, mis pääsevad monoklonaalsest antikehast LY-CoV555 ja selle kokteilist LY-CoV016-ga. Cell Rep Med. 2021;2(4):100255.
37. Baum A et al. REGN-COV2 antikehad hoiavad ära ja ravivad SARS-CoV-2 nakkust reesusmakaakidel ja hamstrites. Teadus. 2020;370(6520):1110–1115.
38. Wu NC, et al. IGHV3-53 antikehade alternatiivne seondumisviis SARS-CoV-2 retseptori sidumisdomeeniga. Cell Rep. 2020;33(3):108274.
39. Wu Y et al. Inimese neutraliseerivate antikehade mittekonkureeriv paar blokeerib COVID-19 viiruse seondumise selle retseptoriga ACE2. Teadus. 2020;368(6496):1274–1278.
40. Yuan M, et al. Antigeense triivi struktuursed ja funktsionaalsed tagajärjed SARS-CoV-2 hiljutistes variantides. Teadus. 2021;373(6556):818–823.
41. Yan Q et al. Idutee IGHV3-53-kodeeritud RBD-sihtivad neutraliseerivad antikehad esinevad tavaliselt COVID-19 patsientide antikehade repertuaaris. Nakatavad esilekerkivad mikroobid. 2021;10(1):1097–1111.
42. Zhang Q et al. Tugevad ja kaitsvad IGHV3- 53/3-66 avalikud antikehad ja nende ühine põgenemismutant SARS-CoV-2 tipul. Nat Commun. 2021;12(1):4210.
43. Wang Z et al. mRNA vaktsiini poolt esile kutsutud antikehad SARS-CoV-2 ja ringlevate variantide vastu. Loodus. 2021;592(7855):616–622.
44. Simon V et al. PARIIS ja SPARTA: SARS-CoV Achilleuse kanna leidmine-2. mSphere. 2022;7(3):e0017922.
45. Starr TN, et al. SARS-CoV-2 RBD antikehad, mis maksimeerivad laiuse ja resistentsuse põgenemisel. Loodus. 2021;597(7874):97–102.
46. Seinad AC, et al. SARS-CoV-2 spike-glükoproteiini struktuur, funktsioon ja antigeensus. Kamber. 2020;181(2):281–292.
47. Henderson R, et al. SARS-CoV-2 spike-glükoproteiini konformatsiooni kontrollimine. Nat Struct Mol Biol. 2020;27(10):925–933.
48. Shrestha LB, et al. Laialdaselt neutraliseerivad antikehad tekkivate SARS-CoV-2 variantide vastu. Front Immunol. 2021;12:752003.
49. Greaney AJ et al. mRNA-1273 vaktsineerimisega esile kutsutud antikehad seonduvad retseptoriga seonduva domeeniga laiemalt kui SARS-CoV-2 nakkuse antikehad. Sci Transl Med. 2021;13(600):eabi9915.
50. Reincke SM, et al. SARS-CoV-2 beetavariandi infektsioon kutsub esile tugevaid liinispetsiifilisi ja ristreaktiivseid antikehi. Teadus. 2022;375(6582):782–787.
51. Wrammert J et al. Inimese B-rakkude vastuses 2009. aasta pandeemilise H1N1 gripiviiruse nakkuse vastu domineerivad laias laastus ristreaktiivsed antikehad. J Exp Med. 2011;208(1):181–193.
52. Guthmiller JJ et al. Esimene kokkupuude pandeemilise H1N1 viiruse poolt indutseeritud laialdaselt neutraliseerivate antikehadega, mis on suunatud hemaglutiniini peaepitoopidele. Sci Transl Med. 2021;13(596):eabg4535.
53. Bajic G et al. Gripi antigeenitehnoloogia keskendub immuunvastustele subdominantsele, kuid üldiselt kaitsvale viiruse epitoobile. Peremeesraku mikroob. 2019;25(6):827–835.
54. Nachbagauer R et al. Kimäärne hemaglutiniinil põhinev universaalne gripiviiruse vaktsiini lähenemisviis kutsub randomiseeritud platseebokontrollitud I faasi uuringus esile laia ja pikaajalise immuunsuse. Nat Med. 2021;27(1):106–114.
55. Angeletti D et al. Ulatuslik immunodominantsus, et sihtida subdominantseid laias laastus neutraliseerivaid epitoope. Proc Natl Acad Sci US A. 2019;116(27):13474–13479.
56. Guthmiller JJ et al. Tõhus meetod monoklonaalsete antikehade genereerimiseks inimese B-rakkudest. Meetodid Mol Biol. 2019;1904:109–145.
57. Amanat F et al. Seroloogiline test SARS-CoV-2 serokonversiooni tuvastamiseks inimestel. Nat Med. 2020;26(7):1033–1036.
58. Stadlbauer D et al. SARS-CoV-2 serokonversioon inimestel: üksikasjalik protokoll seroloogiliseks testiks, antigeeni tootmiseks ja testi seadistamiseks. Curr Protoc Microbiol. 2020;57(1):e100.
59. Torres JL et al. Struktuursed ülevaated väga tõhusast pan-neutraliseerivast SARS-CoV-2 inimese monoklonaalsest antikehast. Proc Natl Acad Sci USA. 2022;119(20):e2120976119.
60. Suloway C, et al. Automatiseeritud molekulaarmikroskoopia: uus Leginoni süsteem. J Struct Biol. 2005;151(1):41–60.
61. Lander GC et al. Appion: integreeritud andmebaasipõhine torujuhe EM-kujutise töötlemise hõlbustamiseks. J Struct Biol. 2009;166(1):95–102.
62. Voss NR, et al. DoG Picker ja TiltPicker: tarkvaratööriistad, mis hõlbustavad osakeste valimist üheosakese elektronmikroskoopias. J Struct Biol. 2009;166(2):205–213.
63. Pettersen EF, et al. UCSF Chimera{1}}visualiseerimissüsteem uurimuslikuks uurimistööks ja analüüsiks. J Comput Chem. 2004;25(13):1605–1612.
64. Punjani A jt. Ebaühtlane viimistlemine: adaptiivne seadustamine parandab üheosakese krüo-EM rekonstrueerimist. Nat meetodid. 2020;17(12):1214–1221.
65. Zhang K. Gctf: Reaalajas CTF-i määramine ja korrigeerimine. J Struct Biol. 2016;193(1):1–12.
66. Zivanov J et al. Uued tööriistad kõrge eraldusvõimega krüo-EM-struktuuride automaatseks määramiseks rakenduses RELION-3. Elife. 2018;7:e42166.
67. Casanal A et al. Praegused arengud elektronkrüo-mikroskoopia ja kristallograafiliste andmete makromolekulaarse mudeli ehitamiseks. Protein Sci. 2020;29(4):1069–1078.
68. Frenz B et al. Glükoproteiini struktuuride vigade automaatne parandamine rosettaga. Struktuur. 2019;27(1):134–139.
69. Klaholz BP. Aatomimudelite tuletamine ja täiustamine kristallograafias ja krüo-EM-is: uusimad Phenixi tööriistad struktuurianalüüsi hõlbustamiseks. Acta Crystallogr D Struct Biol. 2019;75 (pt 10):878–881.
70. Pettersen EF, et al. UCSF ChimeraX: struktuuride visualiseerimine teadlastele, koolitajatele ja arendajatele. Protein Sci. 2021;30(1):70–82.
71. Otwinowski Z, Minor W. Võnkerežiimis kogutud röntgendifraktsiooniandmete töötlemine. Meetodid Enzymol. 1997;276:307–326.
72. McCoy AJ et al. Phaser kristallograafia tarkvara. J Rakendus Crystallogr. 2007; 40 (pt 4): 658–674.
73. Qiang M et al. SARS CoV{1}} neutraliseerivad antikehad valiti aastakümneid tagasi ehitatud inimese antikehade raamatukogust. Adv Sci (Weinh). 2022;9(1):e2102181.
74. Emsley P, Cowtan K. Coot: mudelite koostamise tööriistad molekulaargraafika jaoks. Acta Crystallogr D Biol Crystallogr. 2004; 60 (pt 12 pt 1): 2126–2132.
75. Adams PD et al. PHENIX: terviklik Pythonil põhinev süsteem makromolekulaarse struktuuri lahenduste jaoks. Acta Crystallogr D Biol Crystallogr. 2010; 66 (pt 2): 213–221.
76. Montiel-Garcia D, et al. Epitoopide analüsaator: struktuuripõhine veebitööriist laialdaselt neutraliseerivate epitoopide analüüsimiseks. J Struct Biol. 2022;214(1):107839.
