Kortikosteroidide signaalide seksuaalne dimorfism neerude arengu ajal
Mar 26, 2022
Abstraktne:Seksuaalne dimorfism hõlmab bioloogiliste sugude vahelisi erinevusi, mis lähevad kaugemale seksuaalomadustest. Imetajatel on tõestatud sugudevahelised erinevused seoses erinevate bioloogiliste protsessidega, sealhulgas vererõhu ja eelsoodumusega hüpertensiooni tekkeks varases täiskasvanueas, mis võib sõltuda varastest sündmustest arengu ja vastsündinu perioodil. Hiljutised uuringud näitavad, et kortikosteroidide signaaliradadel (mis hõlmavad glükokortikoidide ja mineralokortikoidide signaaliülekandeteid) on selle spetsiifilise ajalise akna ajal soost sõltuv koespetsiifiline ekspressioon ja regulatsioon, eritineerud. Selles ülevaates tuuakse välja tõendid soolise erineva ekspressiooni ja neerukortikosteroidide signaaliradade aktiveerimise kohta imetaja lootel ja vastsündinul, hiirtest inimeseni, mis võivad soodustada mineralokortikoidide signaaliülekannet naistel ja glükokortikoidide signaaliülekannet meestel. Selliste erinevuste mõju kindlaksmääramine võib selgitada lühi- ja pikaajalisi patofüsioloogilisi tagajärgi, eriti meestel.
Märksõnad:aldosteroon; kortisool; mineralokortikoidi ja glükokortikoidi retseptorid; vastsündinud;neerud; arendamine;seksuaalnedimorfism
Kontakt:ali.ma@wecistanche.com

Klõpsake maca ginseng cistanche merihobune neerufunktsiooni jaoks
1. Sissejuhatus
Kortikosteroidid (mineraalkortikosteroidid ja glükokortikosteroidid) on olulised hormoonid, mis on seotud paljude kudede funktsiooniga homöostaasi säilitamiseks. Nende peamised toimed sõltuvad nende seondumisest mineralokortikoidi ja glükokortikoidi retseptoritega (vastavalt MR ja GR). Hiljutised uuringud on rõhutanud teatud ajalist akentneerudareng, mis on imetajate vahel hästi säilinud, kus kortikosteroidide signaaliradadel on spetsiifiline ekspressiooni- ja regulatsioonimuster, mis on seotud loote ja vastsündinu kohanemisega, üleminekuga veest õhukeskkonda. Selles ülevaates kirjeldatakse esmalt mineralokortikoidide ja glükokortikoidide signaaliülekanderadu (aldosterooni ja kortisooli biosünteesist kuni MR ja GR reguleerimise ja toime mehhanismideni).neerudarengut. Erilist rõhku pannakse hiljutistele uuringutele, mis tõstavad esile seksuaalselt dimorfset väljendust, millel võib olla patofüsioloogiline mõju, eriti meestel/poistel, kellel on vastsündinu perioodil suurenenud kohanemisraskused ja kellel on suurem risk varase hüpertensiooni tekkeks hilisemas elus.
2. Mineralokortikoidi signaalirada
2.1. Aldosterooni sünteesi reguleerimine
Aldosteroon, steroidhormoon, mida eritab neerupealiste koore välimine kiht Zona Glomerulosa (ZG), on naatriumi peetuse kaudu ülioluline kehavedelike ja elektrolüütide homöostaasi säilitamiseks ja seeläbi vererõhu kontrollimiseks [1]. Kuna neerupealiste ZG ei suuda pärast selle tootmist aldosterooni säilitada, on selle sekretsiooni reguleerimine lahutamatult seotud nii transkriptsioonilise aktivatsiooni kui ka steroidogeensete ensüümide transkriptsioonijärgsete modifikatsioonidega. Ägeda aldosterooni tootmist kontrollib kolesterooli omastamise ja pregnenolooniks muutumise varajane regulatiivne etapp, mida vahendab steroidogeense ägeda regulatoorse valgu StAR (kodeeritud STAR geeniga) suurenenud ekspressioon ja fosforüülimine. Hiline regulatiivne etapp, mis kontrollib biosünteesi ensüümide, eriti CYP11B2 (aldosterooni süntaas, mida kodeerib CYP11B2 geen), ekspressiooni, reguleerib kroonilist aldosterooni tootmist [2]. Aldosterooni biosünteesi ZG-s reguleerivad füsioloogiliselt angiotensiin II (Ang II), kaalium (K pluss) ja vähemal määral adrenokortikotroopne hormoon (ACTH). Aldosterooni sekretsiooni stimuleerivad ka teised bioaktiivsed ühendid (serotoniin, leptiin, endoteliin, lämmastikoksiid, katehhoolamiinid, kodade natriureetiline peptiid, neuropeptiid P) adipotsüütide, nuumrakkude, kromafiinirakkude või ZG-rakkude lähedal asuvate närvilõpmete kaudu. 3,4]. Reniin-angiotensiini süsteemi (RAS) stimuleerimine algab sümpaatilise aktiivsuse suurenemisest, perfusioonirõhu langusest neeru aferentsetes arterioolides või naatriumisisalduse vähenemisest neerude distaalsete tuubulite makula densas, mis viib reniini vabanemiseni juxtaglomerulaarsetest rakkudest. . Seejärel muudab reniin ringleva maksas toodetud angiotensinogeeni angiotensiin I-ks (Ang I), mis seejärel lõhustatakse angiotensiini konverteeriva ensüümi (ACE) toimel, moodustades oktapeptiidi Ang II. Ang II seondumine selle AT1 retseptoriga (AT1R) vallandab kaltsiumi vabanemise rakusisestest varudest, mis on aldosterooni sekretsiooni peamine määraja [3]. Väike ekstratsellulaarse K pluss depolariseerib glomeruloosrakku, suurendades ka kaltsiumi sissevoolu pingepõhiste kaltsiumikanalite kaudu, mis stimuleerivad CYP11B2 ja StAR transkriptsiooni [5]. Lõpuks stimuleerib ACTH üksi aldosterooni sekretsiooni ägedalt ja mööduvalt, kuid vähemal määral kui Ang II ja K plus. ACTH seondumine selle melanokortiini retseptoriga 2 (MC2R) stimuleerib StAR ekspressiooni adenülaattsüklaasi aktiveerimise kaudu [6]. Arengu ajal toimub loote aldosterooni tootmine lõplikus tsoonis, mis on täiskasvanu neerupealise koore ZG vaste. Kui StAR ja teiste oluliste ensüümide ekspressioon tõuseb raseduse ajal järk-järgult [7], siis CYP11B2 ekspressioon ilmneb alles umbes 24. rasedusnädalal (GW) [8]; seejärel suureneb see, jõudes sündides samale tasemele kui täiskasvanud neerupealistes [9]. Aldosterooni tuvastatav plasmakontsentratsioon on enneaegsetel vastsündinutel juba 25 GW [10], kuid aldosterooni tootmine jääb madalaks kuni 30 GW [9]. Aldosterooni kontsentratsioon suureneb seejärel kuni sünnituseni [10] seoses loote neosünteesiga [11]. Seksuaalset dimorfismi ei ole täheldatud plasma aldosterooni taseme osas lootel ega sünnihetkel [12].
2.2. Mineralokortikoidi retseptor (MR)
2.2.1. Geen, transkriptid ja valgu variandid
MR kuulub tuumaretseptorite superperekonda, mis vahendab aldosterooni naatriumi säilitavat toimet distaalses nefronis [13]. Seda transkriptsioonifaktorit kodeerib NR3C2 geen, mis asub inimestel lookuses 4q31.1–4q31.2 [14,15] ja kodeerib 984 aminohappest koosnevat valku (≈107 kDa) [16], mis on organiseeritud neljaks erinevaks. struktuursed domeenid: N-terminaalne domeen (NTD), DNA sidumisdomeen (DBD), hingepiirkond ja ligandi siduv domeen (LBD). Näidati, et MR-funktsioone moduleerivad splaissinguvariandid, millel puudus kas ekson 6 või mõlemad eksonid 5 ja 6 [17, 18]. Inimese MR kaks peamist varianti, nimega MRA ja MRB, genereeritakse vastavalt metioniini 1 ja 15 translatsiooni alternatiivsete initsiatsioonikohtade kaudu. Nendel MR-variantidel on erinev transaktiveerimisvõime in vitro [19].
2.2.2. MR ekspressiooni ja aktiivsuse reguleerimise mehhanismid
Kaks alternatiivset promootorit juhivad NR3C2 geeni ekspressiooni [20], proksimaalne P1 promootor, mis on transkriptsiooniliselt aktiivne kõigis MR sihtkudedes ja distaalne P2 promootor, mis on nõrgem ja transkriptsiooniliselt aktiivne kesknärvisüsteemis teatud arenguetappidel või füsioloogilised olukorrad [21]. Eriti huvitav on see, et selle tuumaretseptori, mis transkriptsiooniliselt reguleerib vee ja naatriumi tasakaalu, ekspressiooni kontrollitakse ka transkriptsioonijärgsel tasemel osmootse tooniga, eriti nefroni distaalsetes osades, kus valitsevad suured rakuvälise toonilisuse variatsioonid [22]. ]. Tõepoolest, MR-i transkripti tase langeb hüpertoonilisuse korral pärast RNA-d siduva valgu (RBP) Tis11b (tetradekanoüülforbolatsetaadiga indutseeritav järjestus 11b) värbamist, mis interakteerub füüsiliselt MR-i transkripti 30 -transleerimata piirkonnaga (30 -UTR). , moduleerides seega selle mRNA käivet vastuseks osmootsele stressile [23]. Vastupidi, MR transkripti tase tõuseb hüpotoonsuse korral tänu inimese antigeeni R (HuR) värbamisele, teise RBP, mis interakteerub MR 30 -UTR-ga neerurakkude tsütoplasmas, et stabiliseerida ja suurendada MR taset, moduleerides seeläbi. MR signaalimine [24]. Koguvad tõendid rõhutavad nüüd mikroRNA-de (miRNA-de), mis on täiendav transkriptsioonijärgsete regulaatorite klass, keskset rolli MR-i ekspressiooni kontrollimisel neerudes [25, 26]. Lisaks nendele regulatiivsetele mehhanismidele moduleerivad MR aktiivsust ja signaaliülekannet ka translatsioonijärgsed modifikatsioonid, nagu ubikvitüülimine, SUMOüülimine, fosforüülimine ja atsetüülimine [13, 27].

3. Glükokortikoidi signaalirada
3.1. Glükokortikoidhormoonid ja hüpotalamuse-hüpofüüsi-neerupealise telg
Glükokortikoidhormoonid (närilistel kortisool ja kortikosteroon) on neuroendokriinsüsteemi hüpotalamuse-hüpofüüsi-neerupealise (HPA) telje efektorhormoonid ja neid toodab neerupealise Zona fasciculata (ZF). Nagu kõigi steroidhormoonide puhul, algab kortisooli süntees kolesteroolist ja sõltub kriitiliselt StAR-valgust, mis hõlbustab kolesterooli kiiret väljavoolu mitokondritesse. Seejärel lõikab CYP11A1 geeni poolt kodeeritud mitokondriaalne ensüüm tsütokroom P450scc kolesterooli külgahela pregnenolooniks. Pregnenoloon difundeerub passiivselt endoplasmaatilisesse retikulumi ja muundatakse progesterooniks 2–3 -hüdroksüsteroiddehüdrogenaasi/∆5-∆4 isomeraasi (3 HSD2) toimel, mida kodeerib HSD3B2 geen. P450c17 spetsiifiline ekspressioon (kodeeritud CYP17A1 geeni poolt) katalüüsib progesterooni 17 -hüdroksüülimist 17OH progesterooniks (17OHP). Seejärel muundatakse 17OHP mikrosomaalse P450c21 ja mitokondriaalse P450c11 (kodeerib CYP11B1 geen) abil järjestikku 11-deoksükortisooliks ja seejärel kortisooliks. Närilistel puudub ZF-s P450c17 ning progesteroon 21- ja 11 -hüdroksüüleeritakse, et saada kortisooli asemel kortikosteroon, mis on nende liikide domineeriv glükokortikoid [2]. Glükokortikoidide süntees on sünnieelsetes ja postnataalsetes neerupealistes erinevalt reguleeritud. Täiskasvanutel kontrollib glükokortikoidide tootmist kriitiliselt HPA telje aktiivsus. Erinevad stiimulid, nagu stress, haigus või ööpäevarütm, aktiveerivad kortikotropiini vabastava hormooni (CRH) vabanemist hüpotalamusest, mis stimuleerib hüpofüüsi eesmist osa, vabastades ACTH. ACTH mõjutab MC2R-i neerupealiste ZF-s, indutseerides kortikosteroidide sünteesi kolesteroolist. Tsirkuleerivad glükokortikoidid avaldavad omakorda tagasisidet reguleerivat toimet hüpotalamusele ja hüpofüüsile, pärssides vastavalt CRH ja ACTH vabanemist [2]. Loote neerupealised on võimelised steroidogeneesiks varsti pärast nende moodustumist 7. GW paiku. Samal ajal hakkab hüpofüüs tootma ACTH-d. Kortisooli sekretsioon suureneb kuni 8–9 GW; seejärel väheneb see kuni 14 GW. See tsükliline glükokortikoidide sekretsioon loote neerupealiste poolt ei ole ACTH kontrolli all, nagu täiskasvanutel [28]. Tõepoolest, ACTH tase jääb sel perioodil konstantseks ja stimuleerib neerupealisi androgeene tootma. 3 HSD2 ekspressioon, mis saavutab maksimumi 9 GW juures, väheneb seejärel suurema osa teisest trimestrist, mis viib glükokortikoidide sünteesi vähenemiseni. 24 GW juures taastub 3 HSD2 ekspressioon ja glükokortikoidide sekretsioon. Kortisool tõuseb sünnituseelsetel nädalatel ja mängib olulist rolli mitmete elundite, näiteks kopsude, diferentseerumisel ja funktsionaalsel arengul [29]. Arvatakse, et HPA telje aktiivsuse seksuaalne dimorfism esineb varases lapsepõlves. Metaanalüüsis väideti, et HPA telje basaalaktiivsus on suurem enne 8-aastastel poistel, mida hinnati sülje kortisooli taseme järgi [30]. 8 aasta pärast näis see suundumus pöörduvat, mis viitab kortisooli metabolismi soopõhisele arengule puberteedieas [31] ja varajase elu programmeerimise võimalikule mõjule [32]. Siiski ei täheldatud sündimisel erinevusi tüdrukute ja poiste kortisooli baastasemes plasmas [33]. Kortisooli metabolism sõltub maksa A-tsükli reduktaaside (5- ja 5- -reduktaas) ja 11-beeta-hüdroksüsteroiddehüdrogenaasi (11 HSD) isoensüümide aktiivsusest. Ensüümi 11 HSD1 ekspresseeritakse peamiselt maksas ja rasvkoes ning see regenereerib kortisooli selle inaktiivsest ühendist kortisoonist. Ensüüm 11 HSD2 katalüüsib pöördreaktsiooni neeruepiteelirakkudes (vt lõik 4.2). Täiskasvanueas leiti, et naistel on kortisooli metaboliitide uriiniga eritumise kiirus meestega võrreldes väiksem, mis oli tingitud väiksemast A-ringi vähenemisest [34]. See sooline erinevus kortisooli metabolismis saab alguse puberteedieas, 10–11-aastaselt [31,35] ja see püsib eakatel isikutel, mis viitab regulatiivsetele mehhanismidele, mis on osaliselt sõltumatud sugunäärmete steroididest [36].
3.2. Glükokortikoidi retseptor
3.2.1. Geen, transkriptid ja valgu variandid
GR on tuumaretseptorite superperekonna asutajaliige. See transkriptsioonifaktor, mis sarnaneb MR-ga, sisaldab 4 peamist domeeni, NTD, DBD, LBD ja hingepiirkonda (HR) DBD ja LBD vahel [37]. Seda kodeerib inimestel kromosoomis 5 (5q31) asuv geen NR3C1. NR3C1 geen sisaldab vähemalt 10 eksonit [38]. Eksoni 9 alternatiivne splaissimine tekitab valgu kaks peamist varianti: GR, mis on aktiivne ligandist sõltuv variant, ja GR, mis on ligandist sõltumatu variant, millel on domineeriv-negatiivne toime [39]. GR on 777 aminohappe pikkune valk [40]. GR-valk sisaldab saite translatsioonijärgsete modifikatsioonide jaoks, nagu SUMOüülimine või fosforüülimine, mis mõjutavad selle transaktiveerimisvõimet. 3.2.2. GR ekspressiooni ja aktiivsuse reguleerimise mehhanismid GR esineb praktiliselt kõigis rakkudes, kuid tundlikkus glükokortikoidide suhtes on kudedest sõltuv ja osaliselt vahendatud GR ekspressiooni reguleerimise kaudu. Seda regulatsiooni vahendavad transkriptsiooni tasemel kaks peamist mehhanismi: 1. eksoni alternatiivne splaissimine ja N-terminaalse domeeni pikkuse varieeruvus. Esimene ja transleerimata ekson sisaldab üheksat liikide vahel hästi säilinud splaissingu doonorsaiti, mis vastavad eksoni 2 [41] splaissingu retsipientsaitidele, millest igaüks on spetsiifilise promootori kontrolli all. Selle varieeruvuse tulemuseks on alternatiivsed mRNA isovormid, mis erinevad oma 50 -UTR piirkondade poolest. Nende mRNA isovormide ekspressioon on koespetsiifiline. 2. ekson sisaldab kaheksat erinevat stardikoodonit, mis kodeerivad kaheksat GR-i varianti (GR-A, GR-B, GR-C1, GR-C2, GR-C3, GR-D1, GR-D2 ja GR-D3). . Nendel variantidel on ligandi suhtes võrdne afiinsus, kuid need erinevad transaktivatsioonivõime ja sihtgeenide poolest, ainult<10% of="" them="" common="" to="" all="" variants="" [42].="" 4.="" mechanism="" of="" corticosteroids="" action="" in="" renal="" principal="" cells="" 4.1.="" subcellular="" distribution="" in="" renal="" principal="" cells,="" corticosteroid="" hormones="" enter="" by="" passive="" diffusion="" and="" bind="" their="" respective="" receptor:="" aldosterone="" to="" the="" mr="" and="" cortisol="" (or="" corticosterone)="" to="" the="" gr.="" in="" the="" absence="" of="" ligands,="" corticosteroid="" receptors="" are="" associated="" with="" chaperone="" proteins="" [43–46],="" which="" protect="" receptors="" from="" degradation="" and="" maintain="" a="" conformation="" suitable="" for="" binding="" to="" ligands.="" thereafter,="" the="" binding="" of="" either="" ligand="" induces="" the="" dissociation="" of="" these="" chaperone="" proteins="" and="" conformational="" changes="" of="" mr="" and="" gr.="" 4.2.="" mineralocorticoid="" selectivity="" given="" the="" homology="" existing="" between="" the="" structure="" of="" aldosterone="" and="" cortisol/="" corticosterone,="" the="" high="" homology="" between="" mr="" and="" gr="" (their="" dbd="" and="" lbd="" have="" 94%="" and="" 57%="" homology,="" respectively="" [47]),="" and="" similar="" affinity="" of="" both="" receptors="" for="" glucocorticoid="" hormones,="" mr="" would="" be="" expected="" to="" be="" permanently="" occupied="" by="" glucocorticoid="">
Tõepoolest, kortisooli plasmakontsentratsioonid on kuni 100–1000 korda kõrgemad kui aldosterooni kontsentratsioonid imetajatel. MR-i ebaseaduslikku hõivamist glükokortikoidhormoonidega piirab aga neerupealistes ja teistes epiteelirakkudes 11 HSD2 [48–50]. See ensüüm oksüdeerib glükokortikoidhormoonide süsiniku 11 poolt kantava alkoholifunktsiooni ketoonfunktsiooniks, luues seega 11 dehüdrogeenitud derivaati (inimestel kortisoon ja närilistel 11-dehüdrokortikosteroon), millel on vähene afiinsus MR või isegi MR suhtes. GR [48]. Seega võimaldab 11 HSD2 aldosteroonil epiteelirakkudes selektiivselt mõjutada MR-i, et avaldada oma bioloogilist mõju naatriumi reabsorptsioonile (joonis 1). Lisaks võib MR eristada ka aldosterooni ja kortisooli, kuna glükokortikoidide dissotsiatsioonikiirus on palju kiirem kui aldosterooni puhul. NTD ja LBD vahelised erinevad interaktsioonid tekivad seetõttu, et aldosterooni-MR kompleksi struktuurne konformatsioon on kuidagi erinev glükokortikoidi-MR kompleksi omast [51]. Lõpuks on näidatud, et ligandi olemus võib samuti muuta ligandi-retseptori kompleksi ja DNA-le reageerivate elementide vahelise interaktsiooni tsüklilisust [52].
4.3. Promootori sidumine ja kaasregulaatorite värbamine
Tuumasse sattudes seostub aldosterooni-MR kompleks enamasti homodimeeridena MR-i sihtgeenide regulatoorsetes piirkondades asuvate mineralokortikoidi vastuse elementidega (MRE-dega) [53]. Seejärel interakteerub MR tsüklilisel, järjestikusel ja/või kombinatoorsel viisil [52] transkriptsiooni kaasregulaatorite [54] ja mõnede põhiliste transkriptsioonifaktorite või masinakomponentidega, et tõhustada transkriptsioonilist aktivatsiooni ja hõlbustada kromatiini ümberkujundamist, mis hõlmab histooni atsetüülimist/metüleerimist. [53]. Huvitaval kombel kasutasid Le Billan jt HK GFP-MR rakke, inimese neeru rakuliini, millel puudub 11 HSD2, et dešifreerida MR/GR ja aldosterooni/kortisooli panus neerukortikosteroidide signaaliülekandesse. Need autorid esitasid tõendeid selle kohta, et MR ja GR interakteeruvad dünaamiliselt ja tsükliliselt sama sihtpromootoriga Period tsirkadiaanvalgu 1 (PER1) geenis spetsiifilise ja erineva transkriptsioonisignatuuriga, seondudes homo- või heterodimeeridena [52]. Tuumas võib GR siduda ka spetsiifilisi järjestusi, mida nimetatakse glükokortikoidi vastuse elementideks (GRE). Igas rakutüübis seob GR erinevaid GRE-sid. Seondumine GRE-ga aktiveerib kromatiini remodelleerivate komplekside ja kaasregulaatorite, näiteks steroidiretseptori koaktivaatori -1 (SRC-1), värbamise, mis võimaldab moodustada transkriptsiooni initsiatsioonikompleksi. Samuti teatati negatiivsest GRE-st (nGRE), mis vastutavad sihtgeenide trans-represseerimise eest. Seondumine nGRE-ga takistab dimeriseerumist ja võimaldab värvata korepressoreid, nagu NCoR või SMRT [55]. GR võib samuti vahendada sihtgeenide trans-represseerimist, sidudes neid, nagu on kirjeldatud MR-i jaoks [53], interaktsioonide kaudu teiste transkriptsioonifaktoritega, nagu NF-κB või AP-1, ilma DNA-ga otseselt seondumata [56].
4.4. MR ja GR sihtgeenid
Aldosteroonitundlikus nefronis osaleb MR soolade tasakaalu kontrollis, stimuleerides ioonsete transporterite, nagu epiteliaalne Na pluss kanal (ENaC) [57] ja Na pluss, K pluss -ATPaasi pump [58], ekspressiooni. Need transporterid võimaldavad naatriumi transepiteliaalset reabsorptsiooni luumenist interstitsiumi. Aldosteroon stimuleerib MR aktiveerimise kaudu ka seerumi varajast ekspressiooni ja glükokortikoididega reguleeritud kinaasi 1 (SGK1) [59], mis fosforüülib ubikvitiini ligaasi Nedd4-2, mis omakorda kontrollib ENaC väljavõtmist apikaalsest membraanist. . Neerudes on tuvastatud ka teisi sihtgeene, sealhulgas seriini/treoniini kinaas ilma lüsiin-K kinaasi (KS-WNK1) [60], N-myc allareguleeritud geen 2 (NDRG2) [61], glükokortikoid- Indutseeritud leutsiini tõmblukkvalk (GILZ) [62], mis mängib samuti keskset rolli aldosterooni vastuste varases faasis [13] (joonis 1). Hiljuti näidati, et aldosteroon reguleerib neerude naatriumi reabsorptsiooni rütmilisust, stimuleerides PER1 geeni varajast ekspressiooni [63]. Samuti teatati, et MR võib sidumismehhanismide kaudu kaudselt seostuda teiste transkriptsioonifaktorite (FOX, EGR1, AP1, PAX5) äratundmismotiividega, nagu on kirjeldatud GR puhul, võimaldades seega sihtgeeni ekspressiooni moduleerimist [53]. Täiskasvanute neerudes, kuna 11 HSD2 ekspressioon on kõrge, ei ole põhitingimustes oodata GR signaaliülekande olulist mõju [64].
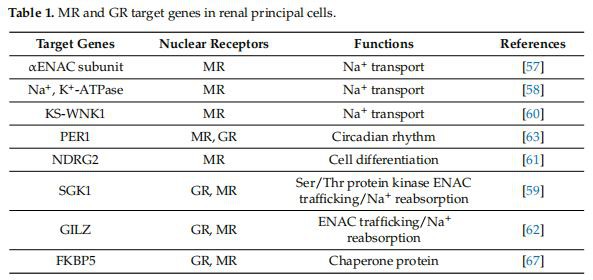
Oluline on see, et meie rühm on hiljuti tuvastanud neerude arengu ajal spetsiifilise ajalise akna, mille jooksul see MR-i signaalimine on MR-i ekspressiooni alareguleerimise tõttu ebaefektiivne [65]. Seetõttu, arvestades, et neerude 11 HSD2 ei ekspresseeru sellel spetsiifilisel perinataalsel perioodil, peaks GR-i signaaliülekanne toimima neerude põhirakkudes, kusjuures plasma kortisooli tase on vastsündinutel tuvastatav füsioloogilistes kogustes, mis on sarnased täiskasvanute tasemega [66]. Selles kontekstis aktiveerib GR tõenäoliselt nii spetsiifilisi neeru sihtgeene kui ka ühiseid sihtgeene MR-i omadega, sealhulgas SGK1 või GILZ. GR- ja MR-spetsiifilised sihtgeenid neerude põhirakkudes on kokku võetud tabelis 1.
Joonis 1. Mineralokortikoidi ja glükokortikoidi signaaliülekanne neeru põhirakkudes. Kortikosteroidhormoonid sisenevad passiivse difusiooni teel ja seovad oma vastava retseptori: aldosteroon MR-ga ja kortisool/kortikosteroon GR-ga. Ligandide puudumisel on kortikosteroidi retseptorid seotud chaperone valkudega. Seejärel kutsub kummagi ligandi seondumine esile nende chaperone-valkude dissotsiatsiooni ning MR-i ja GR-i konformatsioonilisi muutusi. Tuumas seostub aldosterooni/MR-kompleks enamasti homodimeeridena mineralokortikoidi vastuse elementidega (MRE). Seejärel interakteerub MR tsüklilisel, järjestikusel ja/või kombinatoorsel viisil transkriptsiooni kaasregulaatorite ja mõnede põhiliste transkriptsioonifaktorite või masinakomponentidega, et tõhustada sihtgeenide transkriptsiooni, sealhulgas epiteeli Na pluss kanal (ENaC), Na plus. , K pluss -ATPaasi pump. Aldosteroon stimuleerib ka seerumi ja glükokortikoidiga reguleeritud kinaasi 1 (SGK1), lüsiin-K kinaasita seriini/treoniini kinaasi (KS-WNK1), N-myc allareguleeritud geeni 2 (NDRG2) ja glükokortikoidi varajast ekspressiooni. -Indutseeritud leutsiini tõmblukkvalk (GILZ). Hiljuti näidati, et aldosteroon stimuleerib tsirkadiaankella geeniperekonda kuuluva PER1 geeni varajast ekspressiooni. Samuti teatati, et MR võib sidumismehhanismide kaudu kaudselt seostuda teiste transkriptsioonifaktorite (FOX, EGR1, AP1, PAX5) äratundmismotiividega. Peamistes neerurakkudes muudab 11 HSD2 glükokortikoidhormoonid kortisooniks või 11-dehüdrokortikosterooniks, millel on vähene või puudub afiinsus MR või isegi GR suhtes. Seega võimaldab 11 HSD2 aldosteroonil selektiivselt mõjutada MR-i, et avaldada oma bioloogilist mõju naatriumi reabsorptsioonile. Lisaks ei ole GR aktiveeritud või on nõrgalt aktiveeritud.MR: Mineralokortikoidi retseptor; GR: glükokortikoidi retseptor; MRE: Mineralokortikoidi reageerimise element; GILZ: glükokortikoididest põhjustatud leutsiini tõmblukk; ENaC: epiteeli Na pluss kanal; Sgk 1: seerumi ja glükokortikoididega reguleeritud kinaas 1; KS-WNK1: ilma lüsiin-K kinaasita; NDRG2: N-mycDown-reguleeritud geen 2; PER 1: kella geeniperiood 1; TM: Transkriptsioonimasinad.

5. Kortikosteroidide signaalide seksuaalne dimorfism peale neeru
Mitmed uuringud on andnud tõendeid MR-i ja GR-i soolise erineva ekspressiooni ja aktiveerimise kohta. Näiteks näidati, et korduv sünnituseelne glükokortikoidravi programmeerib HPA funktsiooni soopõhiselt ja need muutused olid seotud MR-i ja GR-i ekspressiooni muutumisega täiskasvanud ajus ja hüpofüüsis [68]. Arengu käigus täheldasid samad autorid GR mRNA vähenemist paraventrikulaarses tuumas, MR mRNA ja MR valgu vähenemist hipokampuses ning GR mRNA ja GR valgu suurenemist hipokampuses. Merisigadel vähendasid emalt manustatud glükokortikoidid loote plasma ACTH ja kortisooli kontsentratsiooni ning mõjutasid oluliselt hipokampuse MR valgu ekspressiooni ning see toime oli suurim meestel. Soolised erinevused GR ja MR ekspressiooni mustris arengu ajal võivad viidata erinevatele haavatavuse akendele sünnieelse glükokortikoidide kokkupuute suhtes loote elus [69]. Samuti näidati, et need kortikosteroidi retseptorid mängivad keskset rolli roti aju stressivastuse moduleerimisel. Tõepoolest, teatud ajupiirkondade soo ja rakukeskkonna panusest MR-i ja GR-i ekspressiooni teatati pärast vaoshoitavat stressi [70]. Lisaks täheldas sama rühm, et emastel rottidel oli kroonilise stressi korral hipokampuses selge GR/MR suhte reguleerimise mehhanism, samas kui emane hüpotalamus oli isastest rohkem altid kortikosteroidi retseptori ekspressiooni muutmisele vastuseks piirangustressile. Vähesed teised uuringud on samuti teatanud soolistest erinevustest MR ekspressioonis ja aktivatsioonis südames [71–73]. Samuti on näidatud, et glükokortikoidid avaldavad oma toimet, eriti põletikuvastast toimet, seksuaalselt dimorfsel viisil [74,75]. Lisaks võivad östrogeenid antagoniseerida GILZ geeni GR-indutseerimist [76]. Kas MR ja GR ekspressiooniga seotud regulatiivsed mehhanismid või nende kaasregulaatorite ekspressioon võivad aidata kaasa seksuaalse dimorfismi tekkele, tuleb veel uurida. Lõpuks, meie teadmiste kohaselt on ainult ühes uuringus teatatud kortikosteroidi retseptorite ekspressiooni seksuaalsest dimorfismist neerudes [77].
6. Soolised erinevused neerude arengus ja organogeneesis
Neeru organogenees on keeruline protsess, mis hõlmab kolme järjestikust struktuuri, millest ainult viimane, metanefros, annab lõpliku neeru [78]. Metanefros areneb kaudaalsetest nefrotoomidest alates 5. GW-st ja selle küpsemine jätkub kuni inimese sünnijärgse elu esimese aasta lõpuni [65] koos nefronite ja kogumiskanalite erinevate osade paralleelse küpsemisega [79] ]. Neerude ontogenees saab alguse metanefroosi mesenhümaalsete rakkude interaktsioonist, mis loob tulevased nefrogeensed struktuurid, ja kusejuha, Wolffi kanalist välja arenenud epiteeli struktuuri, millest areneb neerude kogumissüsteem järjestikuste dihhotoomiate teel. klassikaline hargnemise morfogenees [80]. Iga kusejuha punga haru on kaetud metanefriliste rakkudega, mis on eellasrakud, mis on võimelised diferentseeruma kõikideks rakutüüpideks, mis moodustavad glomeruleid ja nefroneid [81]. Need diferentseerimismehhanismid on võimalikud tänu kahe struktuuri vahelisele dialoogile ja erinevate signaaliradade järjestikusele ekspressioonile [82, 83], millest mõned on epigeneetiliselt reguleeritud [84] ja seega võivad neid mõjutada raseduse ajal esinevad kõrvalnähud. Eelkõige vahendab AT1R-le toimiv Ang II neerutuubulite kasvu ja proliferatsiooni ning hargnevate morfogeneesi [85]. Seevastu loote neeru AT2 retseptoril (AT2R) on proliferatsioonivastane toime adrenomedullaarsetes interstitsiaalsetes rakkudes ja see toimib apoptoosi vahendajana [86]. Kõik need protsessid on üliolulised nefronite lõpliku arvu määramisel neeru kohta, mis on otseses korrelatsioonis neerufunktsiooniga täiskasvanueas. Nefrogenees on peamiselt sünnieelne [87], 5. ja 36. GW vahel, kuid täpsemalt 17. ja 32. GW vahel, mille tulemuseks on nefronite koguarv inimestel 300, 000 kuni 1,1 miljonit [88]. Lahkamiste või doonori neerudega läbiviidud uuringutest on teada, et täiskasvanueas esineb neerude mõõtmisel seksuaalset dimorfismi nii absoluutväärtustes kui ka suhtelistes väärtustes kehapinna suhtes, kusjuures meestel on oluliselt kõrgemad väärtused [89,90 ]. See tähendab, et meestel võib nefronite koguarv olla suurem kui naistel, kuigi inimliikide puhul pole seda ametlikult tõestatud. Huvitaval kombel tekib see seksuaalne dimorfism varakult nefrogeneesi ajal, kuna raseduse kolmandal trimestril lootel ja kuni 4-aastastel imikutel on leitud erinevusi neerude mahus [91–93]. Teisest küljest ei leitud neonataalsel perioodil seksuaalset dimorfismi nefronite arvu osas [94], kuid neid andmeid on väga väikeste kohortide kohta vähe uuritud. Neerude ontogenees on hiirel suhteliselt sarnane inimliigi omaga, järgneb kolm struktuuri, pronefros alates 8. tiinuse päevast (E8), mesonephros alates E9 ja metanephros alates E11. Peamine erinevus seisneb selles, et hiireliikidel jätkub nefrogenees postnataalselt kuni esimese elunädala lõpuni. Lisaks ei esine hiirtel vastsündinu perioodil neerude mahu seksuaalset dimorfismi [95], mis võib olla seotud uute nefronite omandamise viivitusega. Siiski ilmneb see märkimisväärselt, koos histoloogiliste struktuurimuutustega, alates 50. elupäevast, st pärast hiirte puberteedi algust [95]. Testosterooni otsest mõju neerude mahule on demonstreeritud noorte kastreeritud isaste hiiremudelites, kes on sekundaarselt kokku puutunud testosterooni või kandjaga [96]. Testosterooni troofilist mõju elundite, sealhulgas neerude arengule on tõestatud ka inimeste kliinilistes uuringutes [97]. Seega võib inimesel juba kolmandal trimestril esinev neeruorganogeneesi seksuaalne dimorfism olla seotud meessoost loodete emakasisese testosterooni sekretsiooniga [98]. Testosterooni prenataalse kokkupuute uuringud on näidanud, et arenev neer on testosterooni suhtes tundlik [99], kuid selle mõju neerude arengule loote füsioloogilistes tingimustes, samuti androgeeni signaaliraja ja teiste signaaliradade vahelised molekulaarsed interaktsioonid, mis on seotud nefrogeneesi, tuleb veel demonstreerida.

7. Mineralokortikoidi ja glükokortikoidi signaalide iseärasused neerude arengu ajal
Neerud on kortikosteroidide signaaliradade kudede sihtmärkide jaoks olulised ja neil on vastsündinu perioodil otsustav roll. Inimestel on vastsündinutel esimestel elukuudel naatriumi ja vee tagasiimendumine halvenenud, mis on seotud osalise tubulaarse resistentsusega aldosterooni suhtes [65], millega kaasneb kõrge aldosterooni tase plasmas esimestel elukuudel koos järkjärgulise normaliseerumisega täiskasvanute väärtustele [10]. Meie rühm on näidanud, et see mööduv ja osaline resistentsus aldosterooni suhtes täisaegsetel tervetel vastsündinutel on seotud madala tubulaarse MR-i ekspressiooniga sündimisel, samas kui MR ekspresseerub ajutiselt loote neerus 14. ja 24. GW vahel [65]. Neerude MR-i ekspressiooni perinataalne allareguleerimine ei ole spetsiifiline neerudele, kuna seda leidub ka teistes mineralokortikoidide sihtkudedes, nagu süda ja aju, mis on vastuolus kopsudega, kus MR-i ekspressioon säilib sündides [100]. Huvitav on see, et seda mineralokortikoidide signaaliülekande ajalist ja koespetsiifilist ekspressiooni leidub nii hiirtel kui ka inimestel, näidates hästi konserveerunud mehhanismi, millel võib olla otsustav roll kohanemisel vees emakasisesest elust maismaaeluga [65]. See varieeruvus MR-i ekspressioonis ei ole seotud aldosterooni kõrge sekretsiooniga sünnihetkel, kuna aldosterooni süntaasi, knockout-hiirtel esineb sama vastsündinu neerude MR-i ekspressiooni allareguleerimine [101]. Kuid kõik teised mineralokortikoidi signaaliraja mängijad järgivad sama kahefaasilist ekspressioonimustrit, näiteks 11 HSD2 või ENaC [65]. Huvitaval kombel ei leidu 11 HSD2 allareguleerimist neerudes platsentas, kus selle ekspressioon on kõrge sünnieelsel perioodil, et kaitsta loodet ema glükokortikoidide liigse immutamise eest [66]. Kuigi mineralokortikoidide signaalirada on perinataalsel perioodil alla reguleeritud, tuvastatakse GR ekspressioon neerutuubulite rakkudes ja plasma kortisooli tase on vastsündinutel füsioloogilistes kogustes tuvastatav [66]. Arvestades, et 11 HSD2 ei tuvastata, on neeru glükokortikoidi rada aktiveeritud ja seda ei saa reguleerida, toetades seega ideed mineraalkortikoidide ja glükokortikoidide signaaliradade vahelise tasakaalu kohta sellel konkreetsel arenguperioodil (joonis 2). Kokkuvõtteks võib öelda, et mineralokortikoidide ja glükokortikoidide signaaliülekandeteed on loote elu jooksul tihedalt reguleeritud ja neil on olenevalt arengustaadiumist kõrge ja madala aktivatsiooni tsüklilised perioodid. Mineralokortikoidide signaaliülekanne väheneb mööduvalt perinataalse perioodi jooksul, samas kui glükokortikoidi sekretsioon on madal vahemikus 14–24 GW ja suureneb eksponentsiaalselt enne sündi. Tsükliline immutamine mineralokortikoidides ja glükokortikoidides näib olevat osa emakavälise eluga kohanemisprotsessist.

8. Seksuaalne dimorfism tasakaalus neerude mineralokortikoidi ja glükokortikoidi signaalide vahel
Mitmetel mittereproduktiivsetel bioloogilistel protsessidel on seksuaalne dimorfne regulatsioon. Vererõhk on üks enim tunnustatud, meeste ja naiste süstoolse vererõhu erinevus enne menopausi on ligikaudu 15 mmHg [102]. See kõrgem süstoolne vererõhk meestel on säilinud kõigil imetajatel, mis viitab hästi säilinud regulatsioonimehhanismidele [103]. Täiskasvanutel on testosterooni otsest mõju vererõhu tasemele näidatud mitme loommudeliga kastreerimise ja testosterooni asenduskatsetega [104], samas kui munasarjade eemaldamine ei mõjutanud emaste rottide vererõhku [105]. On teada, et sugusteroidid mõjutavad RAS-i aktiivsust täiskasvanutel: testosteroon soodustab Ang II toimet AT1R kaudu, samas kui östrogeen vähendab AT1R/AT2R suhet, kutsudes esile erineva vastuvõtlikkuse Ang II suhtes [103]. Meie rühm täheldas täiskasvanud hiirtel kortikosteroidide signaaliülekanderaja sihtgeenide soo- ja elundispetsiifilist regulatsiooni koos neeru-11 HSD2 kõrgema ekspressiooniga emastel hiirtel, soodustades aldosterooni selektiivsust selle retseptori suhtes [77]. See mineralokortikoidi raja suurenenud aktiveerimine naistel ei tõsta vererõhku, kuid selle eesmärk võib olla kaaliumi eritumise peenem reguleerimine distaalsete tuubulite kaudu, mis on adaptiivne mehhanism, mis on optimeeritud ema ja loote homöostaasi jaoks raseduse ajal [106]. Eriti huvitav on Zheng et al. teatas, et aldosterooni toime plasma K plussile oli naistel suurem kui meestel. Need autorid näitasid, et mõlemad östrogeeniretseptorid (ER ja ER ) aitasid kaasa östrogeenist põhjustatud plasma K pluss ja AT1R seondumise vähenemisele emastel rottidel, kellel oli eemaldatud munasarjad [107]. Andmed areneva loote ja vastsündinu kohta on vähem ulatuslikud. Kuigi isas- ja naisloote vahel ei ole arengu või sündimise ajal täheldatud erinevusi CYP11B1 ja CYP11B2 geeniekspressioonides ega aldosterooni ja kortisooli/kortikosterooni steroidide kontsentratsioonides, on tõestatud soospetsiifiline MR ja 11 HSD2 ekspressioon [77]. Meie rühm teatas seksuaalsest dimorfismist MR-i ja selle sihtgeenide neeruekspressioonis perinataalsel perioodil, sihtgeenide MR-i, GR- ja mRNA-ekspressiooni maksimum oli 17,5-päevasel tiinuspäeval emastel hiirtel, kuid mitte isastel. Need andmed on kooskõlas Codoni jt varasema uuringuga, mis näitab 11 HSD2 suuremat aktiivsust naissoost loote neerudes 15. raseduspäeval [108]. Näib, et hiirtel soodustab MR ja GR signaaliradade vaheline tasakaalustamatus neerudes sünnieelsel perioodil mineralokortikoidide signaaliülekannet emastel. See võib anda naistele adaptiivse eelise, eriti kopsudes, võimaldades ENaC suurenenud ekspressiooni tõttu kopsuvedelikku resorptsiooni sünnihetkel [100]. Seega võib meestel leitud ekspressiooniprofiili tõlgendada kui ebasoodsat ja korrelatsioonis poiste suurema haigestumusega sündimisel, eriti hingamisteede kohanemise osas [101]. Veelgi enam, see viitab sellele, et glükokortikoidide signaaliülekande rada võib eelistatavalt aktiveerida meestel, kes võivad seejärel olla altid patoloogilisele arenguprogrammile pärast kokkupuudet stressi või glükokortikoididega raseduse ajal.
9. Tagajärjed patofüsioloogias
Arvestades glükokortikoidide ja mineralokortikoidide signaaliülekanderadade vahelist tasakaalustamatust meeste ja naiste vahel perinataalsel perioodil, on võimalik, et see võib teatud patofüsioloogilistes tingimustes avaldada mõju, kusjuures meestel on suurem vastuvõtlikkus pikaajaliste tagajärgede tekkeks. Hüpotees "Tervise ja haiguste arengu päritolu" on tekitanud taas huvi loote arengut reguleerivate tegurite mõistmise vastu. Täiskasvanueas haiguste, sealhulgas südame-veresoonkonna ja neeruhaiguste tekkega võivad kaasneda mitmesugused sünnieelsed häired. Meie hüpoteesi kinnitab sooline erinevus südame-veresoonkonna haiguste, nagu kõrge vererõhu ja südamepuudulikkuse esinemissageduses [109, 110], mis võib olla varaste perinataalsete sündmuste tagajärg [111].
Loote kasvu piiramine
Inimestel põhjustab ema glükokortikoidide liig loote kasvupiirangut ja suuremat hüpertensiooni riski hilisemas elus [112,113]. Uuringud (vaadatud artiklis [114]), milles kasutati loommudeleid (lamba-, hiire- ja rotimudelid), mis käsitlevad loote kasvupiiranguid, nagu ema glükokortikoidide kokkupuude, ema kalori- või valgupiirangud ja uteroplatsentaarne puudulikkus, mille tulemuseks on kas 11 HSD2 platsenta vähenemine. ekspressioon või loote otsene liigne kokkupuude glükokortikoididega [115] (mis võib kutsuda esile neeru glükokortikoidide signaaliraja üleaktiveerumise) on tuvastanud muutused neerude arengus kui sagedaseks tunnuseks. Huvitav on see, et paljudes arenguprogrammide loommudelites on isas- ja emasloomade vahel seksuaalne dimorfism haiguse alguse ajas ja raskusastmes. Tegelikult ei mõjuta sama sünnieelne solvang mehi ja naisi alati sarnaselt või samal määral [114]. Madala nefronisisalduse moodustumine võib põhjustada neerufunktsiooni häireid ja omakorda soodustada haigusi. Nendel loommudelitel tekib programmeeritud hüpertensioon, mis on osaliselt tingitud muutunud neerude arengust, mille tulemuseks on järglaste nefronisisalduse püsiv vähenemine [116]. Inimestel on nefronite arv korrelatsioonis sünnikaaluga ja hinnanguline juurdekasv on ligikaudu 237 426 nefroni kilogrammi täiendava sünnikaalu kohta, kuid meestel on see märgatavam [117], mis võib viia hüpertensiooni erineva arenguprogrammini isased ja emased. Oluline on see, et nefrogeneesi periood on liikide lõikes erinev, kuna inimestel ja lammastel on nefroni moodustumine enne sündi lõppenud, samas kui närilised jätkavad seda arenguprotsessi ka pärast sündi [116]. See tähendab, et nii sünnieelne kui ka postnataalne keskkond võivad mõjutada nefronite aktiivsust hiirel. Lisaks nefronitele on nendes mudelites näidatud modifikatsioone kortikosteroidide signaaliülekanderadade erinevate osalejate ekspressioonis [114], mis ei ole alati seotud nefronite arvu vähenemisega, mis viitab sellele, et arengu programmeerimisega on seotud ka teised mehhanismid. kõrge vererõhu korral [118]. AT1R ja AT2R, mis ekspresseeruvad neerudes varases tiinuse ajal, omavad ülemäärase glükokortikoidi loote immutamise loommudelites seksuaalselt dimorfset ekspressiooni, mille tulemuseks on tavaliselt AT1R suurenenud ekspressioon isasloomadel, olenevalt sünnieelse solvamise ajast [114 ]. Meie rühma esialgsed tulemused viitavad ka neerude MR-i ekspressiooni vähenemisele perinataalse glükokortikoidi üleekspositsiooni korral koos varajase hüpertensiooni tekkega, eriti meestel.
• Enneaegsus
Enneaegset sünnitust seostatakse suurenenud suremuse ja haigestumuse riskiga [119]. Uuringud enneaegsetel imikutel on näidanud, et meestel on suurem risk haigestuda, sealhulgas respiratoorse distressi sündroomi, hilise algusega sepsise, bronhopulmonaarse düsplaasia ja intraventrikulaarse verejooksu tekkeks kui naistel [120] ja pikaajalised neuroloogilised tagajärjed [121]. Lisaks on endistel enneaegsetel imikutel suurem risk varase hüpertensiooni tekkeks täiskasvanueas [122], eriti enneaegsetel poistel [123]. Need soolised erinevused ei ole seotud HPA telje funktsiooni varieeruvusega [33], kuid need võivad olla seotud poiste suurema tundlikkusega sünnieelsete kortikosteroidide manustamise suhtes [124]. Meie rühma loodud lipopolüsahhariididest põhjustatud enneaegsuse mudelis täheldasime, et endistel enneaegsetel meestel areneb täiskasvanueas märkimisväärne hüpertensioon [125]. Seda hüpertensiooni seostatakse varajaste muutustega kortikosteroidide signaaliülekande raja erinevate osalejate ekspressioonis vastsündinute perioodil. Tõepoolest, enneaegsetel hiirtel ilmnes kortikosteroidide sihtgeenide (ENac, Sgk1 ja Girlz) ekspressiooni väga tugev organ-spetsiifiline neerude aktiveerimine, mis on kontrastiks neerude MR-i ekspressiooni olulise vähenemisega. See viitab GR-i aktiveerimisele glükokortikoidide poolt, mis võivad programmeerida neerude funktsionaalseid või molekulaarseid muutusi, mis põhjustavad täiskasvanueas hüpertensiooni. Hüpertensiooni arenguprogrammi on kirjeldanud Barker et al. [126] ning välja kutsutud mehhanismid olid peamiselt nefronite omandamine, mis viis olemasolevate nefronite kompenseeriva hüperfiltratsioonini koos glomeruloskleroosi ja proteinuuriaga täiskasvanueas [127]. Vähesed uuringud on näidanud seksuaalset dimorfismi selles enneaegsusest põhjustatud nefroni vähenemises inimestel, kuid hiirtel ei ole erinevusi näidatud [128]. Meie mudelis tekkis varem enneaegsetel isastel hiirtel hüpertensioon, sõltumata nefronite arvu vähenemisest täiskasvanueas, mis viitab muudele kaasatud patofüsioloogilistele mehhanismidele. Lisaks viitas inimestel läbi viidud uuring, et hüpertensiooni programmeerimine võib kanduda endiste enneaegsete imikute lastele; valimi väike suurus ei võimaldanud aga eristada seksuaalset dimorfismi [129]. Meie hiiremudelis tuvastasime vererõhu düsregulatsiooni ülekandumise järgmistele põlvkondadele enneaegsetest vastsündinutest kuni kolmanda põlvkonnani. Huvitaval kombel kandus see vaskulaarne anomaalia ainult teise ja kolmanda põlvkonna meestel, mis on seotud kortikosteroidi sihtgeeni Girlz ekspressiooni olulise suurenemisega ja selle promootori globaalse hüpometüleerimisega [125]. See uuring näitab, et eelsoodumus arteriaalse hüpertensiooni tekkeks võib meestel olla epigeneetiliselt programmeeritud eelmiste põlvkondade perinataalse perioodi jooksul toimunud sündmuste tõttu kortikosteroidide signaaliülekanderaja seksuaalselt dimorfse ebasoodsa aktiveerimise kaudu.
• Mööduv
Pseudo-hüpoaldosteronism Varasel postnataalsel perioodil võib neerude mineralokortikoidide ja glükokortikoidide tasakaalustamatust mõjutada ka kuseteede infektsioon. Tõepoolest, ülemiste kuseteede infektsiooni (püelonefriidi) korral koos uropaatiaga või ilma võib ilmneda mööduv, mittefüsioloogiline pseudohüpoaldosteronism [130]. Selle tagajärjeks on hüponatreemia, hüperkaleemia, metaboolne atsidoos ja tõsine dehüdratsioon, millega kaasneb suur naatriumikaotus uriinis, mis nõuab ägedas faasis naatriumi lisamist. Mööduv pseudo-hüpoaldosteronism esineb peamiselt alla 3 kuu vanustel imikutel, seoses neerude MR-i madala ekspressiooniga sellel arenguperioodil [65] ja 88 protsendil juhtudest meestel [130]. Patofüsioloogia võib olla seotud põletikuga (NF-κB faktori aktiveerimise kaudu), mis veelgi vähendab MR ekspressiooni ja aktivatsiooni [131]. Kuna MR ekspressioon on perinataalsel perioodil meestel madalam [77], tunduvad nad selle ekspressiooni languse suhtes tundlikumad. Lisaks võib põletikust põhjustatud glükokortikoidide sekretsiooni suurenemine meestel (kellel on madalam 11 HSD2 tase) vallandada neerude GR üleaktiveerumise ja kutsuda esile alternatiivseid kõrvalmõjusid. Üldiselt võivad varased perinataalsed sündmused, mis seavad kahtluse alla neerude kortikosteroidide signaaliülekanderadu, põhjustada soost sõltuvaid lühi- ja pikaajalisi tagajärgi. Joonisel 3 on kokkuvõte selline neerukortikosteroidide tasakaalustamatus bioloogiliste sugude vahel ja sellega seotud häired kogu arengu vältel.

10. Järeldused
Kokkuvõttes oli selle ülevaate eesmärk demonstreerida ajalise akna olemasolu neerude arengu ajal koos spetsiifilise ja ajalise tasakaalustamatusega glükokortikoidide ja mineralokortikoidide signaalide aktiveerimisel koos seksuaalse dimorfse regulatsiooniga. See soo-diferentsiaalne ekspressioon ja neerukortikosteroidide signaaliradade aktiveerimine imetaja lootel ja vastsündinul, mis on säilinud liikide vahel, näivad soodustavat mineralokortikoidide signaaliülekannet naistel ja glükokortikoidide signaaliülekannet meestel. Need erinevused võivad tuleneda sugusteroidide otsesest või kaudsest mõjust; aga tõenäoliselt on kaalul ka muud mehhanismid. Selliste regulatiivsete mehhanismide dešifreerimine võib tuua valgust lühi- ja pikaajalistele patofüsioloogilistele tagajärgedele, eriti meestele, ning aidata parandada sugudimorfsete haiguste, näiteks varajase hüpertensiooni ennetamist ja ravi.

1 Université Paris-Saclay, Inserm, Physiologie et Physiopathologie Endocriniennes, CEDEX, 94276 Le Kremlin-Bicêtre, Prantsusmaa; margaux.laulhe@universite-paris-saclay.fr (ML);laurence.dumeige@aphp.fr (LD); thi-an.vu@universite-paris-saclay.fr (TAV);imene.hani@universite-paris-saclay.fr (IH); eric.pussard@aphp.fr (EP);marc.lombes@universite-paris-saclay.fr (ML); say.viengchareun@universite-paris-saclay.fr (SV)
2 Laste endokrinoloogia osakond, Hôpital Universitaire Robert Debre, Prantsusmaa ja Université de Paris, 75019 Pariis, Prantsusmaa
3 Service de Génétique Moléculaire, Pharmacogénétique et Hormonologie, Hôpital de Bicêtre, Assistance Publique-Hôpitaux de Paris, 94275 Le Kremlin-Bicêtre, Prantsusmaa
Viited
1. Seccia, TM; Caroccia, B.; Gomez-Sánchez, EP; Gomez-Sánchez, CE; Rossi, GP Normaalse glomeruloosi ja aldosterooni tootva adenoomi bioloogia: patoloogilised tagajärjed. Endocr. Rev 2018, 39, 1029–1056.
2. Miller, WL Steroidogenees: vastamata küsimused. Trends Endokrinool. Metab. 2017, 28, 771–793.
3. Lefebvre, H.; Duparc, C.; Naccache, A.; Lopez, A.-G.; Castanet, M.; Louiset, E. Aldosterooni sekretsiooni parakriinne regulatsioon füsioloogilistes ja patofüsioloogilistes tingimustes. Vitam. Horm. 2019, 109, 303–339.
4. Wils, J.; Duparc, C.; Cailleux, A.-F.; Lopez, A.-G.; Guiheneuf, C.; Boutelet, I.; Boyer, H.-G.; Dubessy, C.; Cherifi, S.; Cauliez, B.; et al. Neuropeptiidne aine P reguleerib aldosterooni sekretsiooni inimese neerupealistes. Nat. Commun. 2020, 11, 2673.
5. MacKenzie, SM; van Kralingen, JC; Davies, E. Aldosterooni sekretsiooni reguleerimine. Vitam. Horm. 2019, 109, 241–263.
6. Clark, BJ ACTH Tegevus StAR-i bioloogias. Esiosa. Neurosci. 2016, 10, 547.
7. Melau, C.; Nielsen, JE; Frederiksen, H.; Kilcoyne, K.; Perlman, S.; Lundvall, L.; Langhoff Thuesen, L.; Juul Hare, K.; Andersson, A.-M.; Mitchell, RT; et al. Inimese neerupealiste steroidogeneesi iseloomustus loote arengu ajal. J. Clin. Endokrinool. Metab. 2019, 104, 1802–1812.
8. Naccache, A.; Louiset, E.; Duparc, C.; Laquerriere, A.; Patrier, S.; Renouf, S.; Gomez-Sánchez, CE; Mukai, K.; Lefebvre, H.; Castanet, M. Nuumrakkude ja steroidogeensete ensüümide ajaline ja ruumiline jaotumine inimese loote neerupealises. Mol. Kamber. Endokrinool. 2016, 434, 69–80.
9. Johnston, ZC; Bellingham, M.; Filis, P.; Sofintini, U.; Hough, D.; Bhattacharya, S.; Simard, M.; Hammond, GL; King, P.; O'Shaughnessy, PJ; et al. Inimese loote neerupealised toodavad kogu teise trimestri jooksul kortisooli, kuid mitte tuvastatavat aldosterooni. BMC Med. 2018, 16, 23.
10. Martinerie, L.; Pussard, E.; Yousef, N.; Cosson, C.; Lema, I.; Husseini, K.; Mur, S.; Lombes, M.; Boileau, P. Aldosterooni signaalimise defekt süvendab naatriumi raiskamist väga enneaegsetel vastsündinutel: Premaldo uuring. J. Clin. Endokrinool. Metab. 2015, 100, 4074–4081.
11. Ishimoto, H.; Jaffe, RB Inimese loote neerupealise koore areng ja talitlus: loote-platsenta üksuse põhikomponent. Endocr. Rev. 2011, 32, 317–355.
12. Abdel Mohsen, AH; Taha, G.; Kamel, BA; Maksood, MA Väga madala sünnikaaluga imikute aldosterooni eritumise hindamine. Saudi J. Kidney Dis. Transpl. 2016, 27, 726–732.
13. Viengchareun, S.; Le Menuet, D.; Martinerie, L.; Munier, M.; Pascual-Le Tallec, L.; Lombes, M. Mineralokortikoidi retseptor: ülevaated selle molekulaar- ja (pato)füsioloogilisest bioloogiast. Nucl. Retsept. Signaal. 2007, 5, e012.
14. Ventilaator, YS; Eddy, RL; Byers, MG; Haley, LL; Henry, WM; Nowak, NJ; Näitab, TB Inimese mineralokortikoidi retseptori geen (MLR) asub 4. kromosoomil, Q31.2. Cytogenet. Cell Genet. 1989, 52, 83–84.
15. Morrison, N.; Harrap, SB; Ariza, JL; Boyd, E.; Connor, JM Inimese mineralokortikoidiretseptori geeni piirkondlik kromosomaalne määramine 4q31.1-le. Humm. Genet. 1990, 85, 130–132.
16. Zennaro, MC; Keightley, MC; Kotelevtsev, Y.; Conway, GS; Soubrier, F.; Fuller, PJ inimese mineralokortikoidi retseptori genoomne struktuur ja ekspresseeritud isovormide identifitseerimine. J. Biol. Chem. 1995, 270, 21016–21020.
17. Lema, I.; Amazit, L.; Lambert, K.; Fagart, J.; Blanchard, A.; Lombes, M.; Corradi, N.; Viengchareun, S. Mineralokortikoidi retseptori uue splaissivariandi HuR-sõltuv redigeerimine paljastab naatriumi homöostaasi osmoregulatoorse ahela. Sci. Vabariik 2017, 7, 4835.
18. Zennaro, MC; Souque, A.; Viengchareun, S.; Poisson, E.; Lombes, M. Uus inimese MR-i splaissivariant on ligandist sõltumatu transaktivaator, mis moduleerib kortikosteroidide toimet. Mol. Endokrinool. 2001, 15, 1586–1598.
19. Pascual-Le Tallec, L.; Demange, C.; Lombes, M. Inimese mineralokortikoidi retseptori A ja B valgu vormid, mis on toodetud alternatiivsete tõlkekohtade kaudu, näitavad erinevat transkriptsioonitegevust. Eur. J. Endocrinol. 2004, 150, 585–590.
20. Zennaro, MC; Le Menuet, D.; Lombes, M. Inimese mineralokortikoidiretseptori geeni 5 iseloomustus/regulatiivne piirkond: tõendid kahe alternatiivse promootori erineva hormonaalse reguleerimise kohta mitteklassikaliste mehhanismide kaudu. Mol. Endokrinool. 1996, 10, 1549–1560.






