Probiootikumide tulevane kasutamine astronaudi tervise säilitamiseks kosmoselendude ajal
Sep 28, 2023
Abstraktne:Astronaudi tervise säilitamine kosmosereisi ajal on ülioluline. Mitmed uuringud on täheldanud erinevaid muutusi soolestiku mikrobioomis ja füsioloogilises tervises. Rahvusvahelise kosmosejaama (ISS) pardal viibivate astronautide soolestikus, ninas ja nahas esines muutusi mikroobikooslustes. Lisaks on astronautidel täheldatud immuunsüsteemi rakkude muutusi koos neutrofiilide, monotsüütide ja T-rakkude muutustega. Probiootikumid aitavad lahendada kosmoselendude ajal tekkivaid terviseprobleeme, inhibeerides patogeenide kleepumist, parandades epiteeli barjääri funktsiooni läbilaskvuse vähendamise kaudu ja tekitades põletikuvastase toime. Mikrogravitatsiooniga kokkupuutel näitasid probiootikumid lühemat viivitusfaasi, kiiremat kasvu, paremat happetaluvust ja sapiresistentsust. Külmkuivatatud Lactobacillus casei tüve Shirota kapsli stabiilsust testiti ISS-is kuu aega ja on näidatud, et see suurendab kaasasündinud immuunsust ja tasakaalustab soolestiku mikrobiootat. B. subtilis'e külmkuivatatud eoste kasutamine osutub kasulikuks pikaajaliste kosmoselendude jaoks, kuna see vastab kõigile kaubanduslike probiootikumide jaoks simuleeritud tingimustes testitud aspektidele. Need tulemused näitavad, et on vaja täiendavalt uurida probiootikumide mõju simuleeritud mikrogravitatsiooni ja kosmoselennu tingimustes ning rakendada neid soolestiku mikrobioomi düsbioosi põhjustatud mõjude ja kosmoselendude ajal tekkida võivate probleemide ületamiseks.

cistanche taime suurendav immuunsüsteem
Märksõnad: astronaut; kosmoselend; probiootikumid; mikrobioom; simuleeritud mikrogravitatsioon (SMG)
1. Sissejuhatus
Inimeste kosmoseuuringud on viimasel ajal suurenenud, kuna erinevad rahvusvahelised kosmoseagentuurid kavandavad rohkem missioone. Riikliku Lennundus- ja Kosmoseameti "Inimuuringute programm" kavandab praegu inimeste pikaajalisi kosmoselende Marsile ja Kuule. Erinevad uuringud näitavad, et astronautidel on raske oma tervist säilitada ja neil on lühikeste ja pikkade kosmoselendude ajal palju terviseprobleeme, kuna neil on kokkupuude paljude stressiteguritega, nagu mikrogravitatsioon ja kiirgus. Seega on vaja mõista kosmosereisidega seotud riske inimeste tervisele. Astronaudid, kes veedavad 6–12 kuud Rahvusvahelise Kosmosejaama (ISS) pardal, on kogenud muutusi soolestiku mikrobiotas ja erinevaid füsioloogilisi muutusi. Need muutused hõlmavad urogenitaaltrakti infektsioone, südame-veresoonkonna probleeme, muutusi bakterite resistentsuses ja virulentsuses, muutusi immuunvastuses ja vähkkasvajate teket kiirgusega kokkupuutest [1,2]. Astronautide tervise säilitamiseks on ülioluline võtta vajalikke ettevaatusabinõusid, kuna kosmosemissioonid kestavad väga pikki ajavahemikke [3]. Maailma Terviseorganisatsioon on iseloomustanud probiootikume kui "elusaid mikroorganisme, mis piisavas koguses manustamisel toovad peremeesorganismile tervisele kasu" [4]. On näidatud, et mõne probiootilise tüve tarbimine reguleerib immuunsüsteemi ja soolefloorat, mis toob kaasa heade bakterite, nagu laktobatsillide ja bifidobakterite arvu suurenemise ning kahjulike mikroobide arvu vähenemise. Probiootikumid, nagu Lactobacillus casei tüvi Shirota (LcS), võivad parandada kaasasündinud immuunsust ja suurendada looduslike tapjarakkude aktiivsust, suurendades peamiselt monotsüütide ja makrofaagide interleukiini -12 tootmist. Allaneelamisel jõuab LcS elusal kujul soole mikrobioomi ja säilitab soolestiku mikrobioomi [5, 6]. On näidatud, et probiootikumid mõjutavad neuroaktiivsete ainete sünteesi ja vabanemist. On näidatud, et Lactobacillus acidophilus moduleerib kannabinoidiretseptorite ekspressiooni [7]. Akkermansia muciniphila potentsiaalse probiootikumina, mis võib seedetrakti mutsiini hästi ära kasutada, on lahutamatult seotud peremeesorganismi ainevahetuse ja immuunvastusega. Sellel võib olla terapeutiline sihtmärk mikrobiotaga seotud haiguste, nagu koliit, metaboolne sündroom, immuunhaigused ja vähk [8]. Selle tulemusena viitab uuring, et Akkermansiast saadud järgmise põlvkonna probiootikumid võivad vähendada kroonilise põletikuga seotud haiguste riski [7]. Hiljuti avastati, et silmapaistva soolestiku mikroobi Faecalibacterium prausnitzii suukaudsel manustamisel on põletikuvastased omadused, suurendades IL-10 (tsütokiini) ja kasvaja nekroosifaktori (TNF) tootmist käärsooles, et parandada soolehaigust [9 ]. Teine uuring näitab ka Bulgaaria omatehtud jogurtist eraldatud Lactobacillus bulgaricus ja Streptococcus thermophilus tüvede põletikuvastast potentsiaali. Lactobacillus, Bifidobacterium ja Streptococcus probiootilisi tüvesid kasutatakse peamiselt suuinfektsioonide ennetamiseks või raviks [10]. Teatud soolestiku mikrobiota mängib olulist rolli toitumise funktsionaalsuses ning aitab kaasa vitamiinide kättesaadavusele ja lühikese ahelaga rasvhapete tootmisele. Soolestiku mikroorganismid võivad toota B12-vitamiini, K-vitamiini, püridoksiini, folaate, biotiini, nikotiinhapet ja tiamiini [11]. Naastud või hambabiokiled põskkoopas põhjustavad suuõõne halba tervist; piimhappebakterid (LAB) aga interakteeruvad selle biokile/naastuga ja hävitavad antimikroobse toime kaudu patogeenid [12]. Pikaajalise kosmoselennu ajal on tõhusa tervisejuhtimise usaldusväärsus hädavajalik. Uuringute kohaselt põhjustab kosmoselend inimese füsioloogias muutusi [13]. Need muutused võivad olla erineva iseloomuga: füsioloogilised, sealhulgas seedetrakti distress, dermatiit ja hingamisteede infektsioonid; immunoloogiline [14] ja mikrobioom [15]. Maal tehtud uuringud on näidanud, et probiootikumid aitavad parandada kosmoselendude ajal tekkivaid terviseprobleeme. Nad aitavad konkureerida patogeenidega, vähendada seedetrakti probleeme, tugevdada tihedaid ühendusi sooleepiteelirakkudes, toota olulisi metaboliite ja suhelda peremeesrakkudega, et soodustada füsioloogilisi ja immuunsüsteemi muutusi [16–18]. See ülevaade keskendub erinevatele kosmoselennuprobleemidele, millega astronaudid kokku puutuvad, ja sellele, kuidas probiootikumide tarbimine võib aidata neid probleeme leevendada, mis võib aidata astronautidel kosmoselendude raskustest üle saada.

cistanche toidulisandi eelised - suurendavad immuunsust
2. Terviseprobleemid kosmoselendude ajal
Kosmos on karm keskkond ning edusammud materjaliteaduses, energiatootmises, robootikas ja meditsiinilistes nõuetes on hädavajalikud, et tagada astronautide ellujäämine asulates ja planeetidevahelistel reisidel. Uue bioastronautika valdkonna eesmärk on käsitleda mõningaid meditsiinilisi probleeme, millega astronaudid kosmoses viibides silmitsi seisavad. Kosmosevaenuliku keskkonna tõttu seisavad astronaudid nii pika kui ka lühiajalise kosmoselennu ajal silmitsi mitmete terviseriskidega [19, 20]. Skemaatiline esitus terviseprobleemidest, millega astronaudid kosmoselendude ajal kokku puutuvad, on näidatud (joonis 1).

Joonis 1. Terviseprobleemide diagramm, millega astronaudid kosmoselendude ajal kokku puutuvad. Pilt loodi kasutades BioRender.com.
2.1. Muutused mikrobioomis
Joshua Lederberg lõi 2001. aastal mõiste "inimese mikrobioom". Ta iseloomustas seda kui "kommensaalsete, sümbiootiliste ja patogeensete mikroorganismide loomulikku võrgustikku, mis jagavad meie keharuumi tõeliselt." Inimese mikrobioom koosneb erinevatest kasulikest sümbiontidest, peamiselt bakteritest, mis tugevdavad aktiivselt tervist. Mikrobioota muutudes võib patogeenide arvu suurenemine mõjutada homöostaasi ja põhjustada erinevaid haigusi. Nii pika- kui ka lühiajaliste kosmosemissioonide käigus on täheldatud muutusi astronautide soolestiku, nina ja suu bakterite profiilis. Need progresseerumised on seotud perekondadest Lactobacillus ja Bifidobacterium pärinevate kasulike mikroobide üldise rikkuse vähenemisega ja oportunistlike mikroorganismide, näiteks Escherichia coli, Clostridium sp., Staphylococcus aureus, Fusobacterium nucleatum ja Pseudomonas aeruginosa [3] aeruginuse kasvuga. ISS-i pardal aasta aega veetnud üheksa astronaudi mikrobiota uurimine näitab, et kosmosemissioonide ajal on seedetrakti (GI) trakti, nina, keele ja naha mikroobide populatsioon muutunud. Uuringus osalenud mikroobiproovidest kogutud DNA-le viidi läbi 16S rRNA geenide sekveneerimine, et määrata mikroobide koostis. See uuring eristas ruumiga seotud Parasutterella sp. number. See on kategooriliselt seotud kroonilise soolestiku süvenemisega inimestel, kellel on põletikuline soolehaigus. Uuringus leiti ka kolme põletikuvastaste omadustega bakteriperekonna populatsiooni vähenemine ruumiga: intestinal Fusicatenibacter, Pseudobutyvibrio ja Akkermansia. Nina mikrobiotas ilmnes lennu ajal vähem muutusi [1, 6].

cistanche tubulosa - parandab immuunsüsteemi
Cistanche Enhance Immunity toodete vaatamiseks klõpsake siin
【Küsi lisa】 E-post:cindy.xue@wecistanche.com / Whats App: 0086 18599088692 / Wechat: 18599088692
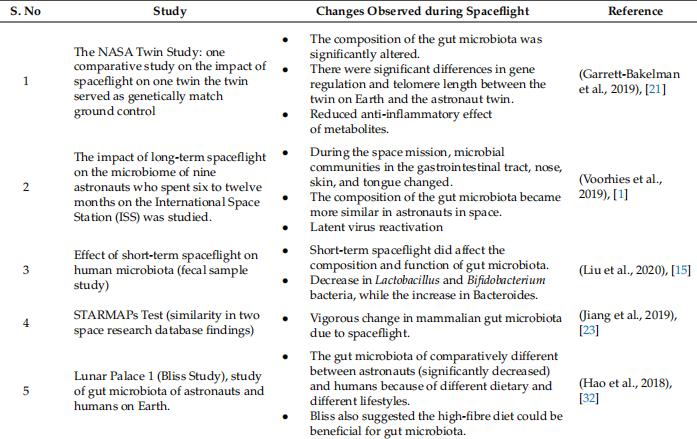
Liu jt uuring. [15] oli esimene, kes näitas lühiajaliste kosmoselendude mõju inimese soolestiku mikrobioomile. Uuring näitas, et Bacteroides'i arvukus suurenes pärast kosmoselendu koos Lactobacilluse ja Bifidobacterium'e vähenemisega. Bakteroidid lagundavad tõhusalt toidukiudaineid inimese soolestikus ning on olulised fenoolhappe ja propionaadi tootjad. Perekonda Bacteroides on mitu patogeenset bakteriliiki, mis paljunevad kiiresti stressirohketes tingimustes. Kosmosekeskkond nõrgestab inimese immuunsüsteemi ja Bacteroides'e arv võib suureneda. Inimese soolestikus on laktobatsillid vastutavad suure piimhappe tootmise eest. Lisaks näitavad uuringud, et Bifidobacterium toodab suhkrutest piim- ja äädikhapet. Lactobacillus'e ja Bifidobacterium'e liikide populatsiooni vähenemine võib häirida peremeesorganismi immuunsüsteemi toimimist soolestikus ja soolestiku mikrobiota tööd ning kosmoselendude poolt mõjutatud immuunsüsteemid võivad põhjustada latentsete viiruste taasaktiveerumist ja oportunistlike patogeenide arvu suurenemist soolestikku. Kaksuuring näitas ka, et metaboliite, nagu 3-indoolpropioonhape, millel on põletikuvastane toime, täheldati kogu uuringu vältel madalal tasemel. Järgmises uuringus leiti ka muutused mikrobioomi funktsioneerimises lennuobjektil võrreldes maapealse subjektiga seoses mikroobikooslustega [21]. Siddiqui jt uuring. [22] kasutas maapinnal tagajäseme mahalaadimise (HU) hiiremudelit, et simuleerida mikrogravitatsioonitingimusi, et uurida muutusi soolestiku mikrobiota bakterite koostises. Nad leidsid, et tagajäsemete mahalaadimine põhjustab muutusi soolestiku mikrobiotas, sealhulgas kasuliku soolestiku mikrobiota mitmekesisuse vähenemist, mis võib põhjustada suurenenud läbilaskvust ja soolepõletikku. Uuring näitas Akkermansia muciniphila, Eubacterium coprostanoligenes'e ja Burkholderiales'e vähenemist hiirtel, kes olid kokku puutunud simuleeritud mikrogravitatsiooniga, võrreldes tavaliste hiirtega. Neid bakterite perekondi seostatakse põletikuvastaste omaduste, soolestiku homöostaasi ja tervisega seotud eelistega, nagu neerukivide ennetamine. Uuring rõhutas ka Firmicutes'i ja Bacteroidetes'i tasakaalustatud osakaalu tähtsust üldise tervise säilitamisel, kusjuures nende proportsioonide muutused põhjustavad düsbioosi ja sellega seotud terviseprobleeme. Firmicutes mängivad rolli peremeesorganismi ainevahetuses ja toitumises, samas kui Bacteroidetes on seotud immunomodulatsiooniga. Need tulemused viitavad sellele, et muutused soolestiku mikrobiotas võivad kaasa aidata kosmoselendudel kogetavatele negatiivsetele tervisemõjudele [22]. Analüütiline tööriist "Akkordantsete ja reprodutseeritavate mikrobioomide arvukuse mustrite sarnasustest" või STARMAP-id testib mikrobiota variatsioonide leidmiseks kahe ruumi uurimisandmekogumite sarnasust. Uuring avastas ka, et kosmoselendudega seotud mikrobiota muutused RR-1 (Rodent Research 1) ja STS-135 (Inimesemissioon) missioonide ajal olid sarnased, mis viitab kosmoselendude tõttu tugevale muutusele imetajate soolestiku mikrobiootas [ 23]. Tabelis 1 on kokku võetud ka mikrogravitatsiooni mõju astronautide soolestiku mikrobiotale kosmoselennu ajal.
2.1.1. Mikrobioota-soolestiku-aju telg ja selle seos astronautide vaimse tervisega
Soolestiku mikrobiota koosneb 106 viirus-, bakteri- ja algloomarakust, mis teeb sellest kõige arvukama inimese mikrobiota koosluse. Aju mõjutab mikrobiota funktsiooni ja koostist, muutes soolestiku läbilaskvust. Aju võib autonoomse närvisüsteemi (ANS) kaudu mõjutada ka immuunfunktsiooni. Soole-aju telg (GBA) on kahesuunaline suhtlusrada kesk- ja enteraalse närvisüsteemi vahel. See seob aju emotsionaalsed ja kognitiivsed keskused perifeersete soolefunktsioonidega. Hiljutised teadusuuringud on rõhutanud soolestiku mikrobiota tähtsust nende koostoimete mõjutamisel [24]. Soolestiku mikrobiota koostis läbib eluea jooksul palju üleminekuid, mis on paralleelsed aju arengu, vananemise ja küpsemise dünaamiliste perioodidega. Düsbioos võib tuleneda keskkonnateguritest, nagu toitumine, gravitatsioon, stress ja kiirgus. Lisaks mängib soolestiku mikrobiota olulist rolli nii adaptiivse kui ka kaasasündinud immuunvastuse kujunemisel. Seedetrakti mikroorganismid toimivad teabe koondamise ja edastamise jaamadena teatud ajupiirkondadesse, eriti väikeaju, mõjutades vaimset tervist. Kosmosereisidega seotud keskkonnategurite mõju nendele mikroorganismidele läheneb [25].
2.1.2. Vaimse tervise väljakutsed, millega astronaudid kosmoselendude ajal silmitsi seisavad
Kosmoselennud on ainulaadne ja keeruline keskkond, mis võib astronautide vaimset tervist oluliselt mõjutada [26]. Isolatsioon, suletus, mikrogravitatsioon, ööpäevarütmide häired ja suhtlemisviivitused võivad kõik kaasa aidata psühholoogilisele stressile, ärevusele, depressioonile ja muudele vaimse tervise probleemidele [27,28]. Uuringud näitavad, et astronaudid on kosmoses viibides tõenäolisemalt emotsionaalsed ja neil on vaimsed häired [29]. Kosmoselendude ajal tekkiv sotsiaalse toetuse ja isolatsiooni puudumine on astronautide vaimse tervise probleemide üks peamisi põhjuseid. Astronaudid on pikkadeks perioodideks oma peredest ja sõpradest isoleeritud, mistõttu on neil raske regulaarselt suhelda. See võib põhjustada eraldatuse, igavuse ja psühholoogilise piina tunde [28]. Teine suur väljakutse on une-ärkveloleku tsükli häired, mis on põhjustatud püsivast kunstliku valgusega kokkupuutest ja loomuliku päeva-öö tsükli puudumisest kosmoses [30]. Ma jt hiljutine uuring. [31] näitas ka seost probiootikumide indutseeritud soolestiku mikrobiomi ja täiskasvanute stressitasemete vahel, tõestades seega soolestiku-aju telje rolli stressi mõjude vähendamisel.
Tabel 1. Mikrogravitatsiooni mõju astronautide soolestiku mikrobiootale kosmoselendude ajal.
Vaimne tervis on kosmoselendude oluline osa ja astronaudid kogevad tõenäolisemalt psühholoogilist stressi, ärevust ja muid vaimse tervise probleeme. Oluline on jätkata kosmoses viibimise ajal astronautide vaimse tervise parandamise tehnikate uurimist ja kasutuselevõttu.
2.2. Urogenitaaltrakti infektsioon
Pikaajalistel kosmosemissioonidel seisavad astronaudid silmitsi paljude füüsiliste väljakutsetega, mis võivad mõjutada nende urogenitaalsüsteemi tervist. Kosmoselennu ajal põhjustab mikrogravitatsioonikeskkond plasmamahu vähenemist ja uriinierituse suurenemist vedeliku nihke tõttu alajäsemetest ülakeha suunas, mis põhjustab uriinivoolu ja uriini staasi vähenemise tõttu kuseteede infektsioonide (UTI) riski. . Lisaks võivad stress ja muutunud une-ärkveloleku tsüklid kosmoselennu ajal kaasa aidata noktuuria esinemissageduse suurenemisele [33]. Meesastronaudid võivad kosmoselendude ajal kiirgusega kokkupuute tõttu kokku puutuda testosterooni taseme langusega, mis põhjustab libiido vähenemist ja erektsioonihäireid. Teisest küljest võivad naisastronaudid kogeda menstruaaltsükli häireid ja vaagna ummikusündroomi, mis põhjustab valu, survet ja ebamugavustunnet vaagnapiirkonnas [33,34]. UTI-d on kosmoses tavalised probleemid, kus naisastronaudid kogevad sagedamini kui meesastronaudid. Uropatogeenid, nagu Staphylococcus saprophyticus ja Escherichia coli, on kõigi kuseteede infektsioonide olulised põhjused, kuna neil on võime kinnituda adhesioonimolekulide kaudu uroepiteelirakkudele. In vitro uuringud on näidanud, et nii patogeensetel kui ka mittepatogeensetel E. coli tüvedel on parem adhesioon ja invasioon mikrogravitatsiooni mõjul. See suurem adhesioon koos E. coli kiirenenud kasvukineetikaga ruumis võib põhjustada haiguse progresseerumist [3].

cistanche toidulisandi eelised - suurendavad immuunsust
2.3. Viiruse taasaktiveerimine kosmoselennul
Sonnenfeld & Sheareri uuring [35] selgitas immuunsüsteemi kahjustamist, pahaloomulise seisundi võimalikku arengut ja latentse viiruse taasaktiveerimisega nakatumist inimestel kosmoselennu ajal. Kosmoselennu ajal on märkimisväärne osa neist sümptomitest seotud immuunsüsteemi nõrgenemisega, mis on tingitud kahe viiruse – Epstein-Barri viiruse ja Varicella-Zosteri viiruse [1] – taasaktiveerumisest. Varjatud viiruse taasaktiveerumine on astronautide immuunsüsteemi seisundi biomarker ja seda soodustavad tegurid on glükokortikoidide sekretsiooni suurenemine, tsütokiinide tootmise muutus ja viiruste elimineerimisele suunatud immuunrakkude funktsiooni vähenemine. Viiruse DNA esinemine kehavedelikes näitab viiruse taasaktiveerumist [36].
2.4. Bakterite resistentsus ja muutused bakterite virulentsuses
Zhang et al. [37] uuris Shenzhou-11 kosmoselaevaga kosmosesse viidud S. enteritidis'e tüve antimikroobse resistentsuse muutusi. Võrreldes maapealse tüvega näitas lennutüvel suurenenud amikatsiiniresistentsust, suurenenud kasvukiirust ja mõningaid ainevahetuse muutusi. Escherichia coli MG1655 näitas antibiootikumiresistentsust, kui see puutus kokku pikaajalise väikese nihkejõuga modelleeritud mikrogravitatsiooniga (LSMMG) ja taustantibiootikumidega, nagu klooramfenikool, tsefalotiin, tetratsükliin, tsefoksitiin, tsefuroksiim ja tsefoksitiin. Tüvi näitas klooramfenikooli ja tsefalotiini suhtes resistentsust rohkem kui 110 põlvkonna jooksul, isegi pärast LSMMG-keskkonna kõrvaldamist ja antibiootikumide jälgi. Escherichia coli genoomijärjestuse kohandatud tüvi näitas umbes 25 muutust. Neid genoomseid muutusi seostati antibiootikumiresistentsusega, muutustega neljas antibiootikumiresistentsuse geenis: ompF, acrB, mdfA ja Marr [38]. Liu jt uuringu kohaselt. [15] Kosmoselend muudab bakterite virulentsust. Virulentsusgeenide uurimisel avastasid nad, et soolestiku mikrobioom mõjutas mõningaid virulentsusfaktoreid (VF). Sellise muutuse näiteks oli faktori VF0367 suurenemine, mis on seotud lipopolüsahhariidide arenguga, mis moodustab Brucellas kaitsekihi [15]. Hiljutine uuring näitas, et Streptomyces EF-Tu mutatsioonimarkeri näitude arv suurenes pärast astronaudi teekonda oluliselt. See marker tuvastab Streptomyces cinnamoneus'e pikenemisfaktori Tu rifamütsiiniresistentsust indutseerivate järjestuste variatsioonid. EF-Tu mutatsioonide suurenemine pärast kosmoselendu näitab, et rifamütsiini resistentsus võib olla suurenenud kosmoselennu asjaolude tõttu [39]. Need uuringud viitavad teatud mikroobide suurenenud patogeensusele pärast kosmoselendu.
2.5. Epiteeli barjääri katkemine ja põletikuline soolehaigus (IBD)
Põletikuline soolehaigus (IBD) on krooniline korduv seedetrakti põletikuline seisund, mida iseloomustab epiteeli barjääri katkemine ja immunoloogiline düsregulatsioon. Hiljutised uuringud on leidnud, et astronaudid kannatavad kosmoses viibides seedetrakti ebamugavustunne, sealhulgas IBD-laadsed sümptomid, mis on tõenäoliselt tingitud mikrogravitatsiooni mõjust sooleepiteelile. Tiheda ristmiku (TJ) valkude muutused põhjustavad epiteeli barjääri katkemist, mis suurendab soole läbilaskvust ja sellele järgnevat luminaalsete antigeenide translokatsiooni läbi epiteeli [40, 41]. TJ-de ekspressiooni või lokaliseerimise muutumine võib põhjustada lekkiva soolestiku seisundi, mis on tingitud valendikust lamina propriasse difundeeruvate molekulide suurenenud läbilaskvusest [42]. Alvarez et al. [43] leidis simuleeritud mikrogravitatsiooni tingimustes viivituse TJ-valkude – okludiini ja ZO-1 lokaliseerimisel. Leiud näitavad, et simuleeritud mikrogravitatsioon kahjustas epiteeli barjääri ja selle aluseks olev tundlikkus barjääri suhtes püsis ka pärast mikrogravitatsiooni seisundi eemaldamist. See barjääri häire muudab astronaudid altid erinevatele sooleepiteelirakkude barjääri defektidele, nagu Crohni tõbi, haavandiline koliit, tsöliaakia ja I tüüpi diabeet [44]. IBD-d on täheldatud astronautidel kosmoselennu ajal, kui TJ valgu katkemise tõttu on suurenenud soolestiku paratsellulaarne läbilaskvus [1, 45]. Uuringus teatati TJ-valkude, nagu okludiin, claudiin-1, claudine 04 ja JAM-A, ekspressiooni ja jaotumise vähenemine ning claudiini-2 ekspressiooni suurenemine [46]. Teine Yi jt uuring. [47] väitsid, et Lactobacillus reuteri LR1 võib ravida soolehäireid, mis on seotud epiteelibarjääri funktsiooni halvenemisega. Nakatumine enterotoksigeense E. coli K88-ga kutsus esile IPEC-1 rakkude monokihtide läbilaskvuse suurenemise. Probiootiline LR1 parandas oluliselt epiteeli barjääri funktsiooni ja vähendas kolibakterite adhesiooni ja kolonisatsiooni.

cistanche tubulosa - parandab immuunsüsteemi
2.6. Immunoloogilised muutused kosmoselennu ajal
Astronauts face the issue of immune cell alteration during spaceflight. Innate immunity, or the first line of defense, plays a vital role in prolonging healthcare among astronauts. Immunological changes observed in astronauts during space flight have been shown in (Table 2). A study conducted at Johnson Space Center, Houston, showed an 85% increase in neutrophils during a 5–11-day spaceflight mission as compared to pre-flight levels along with remarkably lower values in phagocytosis [48]. An increase in the number of white blood cells, polymorphonuclear leukocytes, was also observed in short-duration spaceflight missions to the ISS [49]. Similar effects have been observed in astronaut long-duration spaceflight missions. An increase in the level of white blood cells [14]. Another study by Makedonas et al. [50] reported an increased inflammation in the astronauts during 1-year NASA "twins" study aboard the International Space Station. Cosmonauts on a long duration (>140 päeva) kosmoselennud on näidanud endokannabinoidide suurenenud vabanemist koos immuunsüsteemi aktiveerumisega, mis jäljendab põletikuga seotud häirete riski inimestel. Suurenenud põletik püsis 30 päeva pärast lendu [51]. Astronautide poolt kogetavad gravitatsioonimuutused võivad mõjutada ka kahe kriitilise esmase lümfoidorgani, harknääre ja luuüdi mikrokeskkonda. Need organid vastutavad lümfotsüütide või valgete vereliblede tootmise eest. Muutused lümfotsüütide tootmises võivad kaudselt mõjutada omandatud immuunvastuseid, muutes immuunsüsteemi tüüpilist reaktsiooni põletikele, infektsioonidele ja kasvajatele [52].
Tabel 2. Kosmoselennu ajal astronautidel täheldatud immunoloogilised muutused.


2.7. Muutused südame-veresoonkonna funktsioonides
Kosmoses seisavad astronaudid silmitsi kaaluta olekuga, mille tulemuseks on kehavedelike ümberjaotumine keha alumisest osast rindkere-pealihase piirkondadesse. See vedeliku ülekanne põhjustab kardiovaskulaarse dekonditsioneerimise sündroomi, mida iseloomustab hüpotensioon, presünkoobi või minestuse võimalus ja vähenenud stressivõime [57]. Kosmoses viibides kogevad astronaudid metaboolset stressi. Metaboolne stress on nii südamehaiguste kui ka II tüüpi diabeedi tugev ennustaja [58]. Kosmoselend kujutab endast ka pahaloomuliste arütmiate tekke ohtu, kuna kosmoselendude ajal tekkinud muutused rõhutavad suurenenud repolarisatsiooni heterogeensust. Kehas toimuvate füsioloogiliste muutuste mõistmiseks on vaja täiendavaid uuringuid, mis aitavad samuti anda sügavama ülevaate inimeste tervise muutustest kosmoselendude kommertsialiseerimisel [59].
2.8. Kosmilise kiirguse mõju astronautidele
Inimesed puutuvad kosmoses viibides kokku kosmosekiirgusega. Need on väljaspool meie päikesesüsteemi tekkivad galaktilised kosmilised kiired, päikesest vabanevad päikeseosakesed ja Maa magnetvälja tõttu piiratud kiirgus. Need kosmosekiirgused ohustavad astronaute, kuna põhjustavad mitut tüüpi vähki. Naisastronautidel on 20% suurem tõenäosus vähki haigestuda kui meesastronautidel. See on peamiselt tingitud sellest, et rinna- ja munasarjavähki esineb sagedamini naistel. Reisimise ajal võivad inimesed kogeda lühiajalisi mõjusid, nagu muutused veres, kõhulahtisus, iiveldus ja oksendamine [3]. Kiirgus vähendab soolefloora mitmekesisust ja muudab soolestiku mikrobiota koostist [60]. Varasemate Apollo, Skylabi ja Venemaa moodulkosmosejaamade (MIR) lendude aruanded viitavad sellele, et astronaudid nägid valgussähvatusi, mis liikusid üle oma vaatevälja, arvatavasti ioniseeriva kiirguse põhjustatud tajumuutuse tõttu, mis näitab, et ka nägemishäired näivad olevat seotud kiirgusega [61]. 6-kuulise missiooni jooksul ISS-ile, Kuule ja mujale puutub astronaut kokku umbes 50–2000 millisiivertiga (mSv) kiirgusega. On dokumenteeritud, et kiirgusdoos üle 100 mSv põhjustab vähki [62]. STARMAP-i statistilise analüüsi uuring näitas, et kosmoselendudega seotud mikrobiota muutused võrreldes kosmoselaadse kiirguse põhjustatud muutustega maapinnal olid erinevad. Nad arvasid, et erinevus võib olla tingitud sellest, et ISS on madalamal orbiidil Van Alleni vöö sees. Seega ei puutunud uuringus osalenud uuritavad kosmilise kiirgusega kokku. Uuring tõestab, et kosmosekiirguse mõistmine Van Allen Beltsist kaugel on lähitulevikus ülioluline [23]. Põletikueelsed reaktsioonid kaalutaolekule, kiirgusele, stressist põhjustatud hüpertermiale või nende tegurite kombinatsioonile kosmoselendude ajal võivad põhjustada "kosmosepalavikku", mis võib mõjutada astronautide tervist ja energiat, toitainete ja vedelikuvajadust ning füüsilist ja kognitiivset jõudlust pika aja jooksul. -kosmoselennu kestus [63].
3. Probiootikumid ja nende roll kosmosebioloogias
Kosmoseuuringud on kutsunud teadlasi üles töötama välja ja kavandama inimestega koostatud missioone Kuule ja Marsile. Sellised pikaajalised missioonid nõuavad ulatuslikke teadmisi selle kohta, kuidas kosmosereisid astronautide tervist mõjutavad. Apollo 11 tulek ning erinevad simulatsioonikatsed Maal ja ISS-il on võimaldanud meil mõista, kuidas kosmos mõjutab mikroobe ja inimesi. Nagu jaotises 2.1 mainitud, on inimese soolestiku mikrobioomi säilitamine pikaajaliste kosmosereiside oluline aspekt. Soolestiku mikrobioomi tasakaalustamatus on põhjustanud palju haigusi ja kosmosereisid on näidanud, et see põhjustab muutusi soolestiku mikrobioomis. Probiootikumid võivad aidata seedetrakti probleemide puhul, nagu äge nakkav kõhulahtisus, Helicobacter pylori infektsioon, antibiootikumidega seotud kõhulahtisus, ärritunud soole sündroom, haavandiline koliit ja kõhukinnisus, ning parandada soolestiku barjääri funktsioone [64, 65]. Probiootikumid aitavad säilitada ka immuunsüsteemi, ennetada vähki ja aitavad psühholoogiliste probleemide korral [66]. Kõige laialdasemalt kasutatavad probiootikumid hõlmavad Lactobacillus, Bifidobacterium või Saccharomyces liikide liikmeid [67]. Näeme edasi, kuidas probiootikumid võivad olla kasulikud toidulisandid (tabel 3).
3.1. Probiootikumide üldine toimemehhanism
3.1.1. Patogeeni sidumise pärssimine
Probiootilised tüved inhibeerivad patogeeni seondumist epiteelikihiga, muutes lima sekretsiooni taset. Probiootikumid võivad parandada soolebarjääri tugevust, suurendades limakihti toetavate pokaalrakkude (sekreteerivate mutsiini) arvu. Limakihil on roll patogeensete bakterite seondumise vähendamisel limaskesta epiteelirakkudega ja probiootikumid indutseerivad lima sekretsiooni [68, 69]. Otte ja Podolsky [70] leidsid, et Lactobacilluse tüved muutsid MUC2, MUC3 ja MUC5AC ekspressiooni HT29 rakkudes. Probiootilised tüved võivad samuti pärssida patogeeni seondumist epiteelikihiga, konkureerides adhesioonikoha pärast. Inimese lima siduvad pilid võimaldavad mõnedel probiootikumidel keha paremini koloniseerida [71]. Probiootikumid konkureerivad epiteelirakkude mikrovilli pinnal olevate glükokonjugaadi retseptorite lektiini sidumiskohtade pärast [72, 73]. On näidatud, et L. plantarum ja Lactobacillus rhamnosus tüvi GG pärsivad patogeense E. coli kinnitumist epiteeli külge [74].
3.1.2. Probiootikumide kasutamine soolehaiguste korral
Ärritatud soole sündroomi (IBS) patogenees võib hõlmata muutunud soolestiku immuunaktivatsiooni, soolestiku mikrobioomi düsbioosi, muutunud aju-soolestiku telge ja suurenenud sooleepiteelirakkude läbilaskvust [75]. Probiootikumid mõjutavad IBS-i sümptomeid, nagu puhitus, kõhupuhitus, muutunud soole liikumine, soolestiku mikrobiota düsbioos ja kõhuvalu [76]. Probiootikumid pärsivad patogeeni kleepumist, suurendavad epiteeli barjääri funktsiooni, vähendades selle läbilaskvust ja tekitavad põletikuvastase toime [77]. GIT terviklikkust säilitavad epiteelirakud, mis toimivad barjäärina peremeesorganismi immuunsüsteemi ja väliskeskkonna vahel. Probiootilise Escherichia coli tüve Nissle 1917 (EcN) puhul viib ülekaalukas signaaliefekt kahjustatud epiteelirakkude taastamiseni. See muudab probiootilise EcN põletikulise soolehaiguse ravis tõhusamaks [41]. Probiootikum Lactobacillus plantarum MB452 parandab ka soolebarjääri terviklikkust, suurendades tihedate ühendusvalkude – tsinguliini ja okludiini – ekspressiooni. Need valgud aitavad säilitada epiteelirakkude paranemist [67]. Bifidobacterium sp. on veel üks probiootikumide rühm, mis aitab säilitada GI limaskesta tihedate ühenduste terviklikkust. Nad kaitsevad epiteeli barjääri ägeda koliidi eest, takistades okludiini ja TJ valkude ümberjaotumist [78].
3.1.3. Immuunsüsteemi hooldus
Probiootikumid võivad immuunsüsteemi moduleerida peamiselt (1) muutes immunoglobuliinide/tsütokiinide sekretsiooni, (2) tugevdades epiteeli soolebarjääri, (3) suurendades makrofaagide või looduslike tapjarakkude aktiivsust, (4) konkureerivalt seondudes epiteelikihiga, takistades patogeensete mikroobide levikut. sidumine ja (5) lima sekretsiooni moduleerimine. Probiootikumide, mitte tervete bakterite toodetud antigeensed osakesed võivad siseneda epiteelirakkudesse ja puutuda kokku immuunrakkudega [79]. Vähesed probiootilised tüved, nagu Lactobacillus rhamnosus GG ja Bifidobacteria, moduleerivad tsütokiinide tootmist erinevatest rakutüüpidest, muutes limaskesta ja süsteemseid kaasasündinud ja adaptiivseid immuunvastuseid [80]. Probiootikumid interakteeruvad epiteelirakkudega ja moduleerivad tsütokiinide vabanemist, muutes raku signaaliülekande radu [81]. Erinevad probiootilised tüved stimuleerivad erinevate immuunsüsteemi komponentide tootmist. Nende hulka kuuluvad IL-10 ja IL-20 tootmise stimuleerimine mononukleaarsete rakkude poolt piimhappebakterites [82], IL-6 tootmise indutseerimine Lactobacillus rhamnosus GG-s [80] ja tsütokiinide poolt indutseeritud apoptoos ja pro-apoptootilise p38 mitogeen-aktiveeritud proteiinkinaasi inaktiveeriv aktiveerimine TNF, IL-1a või gamma-interferooni poolt Lactobacillus rhamnosus GG-s [83], mis viitab soolerakkude suurenenud ellujäämisele [79]. Arvestades mõju immuunsusele, suurendaks probiootikumide kasutamine SCFA moodustumise soodustamiseks toitumis- ja metaboolseid ressursse ning lümfotsüütide võimet viirust elimineerida, vähendades potentsiaalselt varjatud viiruste taasemissiooni [84].
3.1.4. Probiootikumide antimikroobne toime
Muud mehhanismid, mille abil probiootikumid pärsivad mikroobide kasvu, hõlmavad orgaaniliste hapete, toksiliste ainete ja bakteriotsiinide sünteesi [85]. Piimhappebaktereid (LAB), propioonhappebaktereid ja bifidobaktereid on konserveerimis- ja kääritamistööstuses kasutatud sajandeid. Tegurid, mis muudavad need konserveerimisel tõhusaks, on tingitud madalast pH-st, süsivesikute kogusest ja antimikroobsete ühendite tootmisest. Need bakterid võivad toota antimikroobseid aineid, muutes need õigeks kandidaadiks probiootikumina [86]. LAB toodab glükoosi kääritamise teel orgaanilisi happeid, nagu äädikhape, piimhape ja propioonhape. Piimhape ja äädikhape pärsivad pärmi, hallitusseente ja baktereid [87]. Lisaks pH tõusule hajub dissotsieerumata hape üle rakumembraani. See dissotsieerub, vabastades tsütoplasmas H+ ioonid, põhjustades elektrokeemilise gradiendi kollapsi ja sellele järgneva bakteriostaasi või bakterite surma [88]. LAB-ga toodetud bakteriotsiinid on antimikroobsed peptiidid, mida sünteesivad ribosoomid [89]. Bakteriotsiinid on suunatud peamiselt rakumembraanile, inhibeerivad eoste idanemist, põhjustavad anioonsete kandjate inaktiveerimist ja muudavad ensümaatilist aktiivsust bakteriostaatilise või bakteritsiidse toimega sõltuvalt raku tundlikkusest. Need peptiidid on tavaliselt tõhusad lähedaste bakteriliikide ja grampositiivsete bakterite puhul [90].
3.1.5. Probiootikumid, mida kasutatakse antibiootikumidega seotud kõhulahtisuse korral
Soolestiku mikrobiota muutub kosmoselendude ajal ja raviks kasutatakse antibiootikume [1]. Kuigi antibiootikumid on bakteriaalsete infektsioonide likvideerimisel üliolulised, kahjustavad nad oluliselt soolestiku mikrobiota mikroorganisme [91]. Antibiootikumide kasutamine võib põhjustada mitmesuguseid probleeme, nagu patogeense Clostridium difficile koloniseerimine, mis põhjustab kroonilisi seedetrakti probleeme ja äärmist kõhulahtisust. Normaalsetes tingimustes konkureerivad C. difficile seedetraktis kommensaalsed bakterid, kuid kui soolestiku mikrobiota on kahjustatud (nagu kosmosereisidel täheldati), võib C. difficile trakti koloniseerida [92]. Probiootikume saab kasutada seedetrakti mikrobiota täiendamiseks ja neid saab kasutada ka C. difficile infektsioonide raviks [93]. Probiootikume saab kasutada antibiootikumidega seotud kõhulahtisuse raviks.
3.1.6. Probiootikumid vähi profülaktikanar
Kiirguskiirguse tõttu on astronautidel suurem tõenäosus vähki haigestuda. Probiootikumidega fermenteeritud sojapiima tarbimine toimib isoflavoonide antiöstrogeense toime kaudu rinnavähi profülaktilise meetmena [94]. Käärsoolevähi areng sõltub mitmest tegurist. Tõendid on näidanud seost soolestiku mikrobiomi koostise muutuste ja kolorektaalse vähi arengu vahel. Probiootikumid võivad mõjutada immuunsüsteemi ja soolestiku mikrobiota suhtlemist ning aidata vältida kolorektaalset vähki [95]. Keefir (probiootikumidega fermenteeritud piim) sisaldab bioaktiivseid ühendeid, nagu polüsahhariide ja peptiide, mis võivad pärssida kasvajarakkude proliferatsiooni ja apoptoosi esilekutsumist. Uuringud on näidanud, et keefir võib mõjuda kolorektaalsele ja rinnavähile [96].

cistanche taime suurendav immuunsüsteem
3.1.7. Probiootikumid stressi/ärevuse vastu
Astronautide emotsionaalse ja füüsilise seisundi säilitamine on tulevaste pikaajaliste kosmosemissioonide jaoks otsustava tähtsusega. Stress on kahtlemata üks murettekitavamaid tegureid, mis võib mõjutada meeskonna üldist heaolu, kuna see mõjutab inimeste tervist ja jõudlust [97]. Ärevus ja stress on seotud soolestiku düsbioosiga. Ma et al. [31] teatas, et Lactobacillus plantarum P-8 tarbimine leevendas inimestel ärevuse/stressi sümptomeid. Samuti avastati, et probiootikumide tarbimine rikastas soolestikust pärineva metaboliidi gamma-aminovõihappe (GABA) sünteesirada Bifidobacterium adolescentis'e poolt, GABA ja histamiin on olulised neurotransmitterid, mis liiguvad vaguse närvi kaudu soole-aju teljele.
3.1.8. Probiootikumid kuseteede infektsioonide jaoks
Probiootikumidel, nagu Lactobacillus rhamnosus GR-1 ja Lactobacillus reuteri RC-14, on nakkusvastased omadused, mida on katsetatud naistel ja mis näivad ennetavat UTI-sid võrreldaval määral kui pikamaa ja väikese portsjoni puhul. antimikroobsed ained ilma reaktsioonideta [3].
Tabel 3. Probiootikumid: toimemehhanism ja nende kasulikkus tervisele.

3.1.9. Lühikese ahelaga rasvhapped ja nende roll soolestiku mikrobiota hooldamisel
Probiootikumid võivad toota lühikese ahelaga rasvhappeid (SCFA) [98]. SCFA-d on kääritamise orgaanilised kõrvalsaadused. Need tekivad soolestiku luumenis, kui seedimatud süsivesikud lagundatakse anaeroobses keskkonnas soolestiku mikrobiota poolt mittetäielikult. SCFA-d koosnevad peamiselt atsetaadist, butüraadist ja propionaadist [99 100]. SCFA-del on oluline osa immuunsüsteemi reguleerimisel. Soole lima säilimine, struktuur ja tootmine sõltuvad soolestiku mikrobiotast ja toitumisest. Kiudainerikas dieet põhjustab soolestiku mikrobiota SCFA-de tootmist, mis parandab lima ja antimikroobsete peptiidide tootmist ning TJ-valkude kõrgemat ekspressiooni. Kiudainevaene toitumine põhjustab soolestiku mikrobioota muutumist, mis põhjustab limakihi langust ja suurendab vastuvõtlikkust infektsioonidele ja kroonilistele põletikulistele haigustele [100]. SCFA-d on ka signaalmolekulid, mis reguleerivad interleukiini -18 moodustumist, seondudes soole epiteelirakkude ja immuunrakkude GPR41 ja GPR43 retseptoritega [101]. Silva jt uurimus. [102] on teatanud, et SCFA-del võib olla otsene mõju ajule, toetades hematoentsefaalbarjääri (BBB) terviklikkust, moduleerides neurotransmissiooni, mõjutades neurotroofsete faktorite taset ja soodustades mälu konsolideerimist. Uuring teatas, et SCFA butüraat suurendab soole barjääri funktsiooni. Adenosiinmonofosfaadiga aktiveeritud proteiinkinaas (AMPK) hõlbustab aktiveerimisel tihedat ühenduskohta ja reguleerib rasvhapete metabolismi ja valgusünteesi metaboolseid radu [103]. MARS 500 oli kuus kuud kestnud maapealne eksperiment, mis hõlmas kuue meeskonnaliikme väljaheidete uurimist. Tulemused näitasid butüraati tootvate Faecalibacterium prausnitzii ja Roseburia faecise suhtelise arvukuse pidevat varieerumist kõigi meeskonnaliikmete soolestiku mikrobiotas. See näitab muutust SCFA tootmises ja võimalikke tagajärgi mikrobiota ja peremeesorganismi vastastikuse suhte toetamisel [7]. Lunar Palace 1 on veel üks katse, mis viidi läbi kohapeal. Bioregeneratiivse elu toetamise süsteemi (BLSS) toimimise testimiseks kasutati kolme meeskonnaliiget. Nad tarbisid kiudainerikast dieeti ja järgisid kindlat ajakava, mis hõlmas olulist käsitsitööd tehase salongis. Tulemused näitasid sarnaseid muutusi soolestiku mikrobiota koostises meeskonnaliikmetel, kellel oli suur hulk Lachnospira, Faecalibacterium ja Blautia mikroorganisme. See näeb ette ka seda, et kiudainerikas dieet ja elustiil võivad olla kasulikud soolestiku terve mikrobiota toetamiseks [32].
3.2. Mikrogravitatsiooni / simuleeritud mikrogravitatsiooni uuringud probiootikumide kohta
Et probiootikum oleks tõhus, peavad sellel olema teatud spetsiifilised omadused. Mõned neist on stabiilsus happe ja sapi suhtes, kleepumine inimese soolerakkudele, antagonism enteraalsete patogeenide suhtes ja antimikroobsete ainete tootmine. Need omadused võivad aga keskkonnategurite ja mikrogravitatsiooni mõjul muutuda. Probiootikumide testimiseks in vitro ja in vivo tingimustes on tehtud mitmeid uuringuid, et mõista nende võimalikku kasu tervisele ja ohutust astronautide tervisele kosmoselendude ajal. Järgmistes lõikudes võtame mõned neist uuringutest kokku. Shao jt poolt läbi viidud uuring. [104] simuleeritud mikrogravitatsioonitingimuste mõju uurimine Lactobacillus acidophilus'ele näitas märkimisväärset mõju mõnele bioloogilisele aktiivsusele ja omadustele. Peamised leiud olid (1) oluliste muutuste puudumine L. acidophilus'e morfoloogias, (2) lühenenud viivitusfaas, (3) suurenenud kasvukiirus, (4) suurenenud taluvus hapete suhtes (pH 2,5) koos resistentsusega sapi suhtes, (5) vähenenud. tundlikkus naatriumpenitsilliini, tsefaleksiini ja väävelgentamütsiini suhtes, (6) L. acidophilus'e adhesioonivõime olulist muutust ei leidnud ja (7) suurenenud antimikroobne toime S. aureus'e ja S. Typhimurium'i vastu. Need muutused, mis on põhjustatud simuleeritud mikrogravitatsioonist (SMG) L. acidophilus probiootikumidel, võivad kosmoselendude ajal astronautidele kasulikud olla. Need probiootikumid taluvad stressirohkeid tingimusi ja püsivad seedetraktis pikema aja jooksul. Kuna selle kleepumisvõime ei muutu, võib see aidata säilitada sooleepiteeli barjääri funktsiooni ja takistada patogeenide sisenemist [103]. Teises uuringus on Senatore et al. [105] uuris Lactobacillus reuteri metabolismi ja geeniekspressiooni SMG tingimustes. Nad ei leidnud muutusi bakterite kasvus, rakkude suuruses ja kujus võrreldes kontrolliga. Teisest küljest täheldati suurenenud tolerantsust seedetrakti läbimise suhtes ja bioaktiivse ühendi reuteriini suurenenud tootmist [32]. Külmkuivatatud Lactobacillus casei tüve Shirota kapsli (LcS) stabiilsust testiti ISS-is kuu aega. Kosmoselennult saadud LcS-kapslid ei erinenud maapealses laboris hoitavate kontrollproovide osas geneetiliste profiilide, kasvumustrite, süsivesikute fermentatsiooni, reaktiivsuse LcS-spetsiifiliste antikehade suhtes ja tsütokiinide indutseerimise võime poolest. On näidatud, et LcS suurendab kaasasündinud immuunsust ja tasakaalustab soolestiku mikrobiotat ning seda saab kasutada kosmoselendudega seotud immuunprobleemide vastu võitlemiseks [6, 44].
3.3. Kaubanduslike probiootikumide säilivusaeg ja ellujäämine simuleeritud seedekulglas
Kolme kaubandusliku probiootikumi, nimelt Lactobacillus acidophilus'e tüve DDS-1, Bifidobacterium longum tüve BB536 ja Bacillus subtilis'e tüve HU58 eoste ellujäämist testiti tingimustes, mida oodatakse 3-aastaringsel Marsi reisil. Testitud parameetrid olid ellujäämine: 1. Pikaajaline säilitamine ümbritseva keskkonna tingimustes; 2. Simuleeritud galaktiline kosmiline kiirgus ja päikeseosakeste sündmuste kiirgus; 3. kokkupuude simuleeritud maovedelikuga; 4. Kokkupuude simuleeritud soolevedelikuga. Uuringu kohaselt ei mõjutanud kiirgus uuritud probiootilisi tüvesid vähe. Kolme tüve kõlblikkusaeg ja ellujäämismäärad erinesid aga oluliselt nende läbimise simuleerimisel seedetrakti ülaosast. Leidude kohaselt võisid kõigis tingimustes ellu jääda ainult Bacillus subtilise eosed. See viitab sellele, et bakterite spooridest koosnevad probiootikumid võivad olla elujõuline valik inimeste pikaajalisteks kosmosereiside jaoks [106].
4. Järeldused
Pikaajaliste kosmosereiside puhul on ülioluline tegur astronaudi tervise säilitamine. Lennumeeskonna tervises on täheldatud mitmesuguseid füsioloogilisi muutusi, sealhulgas soolestiku mikrobioomi muutus, mis põhjustab MGB telje mõju vaimsele tervisele, urogenitaaltrakti infektsioonid, viiruse taasaktiveerumine, bakterite resistentsus ja muutused virulentsuses, immuunsuse vähenemine ja muutused immuunvastuses, südame-veresoonkonna probleemid ja kiirgusega kokkupuutest tingitud vähi areng. See ülevaade püüab mõista probiootikumide võimalikku kasutamist, mida saab kasutada kosmoselendudest põhjustatud terviseprobleemide lahendamiseks. Soolestiku mikrobioomi säilitamine on oluline pikaajaliste kosmosereiside jaoks ning paljud haigused on põhjustatud soolestiku mikrobioomi muutustest või tasakaalustamatusest. Probiootikumide teadaolevate eeliste tõttu soolestiku mikrobioomile ja üldisele tervisele võib nende kasutamine toidulisandina või toidulisandina kosmoselendude ajal olla paljulubav alternatiiv kosmosereisijate kogetud regulatsioonihäirete ja tervisemõjude vastu. Probiootikumidega simuleeritud mikrogravitatsioonitingimustes tehtud katsed ei jäljenda aga täielikult pikaajalist kosmosereisi. Probiootikumide kohta tuleb läbi viia rohkem uuringuid, et kinnitada nende kasutamist kosmoses, kontrollida nende efektiivsust ülalmainitud terviseprobleemide vastumeetmetena ja muuta probiootikumide omadusi, mis võivad ilmneda kosmoselendude ajal.
Viited
1. Voorhies, AA; Mark Ott, C.; Mehta, S.; Pierson, DL; Crucian, BE; Feiveson, A.; Oubre, CM; Torralba, M.; Moncera, K.; Zhang, Y.; et al. Rahvusvahelise kosmosejaama pikaajaliste kosmosemissioonide mõju uurimine astronautide mikrobioomile. Sci. Rep. 2019, 9, 9911. [CrossRef] [PubMed]
2. Yim, J.; Cho, SW; Kim, B.; Park, S.; Han, YH; Seo, SW Probiootilise Escherichia coli issue 1917 tüve transkriptsiooniline profileerimine simuleeritud mikrogravitatsioonil. Int. J. Mol. Sci. 2020, 21, 2666. [CrossRef]
3. Urbaniak, C.; Reid, G. Mikrobioota ja probiootikumide võimalik mõju naistele pikkade kosmoselendude ajal. Womens Health 2016, 12, 193–198. [CrossRef]
4. Hill, C.; Guarner, F.; Reid, G.; Gibson, GR; Merenstein, DJ; Pot, B.; Morelli, L.; Canani, RB; Flint, HJ; Salminen, S.; et al. Rahvusvahelise Probiootikumide ja Prebiootikumide Teadusliku Assotsiatsiooni konsensusavaldus termini probiootikum ulatuse ja asjakohase kasutamise kohta. Nat. Rev Gastroenterol. Hepatol. 2014, 11, 506–514. [CrossRef]
5. Matsumoto, K.; Takada, T.; Shimizu, K.; Kado, Y.; Kawakami, K.; Makino, I.; Yamaoka, Y.; Hirano, K.; Nishimura, A.; Kajimoto, O.; et al. Lactobacillus casei tüve Shirota sisaldava probiootilise piimatoote mõju mitteoptimaalse tervisliku seisundiga vabatahtlike roojamissagedusele ja soolestiku mikrofloorale: Randomiseeritud platseebokontrolliga ristuuring. Biosci. Mikrofloora 2006, 25, 39–48. [CrossRef]
6. Sakai, T.; Moteki, Y.; Takahashi, T.; Shida, K.; Kiwaki, M.; Shimakawa, Y.; Matsui, A.; Chonan, O.; Morikawa, K.; Ohta, T.; et al. Probiootikumid avakosmosesse: kapseldatud külmkuivatatud probiootikumide teostatavushinnangud 1-kuulise ladustamise ajal rahvusvahelises kosmosejaamas. Sci. Rep. 2018, 8, 10687. [CrossRef] [PubMed]
7. Turroni, S.; Rampelli, S.; Biagi, E.; Consolandi, C.; Severgnini, M.; Peano, C.; Quercia, S.; Soverini, M.; Carbonero, FG; Bianconi, G.; et al. Soolestiku mikrobiota ajaline dünaamika inimestel, kes jagavad piiratud keskkonda, 520-päevane maapealne kosmosesimulatsioon, MARS500. Microbiome 2017, 5, 39. [CrossRef] [PubMed]
8. Zhang, T.; Li, Q.; Cheng, L.; Buch, H.; Zhang, F. Akkermansia muciniphila on paljulubav probiootikum. Microb. Biotehnoloogia. 2019, 12, 1109–1125. [CrossRef] [PubMed]
9. Sokol, H.; Pigneur, B.; Watterlot, L.; Lakhdari, O.; Bermúdez-Humarán, LG; Gratadoux, JJ; Blugeon, S.; Bridonneau, C.; Furet, JP; Corthier, G.; et al. Faecalibacterium prausnitzii on põletikuvastane kommensaalne bakter, mis tuvastati Crohni tõvega patsientide soolestiku mikrobiota analüüsiga. Proc. Natl. Acad. Sci. USA 2008, 105, 16731–16736. [CrossRef]
10. Gotova, I.; Dimitrov, Z.; Najdenski, H. Bulgaaria jogurti valitud Lactobacillus bulgaricus ja Streptococcus thermophilus tüvedel on märkimisväärne põletikuvastane potentsiaal. Acta Microbiol. Bulg 2017, 33, 137–142.
11. Päev, RL; Harper, AJ; Woods, RM; Davies, OG; Heaney, LM Probiootikumid: praegune maastik ja tulevikuhorisondid. Future Sci. OA 2019, 5, FSO391. [CrossRef] [PubMed]
12. Saraf, K.; Shashikanth, MC; Priy, T.; Sultana, N.; Chaitanya, NC Probiootikumidel on oma roll meditsiinis ja hambaravis. J. Assoc. Physicians India 2010, 58, 488–490.
13. Douglas, G.; Voorhies, A. Tõenditel põhinev probiootiliste tüvede valik astronautide tervise edendamiseks või haigussümptomite leevendamiseks pikaajalistel kosmoselendude missioonidel. Kasu. Mikroobid 2017, 8, 727–737. [CrossRef] [PubMed]
14. Crucian, B.; Stowe, RP; Mehta, S.; Quiriarte, H.; Pierson, D.; Sams, C. Adaptiivse immuunsuse muutused püsivad pikaajalise kosmoselennu ajal. npj Microgravity 2015, 1, 15013. [CrossRef] [PubMed]
15. Liu, Z.; Luo, G.; Du, R.; Sun, W.; Li, J.; Lan, H.; Chen, P.; Yuan, X.; Cao, D.; Li, Y.; et al. Kosmoselendude mõju inimese soolestiku mikrobiota koostisele ja funktsioonile. Soolestiku mikroobid 2020, 11, 807–819. [CrossRef]
16. O'Flaherty, S.; Klaenhammer, TR Probiootiliste bakterite roll ja potentsiaal soolestikus ning suhtlus soolestiku mikrofloora ja soolestiku/peremehe vahel. Int. Meierei J. 2010, 20, 262–268. [CrossRef]
17. Turroni, F.; Ventura, M.; Butto, LF; Duranti, S.; O'Toole, PW; Motherway, MO; Van Sinderen, D. Molekulaarne dialoog inimese soolestiku mikrobiota ja peremeesorganismi vahel: Lactobacillus and Bifidobacterium perspektiiv. Kamber. Mol. Life Sci. 2014, 71, 183–203. [CrossRef]
18. Wall, R.; Cryan, JF; Ross, RP; Fitzgerald, GF; Dinan, TG; Stanton, C. Psühhobiootikumide poolt toodetud bakteriaalsed neuroaktiivsed ühendid. Adv. Exp. Med. Biol. 2014, 817, 221–239.
19. Blaber, E.; Marçal, H.; Burns, BP Bioastronautika: mikrogravitatsiooni mõju astronautide tervisele. Astrobioloogia 2010, 10, 463–473. [CrossRef]
20. Crucian, B.; Babiak-Vazquez, A.; Johnston, S.; Pierson, DL; Ott, CM; Sams, C. Kliiniliste sümptomite esinemine pikaajalise orbitaalse kosmoselennu ajal. Int. J. Gen. Med. 2016, 2016, 383–391. [CrossRef]
21. Garrett-Bakelman, FE; Darshi, M.; roheline, SJ; Gur, RC; Lin, L.; Macias, BR; McKenna, MJ; Meydan, C.; Mišra, T.; Nasrini, J.; et al. NASA kaksikud uurivad inimese aasta kestnud kosmoselennu mitmemõõtmelist analüüsi. Science 2019, 364, 6436. [CrossRef]
22. Siddiqui, R.; Qaisar, R.; Khan, NA; Alharbi, AM; Alfahemi, H.; Elmoselhi, A. Mikrogravitatsiooni mõju soolestiku mikrobiota bakterite koostisele tagajäseme mahalaadimise mudelis. Elu 2022, 12, 1865. [CrossRef] [PubMed]
23. Jiang, P.; roheline, SJ; Chlipala, GE; Turek, FW; Vitaterna, MH Reprodutseeritavad muutused soolestiku mikrobioomis viitavad nihkele mikroobide ja peremeesorganismi ainevahetuses kosmoselennu ajal. Microbiome 2019, 7, 113. [CrossRef] [PubMed]
24. Carabotti, M.; Scirocco, A.; Maselli, MA; Severi, C. Soole-aju telg: enteraalse mikrobiota, kesk- ja enteraalse närvisüsteemi vahelised interaktsioonid. Ann. Gastroenterool. 2015, 28, 203–209. [PubMed]
25. Sajdel-Sulkowska, Mikrobioota-soole-aju (MGB) telje häired ja astronautide vaimne tervis pikaajalisel kosmosereisil. Väikeaju ja väikeaju häirete käsiraamatus; Manto, M., Gruol, D., Schmahmann, J., Koibuchi, N., Sillitoe, R., toim.; Springer: Cham, Šveits, 2019. [CrossRef]
26. Palinkas, LA Psühhosotsiaalsed probleemid pikaajalisel kosmoselennul: ülevaade. Gravit. Space Biol. Bull. 2001, 14, 25–33.
27. Mallis, MM; DeRoshia, CW ööpäevased rütmid, uni ja jõudlus ruumis. Aviat. Kosmose keskkond. Med. 2005, 76, B94–B107. [PubMed]
28. Oluwafemi, FA; Abdelbaki, R.; Lai, JCY; Mora-Almanza, JG; Afolayan, EM Ülevaade astronautide vaimsest tervisest mehitatud missioonidel: potentsiaalsed sekkumised kognitiivsete ja vaimse tervise probleemide lahendamiseks. Life Sci. Space Res. 2021, 28, 26–31. [CrossRef]
29. Arone, A.; Ivaldi, T.; Loganovski, K.; Palermo, S.; Parra, E.; Flamini, W.; Marazziti, D. Kosmoseuuringute koormus astronautide vaimsele tervisele: narratiivne ülevaade. Clin. Neuropsychiatry 2021, 18, 237. [PubMed]
30. Zivi, P.; De Gennaro, L.; Ferlazzo, F. Sleep in isolated, confined and extreme (ICE): ülevaade erinevatest teguritest, mis mõjutavad inimese und ICE-s. Esiosa. Neurosci. 2020, 14, 851. [CrossRef]
31. Ma, T.; Jin, H.; Kwok, LY; Sun, Z.; Liong, MT; Zhang, H. Probiootikumide tarbimine leevendas inimese stressi ja ärevussümptomeid, tõenäoliselt moduleerides soolestiku mikrobiota neuroaktiivset potentsiaali. Neurobiol. Stress 2021, 14, 100294. [CrossRef]
32. Hao, Z.; Li, L.; Fu, Y.; Liu, H. Regeneratiivse elu toetava süsteemi toitumisstruktuuri ja elustiili mõju soolestiku mikrobiootale: 105-päevane maapealne kosmosesimulatsioon Lunar Palace'is 1. Environ. Microbiol. 2018, 20, 3643–3656. [CrossRef] [PubMed]
33. Jones, JA; Jennings, R.; Pietryzk, R.; Ciftcioglu, N.; Stepaniak, P. Urogenitaalprobleemid kosmoselendude ajal: ülevaade. Int. J. Impot. Res. 2005, 17 (lisa 1), S64–S67. [CrossRef] [PubMed]
34. Mishra, B.; Luderer, U. Naiste ja meeste kosmosereiside paljunemisohud. Nat Rev Endokrinool. 2019, 15, 713–730, Erratum in Nat. Rev. Endokrinol. 2019, 15, 713–730. [CrossRef] [PubMed]
35. Sonnenfeld, G.; Shearer, WT immuunfunktsioon kosmoselennu ajal. Toitumine 2002, 18, 899–903. [CrossRef] [PubMed]
36. Rooney, BV; Crucian, BE; Pierson, DL; Laudenslager, ML; Mehta, SK Herpesviiruse taasaktiveerimine astronautidel kosmoselendude ajal ja selle rakendamine maa peal. Esiosa. Microbiol. 2019, 10, 16. [CrossRef]
37. Zhang, B.; Bai, P.; Zhao, X.; Yu, Y.; Zhang, X.; Li, D.; Liu, C. Salmonella enteritidis'e suurenenud kasvukiirus ja amikatsiiniresistentsus pärast ühekuulist kosmoselendu Hiina kosmoseaparaadil Shenzhou{2}}. MicrobiologyOpen 2019, 8, e00833. [CrossRef]
38. Tirumalai, MR; Karouia, F.; Tran, Q.; Stepanov, VG; Bruce, RJ; Ott, CM; Pierson, DL; Fox, GE Omandatud antibiootikumiresistentsuse hindamine Escherichia coli's, mis on kokku puutunud pikaajalise väikese nihkejõuga modelleeritud mikrogravitatsiooni ja antibiootikumide taustaga kokkupuutega. MBio 2019, 10, e02637-18. [CrossRef]
39. Morrison, MD; Thissen, JB; Karouia, F.; Mehta, S.; Urbaniak, C.; Venkateswaran, K.; Smith, DJ; Jain, C. Kosmoselendude põhjustatud muutuste uurimine astronautide mikrobioomides. Esiosa. Microbiol. 2021, 12, 659179. [CrossRef]
40. Turner, JR Soole limaskesta barjääri funktsioon tervise ja haiguste korral. Nat. Rev. Immunol. 2009, 9, 799–809. [CrossRef]
41. Zyrek, AA; Cichon, C.; Helms, S.; Enders, C.; Sonnenborn, U.; Schmidt, MA Escherichia coli Nissle 1917 probiootilise toime aluseks olevad molekulaarsed mehhanismid hõlmavad ZO-2 ja PKCζ ümberjaotumist, mille tulemuseks on tihe ristmik ja epiteeli barjääri paranemine. Kamber. Microbiol. 2007, 9, 804–816. [CrossRef]
42. Johnson-Henry, KC; Donato, KA; Shen-Tu, G.; Gordanpour, M.; Sherman, PM Lactobacillus rhamnosuse tüvi GG hoiab ära enterohemorraagilise Escherichia coli O157:H7- põhjustatud muutused epiteeli barjääri funktsioonis. Nakata. Immun. 2008, 76, 1340–1348. [CrossRef] [PubMed]
43. Alvarez, R.; Stork, CA; Sayoc-Becerra, A.; Marchelletta, RR; Prisk, GK; McCole, DF Simuleeritud mikrogravitatsioonikeskkond põhjustab epiteeli barjääri funktsiooni püsivat defekti. Sci. Rep. 2019, 9, 17531. [CrossRef] [PubMed]
44. Arrieta, MC; Bistritz, L.; Meddings, JB Muutused soolestiku läbilaskvuses. Gut 2006, 55, 1512–1520. [CrossRef]
45. Lee, SH Intestinal Permeability Regulation by Tight Junction: Impplication on Inflammatory Bowel Diseases. Intest. Res. 2015, 13, 11. [CrossRef]
46. Blair, SA; Kane, SV; Clayburgh, DR; Turner, JR Epiteeli müosiini kerge ahela kinaasi ekspressioon ja aktiivsus on põletikulise soolehaiguse korral ülesreguleeritud. Lab. Uurige. 2006, 86, 191–201. [CrossRef]
47. Yi, H.; Wang, L.; Xiong, Y.; Wang, Z.; Qiu, Y.; Wen, X.; Jiang, Z.; Yang, X.; Ma, X. Lactobacillus reuteri LR1 Tight Junction Proteins'i geenide parem ekspressioon MLCK raja kaudu IPEC-1 rakkudes enterotoksigeense Escherichia coli K88-ga nakatumise ajal. Mediat. Põletik. 2018, 2018, 6434910. [CrossRef] [PubMed]
48. Kaur, I.; Simons, ER; Castro, VA; Mark Ott, C.; Pierson, DL Muutused astronautide neutrofiilide funktsioonides. Aju käitumine. Immun. 2004, 18, 443–450. [CrossRef]
49. Stowe, RP; Sams, CF; Pierson, DL Missiooni kestuse mõju astronautide neuroimmuunvastustele. Aviat. Kosmose keskkond. Med. 2003, 74, 1281–1284.
50. Makedonas, G.; Mehta, S.; Choukèr, A.; Simpson, RJ; Marshall, G.; oranž, JS; Aunon-kantsler, S.; Smith, SM; Zwart, SR; Stowe, RP; et al. Spetsiifiline immunoloogiliste vastumeetmete protokoll süvakosmose uurimise missioonide jaoks. Esiosa. Immunol. 2019, 10, 2407. [CrossRef]
51. Buchheim, JI; Matzel, S.; Rykova, M.; Vassiljeva, G.; Ponomarjov, S.; Nichiporuk, I.; Hörl, M.; Moser, D.; Biere, K.; Feuerecker, M.; et al. Stressiga seotud nihe põletiku suunas kosmonautidel pärast pikaajalist kosmoselendu. Esiosa. Physiol. 2019, 10, 85. [CrossRef]
52. Akiyama, T.; Horie, K.; Hinoi, E.; Hiraiwa, M.; Kato, A.; Maekawa, Y.; Takahashi, A.; Furukawa, S. Kuidas kosmoselend mõjutab omandatud immuunsüsteemi? npj Microgravity 2020, 6, 14. [CrossRef]
53. Kaur, I.; Simons, ER; Castro, VA; Ott, CM; Pierson, DL Muutused astronautide monotsüütide funktsioonides. Aju käitumine. Immun. 2005, 19, 547–554. [CrossRef] [PubMed]
54. Voss, EW Pikaajaline kaaluta olek ja humoraalne immuunsus. Teadus 1984, 225, 214–215. [CrossRef] [PubMed]
55. Mills, PJ; Meck, JV; Waters, WW; D'Aunno, D.; Ziegler, MG Perifeersete leukotsüütide alampopulatsioonid ja katehhoolamiinide tase astronautidel missiooni kestuse funktsioonina. Psühhosoom. Med. 2001, 63, 886–890. [CrossRef] [PubMed]
56. Stowe, RP; Sams, CF; Mehta, SK; Kaur, I.; Jones, ML; Tagasiside, DL; Pierson, DL Leukotsüütide alamhulgad ja neutrofiilide funktsioon pärast lühiajalist kosmoselendu. J. Leukoc. Biol. 1999, 65, 179–186. [CrossRef]
57. Guell, A.; Braak, L. Südame-veresoonkonna dekonditsioneerimise sündroom kosmoselendude ajal. Ann. Kardiol. D'angéiol. Pariis 1989, 38, 499–502.
58. Tang, H.; Tõusev, HH; Majji, M.; Brown, RD pikaajaline kosmose toitumine: ulatuse ülevaade. Toitained 2021, 14, 194. [CrossRef]
59. Caiani, EG; Martin-Yebra, A.; Landreani, F.; Bolea, J.; Laguna, P.; Vaida, P. Kaalutus ja südame rütmihäired: praegused teadmised kosmoselendude ja voodipuhkuse uuringutest. Esiosa. Astron. Space Sci. 2016, 3, 27. [CrossRef]
60. Jian, Y.; Zhang, D.; Liu, M.; Wang, Y.; Xu, Z.-X. Soolestiku mikrobiota mõju kiirgusest põhjustatud enteriidile. Esiosa. Kamber. Nakata. Microbiol. 2021, 11, 586392. [CrossRef]
61. Tesei, D.; Jewczynko, A.; Lynch, A.; Urbaniak, C. Astronaudi mikrobioomi keerukuse ja muutuste mõistmine edukate pikaajaliste kosmosemissioonide jaoks. Elu 2022, 12, 495. [CrossRef]
62. Durante, M.; Cucinotta, FA Raskeioonide kantserogenees ja inimese kosmoseuuringud. Nat. Rev. Cancer 2008, 8, 465–472. [CrossRef] [PubMed]
63. Stahn, AC; Werner, A.; Opatz, O.; Maggioni, MA; Steinach, M.; von Ahlefeld, VW; Moore, A.; Crucian, BE; Smith, SM; Zwart, SR; et al. Pikaajaliste kosmosemissioonide ajal astronautide kehatemperatuuri tõus. Sci. Rep. 2017, 7, 16180. [CrossRef] [PubMed]
64. Kligler, B.; Cohrssen, A. Probiootikumid. 2008. Internetis saadaval: www.aafp.org/afp (kasutatud 25. jaanuaril 2022).
65. Cunningham, M.; Azcarate-Peril, MA; Barnard, A.; Benoit, V.; Grimaldi, R.; Guyonnet, D.; Holscher, HD; Hunter, K.; Manurung, S.; Obis, D.; et al. Probiootikumide ja prebiootikumide tuleviku kujundamine. Trends Microbiol. 2021, 29, 667–685. [CrossRef]
66. Shi, LH; Balakrishnan, K.; Thiagarajah, K.; Mohd Ismail, NI; Yin, OS Probiootikumide kasulikud omadused. Trop. Life Sci. Res. 2016, 27, 73–90. [CrossRef]
67. Ulluwishewa, D.; Anderson, RC; McNabb, WC; Moughan, PJ; Wells, JM; Roy, NC Soolebakterite ja toidukomponentide tiheda ristmiku läbilaskvuse reguleerimine. J. Nutr. 2011, 141, 769–776. [CrossRef] [PubMed]
68. Mack, DR; Ahrne, S.; Hyde, L.; Wei, S.; Hollingsworth, MA Ekstratsellulaarne MUC3 mutsiini sekretsioon järgneb Lactobacillus'e tüvede kleepumisele in vitro sooleepiteelirakkudele. Gut 2003, 52, 827–833. [CrossRef]
69. Caballero-Franco, C.; Keller, K.; De Simone, C.; Chadee, K. VSL#3 probiootiline valem kutsub esile mutsiini geeniekspressiooni ja sekretsiooni käärsoole epiteelirakkudes. Olen. J. Physiol. – Seedetrakt. Maksa füsiool. 2007, 292, G315–G322. [CrossRef]
70. Otte, JM; Podolsky, DK Enterotsüütide funktsionaalne moduleerimine grampositiivsete ja gramnegatiivsete mikroorganismide poolt. Olen. J. Physiol. – Seedetrakt. Maksa füsiool. 2004, 286, G613–G626. [CrossRef]
71. Kankainen, M.; Paulin, L.; Tynkkynen, S.; Von Ossowski, I.; Reunanen, J.; Partanen, P.; Satokari, R.; Vesterlund, S.; Hendrickx, APA; Lebeer, S.; et al. Lactobacillus rhamnosus GG võrdlev genoomanalüüs näitab pilusid, mis sisaldavad inimese lima siduvat valku. Proc. Natl. Acad. Sci. USA 2009, 106, 17193–17198. [CrossRef]
72. Mukai, T.; Kaneko, S.; Matsumoto, M.; Ohori, H. Bifidobacterium bifidum'i ja Lactobacillus reuteri sidumine maapähkli aglutiniini poolt äratuntavate soole glükolipiidide süsivesikute osadega. Int. J. Food Microbiol. 2004, 90, 357–362. [CrossRef]
74. Tallon, R.; Arias, S.; Bressollier, P.; Urdaci, MC Lactobacillus plantarum'i tüvest ja maatriksist sõltuvat adhesiooni vahendavad valgulised bakteriaalsed ühendid. J. Appl. Microbiol. 2007, 102, 442–451. [CrossRef] [PubMed]
74. Wilson, KH; Perini, F. Toitainete konkurentsi roll käärsoole mikrofloora poolt Clostridium difficile pärssimisel. Nakata. Immun. 1988, 56, 2610–2614. [CrossRef] [PubMed]
75. Dai, C.; Zheng, CQ; Jiang, M.; Ma, XY; Jiang, LJ Probiootikumid ja ärritunud soole sündroom. Maailm J. Gastroenterool. 2013, 19, 5973–5980. [CrossRef] [PubMed]
76. Toi, M.; Hirota, S.; Tomotaki, A.; Sato, N.; Hozumi, Y.; Anan, K.; Nagashima, T.; Tokuda, Y.; Masuda, N.; Ohsumi, S.; et al. Probiootiline jook soja isoflavooniga rinnavähi ennetamiseks: juhtumite kontrolli uuring. Curr. Nutr. Food Sci. 2013, 9, 194–200. [CrossRef]
77. Buckley, ND; Šampanja, CP; Masotti, AI; Wagar, LE; Tompkins, TA; Green-Johnson, JM Funktsionaalsete toidustrateegiate rakendamine kosmosereiside terviseprobleemide lahendamiseks – fermenteeritud soja astronautide toitumiseks. Acta astronaut. 2011, 68, 731–738. [CrossRef]
78. Rao, RK; Samak, G. Probiootikumide soolebarjääri kaitsmine ja taastamine: toitumis- ja kliiniline mõju. Curr. Nutr. Food Sci. 2013, 9, 99–107. [CrossRef] [PubMed]
79. Galdeano, CM; Perdigón, G. Probiootiliste tüvede elujõulisuse roll nende säilimisel soolestikus ja limaskestade immuunsüsteemisstimuleerimine.J. Appl. Microbiol.2004, 97, 673–681. [CrossRef]
