4-Aminopüridiini neuroprotektiivsed omadused
Mar 19, 2022
Kontakt: Audrey Hu Whatsapp/hp: 0086 13880143964 E-post:audrey.hu@wecistanche.com
Michael Dietrich, PhD, Hans-Peter Hartung, MD, PhD, FRCP ja Philipp Albrecht, MD
Abstraktne
Pingepõhiste kaaliumikanalite (Kv) antagonistina kasutatakse 4-aminopüridiini (4-AP) sümptomaatilise ravina mitmete neuroloogiliste häirete korral. Nägemisfunktsiooni ja motoorsete oskuste paranemist ning väsimuse leevendamist SM-ga patsientidel on seostatud 4-AP-ga. Selle toimeainet prolongeeritult vabastav ravimvorm (fampridiin) on heaks kiidetud SM-i kõndimispuude sümptomaatiliseks raviks. Kasulikke mõjusid seletati aksonaalsete Kv-kanalite blokeerimisega, suurendades seeläbi juhtivust mööda demüeliniseerunud aksoneid. Üha rohkem tõendeid viitab aga sellele, et 4-AP-l võib lisaks sümptomaatilisele toimeviisile olla täiendavaid omadusi. Selles ülevaates võtame kokku prekliinilised ja kliinilised andmed 4-AP võimalike neuroprotektiivsete omaduste kohta.
4-Aminopüridiin neuroloogiliste haiguste korral
Aminopüridiinid on rühm püridiini monoamiini ja diamino derivaate, mis inhibeerivad pingepõhiseid kaaliumi (Kv) kanaleid. Eriti on uute uuritavate ainetena kasutatud kahte laia toimespektriga kaaliumikanali blokaatorit 4-aminopüridiini (4-AP) ja 3,4-aminopüridiini (3,4- DAP). mitmesuguste neuroloogiliste haiguste korral. Kuigi 3,4-DAP on tugevam kaaliumikanalite antagonist, 4-AP läbib hematoentsefaalbarjääri kergemini1 ja oli SM-ga patsientidel kliiniliselt parem, eriti nägemisfunktsiooni parandamisel,2 väsimuse korral. ,3 tunnetus,4 ja kõndimiskiirus.1 Lisaks on teatatud, et 4-AP hõlbustab närvijuhtivust muude neuroloogiliste haiguste korral kui MS.5,6
Tistanche mõju: Kaitske neuroneid
Tervetel aksonitel on kanalid Kv1.1 ja Kv1.2 koondunud Ranvieri sõlmede lähedusse.7 Need kanalid paljastuvad pärast demüeliniseerumist ja migreeruvad läbi demüeliniseerunud segmendi. Samal ajal suureneb nende kanalite ekspressioon mitu korda.8 Selline Kv-kanalite vale ümberjaotumine kahjustab aktsioonipotentsiaalide ülekandmist, mis viib püsiva puudeni. 4-AP blokeerib need avatud kaaliumikanalid ja suurendab seetõttu signaaliülekannet.9,10Kv1.3 kanal avastati inimese T-rakkudes,11 leiti, et see ekspresseerub tugevalt põletikulistel infiltraatidel MS ajus12 ja on mida ekspresseeritakse makrofaagidel, mikrogliia ja efektormälu T-rakkudel.13 Selektiivsed ja mitteselektiivsed Kv1.3 kanali blokaatorid võivad seega pakkuda immunomoduleerivaid omadusi, pärssides rakkude proliferatsiooni ja põletikueelset tsütokiini sekretsiooni.14 Enne 2009. aastat tehtud uuringud ei suutnud kindlaks teha 4-AP-d SM sümptomaatiline ravi, kuna ravimite tase veres oli patsientidel ettearvamatu ning ülemääraseid annuseid seostati epilepsiahoogude ja teadvusehäirete riskiga.15–18 Seetõttu töötati välja fampridiin, 4-AP toimeainet prolongeeritult vabastav ravimvorm ja on hiljem heaks kiidetud SM-i kõndimispuude sümptomaatiliseks raviks.19–23 Huvitaval kombel viitab viimasel ajal üha rohkem tõendeid, et peale nende tunnustatud sümptomaatilise toime tõttu võib 4-AP-l olla täiendavaid kaitsvaid omadusi.
4-AP hindamine, kasutades in vitro mudeleid
In vitro on paljudes mudelites täheldatud 4-AP neuroprotektiivset toimet. Kui amüotroofse lateraalskleroosiga patsientide indutseeritud pluripotentsetest tüvirakkudest diferentseeruvad motoorsed neuronid (MN-id) puutusid kokku 4-AP-ga, ioonkanalite tasakaalustamatus paranes, neuronite aktiivsuse tase tõusis, endoplasmaatiline retikulum stress vähenes ja kaspaaside aktiveerimine nõrgeneb. Mutantsed MN-id näitasid madalamat naatriumivoolu ja Na pluss / K pluss suhet, mis võib vähemalt osaliselt olla nende ülierutuvuse põhjuseks. See muutus pärast 4-AP-ravi, mis viis kaaliumivoolu vähenemiseni ning spontaansete aktiivsusmustrite ja sünaptilise sisendi taastamiseni MN-des.24 4-AP-ravi vähendas põletikueelsete vahendajate vabanemist inimese mikrogliiast, mis oli nakatatud amüloid- beeta- ja kaitstud kultiveeritud roti hipokampuse neuronid, mis ujutati amüloid-beetaga töödeldud mikrogliia supernatantides.25 4-AP derivaat vähendas Parkinsoni tõve in vitro mudelis väidetavalt sünukleiini akumulatsiooni, oksüdatsiooni, põletikku ja Rho kinaasi aktivatsiooni.26 Teised in vitro uuringud teatasid, et 4-AP suurendas cAMP-reaktsiooni elemente siduva valgu fosforüülimist, mis on kaitstud rakulise stressi eest glutamaadi, NMDA ja 3-nitropropioonhappe poolt, mis avaldasid roti vastsündinute väikeaju graanulite neuronitele. Glutamaat põhjustab elujõulisuse vähenemist ka rakkudes, mis on eelkonditsioneeritud 4-AP-ga, kuid ilma kaspaasi olulise aktiveerimiseta{16}}. Need tähelepanekud näitasid, et 4-AP on peamiselt efektiivne nekrootilise eksitotoksilisuse vastu.27 Samuti näidati, et see kaitseb primaarseid neuronaalseid kultuure hapniku-glükoosi puuduse või ouabaiini/DL-kolme{21}}bensüüloksüasparagiinhappe toksilisuse eest.28

Cistanche neuroprotektiivne toime
Prekliinilised in vivo uuringud 4-AP kohta
Mitmed uuringud on uurinud 4-AP kaitsvat toimet erinevate haigusmudelite puhul (tabel 1). Perifeersete närvikahjustuste närvipurustusmudelites ajendas profülaktiline ja varajane 4-AP-ravi närvijuhtivuse kiiruse taastuma, soodustas remüeliniseerumist ja suurendas aksonite piirkonda. Viimaseid tähelepanekuid seletati elektrilise stimulatsiooni järgsete mõjudega, näiteks neuronite ajust pärineva neurotroofse faktori (BDNF) taseme tõus.29 Alzheimeri tõve mudelis amüloid-beeta süstimine Sprague Dawley hipokampusesse. rotid põhjustasid neuronite kahjustusi ja suurendasid mikrogliia aktivatsiooni. Leiti, et 1 mg/kg 4-AP igapäevane manustamine pärsib mikrogliia aktivatsiooni ja tagab neuroprotektsiooni. Selle põhjuseks oli 4-AP võime blokeerida mitteinaktiveeriv väljapoole rektiveerivat K pluss voolu aktiveeritud mikroglias ja vähendada põletikueelsete tsütokiinide tootmist rakkudes.25 Uuringud, milles kasutati kainaadist põhjustatud hipokampuse neurotoksilisuse in vivo mudelit, näitasid { tugevat neuroprotektiivset toimet. {11}}AP, mille võib tühistada mittekonkureeriv NMDA retseptori antagonist MK-801 ja adenosiini A1 antagonist 8-tsüklopentüülteofülliin. Need tähelepanekud viitavad sellele, et NMDA retseptorid on selles mudelis 4-AP-vahendatud kaitse jaoks olulised.30 Lewise rottide autoimmuunse neuropaatia loommudelis parandas 4-AP kliinilist raskust ja patoloogilisi elektrofüsioloogilisi leide. Autorid väitsid, et aksonite kaitse tagati naatriumi vahendatud sissepoole suunatud voolude blokeerimine varases faasis, kuna kõrge membraanipotentsiaal põletiku ägedas faasis võib olla neurotoksiline. Kroonilises faasis paranes närvijuhtivus potentsiaalselt, blokeerides kaaliumi vahendatud väljavoolu.1

Eksperimentaalse autoimmuunse entsefalomüeliidi (EAE) puhul, mis on immuunvahendatud kesknärvisüsteemi põletiku mudel, mis replitseerib MS põhilisi tunnuseid, inhibeerib Kv-kanalite blokaad T-rakkude aktivatsiooni, potentsiaalselt Kv1.3 alamperekonna kanalite blokeerimise ja aksonaalse demüelinisatsiooni nõrgenemise kaudu. ja degeneratsioon, toimides astroglia K.3.1 kanalile, mis võib potentsiaalselt indutseerida BDNF signaali. molva. SJL-hiirte proteolipiidvalgu poolt indutseeritud EAE korral parandas AP-ravi märkimisväärselt digitaalseid skoori, mis kinnitati patoloogiliselt. Täheldati, et gliafibrillaarse happelise valgu ekspressioon oli 4-AP-ga ravitud hiirtel allareguleeritud ning T-rakkude aktivatsioon ja Th1/17 polarisatsioon olid leevendunud. Kuid kroonilise müeliini oligodendrotsüütide glükoproteiini (MOG) peptiidiga indutseeritud EAE mudelis C57BL/6 hiirtel ei muutnud 4-AP EAE kulgu.5 Teises uuringus uuriti ka {{19} }AP MOG-EAE mudelis C57BL/6 hiirtel ja teatati sümptomaatilisest, kuid mitte haigust modifitseerivast toimest. Ei profülaktiline ega terapeutiline 4-AP-ravi ei vähendanud digitaalse EAE kulgu raskust, samas kui 4-AP-ga ravitud loomade liikuvus paranes jalajälje ja rotarodanalüüsi põhjal. Seljaaju demüelinisatsioon, neuronite kahjustused ja aju mahu muutuste MRI-kujutised ei muutunud. Samuti ei mõjutanud CD4* T-rakkude proliferatsioon, IL17 või IFN-y tootmine.3
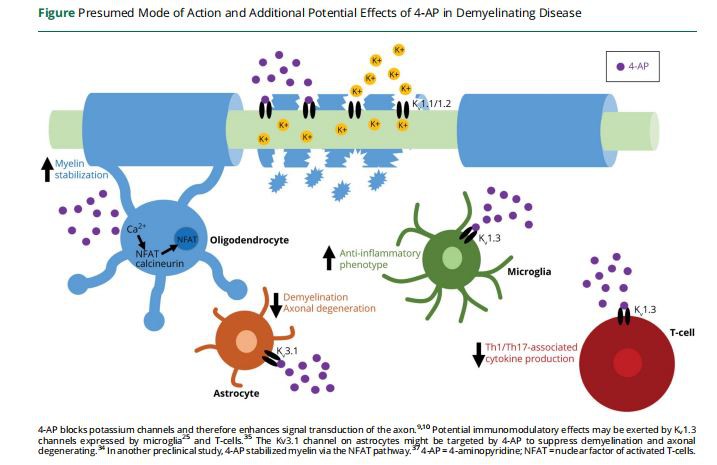
Hiljuti oleme näidanud, et lisaks sümptomaatilisele mõjule närvijuhtivuse parandamisele võib 4-AP ennetada võrkkesta neurodegeneratsiooni MOG-peptiidist põhjustatud eksperimentaalse optilise neuriidi (EAEON) ajal C5BL6 hiirtel.'Kasutades in vivo optilise koherentsus tomograafiat( OCT) pildistamise, visuaalse funktsiooni testimise ja histoloogilise hindamise käigus täheldasime EAEON-i mudelites võrkkesta sisekihtide degeneratsiooni ulatuse vähenemist nii profülaktilise kui ka terapeutilise 4-AP manustamise korral. Selles mudelis võimendas 4-AP sfingosiin-1-fosfaatretseptori modulaatori fingolimoodiga immunomoduleeriva ravi mõju, mis viitab sõltumatutele toimeviisidele. On mõistlik eeldada, et see toime ei piirdu ainult fingolimoodiga ja on rakendatav 4-AP-le koos teiste MS immunomoduleerivate ravimitega. Meie uuringus selgus nägemisnärvi histoloogiast, et erinevalt fingolimoodist ei avaldanud 4-AP olulist mõju mikrogliia aktivatsioonile ja/või lümfotsüütide või makrofaagide infiltratsioonile, mis viitab sellele, et kaitsev toime ei olnud seotud põletikuvastase režiimiga. tegevusest. Kooskõlas sellega ei mõjutanud 4-AP-ravi EAE indutseerimist, mida kinnitas T-rakkude restimulatsioonianalüüs. Lisaks täheldasime 4-AP-ravi ajal märkimisväärset kaitset võrkkesta neurodegeneratsiooni eest ka mittepõletikulise nägemisnärvi purustamise mudeli puhul, samas kui fingolimoodil ei olnud siin mingit mõju. Huvitaval kombel ei suutnud 4-AP-ravi in vitro võrkkesta ganglionrakke otseselt kaitsta. Selle asemel näitasid histoloogia ja in vitro katsed 4-AP-vahendatud müeliini ja oligodendrotsüütide prekursorrakkude stabiliseerumist. Seda toimet seostati suurenenud kaltsiumi sissevoolu ja aktiveeritud T-rakkude tuumafaktori (NFAT) tuuma translokatsiooniga. Varem on näidatud, et 4-AP reguleerib kaltsiumi homöostaasi, tõstes inositooltrifosfaadi taset ja põhjustades seeläbi kaltsiumi vabanemist rakusisest kaltsiumivarudest. Siiski võivad nende seisundite kinnitamiseks abiks olla täiendavad uuringud 4-AP kohta demüeliniseerivatel mudelitel, näiteks kuprisoonravi või indutseeritava oligodendrotsüütide ablatsiooniga transgeensed hiiremudelid. Olemasolevad demüelinisatsiooni loommudelite uuringud keskenduvad peamiselt 4-AP võimele taastada aktsioonipotentsiaal, kuid puudusid oligodendrogliiarakkude edasised uuringud (joonis).

Oluline on mainida, et nende toime saavutamiseks in vitro vajalikud annused on ligikaudu 100-1,000x suuremad kui patsientidel saavutatud kontsentratsioon. Seetõttu võivad in vivo ja in vitro tehtud vaatluste jaoks olla olulised täiendavad või muud mehhanismid. Nende hulka kuuluvad (kuid mitte ainult) demüeliniseerunud aksonite vähenenud energia hajumine, mis on tingitud kaaliumi lekke blokeerimisest ning aju tugevamatest kaitse- ja reparatiivsetest võimetest, mis on kaudselt tingitud suurenenud liikuvusest ja suuremast treeningust.
Lisaks ei saa välistada 4-AP immunomoduleerivaid mehhanisme, eriti kuna PLP-indutseeritud EAE SJL hiirtel on näidatud T-rakkude aktivatsiooni ja Th1/17 polarisatsiooni vähenemist.3 Lisaks leiti teiste haigusmudelite prekliinilistes uuringutes. põletikueelsete vahendajate nõrgenenud aktiveerimine ja vähenenud vabanemine mikrogliia poolt. Need vastuolulised tulemused toovad esile erinevate loommudelite mitmekesised patoloogilised mehhanismid, kus immuunrakud on ravistrateegiatele enam-vähem vastuvõtlikud. Lahknevused meie tulemuste ja varasemate teadete vahel, mis käsitlevad MOG peptiidist põhjustatud EAE sümptomaatilist toimet C57BL6 hiirtel", võib vähemalt osaliselt seletada (1) erinevustega annustes, kuna teised kasutasid annuseid 100 ug ja 600 ug hiire kohta päevas, arvestades, et me manustasime 250 ug hiire kohta päevas;(2) ravi kestus (vastavalt 40, 60 ja 90 päeva, Göbel jt*, Moriguchi jt,3 ja Dietrich jt); ja (3) immuniseerimiseks kasutatud MOG kogus, kuna me kasutasime 200 ug MOG hiire kohta, samas kui teised kasutasid ainult 100 ug MOG hiire kohta. Hiljutised uuringud keskenduvad soolestiku mikrobiota rollile EAE esilekutsumise ja raskuse mõjutamisel, muutes efektor- ja regulatoorsete T- ja B-rakkude tasakaalu. Näriliste mikrobioom võib loomarajatiste vahel erineda, mille tulemuseks on erinevused EAE raskusastmes, kulgemises ja võib-olla isegi ravivastuses. Kokkuvõttes võivad need tegurid põhjustada uuringutulemuste heterogeensust.

Cistanche neuroprotektiivne toime
Kliiniline lähenemine 4-AP-le MS-ga patsientidel
Mitmed kliinilised uuringud alates 1980. aastatest viitasid juba 4-AP kasulikule mõjule MS-ga inimestele. Muuhulgas tuvastasid nad motoorsete40-2 ja visuaalsete funktsioonide-44 paranemise ja väsimuse.5-7 Kuid uuringu piirangud, homogeense uuringuplaani puudumine ja väike patsientide arv keelasid {{ heakskiitmise. 5}}Tavaliste ametivõimude poolt AP ja see põhjustas märgistusevälist kasutamist enam kui 3 aastakümne jooksul.4 Teisest küljest hõlbustasid mõned neist uuringutest toimeainet prolongeeritult vabastava preparaadi (SR-4-AP või fampridiin) väljatöötamist, kuna nad leidsid, et esialgse koheselt vabastava ühendi plasmatasemed on ebajärjekindlad ja ettearvamatud. Esimese kliinilise uuringu SR-4-AP-ga viisid läbi 1997. aastal Schwid et al.,49 mis näitas kõndimiskiiruse märkimisväärset paranemist ja lihasjõu paranemise suundumust.
Pikendatud vabanemisega tehnoloogiasüsteemi töötas välja Elan Pharmaceuticals. Selles kasutati niinimetatud maatriksravimite absorptsioonisüsteemi, mis koosneb patenteeritud polümeermaatriksist, mis kontrollib vabanemist difusiooni ja seedetrakti ensüümide erosiooni teel. Selle tulemuseks oli madalam ravimi maksimaalne tase plasmas ja pikem toimeaeg.1 Esialgu testiti SR-4-AP-d neljas uuringus. 2007. aastal viisid Goodman jt 1 läbi 36 SM-ga patsiendil annusevahemiku 5 mg kaupa 10 kuni 40 mg kaks korda päevas. Ajastatud 25 jala kõndimise testis (T25FW) olulisi muutusi ei täheldatud, samas kui post hoc analüüs, mis teisendas andmed kõndimiskiiruseks (ft/s), saavutas olulisuse. Lisaks täheldati enesest teatatud väsimuse paranemist. 2008. aastal läbiviidud annuste võrdlusuuringus (randomiseeritud, topeltpime, platseebokontrolliga) värbasid Goodman jt 206 patsienti, kes said platseebot või annuseid 10, 15 või 20 mg kaks korda päevas. Jällegi leidis post hoc analüüs, milles võrreldi kõndimiskiiruse paranemist, oluliselt paremaid tulemusi kõigi ravirühmade puhul eraldi ja kõigi SR-4-AP-ga ravitud patsientide puhul, võrreldes platseeboga. Muusa tugevus paranes 10-mg ja 15-mg-ga ravitud rühmades, kuid mitte 20 mg-ga ravitud rühmades võrreldes platseebot saanud isikutega. Kahes järgnevas faasi Ⅲ kliinilises uuringus (21-nädalane topeltpime platseebokontrolliga randomiseeritud uuring, 301 patsienti ja 14-nädalane topeltpime platseebokontrolliga uuring, 239 patsienti) 10 mg kaks korda päevas patsiendid jagati ravile reageerivateks ja mittereageerivateks rühmadeks, mis määratleti T25FW pideva paranemisega. Mõlemas uuringus oli kõndimiskiiruse suurenemine märkimisväärne võrreldes mittereageerivate või platseeborühmaga. Lisaks paranes vastajate 12-Item MS Walking Scale (MSWS-12) skoor.2122
Nende uuringute avatud jätkuuuringus näidati, et kliiniline paranemine kadus pärast ravimi ärajätmist, kuid taastus 2 nädalat pärast SR-4-AP.Ampyra/Fampyra, SR{ tablettide koostise taasalustamist. {3}}AP sai 2010. aasta jaanuaris Toidu- ja Ravimiametilt täieliku heakskiidu SM-ga patsientide kõndimise parandamiseks, kuid 2011. aastal andis Euroopa Ravimiamet (EMA) välja ainult tingimusliku müügiloa. Mainitud uuringute põhjal eeldati heakskiitmist, et anda rohkem pikaajalisi efektiivsus- ja ohutusandmeid. Seetõttu algatati II faasi uurimuslik (MOBILE) ja I faasi kinnitav uuring (ENHANCE).
132 osalejaga uurimuslikus MOBLE-uuringus leiti patsiendi globaalse muutuse mulje (PGIC), MSWS-12 ja Timed Up and Go (TUG) kiiruse paranemine23 Et hinnata ravimi pikaajalist tõhusust ja ohutust. Viidi läbi kinnitav ENHANCE uuring SR-4-AP (10 mg kaks korda päevas 646 SM patsiendil). Lisaks MOBILE-i uuringus kirjeldatud täiustustele leidsid autorid, et SR-4-AP-ga ravitud patsientide arv paranes oluliselt 29-Item MS Impact Scale.5. Seejärel andis EMA SR{ tingimusteta heakskiidu. {11}}AP kõndimispuudega SM-ga patsientide raviks. ENABLE faasi vaatlusuuring 901 patsiendiga näitas, et ravi SR-4-AP-ga on kasulik SM-ga patsientidele, kuna nende füüsiline toimimine ja psühholoogiline tervis reaalses maailmas on enesetunnetatud2 (tabel 2).
Tuginedes ülalkirjeldatud paljulubavatele prekliinilistele andmetele kaitse kohta võrkkesta neurodegeneratsiooni eest, viis meie rühm läbi retrospektiivse, mitmekeskuselise OCT-uuringu, et võrrelda võrkkesta neurodegeneratsiooni pikisuunas 52 pidevat 4-AP-ravi saanud patsiendi ja 51 kontrollrühma vahel, mis sobitati kõigi asjakohaste ühismuutujate jaoks. kasutades eelnevalt määratletud sobitusalgoritmi. Kooskõlas eksperimentaalsete andmetega vähenes samaaegse 4-AP-ravi ajal võrkkesta kollatähni närvikiu kihi degeneratsioon 2 aasta jooksul. Neid leide tuleb siiski kinnitada sõltumatutes ja ideaalis perspektiivsetes kohortuuringutes, eriti kuna efekti suurus oli väike ning peripapillaarse võrkkesta närvikiu kihi ja kollatähni ganglionrakkude / sisemise pleksiformse kihi hõrenemise määr ei erinenud rühmade vahel oluliselt. . Neid 4AP kaitsva toime erinevusi ainult mRNFL-ile, kuid mitte pRNFL-is ega McGillil, ei ole lihtne seletada. Oluline on mainida, et kuna 4AP on litsentseeritud ainult EDSS 3-ga patsientide kõndimispuude parandamiseks.5-5, uuriti analüüsitud muutuste määra haiguse hilisemates staadiumides ja ilma ägeda optilise neuriidita. Sellises keskkonnas tekivad ainult väga väikesed võrkkesta muutused ja raviefektide tuvastamiseks on vaja suuri kohorte. Seetõttu ei olnud patsientide retrospektiivne uuring kindlasti piisava võimsusega, et usaldusväärselt tuvastada kaitsvat ravitoimet, ja pole üllatav, et ainult üks tulemustest osutus positiivseks. Võimalik, et mRNFL oli raviefektide tuvastamiseks kõige tundlikum kiht.5"
Kokkuvõtteks võib öelda, et kasvav hulk in vivo tõendeid viitab sellele, et 4-AP võib lisaks oma tuntud sümptomaatilisele toimele neurodegeneratsiooni ennetamise kaudu muuta EAEON-i haiguse kulgu ja võib-olla isegi MS-ga patsiente. Esialgsed in vitro tõendid viitavad rakulise kaltsiumi taseme ja NFAT raja kaasamisele, kuid täiendavad uuringud on õigustatud, et selgitada 4-AP neuroprotektiivse toime aluseks olevaid täpseid molekulaarseid mehhanisme immuunvahendatud põletikulises demüelinisatsioonis. Need leiud võivad avaldada märkimisväärset mõju MS-i ravistrateegiatele, kui need kinnitatakse tulevases randomiseeritud kontrollitud kliinilises uuringus.

Cistanche'i mõju
Viited
1. Leussink VI, Montalban X, Hartung HP. Aksonite funktsiooni taastamine 4-aminopüridiiniga: kliiniline efektiivsus hulgiskleroosi korral ja mujal. KNS ravimid 2018;32:637–651.
2. Horton L, Conger A, Conger D jt. 4-Aminopüridiini mõju nägemisnärvi neuropaatiaga hulgiskleroosiga patsientidele. Neurology 2013;80:1862–1866.
3. Morrow SA, Rosehart H, Johnson AM. Fampridine-SR mõju kognitiivsele väsimusele randomiseeritud topeltpimedas ristuuringus MS-ga patsientidel. Mult Scler Relat Disord 2017;11:4–9.
4. Vend SD, Filli L, Geissler O jt. Fampridiini positiivne mõju kognitsioonile, väsimusele ja depressioonile üle 2 aasta vanuste hulgiskleroosiga patsientidel. J Neurol 2018; 265:1016–1025.
5. Hayes KC, Blight AR, Potter PJ jt. 4-aminopüridiini prekliiniline uuring kroonilise seljaajukahjustusega patsientidel. Paraplegia 1993;31:216–224.
6. Iaci JF, Parry TJ, Huang Z jt. Dalfampridiin parandab sensomotoorset funktsiooni kroonilise puudujäägiga rottidel pärast keskmise ajuarteri oklusiooni. Insult 2013;44: 1942–1950.
7. Trimmer JS, Rhodes KJ. Pingepõhiste ioonikanalite lokaliseerimine imetajate ajus. Annu Rev Physiol 2004;66:477–519.
8. Rodr´ ıguez-Rangel S, Bravin AD, Ramos-Torres KM, Brugarolas P, S´anchez Rodr´ ıguez JE. Nelja uudse 4-aminopüridiin K(pluss) kanaliblokaatori struktuuri ja aktiivsuse suhte uuringud. Sci Rep 2020;10:52.
9. Bostock H, Sears TA, Sherratt RM. 4-Aminopüridiini ja tetraetüülammooniumiioonide mõju normaalsetele ja demüeliniseerunud imetajate närvikiududele. J Physiol 1981;313:301-315.
10. Huynh W, Pickering H, Howells J et al. Fampridiini mõju aksonite erutuvusele hulgiskleroosi korral. Clin Neurophysiol 2016;127:2636–2642.
11. DeCoursey TE, Chandy KG, Gupta S, Cahalan MD. Pingepõhised K pluss kanalid inimese T-lümfotsüütides: roll mitogeneesis? Loodus 1984;307:465–468.
12. Rus H, Pardo CA, Hu L jt. Pingega sõltuv kaaliumikanal Kv1.3 ekspresseerub tugevalt põletikulistel infiltraatidel hulgiskleroosi ajus. Proc Natl Acad Sci USA 2005;102:11094–11099.
13. Wang X, Li G, Guo J jt. Kv1.3 kanal kui neuropõletikuliste haiguste peamine terapeutiline sihtmärk: tehnika tase ja kaugemalgi. Front Neurosci 2019;13:1393.
14. Wulffff H, Calabresi PA, Allie R, et al. Pingepõhine Kv1,3 K(pluss) kanal efektormälu T-rakkudes on MS-i uus sihtmärk. J Clin Invest 2003;111:1703–1713.
15. Burton JM, Bell CM, Walker SE, O'Connor PW. 4-aminopüridiini toksilisus tahtmatu üleannustamisega neljal hulgiskleroosiga patsiendil. Neurology 2008;71: 1833–1834.
16. Johnson NC, Morgan MW. Ebatavaline 4-aminopüridiini toksilisuse juhtum. J Emerg Med 2006;30:175–177.
17. Schwam E. Raske juhuslik 4-aminopüridiini üleannustamine apteegi segavea tõttu. J Emerg Med 2011;41:51–54.
18. Etemadifar M, Saboori M, Chitsaz A jt. Fampridiini mõju sclerosis multiplex'iga patsientide krambihoogude tekkeriskile. Mult Scler Relat Disord 2020;43:102188.
19. Goodman AD, Cohen JA, Cross A jt. Fampridiin-SR hulgiskleroosi korral: randomiseeritud, topeltpime, platseebokontrolliga, annusevahemiku uuring. Mult Scler 2007; 13:357–368.
20. Goodman AD, Brown TR, Cohen JA jt. Toimeainet prolongeeritult vabastava fampridiini annuste võrdluskatse hulgiskleroosi korral. Neurology 2008;71:1134–1141.
21. Goodman AD, Brown TR, Krupp LB jt. Toimeainet prolongeeritult vabastav suukaudne fampridiin hulgiskleroosi korral: randomiseeritud topeltpime kontrollitud uuring. Lancet 2009;373: 732–738.
22. Goodman AD, Brown TR, Edwards KR jt. Toimeainet prolongeeritult vabastava suukaudse dalfampridiini 3. faasi uuring hulgiskleroosi korral. Ann Neurol 2010;68:494–502.
23. Hupperts R, Lycke J, Short C et al. Toimeainet prolongeeritult vabastav fampridiin ning kõndimine ja tasakaal MS-s: randomiseeritud kontrollitud MOBILE uuring. Mult Scler 2016;22:212–221.
24. Naujock M, Stanslowsky N, Buflfler S et al. 4-Aminopüridiiniga indutseeritud aktiivsus päästab amüotroofse lateraalskleroosiga patsientide poolt indutseeritud pluripotentsetest tüvirakkudest hüpoergastuvad motoorsed neuronid. Tüvirakud 2016;34:1563–1575.
25. Franciosi S, Ryu JK, Choi HB, Radov L, Kim SU, McLarnon JG. 4-Aminopüridiini laia spektriga toimed amüloid-beeta1-42-indutseeritud rakusignaalide ja funktsionaalsete reaktsioonide moduleerimiseks inimese mikrogliias. J Neurosci 2006;26:11652–11664.
26. Li S, Wei D, Mao Z jt. Mitmete 4-aminopüridiini derivaatide kui Parkinsoni tõve ravis kasutatavate potentsiaalsete neuroprotektiivsete ainete kavandamine, süntees, immunotsütokeemia hindamine ja molekulaarse dokkimise uurimine. Bioorg Chem 2017;73:63–75.
27. Smith AJ, Tauskela JS, Stone TW, Smith RA. Eelkonditsioneerimine 4-aminopüridiiniga kaitseb väikeaju graanulite neuroneid eksitotoksilisuse eest. Brain Res 2009; 1294: 165–175.
28. Tauskela JS, Aylsworth A, Hewitt M, Brunette E, Blondeau N. Eelkonditsioneerimisest põhjustatud neuroprotektsiooni ebaõnnestumine ja päästmine raskete insuldilaadsete solvangute korral. Neurophar mycology 2016;105:533–542.
29. Tseng KC, Li H, Clark A jt. 4-Aminopüridiin soodustab funktsionaalset taastumist ja remüeliniseerumist ägeda perifeerse närvikahjustuse korral. EMBO Mol Med 2016;8:1409–1420.
30. Ogita K, Okuda H, Watanabe M, Nagashima R, Sugiyama C, Yoneda Y. In vivo töötlemine K pluss kanali blokaatoriga 4-aminopüridiiniga kaitseb kainaadist põhjustatud neuronaalse rakusurma eest, aktiveerides hiire NMDA retseptoreid hipokampus. Neurofarmakoloogia 2005;48:810–821.
31. Moriguchi K, Miyamoto K, Kusunoki S. 4-Aminopüridiin leevendab eksperimentaalset autoimmuunneuriiti Lewise rottidel. J Neuroimmunol 2017;305:72–74.
32. Schmalhofer WA, Bao J, McManus OB et al. Immunosupressiivsete omadustega pingepõhise kaaliumikanali Kv1.3 inhibiitorite uue klassi tuvastamine. Biochemistry 2002;41:7781–7794.
33. Varga Z, Ettevõte T, Papp F jt. Kaaliumikanali ekspressioon inimese CD4-s pluss tervete isikute ja hulgiskleroosiga patsientide regulatoorsetes ja naiivsetes T-rakkudes. Immunol Let 2009; 124:95–101.
34. Jukkola P, Gu Y, Lovett-Racke AE, Gu C. Põletikulise demüelinisatsiooni ja aksoni degeneratsiooni pärssimine Kv3 kanalite pärssimise kaudu. Front Mol Neurosci 2017;10:344.
35. Moriguchi K, Miyamoto K, Fukumoto Y, Kusunoki S. 4-Aminopüridiin leevendab SJL/J hiirte retsidiveeruvat-remittuvat eksperimentaalset autoimmuunset entsefalomüeliiti. J Neuroimmunol 2018;323:131–135.
36. Gobel K, Wedell JH, Herrmann AM jt. 4-Aminopüridiin parandab hulgiskleroosi loommudelis liikuvust, kuid mitte haiguse kulgu. Exp Neurol 2013;248: 62–71.
37. Dietrich M, Koska V, Hecker C jt. 4-Aminopüridiini kaitsev toime eksperimentaalse optilise neuriidi ja hulgiskleroosi korral. Aju 2020;143:1127–1142.
38. Grimaldi M, Atzori M, Ray P, Alkon DL. Kaltsiumi mobiliseerimine intratsellulaarsetest varudest, neurotransmitteritest põhjustatud kaltsiumi transientide võimendamine ja kaltsiumi mahtuvuslik sisenemine 4-aminopüridiini poolt. J Neurosci 2001;21:3135–3143.
39. van Diemen HA, Polman CH, Koetsier JC, van Loenen AC, Nauta JJ, Bertelsmann FW. 4-Aminopüridiin hulgiskleroosiga patsientidel: efektiivsuse ja ohutusega seotud annus ja seerumitase. Clin Neuropharmacol 1993;16:195–204.
40. Davis FA, Stefoski D, Rush J. Suukaudselt manustatud 4-aminopüridiin parandab hulgiskleroosi kliinilisi tunnuseid. Ann Neurol 1990;27:186–192.
41. Stefoski D, Davis FA, Faut M, Schauf CL. 4-Aminopüridiin parandab hulgiskleroosi kliinilisi tunnuseid. Ann Neurol 1987;21:71–77.
42. Stefoski D, Davis FA, Fitzsimmons WE, Luskin SS, Rush J, Parkhurst GW. 4- Aminopüridiin hulgiskleroosi korral: pikaajaline manustamine. Neurology 1991;41: 1344–1348.
43. Jones RE, Heron JR, Foster DH, Snelgar RS, Mason RJ. 4-Aminopüridiini toime hulgiskleroosiga patsientidele. J Neurol Sci 1983;60:353-362.
44. van Diemen HA, Polman CH, van Dongen TM jt. 4-Aminopüridiini mõju sclerosis multiplex'i kliinilistele nähtudele: randomiseeritud platseebokontrollitud topeltpime ristuuring. Ann Neurol 1992;32:123–130.
45. Polman CH, Bertelsmann FW, van Loenen AC, Koetsier JC. 4-aminopüridiin hulgiskleroosiga patsientide ravis. Pikaajaline efektiivsus ja ohutus. Arch Neurol 1994;51:292–296.
46. Romani A, Bergamaschi R, Candeloro E, Alfonsi E, Callieco R, Cosi V. Väsimus hulgiskleroosi korral: mitmemõõtmeline hindamine ja reaktsioon sümptomaatilisele ravile. Mult Scler 2004;10:462–468.
47. Rossini PM, Pasqualetti P, Pozzilli C jt. Väsimus progresseeruva hulgiskleroosi korral: suukaudse 4-aminopüridiini randomiseeritud, topeltpime, platseebokontrollitud ristuuringu tulemused. Mult Scler 2001;7:354–358.
48. Hauser SL, Johnston SC. 4-aminopüridiin: uus elu vanale ravimile. Ann Neurol 2010; 68:A8–A9.
49. Schwid SR, Petrie MD, McDermott MP, Tierney DS, Mason DH, Goodman AD. Toimeainet prolongeeritult vabastava 4-aminopüridiini kvantitatiivne hindamine hulgiskleroosi sümptomaatiliseks raviks. Neurology 1997;48:817–821.
50. Goodman AD, Bethoux F, Brown TR jt. Dalfampridiini pikaajaline ohutus ja efektiivsus kõndimishäirete korral hulgiskleroosiga patsientidel: kahe 3. faasi kliinilise uuringu avatud pikendamise tulemused. Mult Scler 2015;21:1322–1331.
51. Hobart J, Ziemssen T, Feys P jt. Kliiniliselt oluliste paranemiste hindamine sclerosis multiplex’iga osalejate enesehinnanguga kõndimisvõimes: tulemused randomiseeritud, topeltpimedast III faasi ENHANCE uuringust toimeainet prolongeeritult vabastava fampridiiniga. KNS ravimid 2019;33:61–79.
52. Macdonell R, Nagels G, Lapland DA et al. Patsientide poolt teatatud hulgiskleroosi paranenud tervisemõju: PR-fampridiini uuring ENABLE. Mult Scler 2016;22: 944–954.
53. Noble M, Tseng K-CC, Li H, Elfar JC. 4-Aminopüridiin kui üksikaine raskete närvimuljumiskahjustuste diagnoosimiseks ja raviks. Mil Med 2019; 184 (suppl 1): 379–385.

