Mineralokortikoidi retseptori aktiveerimine ja antagonism südame-veresoonkonna haiguste korral: rakulised ja molekulaarsed mehhanismid
Jul 07, 2022
Aldosteroon kontrollib soolase vee homöostaasi, toimides neeru epiteelirakkudes mineralokortikoidi retseptorile (MR), ligandiga aktiveeritavale transkriptsioonifaktorile. Nüüd on aga ilmne, et MR ekspresseerub mitmetes rakutüüpides ja kudedes, toimides südame-veresoonkonna haiguste peamise tõukejõuna. MR-antagonistid on osutunud väga tõhusaks südamepuudulikkuse ja vähenenud väljutusfraktsiooniga patsientidel ning on tänapäevase ravi nurgakiviks. Viimase kümnendi jooksul avastasid mitmed eksperimentaalsed uuringud, milles kasutati rakutüübispetsiifilise MRS-iga mudeleid, raku- ja molekulaarsed mehhanismid, mis on selle kahjuliku mõju aluseks vasaku vatsakese remodelleerumisele. Nende leidude põhjal on MR-antagonistide potentsiaali hinnatud teiste südame-veresoonkonna haiguste, sealhulgas koronaararterite haiguse, arteriaalse hüpertensiooni, säilinud väljutusfraktsiooniga südamepuudulikkuse, pulmonaalse hüpertensiooni, kodade virvenduse ja südameklapihaiguste korral. Käesolev ülevaade võtab kokku praegused teadmised MR-i aktiveerimise ja antagonismi kohta südame-veresoonkonna haiguste korral.

Klõpsake maca ženšenni cistanche neerude jaoks
Aldosteroon, steroidhormoon, mida toodavad neerupealise koore glomerulosa rakud, on reniin-angiotensiin-aldosterooni süsteemi keskne efektorhormoon.1,2 Aldosterooni füsioloogiline roll on kontrollida soola-vee homöostaasi, toimides mineralokortikoidi retseptoritele. (MR), ligandiga aktiveeritud transkriptsioonifaktor neeru epiteelirakkudes. Aldosteroon MR kaudu viib amiloriiditundliku epiteeli Naþ kanali ülesreguleerimisele ja aktiveerimisele, suurendades seeläbi Naþ reabsorptsiooni ja Kþ sekretsiooni.2 Esimene MR antagonist (MRA), spironolaktoon, töötati välja antihüpertensiivse ravimina eesmärgiga ennetada Naþi teket. retentsioon ja veremahu vähenemine.3,4 Kuid kuna spironolaktoon on aktiivsusega progesterooni retseptoril ja teistel tuumaretseptoritel, võib see põhjustada olulisi kõrvaltoimeid, nagu günekomastia.3 Seda toimet võib leevendada teise põlvkonna ühend eplerenoon ja hiljuti uus klass väga selektiivseid, tugevatoimelisi mittesteroidseid MRA-sid. nagu fifinerenoon ja esakserenoon.3,4
Johann Bauersachs1 ja Achim Lother2,3
1 Hannoveri meditsiinikooli kardioloogia ja angioloogia osakond, Hannover, Saksamaa;
2 I kardioloogia ja angioloogia osakond, ülikooli südamekeskus, meditsiinikeskus – arstiteaduskond, Freiburgi ülikool, Freiburg, Saksamaa; ja
3 Eksperimentaalse ja kliinilise farmakoloogia ja toksikoloogia instituut, arstiteaduskond, Freiburgi ülikool, Freiburg, Saksamaa
MRA-de kardiovaskulaarset kaitsvat toimet seostati esmalt nende mõjuga diureesile, veremahule ja elektrolüütide homöostaasile.5 Kuid MR ekspresseerub mitmetes rakutüüpides ja kudedes väljaspool neeru ning nüüd on ilmne, et MR neeruvälistes kudedes on haiguse peamine tegur (joonis 1).6,7 Rohkem kui 20 aastat tagasi andsid suuremad kliinilised uuringud tõendeid selle kohta, et MRA-ravi parandab südamepuudulikkusega patsientide suremust ja haigestumust vähenenud väljutusfraktsiooniga (HFrEF), mille tulemuseks on IA klassi juhis. soovitus.8–10 Sellest ajast alates on mitmed eksperimentaalsed uuringud avastanud raku- ja molekulaarsed mehhanismid, mis on vasaku vatsakese (LV) remodelleerumisele soodsa mõju aluseks. Nende leidude põhjal on hinnatud MRA-de potentsiaali teiste südame-veresoonkonna haiguste, sealhulgas koronaararterite haiguse, arteriaalse hüpertensiooni, säilinud väljutusfraktsiooniga (HFpEF) südamepuudulikkuse, pulmonaalse hüpertensiooni (PH) ja südameklapihaiguste korral. Käesolev ülevaade võtab kokku praegused teadmised MR-i aktiveerimise ja antagonismi kohta südame-veresoonkonna haiguste korral.
HFrEF ja müokardiinfarkti järgsed remodelleerivad MRA-d on tõestanud ravimeid kroonilise HFrEF-i ravis, nagu on tõestatud mitmetes uuringutes.8 Eplerenone in Mild Patients Hospitalisation and Survival Study in Heart Failure (EMPHASIS-HF) näitas suremuse vähenemist 24 protsenti HFrEF-i ja kergete sümptomitega patsientidel, keda raviti eplerenooniga võrreldes platseeboga.11 Randomiseeritud aldaktooni hindamise uuringus (RALES) oli spironolaktoonil sarnane toime raskete südamepuudulikkuse sümptomitega patsientidel, kelle suremus vähenes platseeboga võrreldes 30 protsenti.12 Uuringud on näidanud, et sarnaselt spironolaktoonile ja eplerenoonile vähendas mittesteroidne MRA finerenoon II faasi uuringutes pro-B-tüüpi natriureetilise peptiidi (BNP) või N-terminaalse BNP (NT-proBNP) taset.13,14 MRA-ravi varajane alustamine leiti, et ägeda südamepuudulikkusega patsiendid on ohutud ja hästi talutavad.15,16 Eplerenoon parandas müokardiinfarkti (MI) järgse LV-funktsiooni kahjustusega patsientide tulemusi.1 7 Hilisemates uuringutes kontrolliti hüpoteesi, et MR-blokaadi algatamine varakult pärast MI-d võib ära hoida südame remodelleerumist ja südamepuudulikkuse teket. Kui MRA-ravi alustati 72 tunni jooksul pärast sümptomite tekkimist, parandas see BNP/NT-proBNP taset patsientidel, kellel ei olnud eelnevalt südamepuudulikkust.18 Hilisemas uuringus täheldati aga varajase MRA-ravi võimalikku kasu kliinilistele tulemustele ainult patsientide alarühmas. kõrge riskiga patsiendid ST elevatsiooniga MI.19 Individuaalne patsienditaseme metaanalüüs kolmest suurest randomiseeritud kontrollitud uuringust HFrEF-iga patsientidel näitas ka kardiaalse äkksurma vähenemist MRA-ravi korral 23 protsenti.20 Äsja diagnoositud HFrEF-iga patsientidel. , oli ravi MRA suuremate annustega seotud LV väljutusfraktsiooni parema paranemisega üle 3 kuu.21
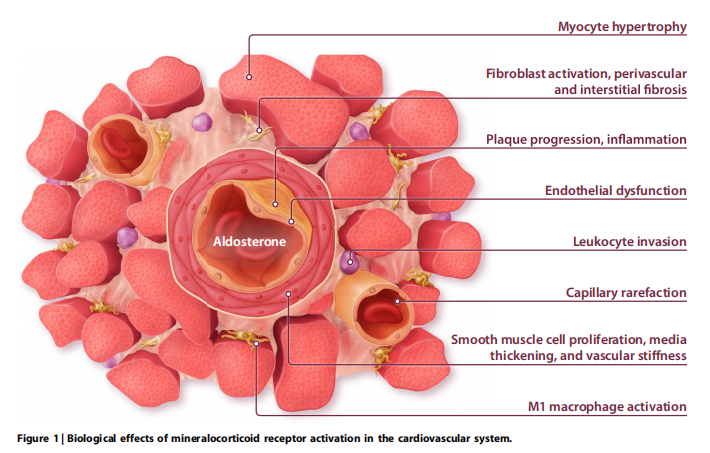
Eksperimentaalsed uuringud, milles kasutati MRA-sid südamepuudulikkuse ja MI-järgse remodelleerumise loommudelites, näitasid soodsat mõju südame hüpertroofiale, fifibroosile või mõlemale (joonis 1).22–25 Seejärel andis rakuspetsiifilise MR-i deletsiooniga hiiremudelite kasutamine tõendeid, et neid toimeid vahendas MR aktiveerimine kardiovaskulaarsetes rakkudes. MR-i deletsioon südame müotsüütidest põhjustas väiksema armi suuruse, väiksema kaugkoe fibroosi ja parema LV funktsiooni.26 Fifibroosi vähenemine pärast isheemilist vigastust oli seotud nõrgenenud oksüdatiivse stressi ja müotsüütide apoptoosiga, kuid müokardis tuvastati suurem arv neutrofiile ja monotsüütide MR-defitsiitsete hiirte kude võrreldes metsiktüüpi hiirtega.26 Märkimisväärselt parandas müeloidrakkude MR deletsioon samuti LV remodelleerumist ja kutsus esile nihke reparatiivsema M2 makrofaagi alatüübi poole.27 MR deletsioon silelihasrakkudest (SMC) nõrgendas LV fifibroosi, kuid neil oli väike mõju LV funktsioonile.25 See tähendab, et MRA-d avaldavad mõju erinevatele rakutüüpidele, mis aitavad sünergiliselt kaasa kahjustuste kontrollile ja paranemisele pärast MI-d.
Põletiku keskne tähtsus MR-i aktiveerimise kahjuliku mõju vahendamisel on kinnitatud kroonilise südamepuudulikkuse mudelites (joonis 2).25–54 MR-i deletsioon müeloidrakkudest takistas südame remodelleerumist vastusena rõhu ülekoormusele või N(G)-nitro- L-arginiini metüülestri (L-NAME)/angiotensiin II infusioon.28,29 Sarnaseid toimeid täheldati hiirtel, kellel puudus T-rakkudes MRS.30 Hiljuti näidati, et SMC MR deletsioon parandab rõhu ülekoormusest põhjustatud LV hüpertroofiat, põletikku, fifibroos ja düsfunktsioon.31 MR-i deletsioon endoteelirakkudest või südame müotsüütidest parandas LV funktsiooni, kuid erinevalt isheemilisest vigastusest ei reguleerinud see pärast rõhu ülekoormust fifibroosi.32,33 Pärast MR-i deletsiooni fibroblastidest erinevusi ei tuvastatud.32 Need leiud viitavad sellele, et MR mõju südame remodelleerumisele ei sõltu mitte ainult rakutüübist, vaid ka vigastuse tüübist.

Aldosterooni / MR-indutseeritud LV remodelleerumise taga olevate molekulaarsete regulatsioonimehhanismide dešifreerimiseks on tehtud olulisi jõupingutusi. MR-i hästi iseloomustatud põletikuliste ja fibrootiliste efektormolekulide hulka südame-veresoonkonna süsteemis on galektiin 3 (LGALS3) ja lipokaliin 2 (NGAL).55–58 Huvitaval kombel on modifitseeritud tsitruseliste pektiini farmakoloogiline inhibeerimine või galektiin 3 geneetiline deletsioon nõrgestanud aldosteroon-indutseeritud aldosterooni. remodelleerimine.55,56 Plasma NGAL-i tasemed olid positiivses korrelatsioonis ringleva aldosterooni taseme ja fifibroosi biomarkeritega inimestel.57 NGAL-i deletsioon immuunrakkudest hoidis ära aldosterooni infusioonile reageerinud LV-fibroosi.58 Samuti parandas MR-i deletsioon müeloidrakkudest pärast südame ümberkujundamist. müokardiinfarkt, mida seostati NGAL-i ekspressiooni vähenemisega südame makrofaagides.27 Hiljutine mikroRNA-de suure läbilaskevõimega sõeluuring tuvastas, et miR-181a on MR-i signaalimise oluline regulaator.59 miR-181üleekspressioon reguleeris NGAL-i alla. ekspressioon in vitro ja in vivo ning südamefunktsiooni paranemine näriliste MI mudelis.59
HFpEF HFpEF-i levimus suureneb ja moodustab juba üle 50 protsendi südamepuudulikkuse juhtudest.60 Vaatamata sümptomite kattumisele peetakse HFpEF-i HFrEF-ist eraldiseisvaks üksuseks.60 Võrreldes HFrEF-iga patsientidega on HFpEF-iga patsiendid vanemad, rohkem. sageli naised ja rasvunud ning neil on rohkem kaasuvaid haigusi, nagu diabeet ja neeruhaigus, mis on seotud kroonilise põletikuga.60,61 MR aktiveerimine suurendab oksüdatiivset stressi ja kahjustab lämmastikoksiidi (NO) signaaliülekannet, mis põhjustab endoteeli düsfunktsiooni, põletikku ja perivaskulaarset Kuigi ideaalne prekliiniline mudel HFpEF-i uurimiseks on veel määratlemata, on selge järeldus, et MR-i aktiveerimine on seotud paljude patofüsioloogiliste tunnustega, mis iseloomustavad HFpEF-i.62,63 MRA-d parandasid rasvumisest, munasarjade eemaldamisest, nefrektoomiast põhjustatud diastoolset düsfunktsiooni, või deoksükortikosteroonatsetaadi (DOCA)/soola hüpertensioon hiirtel.64–67 Rakutüübispetsiifiline MR deletsioon südame müotsüütidest nõrgeneb Leukotsüütide invasioon ja fifibroos pärast DOCA-ravi.68 Kooskõlas süsteemse põletiku paradigmaga HFpEF-is näitas MR-i deletsioon endoteelirakkudest või müeloidrakkudest kõige silmatorkavamat mõju südame remodelleerumisele (joonis 2).35–38,54,69
Varased kliinilised uuringud viitasid MRA-de kasulikule mõjule HFpEF-iga patsientidele.70–72 Seega oli ootamatu, et spironolaktoon ei parandanud kardiovaskulaarsetest põhjustest põhjustatud surma, katkestatud südameseiskuse või suures faasis südamepuudulikkuse tõttu haiglaravi kombineeritud esmast tulemust. III Südametalitluse säilinud südamepuudulikkuse ravi aldosterooni antagonisti (TOPCAT) uuringuga.73 Kuid tõsine mure uuringu läbiviimise pärast seab uuringu kehtivuse kahtluse alla.74,75 Finerenoonis südame-veresoonkonna suremuse ja haigestumuse vähendamisel diabeetilise neeruhaiguse korral. (Joonis ARO-DKD) uuringus, vähendas mittesteroidne MRA finerenoon kardiovaskulaarsete sündmuste esinemissagedust diabeetilise neeruhaigusega patsientidel76, mis on kõrge HFpEF-i tekkeriskiga patsientide rühm.60 Finrenooni kasulikku mõju mõjutas peamiselt südamepuudulikkuse tõttu hospitaliseerimiste määr oli väiksem, kuigi juba olemasoleva HFrEF-iga patsiendid jäeti uuringust välja.76 Kaks täiendavad III faasi kliinilised uuringud, milles võrreldi spironolaktooni (Spironolaktoon südamepuudulikkuse ravis [SPIRIT-HF]; NCT04727073; EudraCT 2017- 000697-11) ja finerenoon (finerenooni uuring platseebost parema efektiivsuse ja ohutuse uurimiseks südamepuudulikkusega patsientidel [FINEARTS-HF]; NCT04435626) koos platseeboga südamepuudulikkuse ja keskmise või säilinud väljutusfraktsiooniga patsientidel jätkuv.

Uuringus Heart "OMics" in aging (HOMAGE) vähendas spironolaktoon I tüüpi kollageeni sünteesi ja suurendas lagunemist ning vähendas vererõhku, vasaku kodade mahtu ja BNP taset inimestel, kellel on risk HFpEF-i tekkeks.77 Kas varajane MRA-ravi võib edasi lükata südamepuudulikkuse esinemine sellistes populatsioonides tuleb veel kindlaks teha.
Ateroskleroos ja koronaararterite haigus
Ateroskleroosi ja koronaararterite haigust peetakse kroonilisteks põletikulisteks haigusteks78 ning ülalkirjeldatud MR-i tugev mõju veresoonte põletikule viitab MR-i rollile nende patofüsioloogias. Apolipoproteiin E knockout hiire mudelis süvendas aldosterooni infusioon ateroskleroosi teket.79 Seevastu MRA-d nõrgendasid põletikku ja reaktiivsete hapnikuliikide moodustumist, kuid parandasid rasvumismudelites NO biosaadavust ja veresoonte funktsiooni.80–83 hiirtel, kellel puudub platsenta kasvufaktor79 või rakkudevaheline adhesioonimolekul 1,84, mis näitab endoteelirakkude ja monotsüütide interaktsiooni protsessis. In vitro soodustas MR põletikuliste molekulide ekspressiooni endoteelirakkudes ja SMC-des.39,54,85–87 In vivo MR-i deletsioon endoteelirakkudest või müeloidrakkudest, kuid mitte SMC-dest, leevendas veresoonte põletikku ateroskleroosi hiiremudelites.39 –41 Lisaks suurendas monotsüütide stimuleerimine aldosterooniga põletikuliste tsütokiinide tootmist, olenevalt rasvhapete sünteesiraja ülesreguleerimisest.88 Van der on kokku võtnud müeloidrakkude MRS-i funktsiooni kohta kaasasündinud immuunsuse ja ateroskleroosi suureneva kirjanduse hulga. Heijden et al. (2018).89 Lisaks nende mõjule ateroskleroosile avaldasid MRA-ravi ja MR-i deletsioon SMC-st või müeloidrakkudest soodsat mõju veresoonte remodelleerumisele pärast mehaanilist vigastust,42,43,90, mis näitab MRA-de potentsiaalset kasu postangioplastika restenoosi korral. Vaatamata nendele kaalukatele eksperimentaalsetele tõenditele on ateroskleroosi MRA kliiniliste uuringute andmeid endiselt vähe.91 Hiljutine Finerenooni uuring neerupuudulikkuse ja diabeetilise neeruhaiguse progresseerumise vähendamises (FIDELIO-DKD) näitas esimest korda, et ravi uudse MRA-ga finerenoon võib vähendada MI esinemissagedust diabeetilise neeruhaigusega patsientidel92, mis näitab MRA potentsiaalset rolli kardiovaskulaarsete sündmuste esmases ennetamises.
Arteriaalne hüpertensioon
Aldosterooni ja MR mõju arteriaalsele hüpertensioonile on tunnustatud aastakümneid. Näiteks aldosterooni infusioon tõstab oluliselt vererõhku uni nefrektoomiaga rottidel, kes saavad kõrge soolasisaldusega dieeti.93,94 Lisaks mõjule Naþile ja vedelikupeetusele kontrollib aldosteroon MR-i kaudu vererõhku neeruvälistes rakkudes.95 Endoteeli MR. aktiveerimine indutseeris reaktiivsete hapnikuühendite tootmist ja kahjustas endoteelist sõltuvat veresoonte lõdvestumist.44,80 Nimelt olid need mõjud emastel hiirtel rohkem väljendunud kui isastel hiirtel.96 MR üleekspressioon tõi kaasa mõõduka vererõhu tõusu.97 Siiski, MR-i deletsioon endoteelirakkudest ei muutnud vererõhku algtasemel ega vastuseks stiimulile, 36, 44, 45, 69, mis näitab, et MR endoteelirakkudes füsioloogilise ekspressioonitaseme juures on vererõhu kontrollimiseks hädavajalik. Seevastu mitmed uuringud osutavad MRS-ile SMC-des kui veresoonte jäikuse ja hüpertensiooni peamiseks määrajaks, eriti eakatel hiirtel (joonis 2).46–48,98 Arvati, et MR võimendab miR-155 represseerimise kaudu. L-tüüpi Ca2þ-kanalite ekspressioon ja aktiivsus SMC-des, mis põhjustab veresoonte toonuse tõusu.46,47 Angiotensiin II-indutseeritud hüpertensioon ja sellele järgnenud elundikahjustused olid märkimisväärselt alla surutud MR-i deletsiooniga T-rakkudest.49 Mis puudutab MR-i rolli müeloidrakud, on teatatud osaliselt vastuolulistest tulemustest vererõhu vastuse kohta DOC/soola hüpertensioonile37 või angiotensiin II/L-NAME.29,38 Spironolaktoon osutus mitmes kliinilises uuringus efektiivseks resistentse hüpertensiooniga patsientidel ja nüüd soovitatakse seda kasutada patsientidel, kellel on püsiv hüpertensioon vaatamata kolmikravile. 99 100 Mittesteroidse MRA esakserenooni efektiivsus oli sarnane eplerenooniga vererõhu alandamiseks ja see on nüüd Jaapanis essentsiaalse hüpertensiooni raviks heaks kiidetud. nsion.101 102 Hiljutises 2b faasi uuringus suutis mittesteroidne MRA KBP-5074 märkimisväärselt langetada vererõhku kroonilise neeruhaigusega ja kontrollimatu hüpertensiooniga patsientidel, hoolimata ravist, mis hõlmas reniin-angiotensiini süsteemi inhibiitorit.103 Seevastu kroonilise neeruhaigusega ja hästi kontrollitud hüpertensiooniga patsientidel oli fifinerenoonil vaid väike lisamõju vererõhule.76 104
PH ja parema südamepuudulikkus
PH-ga patsientidel ja hiirtel on pärast kroonilise hüpoksiaga kokkupuudet täheldatud aldosterooni taseme tõusu plasmas, mis viitab MR-i rollile kopsuveresoonte remodelleerumisel. Tegelikult indutseerib aldosterooni stimuleerimine PH fenotüüpe in vivo ja kultiveeritud SMC-des või endoteelirakkudes in vitro.50,107–109 MRA-d parandavad kroonilise hüpoksia või monokrotaliini poolt indutseeritud veresoonte remodelleerumist ja parema vatsakese funktsiooni hiirtel ja rottidel.50,107,110 MRA-ravil ei olnud aga mingit mõju. kopsuarterite vöötmudelis, mis viitab sellele, et MRA-de kasulikkust parema vatsakese funktsioonile saab kaudselt seletada vähenenud järelkoormusega.110 Eksperimentaalsed uuringud, milles kasutati rakutüübispetsiifilise MR-i deletsiooniga hiiri, näitasid, et aldosterooni kahjulik mõju kopsuveresoonkonnale vahendab MR endoteelirakkudes, mitte SMC-des, fibroblastides või makrofaagides (joonis 2).50 Geeniekspressiooni analüüsid ja in vitro uuringud osutavad interaktsioonile endoteelirakkude ja teiste rakutüüpide vahel protsessis, mis hõlmab endoteliini.{13 }} signalisatsioonirada ja parakriinne läbirääkimine eksosoomide kaudu.50,108,109,111 Post hoc analüüs Ambrisentanist ravi jaoks Pulmonaalarteriaalse hüpertensiooni (ARIES) 1. ja 2. uuringud viitasid spironolaktooni kasulikule toimele, kui seda lisatakse endoteliini-1 retseptori antagonistile ambrisentaanile PH.112-ga patsientidel. Praegu on käimas prospektiivne randomiseeritud 2. faasi kliiniline uuring MRA kasutamise kohta PH korral. käimas (NCT01712620).

Võimalikud tulevikusuunad Teadmised MR-i mõjudest südame-veresoonkonna haiguste korral täienevad, osutades uutele potentsiaalsetele MRA-de näidustustele. Uute mittesteroidsete MRA-de kättesaadavus võib veelgi laiendada näidustuste spektrit ja võimaldada MRA-de kliinilist kasutamist kõrge riskiga patsientide populatsioonides.4 Prekliinilised ja varajased kliinilised andmed viitavad sellele, et MRA-d võivad olla tõhusad kemoteraapiast põhjustatud kardiotoksilisuse ennetamisel, mis on oluline kõrvalmõju. 51 113 114 Lisaks näitavad kasvavad tõendid, et MR aktiveerimine põhjustab mitte ainult vatsakeste, vaid ka kodade ebasoodsat ümberkujunemist. Primaarse aldosteronismiga patsientidel on suurem risk kodade virvendusarütmia tekkeks võrreldes essentsiaalse hüpertensiooniga patsientidega.115 Huvitaval kombel nõrgendas kasvufaktori b transformatsioonist põhjustatud kodade fibroosi MR-i deletsioon osteoblastides (joonis 2).52 Erinevates katsemudelites vähenesid MRA-d. kodade fibroos ja seega kodade arütmia koormus, 116–118 mis viitab MRA potentsiaalsele kasule kodade virvendusarütmiaga patsientidel. Kooskõlas selle võimalusega näitas kliiniliste uuringute metaanalüüs kodade virvendusarütmia esinemissageduse olulist vähenemist MRA-ga ravitud patsientidel võrreldes kontrollrühmadega.119
Mitraalregurgitatsioon on tavaline südameklapi häire, mida sageli seostatakse struktuurse halvenemise ja mitraalklapi infolehtede häiritud ekstratsellulaarse maatriksiga.120 Hiljutised tõendid näitavad, et aldosteroon, aktiveerides MR-i, juhib proteoglükaanide tootmist interstitsiaalsete rakkude poolt ja endoteeli-mesenhümaalset üleminekut. mitraalklapid.53 Hiirtel nõrgestas MRA-ravi või MR-i deletsioon endoteelirakkudes mitraalklapi remodelleerumist.53 Selle toimega kaasnes fibrootiliste markerite ekspressiooni vähenemine LV-koes spironolaktooniga ravitud hiirtel.121 Kuigi praegu piirdub see sekkumise või kirurgilise parandamisega, MRA-d võivad seega kujutada endast mitraalregurgitatsiooni uut ravivõimalust.6120
Järeldused
Tõendeid koguneb mitmetest eksperimentaalsetest uuringutest, mis näitavad, et südame müotsüütides, endoteelirakkudes, SMC-des, müeloidrakkudes, T-rakkudes ja osteoblastides on proua otsene mõju südamepuudulikkusele ja teistele südame-veresoonkonna haigustele. Sõltuvalt haiguse või stiimuli tüübist on erinevatel rakutüüpidel MRS, millel on erinevad funktsioonid, mis aitavad kaasa põletiku ja fibroosi netomõjule pärast aktiveerimist. Selles ülevaates käsitletud saadaolevad teadmised loovad aluse edasiseks arendamiseks ja klassikaliste ja uudsete MRA-de hindamiseks täiendavate kardiovaskulaarsete näidustuste jaoks.
VIITED
1Lother A, Moser M, Bode C jt. Mineralokortikoidid südames ja veresoonkonnas: uued teadmised vanade hormoonide kohta. Annu Rev Pharmacol Toxicol. 2015;55:289–312.
2. Shibata S. 30 aastat mineralokortikoidi retseptorit: mineralokortikoidi retseptor ja NaCl transpordimehhanismid neeru distaalses nefronis. J Endokrinool. 2017;234:T35–T47.
3. Kolkhof P, Barfacker L. 30 aastat mineralokortikoidi retseptorit: mineralokortikoidi retseptori antagonistid: 60 aastat uurimis- ja arendustegevust. J Endokrinool. 2017;234:T125–T140.
4. Agarwal R, Kolkhof P, Bakris G jt. Steroidsed ja mittesteroidsed mineralokortikoidi retseptori antagonistid kardiorenaalses meditsiinis. Eur Heart J. 2021;42:152–161.
5. Struthers AD. Miks parandab spironolaktoon kroonilise südamepuudulikkuse korral suremust lisaks AKE inhibiitoritele? Br J Clin Pharmacol. 1999;47:479–482.
6. Lother A. Mineralokortikoidi retseptorid: rakuvälise maatriksi remodelleerumise peamised regulaatorid. Circ Res. 2020;127:354–356.
7. Bauersachs J, Jaisser F, Toto R. Mineralokortikoidi retseptori aktiveerimine ja mineralokortikoidi retseptori antagonisti ravi südame- ja neeruhaiguste korral. Hüpertensioon. 2015;65:257–263.
8. Ponikowski P, Voors AA, Anker SD jt. 2016. aasta ESC juhised ägeda ja kroonilise südamepuudulikkuse diagnoosimiseks ja raviks: Euroopa Kardioloogide Seltsi (ESC) ägeda ja kroonilise südamepuudulikkuse diagnoosimise ja ravi töörühm. Välja töötatud ESC südamepuudulikkuse assotsiatsiooni (HFA) erilise panusega. Eur Heart J. 2016;37:2129–2200.
9. Berliner D, Hanselmann A, Bauersachs J. Südamepuudulikkuse ravi vähendatud väljutusfraktsiooniga. Dtsch Arztebl Int. 2020;117:376–386.
10. Lother A, Hein L. Südamepuudulikkuse farmakoloogia: alusteadusest uudsete ravimeetoditeni. Pharmacol Ther. 2016;166:136–149.
11. Zannad F, McMurray JJ, Krum H jt. Eplerenoon süstoolse südamepuudulikkuse ja kergete sümptomitega patsientidel. N Engl J Med. 2011;364: 11–21.
12. Pitt B, Zannad F, Remme WJ jt. Spironolaktooni mõju haigestumusele ja suremusele raske südamepuudulikkusega patsientidel. Randomiseeritud Aldactone Evaluation Study uurijad. N Engl J Med. 1999;341:709–717.
13. Pitt B, Kober L, Ponikowski P jt. Uue mittesteroidse mineralokortikoidi retseptori antagonisti BAY 94-8862 ohutus ja talutavus kroonilise südamepuudulikkuse ja kerge või mõõduka kroonilise neeruhaigusega patsientidel: randomiseeritud topeltpime uuring. Eur Heart J. 2013;34:2453–2463.
14. Filippatos G, Anker SD, Bohm M jt. Randomiseeritud kontrollitud uuring fifinerenooni ja eplerenooni kohta kroonilise südamepuudulikkuse ja suhkurtõve ja/või kroonilise neeruhaigusega patsientidel. Eur Heart J. 2016;37:2105–2114.
15. Butler J, Anstrom KJ, Felker GM jt. Spironolaktooni efektiivsus ja ohutus ägeda südamepuudulikkuse korral: ATHENA-HF randomiseeritud kliiniline uuring. JAMA Cardiol. 2017;2:950–958.
16. Asakura M, Ito S, Yamada T jt. Eplerenoonravi varajase alustamise tõhusus ja ohutus ägeda südamepuudulikkusega patsientidel (VAREM uuring): mitmekeskuseline, randomiseeritud, topeltpime platseebokontrolliga uuring. Eur Heart J Cardiovasc Pharmacother. 2022;8:108–117.
17. Pitt B, Remme W, Zannad F jt. Eplerenoon, selektiivne aldosterooni blokaator, patsientidel, kellel on pärast müokardiinfarkti vasaku vatsakese düsfunktsioon. N Engl J Med. 2003;348:1309–1321.
18. Montalescot G, Pitt B, Lopez de Sa E jt. Varajane ravi eplerenooniga patsientidel, kellel on äge ST-tõusuga müokardiinfarkt ilma südamepuudulikkuseta: Randomiseeritud topeltpime meeldetuletusuuring. Eur Heart J. 2014;35:2295–2302.
19. Beygui F, Cayla G, Roule V jt. Varajane aldosterooni blokaad ägeda müokardiinfarkti korral: ALBATROSSi randomiseeritud kliiniline uuring. J Am Coll Cardiol. 2016;67:1917–1927.
20. Rossello X, Ariti C, Pocock SJ jt. Mineralokortikoidi retseptori antagonistide mõju südame äkksurma riskile südamepuudulikkuse ja vasaku vatsakese süstoolse düsfunktsiooniga patsientidel: kolme randomiseeritud kontrollitud uuringu individuaalne patsienditaseme metaanalüüs. Clin Res Cardiol. 2019;108:477–486.
21. Duncker D, Konig T, Hohmann S jt. Enneaegse siirdatava kardioverteri/defibrillaatori implanteerimise vältimine südamepuudulikkuse ravi tõhustatud optimeerimise abil, mida toetab kantav kardioverter/defibrillaator – uuring PROLONG. J Am Heart Assoc. 2017;6:e004512.
22. Kuster GM, Kotlyar E, Rude MK jt. Mineralokortikoidi retseptori inhibeerimine parandab üleminekut müokardi puudulikkusele ja vähendab kroonilise rõhu ülekoormusega hiirte oksüdatiivset stressi ja põletikku. Tiraaž. 2005;111:420–427.
23. Fraccarollo D, Galuppo P, Schmidt I jt. Vasaku vatsakese remodelleerumise ja molekulaarsete muutuste täiendav leevendamine kombineeritud aldosterooni ja angiotensiini retseptori blokaadiga pärast müokardiinfarkti. Cardiovasc Res. 2005;67:97–105.
24. Fraccarollo D, Galuppo P, Schraut S et al. Vahetu mineralokortikoidi retseptori blokaad parandab müokardiinfarkti paranemist, moduleerides põletikulist reaktsiooni. Hüpertensioon. 2008;51:905–914.
25. Gueret A, Haruki N, Favre J jt. Vaskulaarsete silelihaste mineralokortikoidi retseptor aitab kaasa koronaar- ja vasaku vatsakese düsfunktsioonile pärast müokardiinfarkti. Hüpertensioon. 2016;67:717–723. 26. Fraccarollo D, Berger S, Galuppo P jt. Kardiomüotsüütide mineralokortikoidi retseptori kustutamine leevendab ebasoodsat ümberkujunemist pärast müokardiinfarkti. Tiraaž. 2011;123:400–408.
27. Fraccarollo D, Thomas S, Scholz CJ et al. Makrofaagide mineralokortikoidi retseptor on müokardiinfarkti paranemise pleiotroopne modulaator. Hüpertensioon. 2019;73:102–111.
28. Li C, Zhang YY, Frieler RA jt. Müeloidse mineralokortikoidi retseptori puudulikkus pärsib hiirtel aordi ahenemisest põhjustatud südame hüpertroofiat. PLoS One. 2014;9:e110950.
29. Usher MG, Duan SZ, Ivaschenko CY jt. Müeloidne mineralokortikoidi retseptor kontrollib hiirtel makrofaagide polarisatsiooni ja kardiovaskulaarset hüpertroofiat ja remodelleerumist. J Clin Invest. 2010;120:3350–3364.
30. Li C, Sun XN, Zeng MR jt. Mineralokortikoidi retseptori puudulikkus T-rakkudes nõrgendab rõhu ülekoormusest põhjustatud südame hüpertroofiat ja düsfunktsiooni T-rakkude aktiveerimise moduleerimise kaudu. Hüpertensioon. 2017;70:137–147.
31. Kim SK, Biwer LA, Moss ME jt. Mineralokortikoidi retseptor silelihastes aitab kaasa rõhu ülekoormusest põhjustatud südamepuudulikkusele. Ringi südamepuudulikkus. 2021;14:e007279.
32. Lother A, Berger S, Gilsbach R jt. Mineralokortikoidi retseptorite ablatsioon müotsüütides, kuid mitte fibroblastides, säilitab südame funktsiooni. Hüpertensioon. 2011;57:746–754.
33. Salvador AM, Moss ME, Aronovitz M jt. Endoteeli mineralokortikoidi retseptor aitab kaasa rõhu ülekoormusest põhjustatud süstoolsele düsfunktsioonile, moduleerimata südame hüpertroofiat või põletikku. Physiol Rep. 2017;5:e13313.
34. Lother A, Hein L. Vaskulaarsed mineralokortikoidi retseptorid: riskifaktorite, hüpertensiooni ja südamehaiguste seostamine. Hüpertensioon. 2016;68:6–10.
35. Jia G, Habibi J, DeMarco VG jt. Endoteeli mineralokortikoidi retseptori deletsioon hoiab ära dieedist põhjustatud südame diastoolse düsfunktsiooni naistel. Hüpertensioon. 2015;66:1159–1167.
36. Rickard AJ, Morgan J, Chrissobolis S jt. Endoteelirakkude mineralokortikoidi retseptorid reguleerivad deoksükortikosterooni / soola vahendatud südame remodelleerumist ja veresoonte reaktiivsust, kuid mitte vererõhku. Hüpertensioon. 2014;63:1033–1040.
37. Rickard AJ, Morgan J, Tesch G jt. Mineralokortikoidi retseptorite kustutamine makrofaagidest kaitseb deoksükortikosterooni/soola poolt põhjustatud südamefibroosi ja vererõhu tõusu eest. Hüpertensioon. 2009;54:537–543.
38. Bienvenu LA, Morgan J, Rickard AJ jt. Makrofaagide mineralokortikoidi retseptori signaalimine mängib aldosteroonist sõltumatus südamefibroosis võtmerolli. Endokrinoloogia. 2012;153:3416–3425.
39. Moss ME, Lu Q, Iyer SL jt. Endoteeli mineralokortikoidi retseptorid soodustavad ateroskleroosi vaskulaarset põletikku soopõhiselt. Arterioscler Thromb Vasc Biol. 2019;39:1588–1601.
40. Shen ZX, Chen XQ, Sun XN jt. Mineralokortikoidi retseptori puudulikkus makrofaagides pärsib ateroskleroosi, mõjutades vahtrakkude moodustumist ja eferotsütoosi. J Biol Chem. 2017;292:925–935.
41. Moss ME, DuPont JJ, Iyer SL jt. Apolipoproteiin-E knockout hiiremudelis ei ole silelihasrakkude mineralokortikoidiretseptoritel ateroskleroosis olulist rolli. Eesmine Cardiovasc Med. 2018;5:81.
lisateabe saamiseks:Ali.ma@wecistanche.com
