Ainevahetushäiretega seotud rasvmaksahaiguse tagajärjed COVID-i korral{0}}
Nov 17, 2023
Abstraktne
Ainevahetusega seotud rasvmaksa häire (MAFLD) iseloomustab kaasasolevaid etioloogiaid (i.e., II tüüpi suhkurtõbi, metaboolne sündroom, ülekaalulisus) inimestel, kellel on rasvmaksahaigus, mis mõjutab 1/3 maailma elanikkonnast. 2020. aastal oli koroonaviirushaiguse 2019 (COVID-19) kriis enneolematu ning erinevate kaasuvate haigustega inimesed muutusid vastuvõtlikumaks raske ägeda respiratoorse sündroomi koroonaviirus 2 põhjustatud infektsioonile.. MAFLD-ga patsiendid on sageli rasvunud, millele lisanduvad metaboolsed ohud, nagu diabeet, hüpertensioon ja düslipideemia, mis põhjustab suuremat COVID-i ohtu-19. MAFLD-ga patsiendid on infektsioonidele 4 kuni 6- korda rohkem altid. COVID-19 kutsub esile maksakahjustuse koos aspartaataminotransferaasi ja alaniinaminotransferaasi ning ebaolulise bilirubiini taseme tõusuga. Seetõttu halvendab MAFLD COVID{4}} patsientide seisundit oluliselt. Tõendid, mis rõhutavad MAFLD ja maksafunktsiooni muutuste vahelist koostoimet COVID-19 korral, viitavad sellele, et olemasoleva MAFLD-ga COVID{6}} patsientidel on suurem risk haigestuda või intensiivravi osakonda sattuda. Mõnede aluseks olevate mehhanismidena peetakse otsest maksakahjustust, põletikuliste tsütokiinide suurenenud taset, maksa mitokondriaalse aktiivsuse vähenemist ja kahjustatud immuunsust. Selle ülevaate põhirõhk on arutada rasvmaksahaigusega seotud metaboolse düsfunktsiooni tagajärgi COVID{8}} patsientidel. Ülevaade analüüsib süstemaatiliselt kahe ülemaailmse pandeemia (MAFLD ja COVID-19) koos tabamise mõju praegusel ajastul.

Tistanche tubulosa eelised - maksa säilitamine
Võtmesõnad:Metaboolne rasvmaksa häire; COVID-19; Metaboolne düsfunktsioon; Maksakahjustus; Tsütokiinide torm
SISSEJUHATUS
2019. aasta koroonaviirushaigust (COVID-19) põhjustab uudne beeta-koroonaviirus, nimelt raske ägeda respiratoorse sündroomi koroonaviirus 2 (SARS-CoV-2). COVID-19 sai alguse 2019. aastal Hiinas Hubei provintsis Wuhanist ja Maailma Terviseorganisatsioon kuulutas selle pandeemiaks 12. märtsil 2020[1]. See on äge ebatüüpiline hingamisteede haigus, mis on suunatud kopsudele ja sümptomid ulatuvad kergest kuni raskeni. COVID-i{10}} levinumad sümptomid on köha, palavik, ninakinnisus, õhupuudus ja hingamisraskused ning raske COVID{11}} võib põhjustada kopsupõletikku, neerupuudulikkust, ägedat rasket respiratoorset sündroomi, septilist šokki, mitut elundipuudulikkus ja surm[2,3]. Seedetrakti sümptomiteks on kõhuvalu, oksendamine ja kõhulahtisus [4]. COVID-iga seotud riskitegurid{15}} on vanem vanus ja kaasnevad haigused (diabeet, hüpertensioon, rasvumine ja koronaartõbi), mis põhjustavad mitme organi puudulikkust ja surma[5]. Lisaks aktiveerib SARS-CoV-2 viirusevastase immuunvastuse ja vabastab põletikueelseid tsütokiine, põhjustades kontrollimatut põletikulist reaktsiooni, mis põhjustab immuunhäireid, mis võivad põhjustada septilist šokki, mitme organi puudulikkust ja mikroobide nakatumist[6]. Rasvmaksahaigusega (MAFLD) (endise nimega mittealkohoolne rasvmaksahaigus) seotud metaboolne düsfunktsioon kujutab ühiskonnale majanduslikku ja tervisealast koormust, mõjutades veerandit maailma elanikkonnast[7]. Lääne- ja Aasia riikides on ülekaalulisuse ja metaboolse sündroomi esinemissagedus järsult suurenenud toitumise ja elustiili muutuste tõttu, mis on oluliselt suurendanud MAFLD esinemist. Histopatoloogiliste tunnuste põhjal võib selle liigitada lihtsaks steatoosiks ja mittealkohoolseks steatohepatiidiks, mis võib areneda maksavähiks ja tsirroosiks. Rasvumine, kasvav vanus ja diabeet on MAFLD-ga patsientide peamised tsirroosiga seotud riskitegurid[8]. MAFLD on mitmesuguste metaboolsete düsfunktsioonide, sealhulgas rasvumise, düslipideemia, II tüüpi suhkurtõve, insuliiniresistentsuse, oksüdatiivse stressi, adipokiinide ja apoptoosi maksa ilming[9].

Cistanche tubulosa eelised
MAFLD JA COVID-19
MAFLD-d seostatakse rasva kogunemise ja põletikuga hepatotsüütides, mis kahjustab maksafunktsiooni ja muudab inimesed vastuvõtlikumaks SARS-CoV{1}} infektsioonile. COVID-19 kutsub esile maksa apoptoosi ja seda täheldatakse maksa steatoosi ja hepatotsüütide kahjustamise korral, mis on tingitud põletikuliste vahendajate, nagu IL-1, IL-6 ja IL-10 suurenenud tasemest. MAFLD-ga patsientidel on raske COVID-i-19 nakkuse risk 4 kuni 6- korda suurem[10], kuna see süvendab viirusega seotud tsütokiinide tormi[11] ja sisaldab mitmeid kaasuvaid haigusi, mis on samuti potentsiaalne COVID-i riskifaktor-19. Rasvunud ja kaugelearenenud fibroosiga MAFLD-ga patsiendid on raske COVID-i suhtes altid{13}}. COVID-19 raskusastet MAFLD-ga patsientidel ei seostata kaugelearenenud maksahaigustega ning MAFLD-rühma suremus on seotud peremeesorganismi suurenenud ja väljendunud põletikulise vastusega[12]. COVID-iga MAFLD-ga patsientidel{16}} on tavaliselt raskemad sümptomid ja nad vajavad intensiivsemat haiglaravi ja pikaajalist jälgimist kui mitte-MAFLD-ga patsientidel[13]. Haigestunud rasvumine, vanem vanus, mitme haigestumuse skoorid, kõrgenenud FIB{21}} skoor ja hüpoksia on haiglaravil viibivate MAFLD-ga patsientide suremuse sõltumatud ennustajad[14]. MAFLD-d seostatakse COVID-19 patsientide suurema haiglaravi riskiga ning metaboolse sündroomi ravi metformiiniga, GLP-1RA ja bariaatriline kirurgia võivad riski vähendada [15].
Esialgse analüüsi tegi Jiet al[16] MAFLD mõju kohta 202 COVID-19 patsiendile. 33% patsientidest täheldati püsivat ebanormaalset maksafunktsiooni alates haiglaravist kuni jälgimiseni. MAFLD on COVID-i progresseerumise sõltumatu riskitegur-19, mis põhjustab maksakahjustusi ja viiruse pikemaajalist levikut. Maksahäirete määr oli haiglaravi ajal 50% ja haiglas viibimise ajal tõusis 75% -ni. Sama tähelepanekut toetas ka Huanget al[17] on 280 patients with COVID-19; 35.7% of patients reported abnormal liver function during admission. The alanine aminotransferase (ALT) level was higher in MAFLD patients compared to non-AFLD ones on admission and during hospitalization. Older age (>50 aastat) ja samaaegne MAFLD on maksakahjustuse riskifaktorid COVID-i põdevatel patsientidel-19. 14 uuringu metaanalüüs, milles osales 1851 MAFLD-ga patsienti, jõudis järeldusele, et võrreldes mitte-MAFLD-ga patsientide rühmaga on suurem risk raske COVID-i{5}} ja intensiivravi osakonda sattumiseks, ilma et MAFLD-i ja mitte-MAFLD-patsientide suremus ei erine. [18,19]. Mitmekeskuseline kohortuuring 65 MAFLD-ga ja 65 mitte-MAFLD-ga patsiendil näitas positiivset korrelatsiooni MAFLD ja metaboolsete riskitegurite ning COVID{13}} vahel mittediabeetilistel patsientidel. MAFLD-d seostati mittediabeetilistel patsientidel neljakordse raske COVID-i{15}} riskiga[20].
MAFLDi/MAFLDi JA COVID-I VAHEL VAHELISELT MÕJUTAVAD TEGURID-19
MAFLD-ga kaasneb riskitegurite kombinatsioon. Seetõttu on MAFLD ja COVID{0}} vahelise vastasmõjuga seotud mitmed riskitegurid, mida selles jaotises käsitletakse.
Vanuse mõju
Vanus on MAFLD-i ja COVID-i vahekorda mõjutav tegur{0}}. Inimesed, kellel on kaasuvad haigused nagu diabeet, hüpertensioon, krooniline kopsuhaigus,jne.on COVID-ile vastuvõtlikud{0}}, eriti eakad patsiendid. Seega on eakad patsiendid MAFLD-le ja COVID-ile vastuvõtlikumad-19. Seega võib vananemist pidada mõlema ülalmainitud haiguse kiire rünnaku üheks süüdlaseks ning nende liitu võib vananemine ka väga sümptomaatiliselt mõjutada. Süstemaatiline mitmekeskuseline analüüs kinnitas, et noorematel COVID-i{2}} patsientidel on MAFLD-i oht suurem kui vanematel patsientidel. Uuringus osales 327 patsienti erinevatest vanuserühmadest. Alla 60-aastased patsiendid rühmitati nooremateks, üle 60-aastased aga vanemateks või eakateks[21]. Andmete kohaselt moodustasid raske COVID{7}} põdevad inimesed, kellel oli MAFLD, 24% eakatest patsientidest ja 55,9% noorematest patsientidest. On silmatorkav, et noortel patsientidel, kuid mitte eakatel, oli MAFLD seotud COVID-i karmusega-19. Vanuse mõju MAFLD ja COVID{12}} liidule vajab endiselt tõestatud mehhanismi. Võrreldes nooremate patsientidega on vanematel patsientidel rohkem kaasuvaid haigusi, mis hõlmavad paljusid elundeid, ja suurem suremus, mis võib kaaluda üles MAFLD mõju COVID-ile-19[22,23].

cistanche toidulisandi eelised - suurendavad immuunsust
Cistanche Enhance Immunity toodete vaatamiseks klõpsake siin
【Küsi lisa】 E-post:cindy.xue@wecistanche.com / Whats App: 0086 18599088692 / Wechat: 18599088692
Hüpertensiooni mõju
Üldpopulatsioonis on MAFLD levimus COVID-i põdevatel patsientidel suhteliselt palju suurem{0}}. Uuringud näitavad, et MAFLD mängib olulist rolli haavatavuses COVID-i suhtes-19. Järk-järgult süvendab COVID{2}} MAFLD arengut. MAFLD-i ja COVID-i suhe{3}} on nagu veeb ja mõlemad on üksteisega väga keeruliselt seotud. COVID-19 soodustab metaboolseid probleeme, nagu hüpertensioon ja lipiidide kolesterooli tase. COVID{5}} areng kiireneb ka MAFLD-ga patsientidel metaboolsete kaasuvate haiguste tõttu, nagu hüpertensioon ja kõrge lipiidide või kolesterooli tase. COVID-iga MAFLD-ga patsientidel-19 võib nende metaboolsete seisundite jälgimine ja ravimine vähendada projektsiooni puudumise riski.
Üks metaboolsetest kaasuvatest haigustest, hüpertensioon, on ülioluline oht, mis mõjutab COVID-i esinemissagedust ja levikut{0}}. COVID-19 ja krooniliste ainevahetushaigustega patsientide kohordiuuringus oli COVID-19 kõrgeim esinemissagedus hüpertensiooniga patsientidel ning 49,7% COVID-19 patsientidest kannatab hüpertensiooni all[24 ]. Hüpertensioon on seotud reniin-angiotensiini süsteemi ebanormaalse initsiatiiviga ja angiotensiini konverteeriva ensüümi -2 (ACE-2) vähenenud aktiivsusega [25]. Seetõttu on hüpertensiooniga patsientidel AKE-2 tase langenud. Seega hüpoteesi kohaselt põhjustavad need vähenenud ACE-2 tasemed COVID-i-19 kerge haavatavuse. Vastupidiselt on eeldatud, et COVID-19 vähendab ACE-2 sagimist ja selle retseptoreid, mille tulemuseks on kõrgem hüpertensiooni esinemissagedus COVID{17}} patsientidel. Hüpertensioon võib suurendada MAFLD-i ohtu COVID{18}}-patsientidel, mille põhjuseks on allutatud aspektid, näiteks süsteemsete põletikuliste reaktsioonide esilekutsumine hüpertensiooni korral, mitte otse ACE{19}}-retseptorid[26]. Umbes 126-l 251-st COVID-19 patsiendist oli retrospektiivses uuringus hüpertensioon. Uuring näitas, et hüpertensiooniga COVID{24}} patsientidel oli kõrgem interleukiini -6 (IL-6) tase ning suurem tundlikkus C-reaktiivse valgu ja prokaltsitoniini suhtes kui mittehüpertensiivsetel patsientidel[27]. . Need statistilised andmed viitavad sellele, et hüpertensiooniga COVID{30}} patsientidel on süsteemne põletikuline retort ilusam kui mittehüpertensiivsetel patsientidel. Retort võib kahjustamata juhtudel mõjutada maksa metabolismi ja põhjustada maksakahjustusi või elundite talitlushäireid.
Düslipideemia mõju
Düslipideemia on metaboolne kaasuv haigus, mis hõlmab triglütseriidide (TG) anomaalset suurenemist ja suure tihedusega lipoproteiinide anomaalset vähenemist. Uuringus COVID{1}} patsientide seas leiti, et düslipideemia on hüpertensiooni järgne korduv tüsistus. Uurimine näitas, et pärast haiguse algust langes organismis oluliselt erinevate kolesteroolide (üldkolesterool (TC)[28,29], TG, kõrge tihedusega lipoproteiini kolesterool (HDL-c) ja madala tihedusega lipoproteiin kolesterool (LDL-c). Nende tasemete muutused põhjustasid jõhkruse ja haiguse püsivuse. Sarnaselt SARS-viirusega ründab SARS-CoV-2 ka peremeesrakke, sünteesides ja pakendades viiruseosakesi lipiidide abil. , mis viib vere lipiidikomponentide vähenemiseni, mida peetakse üheks düslipideemia püsivaks tunnuseks. COVID-i{10}} esinemissageduse suurenemist täheldati triglütseriidide ja üldkolesterooli taseme anomaalse tõusu tõttu MAFLD-ga patsientidel. Seetõttu metaboolse sündroomi ja düslipideemiaga patsientidel on korduvalt maksa lipiidide ainevahetuse ülejääk, mis võib koos COVID-iga -19 kombineerituna avaldada harmoonilist efekti, mis võib samuti olla üks maksakahjustuse põhjusi. Selle autentimiseks on aga vaja täpsemaid uuringuid kontseptsioon.
Rasvumise mõju
Rasvumine on COVID-i suveräänne oht-19. Kohordiuuring, milles osales umbes 350 SARS-CoV-ga nakatunud patsienti-2, näitas, et 52% patsientidest oli rasvunud[30]. Sarnane uuring näitas, et ligikaudu 19% COVID{7}} rasvunud patsientidest põdes MAFLD-d[31]. Selle täpset mehhanismi ei ole siiani selgitatud, kuigi arvukad tõenäolised põhjused võivad seda seisukohta valgustada. Peamine põhjus on see, et rasvunud patsiendid kannatavad sageli vistseraalse rasva kogunemise tõttu MAFLD-st. MAFLD enda põletikuline reaktsioon võib põhjustada kroonilist maksakahjustust. Seetõttu võivad COVID-19 ja COVID{10}} raviks kasutatavad ravimid maksaprobleeme veelgi süvendada. Teine põhjus on maksakahjustus, mis tuleneb rasvunud patsientide aeratsiooni nõrgenemisest, mis põhjustab uneapnoe sündroomi ja hüpokseemiat ning lisaks anoksilist atmosfääri maksa metabolismis. Kolmas põhjus on ülekaalulisuse tõttu kahjustatud immuunsüsteem[32]. Võrreldavaid funktsioone täitvate adipotsüütide ja immuunrakkude tõttu tekib arvukalt põletikulisi reaktsioone[31]. Rasvunud patsientidel võib adipotsüütide ja immuunsüsteemi regulatsiooni erinevus toetada COVID-i põhjustatud provokatiivse tormi esinemist-19. Seega võib olukord lõppeda mitmesüsteemse elundi vigastusega.
Diabeedi mõju
Üks asjakohane uuring näitas, et umbes 74% COVID{1}} diabeediga patsientidest kannatab maksakahjustuse all. Tulemused väidavad, et suhkurtõbi on üks peamisi tegureid, mis põhjustavad COVID{2}} ja MAFLD[33]. Selle mehhanism pole ikka veel väga selge. Siiski võib kõrge glükoositaseme mõju SARS-CoV-2 replikatsioonile pidada üheks tugevaks aluseks, mis mõjutab viiruse sissetungi astet. Selle nähtuse tulemuseks on süvenev süsteemne põletikuline reaktsioon, mille tulemuseks on mitme organi, sealhulgas maksa kahjustus. Teine põhjus on diabeet kui autoimmuunne ja kestev põletikuline haigus (erinevused CD4+ või CD8+ T-lümfotsüütides), mida COVID{8}} veelgi võimendab. Maks on üks kriitilisemaid immuunorganeid, mis osaleb eksogeensete mikroorganismide fagotsütoosis ja vabastab tsütokiine ning maksa immunomoduleeriv koormus võib COVID-ga diabeedihaigetel suureneda-19. Viimaseks põhjuseks on diabeedivastased ravimid, mis põhjustavad ebaregulaarset transaminaaside tõusu ja intensiivistavat immuunvahendatud maksakahjustust[34]. Diabeet on COVID-i jaoks suveräänne risk{13}}.
Soo mõju
Esmased uuringutulemused soovitavad COVID{0}} esinemissageduse soolist ebavõrdsust. Nende leidude kohaselt olid mehed tavaliselt suuremas ohus kui naised. Näiteks Hiinas läbiviidud kliiniline uuring teatas, et ligikaudu 58% patsientidest olid mehed ja WHO andmetel oli COVID-i -19 surmajuhtum meestel suurem (ligikaudu 65%) kui naistel. Seda soolist ebavõrdsust põhjendati järgmiste täpsustustega: mittenakkushaiguste (nt südamehaigused, vähid, diabeet jne) suure koormuse tõttu meestel on COVID{6}} meespatsientide suremus suurem kui naistel. . Mehed on hoolimatumad heade terviseharjumuste suhtes ja neid paeluvad rohkem elustiilist tulenevad harjumused, nagu sõltuvus, suitsetamine, ebaregulaarsed unetsüklid ja suurem huvi meedia vastu, mis muudab mehed SARS-CoV{9}} nakkuse suhtes vastuvõtlikumaks. Paljud uuringud toetavad naiste tugevamat immuunsüsteemi kui meestel, mis on ka üks kergete COVID{10}}- ja MAFLD-rünnakute põhjusi.
Selle asemel, et COVID-i{0}} ja MAFLD-i riskiga meeste protsent on suurem, on vähesed naiste rühmad, näiteks rasedad naised, mõlema haiguse suhtes suuremas ohus. Sellegipoolest näitasid täiustatud uuringud, et COVID{1}} ja MAFLD puhul puudub sooline piirang, kuna naistel on meestega võrreldes ka palju isiklikke ja sotsiaalseid kohustusi, mis põhjustavad neil vaimset traumat koos nõrga immuunsusega, mis põhjustab maksafunktsiooni häireid ja COVID-i kerget rünnakut{ {2}}[35,36].

Cistanche deserticola ma
Uimastitest põhjustatud maksavigastus COVID{1}}-RAVI
Ravimitest põhjustatud maksakahjustus (DILI) kujutab endast ravimitest tingitud maksakahjustusi või maksafunktsiooni häireid. Kõige tõenäolisem maksakahjustuse põhjus COVID-19 patsientidel võib olla tingitud mitmete ravimite, näiteks antibiootikumide, viirusevastaste ravimite, valuvaigistite, palavikualandajate, paljude traditsiooniliste hiina ravimite, ajurveeda ravimite, kasutamisest COVID-19 raviks. jne. DILI riski järjekord on kujutatud joonisel 1. Selle fakti toetuseks viidi läbi üks hiljutine uuring, sealhulgas COVID-iga patsiendi maksa biopsia-19, mis näitas maksaensüümide aktiivsuse suurenemist, mis oli tingitud osaliselt ravimid, mida kasutatakse COVID-19 raviks, mis põhjustab sepsise ja šoki tagajärjel maksafunktsiooni häireid. Kuigi DILI esinemine on haruldane, on raske diagnoosi ja maksapuudulikkuse ohtlike tagajärgede tõttu suremuse või mõnikord ka maksa siirdamisega see meditsiinivendluse jaoks väga murettekitav ja väljakutseid pakkuv. COVID-19 ravi polüteraapia muudab DILI keerulisemaks, kuna ravimite toksilisus võib soo, vanuse ja rassi järgi erineda. Paljud ravimid võivad kahjustada maksafunktsiooni ja kahjustada maksa; mõned neist võivad asümptomaatiliselt tõsta maksaensüümide taset; muudel juhtudel võib avalduda äge hepatiit. Lisaks on maksakahjustuse vahemik kooskõlas kasutatud ravimi annusega, samas kui mõnel juhul ei ole ravimi annus kõigil juhtudel seotud maksakahjustusega. Kõige tavalisemad maksakahjustuse või hepatotoksilisuse tekitajad on antibiootikumid, põletikuvastased, malaaria- ja viirusevastased ained[37].
MAKSAVIGASTUSE MEHHANISM COVID-IDIGA PATSIENTIDEL-19
Raskemaid COVID-i{0}} juhtumeid võib MAFLD-ga patsientidel tuvastada kaasasündinud immuunsuse kahjustuse tõttu. Joonisel 2 on loetletud erinevad maksakahjustuse mehhanismid COVID-iga -19-ga patsientidel[38].
Otsene tsütopaatiline toime Otsese tsütopaatilise toime korral piirab peremeesrakke koroonaviiruse sisenemine ACE kaudu-2. Seejärel nakatab viirus ülemisi hingamisteid ja kopsurakke. Rasketel COVID-19 patsientidel on seerumi gamma-glutamüültransferaasi (GGT) (kolangiotsüütide kahjustuse latentne uurimisindikaator) leitud kuni 72% võimendatud tasemel. See ACE-2 retseptori seondumine kolangiotsüütidega põhjustab maksa talitlushäireid[39].
Düsreguleeritud ja kontrollimatu süsteemne põletik
Düsreguleeritud ja kontrollimatu süsteemne põletik on COVID-iga patsientide maksakahjustuse jaoks äärmiselt usaldusväärne põhjus{0}}. See süsteemne põletik ei ole suur haigus. Selle kontrollimatu süsteemse põletiku algpõhjus on aga loomuliku ja rakulise immuunsuse reguleerimata aktiveerumine, mille tagajärjeks on mitme organi kahjustus, sealhulgas mahajäetud tsütokiini "orkaani" tõttu maksafunktsiooni häired. Jällegi on selle kontrollimatu süsteemse põletiku peamine süüdlane kaasasündinud immuunsuse kahjustus. Viimased uurimistulemused kinnitavad, et rasvumine on vaieldamatult seotud MAFLD-ga ja toetab M2-makrofaagide (mis on põletikku pärssiv) muutumist põletikueelseteks M1-makrofaagideks. Seda makrofaagide eksklusiivset lahknemist kutsuvad esile rasvhapped, mis soodustavad ektoopilise lipiidide kogunemist ja lokaalset ja süsteemset kroonilist halvemat hellust. See metaboolne ja immunoloogiline düsregulatsioon võib süvendada SARS-COV-2 põhjustatud infektsiooni ja viia COVID{6}}-haiguse kaunimaks muutumiseni[38].
Ravimitest põhjustatud maksakahjustus
Kõige tõenäolisem maksakahjustuse põhjus COVID{0}} patsientidel võib olla tingitud mitmete ravimite, näiteks antibiootikumide, viirusevastaste ravimite, valuvaigistite, palavikualandajate, paljude traditsiooniliste hiina ravimite ja ajurveeda ravimite kasutamisest COVID-19 raviks. . Selle toetuseks näitas üks hiljutine leid, sealhulgas COVID-i põdeva patsiendi maksa biopsia-19, maksaensüümide aktiivsuse suurenemist osaliselt COVID-i ravis kasutatavate ravimite tõttu-19, mis põhjustas maksafunktsiooni häireid. sepsis ja šokk. Kuigi DILI juhtumid on haruldased, on raske diagnoosi ja maksapuudulikkuse ohtlike tagajärgede tõttu suremuse või maksa siirdamisega tegemist meditsiinivendluse jaoks väga murettekitav ja väljakutseid pakkuv. COVID{4}}-ravi polüteraapia muudab DILI keerulisemaks, kuna ravimite maksatoksilisus võib soo, vanuse ja rassi lõikes erineda[39]. Paljud ravimid, mida me kasutame, võivad muuta maksafunktsiooni, põhjustades maksakahjustusi. Asümptomaatiline maksaensüümide aktiivsuse tõus ja äge hepatiit on mõned näited sellistest seisunditest. Maksakahjustus võib olenevalt ravimi annusest erineda; näiteks põhjustab paratsetamooli üleannustamine ägedat hepatotoksilisust. Eeldatakse, et olemasolevad metaboolsed maksahäired võivad suurendada ravimite hepatotoksilisust, kuna need kahjustavad seedeensüümide tööd, põhjustavad oksüdatiivset stressi, kahjustavad mitokondreid ja mõjutavad lipiidide tasakaalu. Vastupidi, mõned ksenobiootikumid võivad viia MAFLD vähenemiseni, st põhjustada rasvmaksa üleminekut mittealkohoolsele steatohepatiidile (NASH) ja seega veenda nekropõletikku ja seejärel fibroosi ja maksatsirroosi kiiret levikut[39].

Joonis 1 Ravimist põhjustatud maksakahjustuse riski järjekord. ALT: alaniini transaminaas; AST: aspartaadi transaminaas; COVID-19: koroonaviirushaigus 2019; SARS-CoV-2: raske ägeda respiratoorse sündroomi koroonaviirus 2; MAFLD: ainevahetusega seotud rasvmaksa häire.
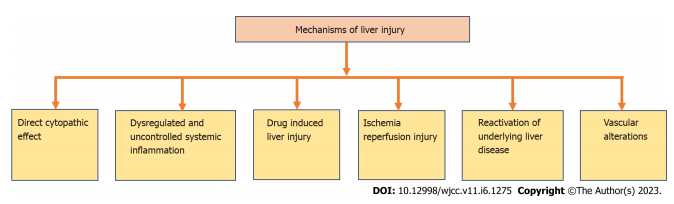
Joonis 2 Maksakahjustuse mehhanismid.
Isheemia-reperfusioonikahjustus
Lisaks reguleerimata ja kontrollimatule immuunsüsteemile on veel üks nähtus isheemia-reperfusioonikahjustus hingamisteede pettumuse või sepsise tõttu. Kui raskete COVID{1}} juhtude korral areneb süsteemse põletikulise vastuse sündroom, põhjustab põletikueelsete tsütokiinide kontrollimatu vabanemine perifeersete arterite laienemist, mis alandab vererõhku ja võib põhjustada kudede ulatuslikku hüpoksiat[40]. Kui äge respiratoorse distressi sündroom (ARDS) tekib samaaegselt, põhjustab see vere hapnikuvaeguse, mis intensiivistab maksaisheemiat ja varem ebasoodsat verevarustust. Lisaks suurenevad reaktiivsed hapniku liigid (ROS) stressi ja hüpoksia korral, kiirendades valkude, DNA ja lipiidide oksüdatsiooni. Peroksüdatsiooniproduktid ja ROS ise käivitavad maksa tähtrakud, et tekitada rakuvälist maatriksit ja kaasasündinud maksa immuunrakke, mis põhjustavad põletikueelsete tsütokiinide tekitamise kaudu veelgi maksakahjustusi [40].
Põhiliste maksahaiguste taasaktiveerimine
COVID{0}} patsientide maksakahjustuse üheks tõenäoliseks põhjuseks võib olla esmase maksahaiguse renessanss. Kliiniliste uuringute kohaselt oli 20%-35% COVID-ga-19 patsientidest pärast vastuvõtmist muutunud maksaensüümide tase ja 15%-30% COVID-ga patsientidest-19 oli esmane maks. haigus. Esialgse maksahaigusega COVID{7}} patsientidel oli maksaensüümide aktiivsus kõrgem võrreldes COVID{8}} patsientidega, kellel ei olnud eelnevalt maksahaigust. B-hepatiidi kordumist võivad esile kutsuda immunosupressiivsed ravimid, mida kasutatakse raske COVID{10}} raviks, nagu kortikosteroidid, IL-1 retseptori antagonistid, IL-6 retseptori antagonistid ja JAK inhibiitorid. Siiski on kordumise oht tagasihoidlik või väike. Hiljutised strateegiad toetavad HBsAg ja anti-HBc sõeluuringut enne immunosupressiivse ravi kasutamist. Profülaktiline HBV-vastane ravi on vajalik kõikide patsientide puhul, kellel on oht B-hepatiidi uuesti haigestuda, ulatudes madalast kuni kõrgeni[41].
Vaskulaarsed muutused
Veresoonte modifikatsioonid on tõenäoline alternatiivne maksakahjustuse allikas. Seda kinnitab ka uuring, mille käigus analüüsiti COVID-i{0}} hingamispuudulikkuse tõttu surnud isikute maksaproove ja tuvastati tühine põletikuline infiltraat. Näha oli, et portaal- ja sinusoidaalsetel veenidel oli osaline või täielik luminaalne tromboos, portaaltraktil oli fibroos ja värativeeni oksad olid laienenud. Kuid need olid kahtlemata tingitud voolu vähenemisest maksas ja viiruse poolt ahvatlevast hüübimiskaskaadist. Kuigi valimi suurus oli väike, leiti ühes teises COVID-19 patsientide lahkamise uuringus, et 88% patsientidest esines maksas rasvumisega seotud muutusi, hoolimata sellest, et neil ei olnud maksa oklusiooni[38].
MAKSAENSÜÜMIDE VARIUMINE COVID-IS-19
SRAS-CoV-2 infektsioon võib vallandada patogeneesi, mis on seotud mitme organi kahjustusega, sealhulgas maksakahjustusega. COVID-i -19 põdevate patsientide maksakahjustusel on erinevad põhjused, näiteks rakkude vigastused otsese viiruserünnaku tõttu ja SARS-CoV-2 sisenemine hepatotsüütidesse maksa- ja sapiteede rakkudes ekspresseeritud ACE2 kaudu. Maksa biopsia ja atsidofiilsete kehade proovides täheldatud hepatotsüütide kahjustused, raku apoptoos ja lobulaarne põletik on SARS-CoV-2 tulemused. Omrani-Nava jt[42] hindasid muutusi maksaensüümide aktiivsuses COVID-i põdevatel patsientidel{11}}. Teadlased hindasid otsese bilirubiini, üldbilirubiini (TBIL), ALT, aspartaataminotransferaasi (AST) ja aluselise fosfataasi (ALP) laboratoorseid uuringuid. Otsese bilirubiini, TBIL, ALT, ALP ja AST tase oli COVID{12}} patsientidel kõrgem kui kontrollrühmas. Kui AST tase tõusis, tõusis ka suremus. Uurijad avastasid COVID{13}} patsientidel maksaensüümide aktiivsuse kõrvalekalde. Yu jt[43] viisid Hiinas läbi kohortuuringu 1099 COVID{16}} patsiendiga. Teadlased leidsid, et 21,4% ja 22,3% patsientidest on kõrgenenud AST ja ALAT tase ning 10,7% patsientidest on bilirubiini tase ebanormaalne. TBIL tase oli üle 17,2 mmol/l, ALP oli suurem kui 135 U/L ja GGT üle 50 U/L. Uurijad jõudsid järeldusele, et COVID-i põdevatel patsientidel tõusis maksaensüümide tase{27}}. Cai jt[44] viisid läbi ka COVID-19-patsientide kliinilise läbivaatuse, pöörates erilist tähelepanu maksaensüümide häiretele. 417 patsiendi laboratoorsed tulemused ja kliiniline uuring saadi Hiinas Shenzhenis asuvast haiglast. Uurijad täheldasid, et 2 nädala jooksul haiglaravist oli 50 (24,4%), 33 (15,2%), 27 (11,7%) ja 52 (24,5%) patsiendil ALT, TBIL, AST ja GGT tase kolm korda kõrgenenud normaalpiir. Seitse ulatuslikku haiglauuringut on näidanud, et 15%-50% COVID-i põdevatest patsientidest-19 on kõrgem ALT ja ASAT tase. Need ensüümid suurenesid märkimisväärselt raske COVID-iga patsientidel-19 [45]. Hoolimata potentsiaalsest seosest COVID{50}} ja erineval määral muutunud maksaensüümide vahel, on SARS-CoV{52}} nakkuse ja maksakahjustuse vahelise seose kindlakstegemiseks vaja läbi viia üksikasjalikum uuring.

cistanche tubulosa - parandab immuunsüsteemi
MAFLDI JA SARS-COV{1}} NAKKUSE VAHEL
Metaboolne sündroom on haiguste kogum, nagu rasvumine, diabeet, hüperlipideemia, hüpertensioon ja insuliiniresistentsus, mis põhjustavad või halvendavad COVID{0}} patsientide seisundit[46]. Suhkurtõbi oli COVID{2}} patsientide seas levinuim haigus ja see suurendas nakatunud patsientide suremust. Hu jt[47] viisid läbi metaanalüüsi, hõlmates 40 000 patsienti Hiinast Wuhanist. Uurijad leidsid, et 8% kõigist patsientidest olid diabeetikud. Teine kõige levinum kaasuv haigus patsientidel pärast DM-i oli hüpertensioon. Uuringus uuriti 214 COVID-i põdevat patsienti-19, kes kuulusid kolme Hiinas Wenzhou haiglasse. 214 COVID{10}} patsiendist oli MAFLD-ga 66 (45 rasvunud ja 21 rasvumiseta). Uurijad täheldasid, et rasvunud MAFLD patsientidel oli kõrgem ALT ja AST tase võrreldes mitterasvunud MAFLD patsientidega. Teadlased leidsid, et rasvunud MAFLD-ga patsientidel oli kuus korda suurem risk COVID-i{15}} tekkeks kui mitte-rasvunud MAFLD-patsientidel[48]. Pan ja tema kolleegid tegid metaanalüüsi COVID{19}} tõsiduse ja MAFLD vahelise seose kohta. Teadlased viisid selle metaanalüüsi läbi PubMedi, Medline'i, EMBASE ja MedRxivi põhjal. Pärast sõeluuringut hõlmasid teadlased kokku kuus uuringut ja nendes osales 1293 osalejat. Metaanalüüsi uuringud näitasid, et suur protsent COVID{23}} patsiente põeb MAFLD-d. Uurijad täheldasid, et MAFLD suurendas COVID-i põdevatel patsientidel haiguse progresseerumise riski-19. Uurijad jõudsid järeldusele, et SARS-COV-ga kokku puutunud MAFLD-ga patsiendid{26}} vajavad paremat intensiivset ravi ja jälgimist[49]. Teises Hiina haiglates läbiviidud uuringus teatati, et MAFLD-ga inimestel oli seerumi IL-6 tõusnud võrreldes patsientidega, kellel seda ei olnud. Uurijad jõudsid järeldusele, et inimestel, kellel on MAFLD ja suurenenud seerumi IL-6 risk, areneb COVID-19[50] raske haigus. Zhou jt[22] uurisid neljas erinevas keskuses (Wenzhou keskhaigla, Wenzhou meditsiiniülikooli haigla, Ningbo nr 2 haigla ja Ruiani rahvahaigla) 327 COVID-i{35}} põdevat täiskasvanud patsienti, kes olid üle 18-aastased. Hiina 2020. aasta jaanuaris. 74 patsienti (23%) olid üle 60-aastased ja põdesid MAFLD-d ja ülejäänud 93 patsiendil oli ka MAFLD. Lisaks põdesid eakatel patsientidel 18 diabeeti ja 32-l diagnoositi hüpertensioon. Noorematest patsientidest (alla 60-aastased) kannatas 45 hüpertensiooni ja 29 diabeeti. Hüpertensiooni ja diabeedi levimus oli eakatel patsientidel suurem kui noorematel patsientidel. Seevastu leidsid teadlased tugeva korrelatsiooni MAFLD ja COVID-19 vahel noorematel patsientidel (χ 2 test P=0,001) võrreldes eakate patsientidega (χ 2 test P=0,66). ). Uurijad täheldasid, et raske COVID{54}} esinemissagedus oli noorematel MAFLD-ga patsientidel (vanuses alla 60 aasta) kaks korda kõrgem kui mitte-MAFLD-ga patsientidel. Uurijad tegid kokkuvõtte, et noorematel MAFLD patsientidel oli suurem risk COVID{57}} kui eakatel MAFLD patsientidel. Uurides 310 COVID{59}} patsienti, kannatas 310-st 94 MAFLD-i. Teadlased kasutasid fibroosi-4 (FIB-4) indeksit fibroosi hindamise peamise kriteeriumina. Uurijad täheldasid, et FIB-4 indeks oli alla 1,3 44 patsiendil, samas kui see väärtus oli vahemikus 1,3 kuni 2,6 36 patsiendil. Kõrge FIB-4 väärtusega MAFLD-ga patsiendid olid tõenäolisemalt rasvunud, vanemad ja diabeetikud ning neil oli kõrgem C-reaktiivne valk, kõrgem maksaensüümide tase ning madalam lümfotsüütide ja trombotsüütide arv võrreldes MAFLD-ga. madal FIB-4 tulemus. Uuringutest on ilmne, et kõrge FIB{75}} skooriga MAFLD patsientidel oli suurem tõenäosus COVID-19[51]. Ji jt[16] uurisid 202 COVID-i põdevat MAFLD-ga patsienti{80}}. Enamikul patsientidest oli maksakahjustus kerge hepatotsellulaarse mustriga ja ainult 3% oli segatud või duktuaalne muster. Erinevad maksaensüümid olid patsientidel kõrgenenud, näiteks TBIL 9%, ALP 2,5% ja AST 17%. ja ALT 50%. Uurijad täheldasid, et MAFLD-ga patsientidel oli suurem risk COVID{87}} progresseerumiseks ja viiruse levikuaeg pikem kui mitte-AFLD-ga patsientidel.
Leiti, et COVID-19 muudab glükoosi homöostaasi, kutsub esile tsütokiinide tormi ja suurendab oksüdatiivset stressi[52]. MAFLD-ga patsientidel, peamiselt rasvunud patsientidel, on täheldatud kõrgenenud IL-6 taset, mis suurendab COVID-i riski-19[53]. MAFLD võib iseloomustada suurenenud eelsoodumust tsütokiini tormi sündroomile, suurenenud C-reaktiivse valgu ja IL-6 taset ning NLR-i perekonna püriini domeeni 3 (NLRP3) aktiveerimist. Isik, kellel on juba olemasolev MAFLD, muudab ta haavatavamaks SARS-CoV{11}} ja sellega seotud tüsistuste suhtes. Erinevad uuringud tõid välja, et raske COVID{12}} on MAFLD-ga inimestel tavalisem, mis põhjustab kriitilisi haigusi ja isegi mittealkohoolse steatohepatiidi väljakujunemist[54]. PubMedi andmebaasi kriitiline analüüs näitas, et alla 60-aastastel patsientidel, kes põevad MAFLD-d (rasvumine ja raske fibroos), on suurem tõenäosus raske COVID-i tekkeks-19. Uurijad leidsid, et COVID{17}} raskusaste suurenes MAFLD-ga patsientidel 4–6 korda võrreldes mitte-MAFLD-patsientidega[10]. Seega võib tsütokiinide kõrgenenud taset ja muutunud maksafunktsiooni pidada oluliseks COVID{22}} raske haiguse korral MAFLD-ga patsientidel.
MAKSAVIGASTUSE MEHHANISM COVID{0}} JA MAFLD-is
Võimalik mehhanism, mis vastutab COVID{0}} eest, mis soodustab MAFLD progresseerumist, hõlmab viiruse otsest toksilisust, süsteemset põletikureaktsiooni sündroomi, DILI-d, hüpoksilist vigastust, soolestiku mikrobiota tasakaalustamatust ja maksa lipiidide metabolismi häireid[55]. Maksa ACE2 ja transmembraanse proteaas seriin 2 (TMPRSS2) ekspressioon paraneb COVID{5}} patsientidel, kellel on juba MAFLD. Need kaks tegurit võivad põhjustada MAFLD-ga patsientide suurenenud vastuvõtlikkust COVID-i suhtes-19[56]. Maksas leidub rohkesti erinevaid kaasasündinud immuunrakke, nagu looduslikud tapjarakud, looduslikud tapja-T-rakud ja makrofaagid[57]. MAFLD ja rasvumine on tavaliselt seotud Kupfferi rakkude ja rasvrakkude (TNF-) põletikueelsete tsütokiinide suurenenud tootmisega. Stimuleeritud makrofaagidel on kahte tüüpi vastuseid, M1 ja M2. M1 makrofaagid vastutavad põletikuliste protsesside algatamise eest, samas kui M2 makrofaagidel on reparatiivsed ja põletikuvastased funktsioonid ning kemokiinide kõrge ekspressioon. Ennustatakse, et MAFLD patogeneesi eest vastutab düsreguleeritud maksa kaasasündinud immuunsus [58]. Võimalik, et maksa makrofaagid nihkuvad suurema tõenäosusega M1-makrofaagidelt (soodustavad põletikku) M2-makrofaagideks (suruvad põletikku), mis viib COVID{18}} progresseerumiseni. Märkimisväärse fibroosiga MAFLD võib intensiivistada viiruse põhjustatud tsütokiinide tormi, tõenäoliselt põletikueelsete tsütokiinide vabanemise tõttu maksas, mis aitab oluliselt kaasa raskele COVID-i tekkele-19.
Teatati, et ACE2 retseptorid esinevad maksas hepatotsüütides ja kolangiotsüütides. Koroonaviirus sihib neid ACE2 retseptoreid siseneda ja eeldatakse, et see põhjustab hepatotsüütide ja kolangiotsüütide kahjustusi[59]. Seevastu üks teine uurimisrühm võttis kokku, et MAFLD-d ei seostata koroonaviiruse infektsiooni jaoks vajalikke valguretseptoreid kodeerivate geenide (nt TMPRSS2, ACE2 ja fosfatidüülinositool3-fosfaat5-kinaas (PIKfyve)) suurenenud ekspressiooniga. Uurijad jõudsid järeldusele, et ACE2 suurenenud ekspressioon MAFLD-COVID{9}} patsientidel ei ole tõsine õigustus suurenenud maksakahjustusele[60]. SARS-CoV{12}} infektsioon vähendas maksa mitokondriaalset aktiivsust ja soodustas hepatotsüütide mitokondriaalset turset, mida kinnitasid ultrastruktuurne uuring ja transkriptoomiline analüüs. Need tulemused soovitavad tungivalt, et SARS CoV{13}} vastutab otseselt tsütopaatiliste mõjude eest ja aitab positiivselt kaasa MAFLD progresseerumisele [61]. SARS-CoV-2 infektsioon soodustab cGAS-STINGi aktiveerimist endoteelirakkudes, vabastades mitokondriaalse DNA, mille tulemuseks on I tüüpi IFN tootmine ja rakusurm. Mitokondriaalne turse hepatotsüütides tekib SARS-CoV{19}} infektsiooni tõttu, mis näitab, et cGAS-STING signaali aktiveerimine võib COVID-i põdevatel patsientidel MAFLD-d süvendada{21}}[62]. MAFLD- ja COVID-i põdevatel patsientidel teatati põletikuliste tsütokiinide taseme tõusust-19[10,63]. Seega põhjustas COVID-19 MAFLD-ga patsientidel tsütokiinitormi tõttu tõsise haiguse. Muutunud peremeesorganismi ACE2 retseptori ekspressioon, otsene viiruse rünnak hepatotsüütidele, kolangiotsüütide funktsiooni katkemine, düsreguleeritud immuunvastused, hüperpõletik, maksa isheemiline ja hüpoksiline kahjustus, ebanormaalne koagulatsioon ja tromboos, DILI ning muutunud glükoosi ja lipiidide hemostaas on mõned mitmefaktorilised mehhanismid. COVID{28}} ja MAFLD[21] halvem tulemus.

Tistanche kasulikud omadused meestele - tugevdavad immuunsüsteemi
COVID{0}} PATSIENTIDE HALDAMINE, KES JUBA MAFLDi KANNATAVAD
Esimene juhtimine on COVID{0}} patsientide varajane ja täpne maksa biokeemiline jälgimine. MAFLD-ga seotud testid tuleks teha võimalikult varakult, et jälgida maksa nõuetekohast toimimist. MAFLD-ga patsiendid võivad olla DILI suhtes haavatavad, seetõttu tuleks vältida korduvaid ravimeid ning keskenduda tuleks ravimi annusele ja kestusele. Diabeediga patsientidel tuleks tõhustada metaboolset kontrolli ja see on SARS-CoV-2 nakkuse esmane ennetav samm. Gripivastane vaktsineerimine vähendab kopsupõletiku riski 45%-50% võrra suhkurtõvega inimeste seas, mida saab kasutada COVID-i põdevatel patsientidel-19[64]. ARDS tekkis COVID-19 patsientidel tavaliselt tsütokiinide vabanemise sündroomi soodustava düsreguleeritud immuunvastuse tõttu. Metformiin, T2DM-i esmavaliku ravim, suurendas immuunvastust ja hoidis ära ARDS-i, võrreldes teiste antihüperglükeemiliste ravimitega. Veelgi enam, glükagoonilaadsed peptiid{12}}-retseptori agonistid, nagu SGLT2 ja GLP{14}}RA, võivad COVID{15}}-patsientidel ka hüperglükeemiat juhtida[21,65]. COVID-i{18}} juhtimine hõlmab metaboolsete patoloogiate sihipäraste sekkumiste parandamist. Vaktsineerimisvastust SARS-CoV-2 vastu tuleb rasvumise ja DM-i patsientidel hoolikalt uurida[66]. COVID-19 nõuab MAFLD-ga patsientidel erilist tähelepanu ja soovitatav on varakult haiglaravi. Lisaks tuleb sellistel patsientidel jätkata arteriaalse hüpertensiooni ravi. Raske haiguse väljakujunemise vältimiseks SARS-CoV{25}} nakkuse korral on vaja ranget elustiili muutmist, sealhulgas toitumisjuhiste järgimist, kehakaalu langetamise meetmeid ja hüperglükeemia ravi[67]. SARS-CoV-2 infektsiooni tõttu võib MAFLD-ga patsientide hepatotsüütides tekkida hüpoksia, millele järgneb tõsine kopsukahjustus, mis viib hüpoksiast põhjustatud tegurite ja ACE2 retseptorite ekspressiooni suurenemiseni. Fibroosi põdevad MAFLD-patsiendid on veel üks väljakutse COVID-iga toimetulemiseks-19. Seega vajavad MAFLD-ga patsiendid SARS-CoV-2 nakkuse ajal erilist hoolt ja piisavat elustiili sekkumist, et COVID-19 tagajärgi ära hoida.
KOKKUVÕTE
MAFLD-ga patsientidel on suurem risk haigestuda COVID-i{0}} ja piisav elustiili sekkumine on SARS-CoV-2 nakkuse põhjustatud kahju minimeerimiseks hädavajalik. COVID-i{3}} põdevatel MAFLD patsientidel on suurem maksakahjustuse oht. Leiti, et COVID-19 muudab glükoosi homöostaasi, suurendab põletikuliste tsütokiinide tormi teket ja suurendab oksüdatiivset stressi, halvendades seega MAFLD patsientide olukorda. COVID-iga patsientidel tuleb jälgida ka südame-, neeru- ja maksafunktsiooni markerite kõrvalekaldeid, samuti lihaskahjustusi ja hüübimisparameetreid.{5}}. Lisaks põhjustab COVID{6}} maksakahjustusi koos kõrgenenud ALT ja ASAT tasemega. COVID{7}} patsientide polüteraapia on tavaline; seega on sellised patsiendid haavatavad ka DILI suhtes, kuna mõned neist võivad põhjustada maksaensüümide aktiivsuse tõusu asümptomaatiliselt. Seega peetakse SARS-CoV-2-infektsiooniga MAFLD-ga patsiente rasketeks ja vajavad kiiret tähelepanu.
VIITED
1 Velavan TP, Meyer CG. COVID{1}} epideemia. Trop Med Int Health 2020; 25: 278-280 [PMID: 32052514 DOI: 10.1111/tmi.13383]
2 Cao X. COVID-19: immunopatoloogia ja selle tagajärjed ravile. Nat Rev Immunol 2020; 20: 269-270 [PMID: 32273594 DOI: 10,1038/s41577-020-0308-3]
3 Ciotti M, Ciccozzi M, Terrinoni A, Jiang WC, Wang CB, Bernardini S. COVID{1}} pandeemia. Crit Rev Clin Lab Sci 2020; 57: 365-388 [PMID: 32645276 DOI: 10.1080/10408363.2020.1783198]
4 Yuki K, Fujiogi M, Koutsogiannaki S. COVID{1}} patofüsioloogia: ülevaade. Clin Immunol 2020; 215: 108427 [PMID: 32325252 DOI: 10.1016/j.clim.2020.108427]
5 Yang L, Liu S, Liu J, Zhang Z, Wan X, Huang B, Chen Y, Zhang Y. COVID-19: immunopatogenees ja immunoteraapia. Signal Transduct Target Ther 2020; 5: 128 [PMID: 32712629 DOI: 10,1038/s41392-020-00243-2]
6 Eslam M, Newsome PN, Sarin SK, Anstee QM, Targher G, Romero-Gomez M, Zelber-Sagi S, Wai-Sun Wong V, Dufour JF, Schattenberg JM, Kawaguchi T, Arrese M, Valenti L, Shiha G, Tiribelli C, Yki-Järvinen H, Fan JG, Grønbæk H, Yilmaz Y, Cortez-Pinto H, Oliveira CP, Bedossa P, Adams LA, Zheng MH, Fouad Y, Chan WK, Mendez-Sanchez N, Ahn SH, Castera L , Bugianesi E, Ratziu V, George J. Uus metaboolse düsfunktsiooniga seotud rasvmaksahaiguse määratlus: rahvusvaheline ekspertide konsensusavaldus. J Hepatol 2020; 73: 202-209 [PMID: 32278004 DOI: 10.1016/j.jhep.2020.03.039]
7 Hashimoto E, Taniai M, Tokushige K. NAFLD/NASH omadused ja diagnoos. J Gastroenterol Hepatol 2013; 28 Lisa 4: 64-70 [PMID: 24251707 DOI: 10.1111/jgh.12271]
8 Kim CH, Younossi ZM. Mittealkohoolne rasvmaksa haigus: metaboolse sündroomi ilming. Cleve Clin J Med 2008; 75: 721-728 [PMID: 18939388 DOI: 10.3949/ccjm.75.10.721]
9 Sharma P, Kumar A. Rasvmaksahaigusega seotud metaboolne düsfunktsioon suurendab raske Covidi haigestumise riski-19. Diabeet Metab Syndr 2020; 14: 825-827 [PMID: 32540736 DOI: 10.1016/j.dsx.2020.06.013] 10 Sachdeva S, Khandait H, Kopel J, Aloysius MM, Desai R, Goyal H. NAFLD ja COVID{12}} : koondatud analüüs. SN Compr Clin Med 2020; 2: 2726-2729 [PMID: 33173850 DOI: 10,1007/s42399-020-00631-3]
11 Forlano R, Mullis BH, Mukherjee SK, Nathwani R, Harlow C, Crook P, kohtunik R, Soubieres A, Middleton P, Daunt A, Perez-Guzman P, Selvapatt N, Lemoine M, Dhar A, Thursz MR, Nayagam S , Manousou P. Haiglas suremus on seotud põletikulise vastusega NAFLD-ga patsientidel, kes on COVID-i tõttu vastu võetud-19. PLoS One 2020; 15: e0240400 [PMID: 33031439 DOI: 10.1371/journal.pone.0240400]
12 Portincasa P, Krawczyk M, Smyk W, Lammert F, Di Ciaula A. COVID-19 ja mittealkohoolne rasvmaksahaigus: kaks ristuvat pandeemiat. Eur J Clin Invest 2020; 50: e13338 [PMID: 32589264 DOI: 10.1111/eci.13338]
13 Younossi ZM, Stepanova M, Lam B, Cable R, Felix S, Jeffers T, Younossi E, Pham H, Srishord M, Austin P, Estep M, Terra K, Escheik C, de Avila L, Golabi P, Kolacevski A, Racila A, Henry L, Gerber L. COVID{1}}-nakkusega haiglaravile sattunud NAFLD-ga patsientide suremuse sõltumatud ennustajad. Hepatol Commun 2022; 6: 3062-3072 [PMID: 34558853 DOI: 10.1002/hep4.1802]
14 Bramante C, Tignanelli CJ, Dutta N, Jones E, Tamariz L, Clark JM, Usher M, Metlon-Meaux G, Ikramuddin S. Mittealkohoolne rasvmaksahaigus (NAFLD) ja Covidi tõttu haiglasse sattumise oht-19. medRxiv 2020 [PMID: 32909011 DOI: 10.1101/2020.09.01.20185850]
15 Bramante C, Tignanelli CJ, Dutta N, Jones E, Tamariz L, Clark JM, Usher M, Metlon-Meaux G, Ikramuddin S. Mittealkohoolne rasvmaksahaigus (NAFLD) ja Covidi tõttu haiglasse sattumise oht-19. medRxiv 2020 [PMID: 32909011 DOI: 10.1101/2020.09.01.20185850]
16 Ji D, Qin E, Xu J, Zhang D, Cheng G, Wang Y, Lau G. Mittealkohoolsed rasvmaksahaigused COVID-iga patsientidel-19: retrospektiivne uuring. J Hepatol 2020; 73: 451-453 [PMID: 32278005 DOI: 10.1016/j.jhep.2020.03.044]
17 Huang R, Zhu L, Wang J, Xue L, Liu L, Yan X, Huang S, Li Y, Zhang B, Xu T, Li C, Ji F, Ming F, Zhao Y, Cheng J, Wang Y, Zhao H, Hong S, Chen K, Zhao XA, Zou L, Sang D, Shao H, Guan X, Chen X, Chen Y, Wei J, Zhu C, Wu C. COVID-iga patsientide kliinilised tunnused-19 Mittealkohoolne rasvmaksahaigus. Hepatol Commun 2020; 4: 1758- 1768 [PMID: 32838108 DOI: 10.1002/hep4.1592]
18 Singh A, Hussain S, Antony B. Alkoholivaba rasvmaksahaigus ja kliinilised tulemused COVID-iga patsientidel-19: põhjalik süstemaatiline ülevaade ja metaanalüüs. Diabeet Metab Syndr 2021; 15: 813-822 [PMID: 33862417 DOI: 10.1016/j.dsx.2021.03.019]
19 Mushtaq K, Khan MU, Iqbal F, Alsoub DH, Chaudhry HS, Ata F, Iqbal P, Elfert K, Balaraju G, Almaslamani M, Al-Ejji K, AlKaabi S, Kamel YM. NAFLD ennustab COVID-19 haiglaravil olevate patsientide maksakahjustust, kuid mitte suremust, haiguse tõsidust ega progresseerumist – arutelu jätkub. J Hepatol 2021; 74: 482-484 [PMID: 33223215 DOI: 10.1016/j.jhep.2020.09.006]
20 Gao F, Zheng KI, Wang XB, Yan HD, Sun QF, Pan KH, Wang TY, Chen YP, George J, Zheng MH. Ainevahetusega seotud rasvmaksahaigus suurendab 2019. aasta koroonaviiruse haiguse raskust mittediabeetilistel patsientidel. J Gastroenterol Hepatol 2021; 36: 204-207 [PMID: 32436622 DOI: 10.1111/jgh.15112]
