Kitosaani hepatoprotektiivne toime tioatsetamiidist põhjustatud maksatoksilisusele isastel albiinorottidel
May 09, 2022
Lisateabe saamiseks. kontaktitina.xiang@wecistanche.com
Abstraktne: Kitosaan, kitiinist saadud looduslik toode, on oma ainulaadsete bioloogiliste aktiivsuste tõttu pälvinud palju tähelepanu kui paljulubav polüsahhariidühend. Selle uuringu eesmärk oli uurida kitosaani kui loodusliku meretoote võimalikku parandavat potentsiaalimaksa regenereeriminetioatsetamiidi poolt põhjustatud hepatotoksilisuses isastel albiinorottidel. Viiskümmend looma jagati 5 rühma, sealhulgas kontrollrühm; rühm, kellele süstiti intraperitoneaalselt ühekordne tioatseetamiidi annus (300 mg/kg kehamassi kohta) maksatoksilisuse esilekutsumiseks; rühm, kes sai 14 päeva jooksul 5 protsenti kitosaani sisaldavat dieeti; rühm sai 14 päeva jooksul dieeti, mis sisaldas 5 protsenti kitosaani, seejärel süstiti neile üks kord tioatseetamiidi (300 mg/kg kehamassi kohta) ja viimane rühm, kellele süstiti üks kord tioatseetamiidi (300 mg/kg kehamassi kohta) dieet, mis sisaldab 5 protsenti kitosaani 14 päeva jooksul. Biokeemilised tulemused näitasid, et kitosaani tarbimine enne või pärast tioatsetamiidimürgistust parandas maksamarkereid (ALAT, ASAT, GGT, ALP, albumiin) ja neerufunktsioone ning ka plasma TNF- . QRT-PCR analüüs näitas, et kitosaan vähendas maksa TNF-, surviviini ja c-Myc kvantitatiivset geeniekspressiooni. Lisaks parandas kitosaan maksa histoloogilist pilti. See uuring näitas kitosaani paljulubavat toimet maksa regenereerimisel.
Märksõnad: tioatseetamiid; kitosaan; maksa regenereerimine;survivin; c-myc; kasvaja nekroosi faktor-.
1. Sissejuhatus
Maksahaigusedon maailmas, eriti Egiptuses, kõige eluohtlikumad vaevused [1]. Egiptuses on maksahaigused iga-aastaste surmade peamine põhjus [2, 3]. Maks on väga mürgine, kuna see osaleb enamiku ksenobiootikumide, näiteks ravimite ja võõrühendite metabolismis. Õnneks võib rakkude proliferatsioon aidata maksal pärast suurt rakkude kadu taastuda [4, 5]. Järelikult on alternatiivsed ravimeetodid hädavajalikud, mis tuleb asendada või kasutada paralleelselt praeguste raviskeemidega. Kitosaan on paljulubav looduslik polüsahhariidühend. Seda võib saada krabide, krevettide ja vähkide koorejäätmetest ja seene rakuseinast.
Kitosaan on hea kiudainete allikas [6,7]. Sellel on palju tervisega seotud eeliseid, nagu immuunsuse reguleerimine, kasvajavastane toime, maksakaitse, diabeedivastane ja antioksüdant[8]. antibakteriaalne, hüpolipideemiline, põletikuvastane [9], haavu parandav toime [10,11] ja hepatoprotektiivne toime [12I. Kuna kitosaan on mittetoksiline ja biolagunev, on see suureks eeliseks oksüdatiivse stressi ohjamisel [13].
Mürgiste ühendite võimalikud allikad on saastunud toit ning kokkupuude keskkonna või keemiliste ainetega tööl. Nendest mürgistest ühenditest on tioatseetamiid (TAA), laialdaselt kasutatav väävlit sisaldav ühend, mida leidub keskkonnas orgaaniliste väävliühenditena ja mida kasutatakse paljudes tehnilistes rakendustes [14]. Samuti kasutatakse seda maksafibroosi esilekutsumiseks rottidel, et uurida fibroosivastaste ravimite terapeutilist toimet [15]. Tavaliselt on TAA sihiks maksa ja kutsub seega esile maksakahjustuse, tekitades reaktiivseid hapniku liike (ROS)[16,17]. TAA tiosulfaatrühm allub edasisele metabolismile oksüdaasisüsteemi kaudu, moodustades atseetamiidi ja TAA-S-oksiidi [18]. Pärast seda. Tekib TAA-S dioksiid, mis seostub kovalentselt maksa makromolekulidega ja algatab maksakahjustuse. See vigastus esineb tsentrilobulaarse nekroosi [19] ja ROS-i moodustumise kujul, mis koos põhjustavad oksüdatiivse stressi kaudu rakusurma [10, 20]. Kuna TAA ühekordne annus põhjustab hepatotsüütide degeneratsiooni, põletikuliste rakkude infiltratsiooni ning tõstab ALP, ALT ja AST taset [21].
Apoptoos on normaalselt esinev rakusurma mehhanism, mida kasutatakse tervete kudede arendamiseks ja säilitamiseks [22]. Düsreguleeritud apoptoosi tõttu võivad tekkida paljud haigused, nagu vähk, neurodegeneratiivsed häired ja immuunpuudulikkuse haigused. Huvitav on see, et apoptoos ise võib stimuleerida rakkude proliferatsiooni ja kudede regeneratsiooni mehhanismis, mida nimetatakse apoptoosist põhjustatud proliferatsiooniks. Lisaks võib apoptootilist protsessi blokeerida perekondlike valkude rühm, mida tuntakse apoptoosivalkude (IAP) inhibiitorina, inhibeerides kaspaasi aktiivsust. Imetajate genoomis on tuvastatud kaheksa IAP perekonna liiget [23]. Selle perekonna kõige olulisem valk on survivin, selle perekonna väikseim liige. Seda kodeerib geen BIRC5, mis asub 17. kromosoomi ribas. Leiti, et 17q25.3.c-myc valk on maksa regenereerimisprotsessis tugevalt suurenenud [24-26]. TNF- võib töötada kahe vastandliku mehhanismi abil. See võib toimida rakusurma initsiaatorina; alternatiivselt võib see suurendada rakkude proliferatsiooni. Järelikult mängib see olulist rolli viirusliku hepatiidi ning alkohoolsete ja mittealkohoolsete maksahaiguste patofüsioloogias [27,28].
Käesolevas uuringus uuriti kitosaani võimet kudede regeneratsiooni suurendamisel TAA poolt põhjustatud maksatoksilisuse vastu rottidel. Uuriti kitosaani mõju maksa- ja neerutalitlusele. Lisaks viidi läbi põletikku soodustava tsütokiini TNF- mõõtmised plasmas ning surviviini, c-Myc geenide ja TNF-i maksakoe geeniekspressioonitasemete kvantitatiivne analüüs. Lisaks uuriti maksa histoloogilisi tunnuseid.
Cistanchesaab reguleerida maksarakkude ultrastruktuuri, soodustada valkude sünteesi ja kaitsta maksa.Fenüületanooli glükosiididvõib suurendada maksa glükogeeni kogust,ehhinakosiidvõib parandada mätaste aktiivsust ja verbaskosiid võib eemaldada vabu radikaale ja vähendada tüvirakkude apoptoosi. Cistanche võib reguleerida ka vereringesüsteemi ja omada järgmisi mõjusid: kaitsta isheemilist müokardit; alandavad vere lipiidide taset, takistavad ateroskleroosi ja takistavad tromboosi; vähendada perifeersete veresoonte resistentsust, laiendada perifeerseid veresooni ja alandada vererõhku; kaitsta maksa ja takistada maksa rasvumist.

2. Materjalid ja meetodid
2.1.Kemikaalid.
TAA osteti firmalt Aldrich Chem Co., Inglismaa, puhaste kristallidena; see lahustati soolalahuses ja valmistati värskelt enne iga süstimist.
Kitosaan (CS) saadi firmalt Sigma-Aldrich (molekulmass =100 KDa). Kitosaan, oluline merelise päritoluga polüsahhariid, valmistatakse koorikloomade kestadest ja seda kasutatakse ravimite väljatöötamisel uue kiudainete allikana, kuna see on suukaudsel manustamisel ohutu [29].
2.2.Katsekujundus.
Viiskümmend täiskasvanud isast Wistari albiinorotti, kes kaalusid ligikaudu 120-150 g, saadi Egiptuse Kairos asuvast riikliku uurimiskeskuse loomamajakolooniast. Loomi peeti roostevabast terasest puurides standardsetes laboritingimustes hea ventilatsiooni ja 12-tunnise valguse-pimeduse tsükliga, suhtelise õhuniiskusega 60 ± 5 protsenti ning vaba juurdepääsu standardsele laboratoorsele toidule ja kraaniveele.
Enne katseprotokolli algust kohandati rotte 2 nädala jooksul katsetingimustega. Inimese hoolitsus rakendati vastavalt asutuse katseloomade hooldamise ja kasutamise standardkriteeriumitele vastavalt riikliku uurimiskeskuse eetikakomitee (FWA 00014747) kinnitatud meetodile, mis jälgib National Institutes of Health Guide'i soovitusi. Loomade hooldamiseks ja kasutamiseks laboris (väljaanne nr.{2}}, muudetud 1985. aastal).
Loomad jagati pärast aklimatiseerumisperioodi viide rühma (igaüks 10 rotti) järgmiselt:
Rühm (1): normaalsed terved loomad olid kontrollrühmaks.
Rühm (2): (TAA) rühm, kus rottidele süstiti intraperitoneaalselt TAA-d (lahustatuna 0,9 protsendilises normaalses soolalahuses) ühekordse annusena (300 mg/kg kehamassi kohta) vastavalt Mustafa et al. [30] maksatoksilisuse esilekutsumiseks.
Rühm (3): kitosaanirühm, kus loomadele anti AboZaid et al. järgi kitosaani segatud põhitoitu, suhtega 5 protsenti (50 g pluss 950 g põhitoitu). [9] 14 päevaks.
Rühm (4): kitosaani ja seejärel TAA rühm, kus loomad said 14 päeva jooksul dieeti, mis sisaldas 5 protsenti kitosaani 9], seejärel süstiti neile intraperitoneaalselt ühekordne annus TAA-d (300 mg/kg kehamassi kohta), nagu eespool mainitud.
Rühm (5): TAA ja seejärel kitosaani rühm, kuhu loomadele süstiti intraperitoneaalselt TAA üksikannust (300 mg/kg kehakaalu kohta), nagu eespool mainitud, ja seejärel toideti 14 päeva jooksul dieeti, mis sisaldas 5 protsenti kitosaani.
Iga looma kehakaal registreeriti igal nädalal ja katse lõpus, et jälgida kehakaalu muutust. Katseperioodi lõpus paastusid loomad 12 tundi. Seejärel anesteseeriti nad dietüüleetri sissehingamise teel; vereproovid võeti retroorbitaalsest venoossest põimikust tsentrifuugitorudes, kasutades hepariniseeritud steriilseid klaaskapillaare.
Plasma eraldamiseks koondati osa kõigist vereproovidest EDTA-le, teine osa antikoagulantidest vabasse katsutisse, et eraldada seerum. Nii seerumi- kui ka plasmaproovid eraldati jahutustsentrifuugimise teel kiirusel 3000 p/min 15 minutit temperatuuril 4 °C. Plasma ja seerumi alikvoodid säilitati biokeemilise analüüsi jaoks -20 kraadi juures.
Niipea kui veri koguti, ohverdati loomad emakakaela pea maharaiumisega
Iga roti maks eemaldati ja pesti põhjalikult isotoonilise soolalahusega, kuivatati ja jagati kaheks osaks; esimene sektsioon külmutati vahetult vedelas lämmastikus ja säilitati -80 kraadi juures enne RNA eraldamist geeniekspressiooni analüüsiks. Seevastu teine osa fikseeriti formaalses soolalahuses (10 protsenti), mida kasutati histopatoloogilises uuringus.
2.3.Biokeemiline analüüs.
Seerumi aspartaataminotransferaasi (ASAT), alaniinaminotransferaasi (ALAT), aluselise fosfataasi (ALP) ja gamma-glutamüültransferaasi (GGT) aktiivsus, samuti albumiin
uurea ja kreatiniini taset hinnati spektrofotomeetriliselt, kasutades Egiptusest bio-diagnostic Co. ostetud reaktiivikomplekte. Plasma kasvaja nekroosifaktor-alfa (TNF-a) kontsentratsiooni hinnati ELISA meetodil, kasutades roti TNF-ELISA komplekti, mis osteti ettevõttest Glory Science Co., Ltd., USA.

2.4. Geeniekspressiooni analüüs.
Kvantitatiivse analüüsi (reaalajas PCR) abil määrati maksakoeproovides surviviini, c-Myc ja TNF-geenide ekspressioon.
2.4.1. RNA eraldamine, puhastamine ja kvantitatiivne reaalajas RT-PCR.
RNA eraldati 100 mg maksakoeproovist Qiazol puhvriga (Qiagen, USA); Seejärel puhastati RNA, kasutades komplekti RNAeasy Mini (Qiagen, USA); RNA pöördtranskribeeriti ja saadud cDNA amplifitseeriti. -aktiini, surviviini, c-myc ja TNF-alfa geeni koopiate arvud kvantifitseeriti, kasutades QuantiFast Sybergreen RT-PCR komplekti (Qiagen, USA). Kõiki proove kasutati kolmes eksemplaris ja koopiate arv normaliseeriti 100,000 majapidamise beeta-aktiini geeni koopiaks. Praimeri järjestused on loetletud tabelis 1. RT ja sellele järgnenud PCR tsüklitingimused olid järgmised: 50 kraadi 10 minutit, 95 kraadi 5 minutit, 95 kraadi 15 sekundit, seejärel 60 kraadi 30 sekundit, tsüklite arv oli 40 tsüklit . Geeniekspressiooni kvantiseerimiseks kasutati MiniOpticonTM Bio-Rad Real-Time Thermal Cyclerit.

2.5. Histopatoloogiline uuring.
Pärast maksakudede fikseerimist 10-protsendilises soolalahuses 24 tundi pesti koeproove jooksvas kraanivees; seejärel dehüdreeriti, kasutades etüüli (jadalahjendused kuni absoluutse etüülini). Proovid puhastati ksüleenis ja sisestati parafiini 56 kraadi juures kuumaõhuahjus 24 tunniks. Vahakoe plokid valmistati 4 mikroni paksuseks lõikamiseks muda mikrotoomiga. Sektsioonid deparafineeriti, värviti hematoksüliini ja eosiiniga ning lõpuks uuriti neid elektrilise valgusmikroskoobiga [31].
2.6. Statistiline analüüs.
Andmeid analüüsiti sotsiaalteaduste arvutipõhise statistikapaketi versiooni 13 abil. Tulemused on väljendatud kolme sõltumatu katse keskmistena ± SD. Erinevuste statistiline olulisus määrati ühesuunalise dispersioonanalüüsi (ANOVA) abil, millele järgnes LSD post hoc võrdlustest p Väiksem või võrdne sellega 0,05, mis määrati statistiliselt oluliseks.
3. Tulemused ja arutelud
3.1.Tulemused.
Joonisel 1 esitatud andmed näitasid, et TAA-ga joobes loomade rühmas vähenes kehakaalu tõus oluliselt (-308,5 protsenti), samas kui ainult kitosaani rühmas ilmnes oluline muutus (50 protsenti), kui mõlemad rühmad olid võrreldes kontrollrühmaga. Huvitav on see, et kitosaani ja seejärel TAA loomade rühmas ilmnes kehakaalu tõus märkimisväärselt (289,7 protsenti); samamoodi näitas TAA ja kitosaani loomade rühmas kehakaalu suurenemine märkimisväärselt (239,56 protsenti), kui mõlemat rühma võrreldi TAA-ga joobestunud loomade rühmaga.

Mis puudutab maksafunktsiooni teste, siis normaalsete rottide toitmine 14 päeva jooksul 5-protsendilise kitosaani baastoiduga ei häirinud ei maksa- ega neerufunktsiooni teste, mis peegeldavad nende ohutut toimet sellisel kontsentratsioonil toidus; vastupidi, TAA-st põhjustatud maksatoksilisus rottidel suurendas märkimisväärselt (94,47 protsenti) seerumi aspartaataminotransferaasi (ASAT) aktiivsust võrreldes kontrollrühmaga. Siiski registreeriti mõlemas kitosaaniga toidetud ravirežiimis (vastavalt kitosaan-TAA ja TAA-kitosaani rühmad) seerumi ASAT-i aktiivsuse oluline langus (-32 protsenti ja -15,4 protsenti) võrreldes TAA-joobes rühm. TAA rühmas registreeriti seerumi alaniini aminotransferaasi (ALAT) aktiivsuse oluline tõus (91,89 protsenti) võrreldes kontrollrühmaga. Paljutõotava efektina põhjustasid kitosaani, seejärel TAA ja TAA ja seejärel kitosaani rühmad seerumi (ALAT) aktiivsuse olulise languse (vastavalt -40,8 protsenti ja 32,3 protsenti) võrreldes TAA rühmaga. Samamoodi tuvastati seerumi aluselise fosfataasi (ALP) aktiivsuse oluline suurenemine (232,9 protsenti) TAA-ga joobes loomade rühmas võrreldes kontrollrühmaga. Rottide toitmine kitosaani segatoiduga 14 päeva enne TAA-ga mürgistust põhjustas seerumi ALP-aktiivsuse olulise languse (-54,06 protsenti); Samuti registreeriti seerumi ALP aktiivsuse oluline vähenemine (-50,6 protsenti) loomade rühmas, kes said pärast TAA mürgistust kitosaani segatoitu, kui mõlemat loomarühma võrreldi ainult TAA-ga ravitud rühmaga.
Mis puudutab seerumi gamma-glutamüültransferaasi (GGT) aktiivsust, siis TAA-ga indutseeritud maksatoksilisus suurendas oluliselt (223,5 protsenti) seerumi GGT aktiivsust, samas kui ainult kitosaani saanud loomade rühm ei halvendanud oma aktiivsust, kui mõlemat rühma võrreldi selle rühmaga. kontrollrühmast. Huvitaval kombel loomade toitmine kitosaani segatoidul enne
TAA-mürgistus näitas seerumi GGT aktiivsuse olulist vähenemist (-50,28 protsenti); samamoodi täheldati GGT aktiivsuse olulist langust (-41.0 protsenti o) loomade rühmas, kes olid enne kitosaani segatoidule saamist joobnud TAA-ga, kui mõlemat võrreldi TAA-ga. joobes grupp. Seerumi albumiini tase langes oluliselt (-36,58 protsenti ) pärast TAA süstimist (TAA rühm), samas kui kitosaani rühmas ilmnes seerumi albumiini tasemes ebaoluline muutus (2,4 protsenti o), kui mõlemat rühma võrreldi kontrollrühmaga . Kuid loomade toitmine kitosaaniga erinevate režiimide järgi, kas enne või pärast TAA-mürgistust, näitas märkimisväärset seerumi albumiinitaseme tõusu (vastavalt 50 protsenti ja 38,4 protsenti), kui neid võrreldi TAA rühmaga (tabel 2).
Seoses neerufunktsiooni munanditega (tabel 2) täheldati TAA-mürgistuse rühmas nii uurea kui ka kreatiniini seerumitaseme olulist tõusu (82,67 protsenti ja 232,77 protsenti); vahepeal oli ainult kitosaaniga ravitud rühmas ebaoluline muutus (vastavalt 19,3 protsenti ja -15 protsenti), kui mõlemat rühma võrreldi kontrollrühmaga. Paljulubaval viisil näitasid kitosaani ja seejärel TAA loomade rühma uurea ja kreatiniini seerumitasemed oluliselt (-36,04 protsenti ja -45,2 protsenti) võrreldes TAA rühmaga. . Veelgi enam, rottide toitmine kitosaani segatoiduga 14 päeva jooksul pärast TAA-mürgistust näitas olulist langust (-30,6 protsenti ja -35,10 protsenti) nii uurea kui ka kreatiniini sisalduses seerumis, kui mõlemat rühma võrreldi TAA-ga ravitud loomade rühmaga.

Nagu on näidatud joonisel (2), registreeriti TAA-ga mürgitatud loomade rühmas alfatuumori nekroosifaktori alfa (TNF-) taseme oluline tõus (98,26 protsenti); samas kui kitosaanirühmas ilmnes plasma TNF-i tasemes ebaoluline muutus (-2,6 protsenti), kui mõlema loomarühma võrreldi kontrollrühmaga. Eelkõige näitas loomade toitmine kitosaani segatoiduga erinevate režiimide järgi, kas enne või pärast TAA-mürgistust, märkimisväärset langust (vastavalt -36,6% ja -31,57%). plasma TNF-tasemes, kui mõlemat võrreldi TAA rühmaga.

3.1.1. Geeni ekspressioon.
Nagu on näidatud joonisel 3, vähenes TAA-ga mürgitatud loomade rühmas surviviini maksa geeniekspressioon märkimisväärselt (-81 protsenti), samas kui ainult kitosaani kasutanud rühmas esines surviviini maksa geeniekspressioonis ebaolulisi muutusi, kui mõlemat rühma võrreldi. kontrollrühmaga. Kahjuks ei ilmnenud nii kitosaaniga, seejärel TAA-ga kui ka TAA-ga, seejärel kitosaaniga ravitud loomade rühmas selles geeniekspressioonis olulisi muutusi (vastavalt 1,27 protsenti ja -3,2 protsenti) võrreldes TAA-ga joobestunud loomadega. loomade rühm.

Mis puudutab c-myc geeniekspressiooni, siis ainult kitosaani rühmas oli märkimisväärne tõus (400 protsenti). Siiski ei mõjutanud TAA-joobes loomade rühm (0,0 protsenti o) selle geeni ekspressiooni, kui mõlemat rühma võrreldi kontrollrühmaga. Lisaks näitasid nii kitosaani, seejärel TAA kui ka TAA ja seejärel kitosaani rühmad c-myc geeni ekspressioonitasemete märkimisväärset tõusu (vastavalt 300 protsenti ja 700 protsenti) võrreldes TAA rühmaga (joonis 4).

Andmed näitasid, et kitosaaniga ravitud loomade rühmas registreeriti ainult märgatav maksa TNF-geeni ekspressioonitaseme tõus (73,33 protsenti); pealegi näitas TAA-ga joobestatud loomade rühm märkimisväärset tõusu (368,3 protsenti), kui võrrelda mõlemat rühma kontrollrühmaga. See tõus vähenes oluliselt (vastavalt -66.5% ja -57.3%) kitosaanraviga, kas enne või pärast TAA-mürgistust, võrreldes TAA loomade rühmaga (joonis 5).

3.1.2.Histoloogiline leid.
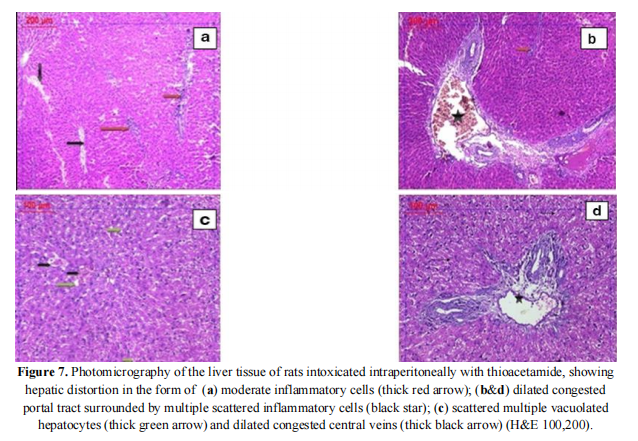
Normaalsel kontrollrühmal oli normaalne maksakoe arhitektuur normaalse keskveeniga, säilinud portaaltrakt minimaalseltpõletikulinerakud ja enamasti normaalsed hepatotsüüdid (joonis 6). Samal ajal näitasid TAA rühma uuringud maksa halvenemist, mida esindasid vakuoleeritud hepatotsüütide rakud, laienenud ülekoormatud keskveen, laienenud ülekoormatud portaaltrakt ja mõõdukad hajutatud põletikulised rakud (joonis 7). Kitosaani ravimite rühmad näitasid normaalset maksakoe arhitektuuri, kergelt laienenud, tsentraalset normaalset portaaltrakti minimaalsete põletikuliste rakkude ja normaalsete hepatotsüütidega (joonis 8). Kitosaani ja seejärel TAA rühmas ilmnes moonutatud laienenud keskveen, hajutatud põletikurakud ja laienenud ülekoormatud sinusoidaalsed ruumid, hepatotsüütide märgatav degeneratsioon koos rasvhapete muutustega ja suurenenud hepatotsüütide paksus (rohkem kui 2 rakku) (joonis 9). Peale selle näitas TAA seejärel kitosaani rühm ülekoormatud laienenud keskveeni hajutatud põletikurakke, märgatavalt laienenud ülekoormatud portaaltrakti ja hajutatud degenereerunud hepatotsüüte (joonis 10).





3.2.Arutelu.
Maks on keha suurim nääre, kus see kontrollib paljusid energiat nõudvaid bioloogilisi protsesse, nagu ainevahetus, biosüntees, eritumine, sekretsioon ja detoksikatsioon. Need suured energiavajadused muudavad maksa väga hapnikust sõltuvaks koeks. Pärast massilist rakkude kadu aitab rakkude proliferatsioon maksa taastuda. Regenereerimine võib aga ebaõnnestuda, kui kaotus ületab teatud piirid, mille tulemuseks on maksapuudulikkus ja lõpuks surm 32].
Viidi läbi palju uuringuid, et testida antioksüdantide toimet maksahaiguste leevendamisel ja normaalse maksa toetamisel. Antioksüdandid on esile kerkinud kui ravivõimalus elustiilist tingitud haiguste raviks ja ennetamiseks. Siiski vajab see täiendavaid uuringuid, et selgitada selle toimeviisi 33, 34]. Kitosaan (CS) on väärtuslik mereline polüsahhariid, mida saadakse mõnede koorikloomade kestadest. Sellel on palju väljakujunenud bioloogilisi eeliseid, nagu immuunsuse reguleerimine, kasvajavastane, maksakaitse, diabeedivastane, antibakteriaalne, antioksüdant, rasvumisvastane, haavade paranemine ja hüpolipideemiline toime [5].
Käesolevas uuringus uuriti kitosaani kaitsvat ja terapeutilist efektiivsust koe regeneratsiooni suurendamisel TAA-indutseeritud maksatoksilisuse korral rottidel. TAA-d kasutatakse traditsiooniliselt maksakahjustuse esilekutsumiseks eksperimentaalsetes loommudelites [15,35]. TAA toksiline toime tuleneb selle metaboliitidest nagu atseetamiid, sulfaat ja sulfoksiidist pärinevad komponendid. See metaboliit põhjustab struktuursete valkude ja ensüümide struktuurseid deformatsioone, mille tulemuseks on nende inaktiveerimine. Oma rolli tõttu muudab TAA metaboliit rakkude läbilaskvust, suurendab tuuma mahtu, kontsentreerib rakusisest kaltsiumi ja pärsib mitokondriaalset aktiivsust, mille tulemuseks on rakusurm. Selle metaboliidi tõttu on leukotrieenide kui maksarakkude poolt eritatava tugeva põletikulise vahendaja kahjustused [36].
Selles uuringus mõjutas ravi kitosaaniga maksaensüüme positiivselt. Vastupidiselt TAA mürgistuse ootustele näitasid seerumi ASAT, ALAT, ALP ja GGT aktiivsus TAA-ga ravitud rühmas normaalse kontrolliga võrreldes olulist suurenemist. Need tulemused on kooskõlas Baskarani jt. [37], Jain ja Singhai [38,39] Osama et al. [40], kes seostas seerumi transaminaaside aktiivsuse tõusu oksüdatiivse stressi ja lipiidide peroksüdatsiooniga, mis on tingitud TAA toksilisest toimest, kus vabade radikaalide toime kahjustab lipiide, valku ja DNA-d, mis põhjustab hepatotsellulaarset insuldi ja nekroos. Tavaliselt eraldavad nekrootilised rakud oma sisu vereringesse, mille tulemusena suureneb transaminaaside aktiivsus. Teisest küljest näitasid kitosaaniga töödeldud kaitsvad ja ravivad rühmad ALAT, ASAT, ALP ja GGT aktiivsuse selget allareguleerimist, mida võis seostada antioksüdantide, immunomodulatsiooni ja/või haavade paranemise ja kitosaani maksakaitsega [9]. Samamoodi vähenes seerumi albumiini tase TAA-ga mürgitatud rottidel valgusünteesi maksa düsfunktsiooni tõttu, mis oli tingitud hepatotsüütide endoplasmaatilise retikulumi ja mitokondritest. Kuid see tase reguleeriti üles ja normaliseeriti kitosaanraviga kas kaitsvates või ravivates rühmades.
TAA-mürgitus põhjustas neerufunktsiooni puudulikkust, kuna seerumi uurea ja kreatiniini tase tõusis; seda halvenemist on piinanud Begum et al. 41], kes teatas tubulaarsest vigastusest ägeda tubulaarse nekroosi korral, vastutab peamiselt glomerulaarfiltratsiooni vähenemise eest. Samuti soovitati, et kaasatud torukujulised kõrvalekalded on tuubulite ummistus, mis põhjustab glomerulaarfiltraadi tagasivoolu. Seega võivad TAA-ga ravitud rottide neerukahjustused olla tingitud ROS-i kahjulikest mõjudest. Kuid see tõus pöördus pärast kitosaanravi kas kaitsva või tervendava ravina. See tähelepanek on kooskõlas Mohamedi [42] tähelepanekuga, kes teatas, et kitosaani allaneelamine vähendas neerupuudulikkusega patsientidel oluliselt uurea ja kreatiniini taset ning omistas selle mõju ühele või kahele võimalikule mehhanismile: esimene neist on neerufunktsiooni aktiveerimine kliirensiks. lämmastiku metaboliit, mille tulemuseks on uurea ja kreatiniinisisalduse vähenemine, samas kui teine võimalus on, et kitosaan ühineb seedetraktis lämmastiku metaboliidiga ja seejärel eritub välja, mille tulemuseks on uurea ja kreatiniinisisalduse vähenemine.
Käesolevas uuringus vähendas TAA äge toksilisus kontrollrühmaga võrreldes oluliselt surviviini geeni ekspressiooni maksakoes. Kuid loomade söötmine kitosaaniga segatud põhitoiduga, ravimikontrollina ja kaitsva ravina enne TAA toksilisust, põhjustas surviviini geeniekspressioonitasemete mitteolulise tõusu. Surviviinil on rakutsükli G2/M faasis väljakujunenud funktsioon; rakkude jagunemise ajal kahjustab surviviin kromosomaalse reisijakompleksi subühikut [43, 44]. Surviviini ekspresseeritakse normaalsetes prolifereeruvates ja regenereeruvates kudedes ning teatati, et see pärsib apoptoosi ja aitab kaasa rakutsükli progresseerumisele [45]. Leiti, et surviviini ekspressioonil on positiivne seos hepatotsüütide arvuga taastuvas maksas. Seda võib seletada järeldusega, et surviviin osaleb mitoosi ajal õdekromatiidide eraldamises 46]; need faktid võivad tõlgendada siin surviviini geeniekspressiooni vähenemist TAA-järgse mürgistuse korral. Hagemann et al. [46] teatasid, et kui surviviini ekspressioon väheneb, katkeb kromosomaalsete reisijate kompleksi liikmete lokaliseerimine ja seetõttu on Aurur B aktiivsuse vähenemisega häiritud tsentromeersete sihtvalkude fosforüülimise ja tsütokineesi protsessid.
Varasemates närilistega tehtud uuringutes suurenes surviviini ekspressioon märkimisväärselt pärast osalist hepatektoomiat ja operatsioonijärgset operatsiooni. Lisaks leiti, et inimese maksa siirdamise korral suureneb surviviini ekspressioon transplantaadis. Nii närilistel kui ka inimestel on surviviini üleekspressioon seotud proliferatsiooniga, mitte apoptoosiga; järelikult on surviviin oluline hepatotsüütide proliferatsioonis ja mitoosis, mitte ainult regeneratsioonis, vaid ka normaalses arengus [46].
TAA-indutseeritud äge toksilisus ei mõjutanud märkimisväärselt c-myc geeni ekspressioonitaset maksakoes. Tõepoolest, kitosaanravi ravimite kontrolli, kaitsva või tervendava ravina reguleeris oluliselt ja dramaatiliselt c-myc geeniekspressiooni taset. Teatati, et normaalsete, transformeerimata rakkude arengu- ja mitogeensed signaalid reguleerivad c-myc ekspressiooni [47]. C-myc peamised rollid on rakkude proliferatsiooni suurendamine ja rakkude diferentseerumise takistamine. Leiti, et c-myc suurendab rakutsükli kulgu, reguleerides peale selle paljusid rakutsüklit kontrollivaid valke, nagu tsükliinid (D, E, A ja B1) ja tsükliinist sõltuvaid kinaase (CDK1.2. 4, 6). E2F transkriptsioonifaktorid. Teisest küljest leiti, et c-myc pärsib mitmel viisil rakutsükli blokaatorite, nagu p15, p21 ja p27, aktiivsust [48].
Kaalu vähenemine ja prolifereeruv raku tuuma antigeen on seotud c-myc valgu ekspressiooni vähenemisega maksa regenereerimise ajal. Lisaks vähenes oluliselt rakutsüklit reguleeriv valk p53 ja rakkude arv rakutsükli G2 faasis. Järelikult peetakse c-myc rakkude proliferatsiooni tugevaks positiivseks regulaatoriks. Lisaks leiti, et c-myc antisense piirab maksa regeneratsiooni rottidel [24,26].
Sarnaselt leiti, et neerukoes aktiveeriti c-mükgeen neerutuubulite rakkudes regeneratsiooni ajal ja pärast foolhappest põhjustatud neerukahjustust in vivo [49]. Samuti leiti, et C-myc soodustab valkude biosünteesi, kus valgusüntees oli c-myc üleekspresseerivates fibroblastides kolm korda suurem kui nende natiivsetes rakuliinides. C-myc avaldab seda toimet, reguleerides ribosoomi transkriptsiooni ja biogeneesi; samuti toimib c-myc koordineeritult tuuma RNA polümeraasidega (RNA pol I ja III), et reguleerida ribosoomi biogeneesi ja translatsiooni.

Lisaks stimuleeris c-myc ribosomaalse RNA transkriptsiooni, mis aktiveerib valgusünteesi [50].
Käesolevates uuringutes põhjustas TAA akuutne toksilisus TNF-geeni ekspressioonitasemete märkimisväärse tõusu maksakoes ja plasmatasemete tõusu, samas kui see tõus oli oluliselt allareguleeritud kitosaanravi korral nii kaitsva kui ka raviva ravina võrreldes TAA-ga. joobes grupp. See leid on kooskõlas Parki jt varasema tähelepanekuga. [51], kes teatasid kitosaani parandavast toimest TNF-i tasemele. Zhang et al. [52] teatasid, et ristseotud karboksümetüülkitosaan suurendas ravi alguses põletikuliste faktorite ensüümide aktiivsust; see aga taastab need pärast seda normaalsele tasemele. Nad viitasid ristseotud karboksümetüülkitosaani haavade paranemisele, kuna see vähendab rottide maksaensüümide aktiivsust.
TNF-i toodetakse neuronaalsetest rakkudest, fibroblastidest, lümfoidrakkudest, nuumrakkudest, endoteelirakkudest ja makrofaagidest. TNF- vahendab selle põletikueelset ja apoptootilist toimet koostoime kaudu nende membraaniretseptoritega (TNF-R1 ja TNF-R2). Mõlemad retseptorid vahendavad kahte erinevat signaalirada ja ühe aktiveerimisega kaasneb teise inaktiveerimine [51].
Meie tulemused viitavad kitosaani positiivsele rollile kudede regenereerimisel, mis on kooskõlas Shilpa jt. [53], kes leidsid, et osaliselt hepatektoomiaga rottide ravi kitosaani nanoosakeste ja gamma-aminovõihappega suurendas triitiumiga tümidiini omastamist võrreldes osaliselt hepatektomiseeritud rühmadega ilma nanoosakesteta. ravi. Kitosaani nanoosakeste töötlemise ja gamma-aminovõihappega töötlemise üldine tulemus on hepatotsüütide regeneratsiooni paranemine ja rakusurma vähenemine võrreldes maksa hepatektoomiaga rottidega. Praegused tulemused on samuti kooskõlas Cheni et al. [54], kes teatasid, et kitosaani nanoosakesed suurendasid ägeda maksapuudulikkuse all kannatavate rottide maksa taastumist. Kitosaani maatriksi sidumisvõime võimaldab makrofaagide kasvu ja aktiveerimist, mis on vajalik kudede regenereerimiseks. Kitosaaniga ravitud koeral tehtud haav paranes täielikult kolme nädala pärast. Kuid soolalahusega töödeldud kontrollrühmas kestab kõvenemisprotsess neli nädalat. Kitosaaniga töödeldud rühmas moodustus keratiinikiht sidekoe regeneratsiooni tõendina. Lisaks moodustati haava neovaskulatuuri kaitsmiseks kollageenkiudude võrgustik [55].
Käesolevas uuringus näitas histoloogiline leid maksakoe mustri halvenemist TAA rühmas; aga see muster paranes oluliselt kitosaani kaitsvas rühmas ja kuidagi ravivas kitosaani rühmas.
4. Järeldused
On jõutud järeldusele, et kitosaan võib TAA-indutseeritud maksatoksilisuse korral suurendada maksa regeneratsiooni kas raviva või proliferatiivse ainena. Lisaks näitas see põletikuvastast toimet, kuna see vähendas TNF-i taset nii geenide kui ka valgu tasemel. Seevastu kitosaan suurendas surviviini ja c-myc geeniekspressiooni, mis on rakkude proliferatsiooni võimendajad. Võib läbi viia täiendavaid uuringuid, et selgitada välja täpne mehhanism, mille abil kitosaan mõjutab c-myc, surviviini ja TNFC-geeni ekspressiooni. Sellest tulenevalt soovitatakse kitosaani kasutada maksahaiguste korral, kus on vaja kudede regenereerimist.
