Neeruvahetusprogrammide andme- ja optimeerimisnõuded
Mar 09, 2022
Abstraktne
Neeruvahetusprogrammid (KEP) on väärtuslikud vahendid elusdoonori võimaluste suurendamiseksneeru siirdaminelõppstaadiumiga patsientideleneeruhaigusimmunoloogiliselt kokkusobimatu elusdoonoriga. KEP-i eeliste maksimeerimiseks on vaja infosüsteemi andmete haldamiseks ja siirdamise optimeerimiseks. Veregruppide ja inimese leukotsüütide antigeenide (HLA) tüüpide ja HLA antikehade põhiteabega seotud süsteemide andmesisendi spetsifikatsioonid on üliolulised, et maksimeerida tuvastatud sobitatud paaride arvu, minimeerides samas ootamatust positiivsest ristist tingitud sobitustõrgete riski. tikud. Põhineb kaheksa riikliku ja ühe rahvusvahelise küsitluselneerudvahetusprogrammi, arutame andmenõudeid KEP-i käitamiseks. Märkame suuri erinevusi erinevate KEP-ide salvestatud andmetes, mis peegeldavad erinevaid meditsiinipraktikaid. Lisaks kirjeldame, kuidas infosüsteem toetab otsuste tegemist kõigis nendesneerudvahetusprogrammid.
Sissejuhatus
Elusdoonorneeru siirdamine (LDKT) on lõppstaadiumis patsientide eelistatud raviviisneeruhaigus(ESKD). LDKT on seotud surnutega võrreldes parema pikaajalise retsipientide ja transplantaadi ellujäämiseganeeruddoonorid.1,2 Kahjuks on kuni 50 protsendil muidu sobivatest potentsiaalsetest elusdoonori/retsipiendi paaridest LDKT peamiseks takistuseks ABO veregruppide kokkusobimatus või inimese leukotsüütide antigeeni (HLA) sensibiliseerimine doonori ja retsipiendi vahel.3 Üks strateegia, mida ületada. HLA ja ABO kokkusobimatus on läbi aNeerVahetusprogramm (KEP). Lihtsamal juhul arvestavad KEP-id kokkusobimatute retsipientide ja doonorite paare. Kaks paari sobitatakse, kui mõlemad doonorid ühilduvad teise paari retsipiendiga. Nii saavad LDKT-d mõlemad retsipiendid.4,5 Võimalikud on ka keerukamad skeemid, sealhulgas pikemad annetustsüklid, mittesihitud annetajad jne.6 KEP-id on loodud paljudes riikides ja need võimaldavad edukalt teha suurel hulgal täiendavaid LDKT-sid.6 Nende KEP-ide edu saavutamiseks on paljud riigid oma KEP-i loomise algusjärgus.7 See on väljakutseid pakkuv ettevõtmine, mida saab teha lihtsamaks, kui õppida väljakujunenud KEP-idest. Teadus- ja tehnoloogiaalase koostöö fondi (COST) kaudu rahastab Euroopa Liit KEPi alast koostööd ja vastastikust õppimist, eelkõige Euroopa KEP-ide koostöövõrgustiku COST tegevuse (ENCKEP) kaudu. Selle töö eesmärk on anda selge ülevaade andmenõuetest ja optimeerimissüsteemist, mida on vaja KEP-i sobitustegevuste nõuetekohaseks haldamiseks. Paber on korraldatud järgmiselt. Järgmises kahes osas anname võhiku kirjelduse immunoloogilise ühilduvuse kohta, kuna see on teatud andmeelementide tähtsuse mõistmiseks ülioluline. Neljandas jaotises käsitleme KEP-i käitamiseks vajalikke andmeelemente. Optimeerimisprotsess, mis on seotud neerud vahetusprogramme kirjeldatakse viiendas osas. Viimane osa sisaldab järeldusi.
Märksõnad:Neeruvahetusprogrammid, andmenõuded, infosÜSTEEMID, neeruhaigused, neeruvahetus

CISTANCHE PARANDAB NEERU-/NEERUHAIGUST
Immunoloogilise ühilduvuse veregruppide ja kudede tüpiseerimise määrajadImmunoloogiline siiriku ja retsipiendi ühilduvus aneeru siirdaminekandidaat (=retsipient) ja doonor sõltuvad peamiselt doonori veregrupist ja HLA koetüübist ning retsipiendi veregrupi ja HLA koe vastastest antikehadest. Veregrupp on esimene element, mida tuleb ühilduvuse hindamisel arvesse võtta. Selle määrab antigeenide A ja B olemasolu või puudumine. Nende antigeenide kombinatsioonid määratlevad neli põhilist veretüüpi O, A, B ja AB. AB-veregrupiga inimese rakud sisaldavad nii A- kui ka B-antigeene. Kuigi O-veregrupi puhul ei esine kumbagi neist kahest. Isikud toodavad antikehi A või B vastu, kui nad ise selliseid antigeene ei ekspresseeri. ABO antikehad seerumis moodustuvad varases eas; nende tootmist stimuleeritakse, kui immuunsüsteem puutub kokku toidus või mikroorganismides "puuduvate" ABO veregrupi antigeenidega. Doonor võib üldjuhul annetada aneerudretsipiendile ainult siis, kui viimasel puuduvad doonori antigeenide vastased antikehad. Sellegipoolest ei ole veregrupispetsiifiliste antikehade (ABO-ab) tase kõigil retsipientidel sama. Mõned retsipiendid võivad läbida siirdamiseelse ABO-ab eemaldamise protseduuri, mis võimaldab siirdada siiriku doonorilt, kellel on muidu kokkusobimatu veregrupp. Mõnel juhul on ABO-ab tiiter piisavalt madal, et võimaldada siirdamist läbi veregrupi barjääri ilma antikehade eemaldamiseta.8 Seetõttu võivad retsipiendi andmed sisaldada lisaks tema enda veregrupile ka teavet vastuvõetava veregrupi kohta. veregrupid, mis on võrdne ühega järgmistest komplektidest: {{A}, {B}, {A pluss B}}. See määratleb selgesõnaliselt siiriku veregrupi aktsepteerimise, mis võib olla kaudselt aktsepteeritud veregruppide superkomplekt, mis põhineb retsipiendi enda veregrupil, nagu eespool kirjeldatud. Kui siirik ei ühildu ABO-ga konkreetse retsipiendiga, kuid on ühe selgesõnaliselt aktsepteeritud veregrupiga, nimetatakse seda ABO-ga mitteühilduvaks vasteks (või ABOi vasteks).
Lisaks veregrupi mittesobivusele võivad doonori-retsipiendi paarid olla ka koetüübiga kokkusobimatud, kui retsipiendil on tekkinud antikehad vähemalt ühe doonorkoe tüüpi iseloomustava antigeeni (doonori-spetsiifilised antikehad ehk DSA) vastu. Kudetüüpide ühilduvus on seotud inimese leukotsüütide antigeenidega (HLA). HLA antigeenide tuvastamist nimetatakse HLA tüpiseerimiseks. Tippimine toimub nii doonori kui ka retsipiendi jaoks. Kõige asjakohasemad HLA antigeenidneeru siirdamineon HLA-A, B, C (I klassi antigeenid) ja HLA-DRB1, DRB3/4/5, DQA1, DQB1, DPA1, DPB1 (II klassi antigeenid). I klassi antigeene ekspresseeritakse praktiliselt kõigil somaatilistel rakkudel, sealhulgas endoteelil, samuti B- ja T-lümfotsüütidel, samas kui II klassi antigeenide ekspressioon piirdub B-lümfotsüütide, antigeeni esitlevate rakkudega (monotsüüdid, makrofaagid ja dendriitrakud) ja aktiveeritud T-lümfotsüüdid. Erinevalt ABO antikehadest puuduvad HLA antikehad tavaliselt normaalsetel inimestel. Antikehade tootmine põhineb immuunsüsteemil, mis on varem puutunud kokku võõrantigeenidega (allosensibiliseerimine). Allosensibilisatsioon tekib tavaliselt naistel raseduse, vereülekande või varasemate elundite siirdamise tõttu. Kui siiriku antigeenidele suunatud antikehade tase on liiga kõrge, lükkab retsipiendi immuunsüsteem siiriku tõenäoliselt tagasi. Äratõukereaktsiooni tõenäosust saab enne elundisiirdamist testida niinimetatud ristsobivuse testiga. Ristsobitamine hõlmab retsipientseerumi (mis võib sisaldada doonorispetsiifilisi anti-HLA antikehi) asetamist doonori lümfotsüütidele. Tsütotoksiline reaktsioon (mida peetakse positiivseks) viitab eelnevalt moodustunud DSAb-de olemasolule, mis näitab kokkusobimatust. Virtuaalne ristsobivus on HLA antikehade tuvastamise analüüside tulemuste hindamise protsess, et ennustada füüsilise ristsobivuse tulemusi.
KEP-i histo-ühilduvuse testimise nõudedHLA tüpiseerimise eesmärk on tuvastada, millised nende antigeenide variandid doonoril ja retsipiendil on. Ajalooliselt oli seroloogiapõhine HLA tüpiseerimine, mis pakub madala eraldusvõimega HLA tüpiseerimist, surnud doonori tahke elundi siirdamise toetamise kuldstandardiks. Siiski võib mitmel alleelil (geenide variandil) olla sama seroloogiline spetsiifilisus, kuid need kutsuvad esile siiski erineva antikehavastuse. Kaasaegsed DNA-põhised tüpiseerimismeetodid suudavad eristada üksikuid alleele (geenide variante)9 ja võimaldavad HLA tüpiseerimist kõrge eraldusvõimega.10 HLA tüpiseerimine on üldiselt mõeldud alleelide kodeerivate piirkondade erinevuste, st DNA järjestuste variatsioonide määratlemiseks. mille tulemuseks on muutused valgu aminohappejärjestuses (HLA antigeen). Erinevused HLA alleelides tuvastavad aminohappejääkide variatsioonid antikehadele ligipääsetavates järjestuste positsioonides HLA molekuli molekuli pinnal ja seega erineva antigeensuse. HLA tähistuste üksikasjaliku kirjelduse jaoks viitame Marshile et al.11. Ühendkuningriigi riikliku tervishoiuteenistuse madala ja kõrge eraldusvõimega HLA üksikasjaliku klassifikatsiooni leiate NHS-ist.12 Antikehade testimine toimub ainult retsipientidel. HLA antikehad tuvastatakse mitme analüüdi profileerimise (Luminex) meetodi abil, mis tuvastab seerumis olevate antikehade reaktsiooni teatud antigeenidega, mis paiknevad helmestel. Selle reaktsiooni tugevust hinnatakse poolkvantitatiivselt MFI-ga (keskmine fluorestsentsi intensiivsus) iga bead'i jaoks. Eelnevalt kindlaksmääratud piirväärtuste põhjal kasutatakse MFI-d sageli asendusena, et teha kindlaks, kas antigeenid on vastuvõetamatud. Arutluseks viitame Sullivanile jt13.

CISTANCHE PARANDAB neeru-/NEerupuudulikkust
Paneelreaktiivsete antikehade (PRA) klassifikatsioon ja arvutatud PRA (cPRA)Mõnedneeru siirdaminekandidaatidel on antikehi doonori HLA koe antigeenide vastu ka sensibiliseerimise tõttu. Patsientide allosensibilisatsiooni taset hinnatakse mõõtmise abil, mida nimetatakse paneelreaktiivseks antikehaks (PRA). PRA arvutatakse tsütotoksilisuse meetodil põhineva ristsobivuse tulemusest. Testides patsiendi seerumit doonorlümfotsüütide paneeli suhtes, on PRA positiivse ristsobivuse protsent testitud doonorite koguarvust. Mida kõrgem on PRA skoor, seda tõenäolisemalt on retsipient juhusliku siirikuga kokkusobimatu. Hiljuti võeti kasutusele arvutatud PRA (cPRA) kontseptsioon, et ületada mõned traditsioonilise PRA mõõtmise nõrkused ja paremini kasutada tahkefaasitehnoloogia abil toodetud tundlikumaid andmeid. cPRA on määratletud kui doonorite protsent, kellel on eeldatavasti kandidaadile vastuvõetamatud HLA antigeenid. See lähenemisviis hõlmab doonori HLA fenotüüpide proovi kogumist ja iga patsiendi kokkusobimatute doonorite protsendi otsest jälgimist nende vastuvõetamatute antigeenide alusel. Seejärel arvutatakse antigeeniprofiilide suurte andmebaaside põhjal välja cPRA skoor.14,15 cPRA skoori alusel saab retsipiendi klassifitseerida kõrge, keskmise või madala koetundlikkuse tasemega.
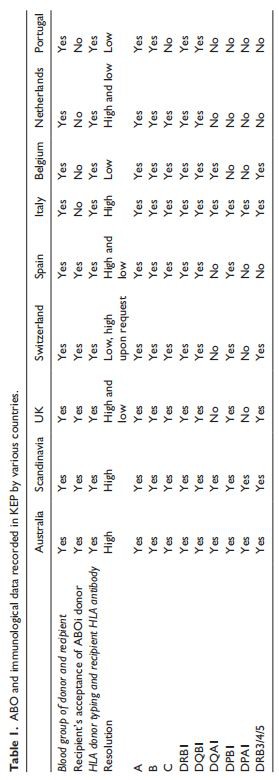
Andmenõuded KEP-idele Hindasime ENCKEP COST Actionis osalevatele riikidele esitatud küsimustiku vastuseid nende KEP-ides salvestatud ja kasutatud andmete kohta, et töötada välja ettepanek riiklike KEP-registrite andmekogumi nõuete kohta (tabel 1). Selle küsimustiku küsimused leiate lisast. Nende küsimustike abil tuvastati peamised andmeelemendid ja nende seosed. Kõige üksikasjalikum vastus saadi Ühendkuningriigist üksuste ja suhete diagrammi kujul, mis on näidatud joonisel 1. Selles jaotises käsitleme neid ja teiste riikide esitatud andmeelemente. Nagu ülalpool kirjeldatud, on retsipiendi ja doonori ABO ja immunoloogilised omadused peamised tegurid nende (mitte)sobivuse määramisel. Täpset ja üksikasjalikku teavet nende omaduste kohta saab kasutada esialgsete mittesobivuste tuvastamiseks, ilma et oleks vaja teha ristsobivustesti. Registreeritud ABO ja immunoloogilised andmed on riigiti erinevad (tabel 1). Need erinevused peegeldavad osaliselt erinevaid meditsiinilisi eelistusi ja ka praktilisi piiranguid.
Isiklik informatsioon Isikuandmed on vajalikud doonorite ja retsipientide ühemõtteliseks tuvastamiseks. Doonorite ja retsipientide minimaalne isikuandmete kogum peaks sisaldama identifitseerimisnumbrit, nime, sugu, sünnikuupäeva, suunavat haiglat, kavandatava doonori ja retsipiendi vahelist suhet ning nende elukohta.
Doonori veregrupi ja HLA andmed Soovitatud andmedkõigi doonorite puhul registreeritakse veregrupp ja HLA tüpiseerimine. Doonori veregruppide osas on soovitatav A-veregrupi doonori alatüüpide määramine juhul, kui KEP-is on arvesse võetud ABO-ga mitteühilduvaid siirdamisi.16 O-retsipientide puhul on A2-veregrupi doonorid vastuvõetavad, olenevalt anti-A tiitrist, kuid A1-doonorid tavaliselt mitte. . HLA-antigeenide registreerimiseks vajaliku minimaalse andmekogumi osas on vastajate vahel märkimisväärne varieeruvus. Kõrge eraldusvõimega HLA tüpiseerimise lisamine vähendab positiivsete ristsobivuste tõenäosust. Praktikas registreerivad Austraalia ja Skandinaavia eranditult kõrge eraldusvõimega HLA-tüüpi sisestamist, Belgias ja Portugalis aga eranditult madalat tippimist. Hispaania lubab mõlemat eraldusvõimet mahutada HLA laboritesse, millel pole kõrget eraldusvõimet. Ühendkuningriigis teatab enamik keskusi kõrge eraldusvõimega, kuid seejärel muudetakse need madalaks, et selgitada välja HLA-ühilduvus. See eeldab, et andmebaas suudab käsitleda mõlemat tüüpi andmeid. Samuti on suur varieeruvus selles, millised HLA-antigeenid registreeritakse (tabel 1). Kõik vastajad registreerivad HLA-A, B, DRB1 ja DQB1. Enamik salvestab ka HLA-C, DRB3/4/5 ja DPB1. Ainult Skandinaavia ja Austraalia KEP salvestab kõik HLA-tüübid (sh DQA1, DPA1).

Retsipiendi veregrupi ja HLA andmedIga vastaja märkis, et retsipientide veregrupp ja HLA antikehade profiil peavad olema registreeritud. KPI-d registreerivad tavaliselt retsipiendi anti-HLA antikehad. Iga spetsiifilisuse jaoks salvestatakse Luminexi tehnikaga MFI väärtused. Kuna antikehade tase võib aja jooksul muutuda, on vaja regulaarset testimist. Praktikas varieeruvad kordustestide intervallid 3 kuust 1 aastani. Potentsiaalselt sensibiliseerivad sündmused nõuavad antikehade taseme värskendamist. Mõned KEP-id pakuvad võimalust loetleda selgesõnaliselt vastuvõetamatud HLA doonorantigeenid, isegi kui retsipiendil pole selle konkreetse antigeeni vastu antikehi. Näiteks Austraalia programmis kasutatakse seda doonori HLA keelamiseks, millel on suur siirdamisjärgse antikehade tekke oht, ja seda kasutatakse spetsiaalselt selleks, et pakkuda KEP-is ühilduvate paaride jaoks paremaid vasteid.19 Kõik programmid kasutavad cPRA-d, et teatada antikehade tasemest. Retsipiendi HLA sensibiliseerimine. cPRA tuleks arvutada standardse valemiga, mis kajastab doonoripopulatsiooni KEP piirkonnas. Riikidevahelise teabe ühtlustamiseks saab kasutada riikidevaheliste organisatsioonide, nagu Eurotransplant või Scandiatransplant, kalkulaatoreid. Lisaks peaksid retsipientide veregrupid ja HLA koetüübid olema dokumenteeritud. Enamik vastajaid lubab oma KEP-is ainult ABO-ga ühilduvat siirdamist; seega määrab retsipiendi veregrupp vastuvõetava doonori veregrupi. Austraalia, Hispaania ja Ühendkuningriigi programmid võimaldavad madala riskiga ABOi siirdamist KEP-i kaudu. See tava nõuab vastuvõetavate veregruppide selgesõnalist registreerimist. Kuna KEP-i sobitamise puhul tuleb eelkõige vältida retsipientide sidumist HLA antikehadega, mis on suunatud potentsiaalsetes doonorites esinevate HLA antigeenide vastu, on retsipientide HLA tüpiseerimisel vähe kaalu. Seetõttu ei nõua retsipient-HLA-antigeeni rekord tingimata samal tasemel HLA tüpiseerimist, mida doonoritelt nõutakse. Kui kaalutakse ühilduvate paaride kaasamist, tuleks ka adressaatidele HLA tippida kõrge eraldusvõimega. Lõpuks tuleks registreerida positiivse rakupõhise ristsobivuse põhjus retsipiendi ja doonori vahel, mis on tuvastatud virtuaalse ristsobivuse abil, et vältida tulevikus sama põhjuse tõttu kokkulangevust.16
Kliiniline teaveKuna kliiniline teave ESKD olukorra kohta võib mõjutada retsipientide prioriteetsust, on oluline registreerida dialüüsravi aeg ja tüüp, nagu on teatanud Holland. Lisaks tuleks registreerida doonorite ja retsipientide tsütomegaloviiruse (CMV) seroloogiline seisund. See teave on oluline, kuna profülaktilist viirusevastast ravi kasutatakse näiteks CMV ja doonori siirdamisel CMV-retsipientidele. Samuti on soovitav B- ja C-hepatiidi doonorite staatus ning märge selle kohta, kas B-hepatiidi põhiantikehade suhtes positiivsed doonorid on retsipientidele vastuvõetavad.6 Kliiniline teave doonori ja retsipiendi anatoomia kohta võib mõne retsipiendi jaoks (eriti nende jaoks, kes ootavad ravi). teine või kolmas siirdamine). Jaotamise reeglid tagavad, et retsipiente ei sobitata kokkusobimatute doonoriteganeerudanatoomia. Soovitatavad andmed, mis adressaadi jaoks salvestatakse, on lahkumise vajadusneerudainult üks arter, üks veen ja pikk veen. Soovitatavad andmed doonori kohta salvestamiseks on millisedneerudsaab annetada, kahe arteri olemasolu ja veeni pikkus paremaleneerud. Sellise teabe algusest peale arvesse võtmine vähendab pärast doonorite ja retsipientide kokkulangemist meditsiinilistel põhjustel tühistatud siirdamiste arvu.20 Mõned muud piirangud, mis on seotud annetatavaga.neerudmuuta need sobimatuks kõigile retsipientidele (tsüstid, kusejuha anatoomia). Selliseid doonoreid ei tohiks KEP-i vastu võtta ja neid tuleks reguleerida vastuvõtupoliitikaga, mitte jaotamise reeglitega (nt Melcher et al.21).
Doonor ja retsipient KEP-i kõige põhilisemas vormis on üks retsipient seotud ühe doonoriga, nagu väitis enamik meie vastajaid. Siiski on võimalikud keerulisemad suhted. Näiteks võib KEP-iga liituda rohkem kui üks doonor, mis on seotud ühe retsipiendiga, või võime kaaluda mittesihitud doonoreid. Retsipiendi ja doonori andmete korraldamise paindlik vorm, mis võimaldab neid juhtumeid, on arvestada eraldi retsipientide ja doonoriandmete struktuuridega. Nii retsipient- kui ka doonorstruktuuride jaoks on olemas andmeelement. See andmeelement näitab mis tahes seoseid vastavalt doonorite ja retsipientidega andmebaasis. Näiteks Ühendkuningriik teatas sellise süsteemi kasutamisest.

CISTANCHE PARANDAB NEeru-/NEERUNEKTSIOONI
Konsensus minimaalsete andmekogumite osasMärgime, et eri riikide registreeritud immunoloogilised andmed on väga erinevad (vt tabel 1). Sellised erinevused peegeldavad tavaliselt erinevaid meditsiinipraktikaid. Näiteks riigid, mis lubavad oma KEP-i kaudu ABO-ga mitteühilduvaid siirdamist, nõuavad lisaandmeid, et teha kindlaks, millised ABO-ga mitteühilduvad siirdamised on teostatavad. Sel põhjusel leiame vähe üksmeelt KEP-i käitamiseks nõutava „minimaalse” andmestiku osas, kuna mõnede riikide jaoks oluliseks peetavaid andmeid teised ei salvesta. Märgime, et aja jooksul suurenevad KEP-ide andmenõuded, kuna kaasatakse täiendavaid siirdamisviise. Täiendavate andmeelementide lisamine andmekogumisse võib aga olla aeganõudev protsess, kuna tarkvara tuleb kohandada ja testida. Sel põhjusel soovitame andmebaaside ja nendega seotud süsteemide kujundamisel võtta arvesse võimalikult palju andmeelemente, isegi kui need ei ole praeguste KEP-tavade jaoks veel asjakohased. Nii takistavad võimalikud hilisemad muudatused meditsiinipoliitikas kõige vähem varasemad valikud.
KEP-ide optimeerimisnõudedKEP-i sees siirdamise korraldamine hõlmab paljusid etappe. Esiteks sisestatakse süsteemi meditsiinilised ja immunoloogilised andmed. Seejärel sõelutakse neid andmeid optimeerimismudeli koostamiseks, et otsustada, millised siirdamised kavandatakse. Järgmisena lahendatakse see mudel ja saadud kavandatud siirdamistest tehakse ristsobivustest. Sõltuvalt KEP-ist võib seejärel järgneda abinõu. Lõpuks on programmi hindamiseks vajalik aruandlus. Selles jaotises kirjeldame esmalt üksikasjalikult KEP-i tehnoloogilisi osi, mis puudutavad paljusid või kõiki faase, enne kui läheme üksikasjalikumalt mõnda üksikut etappi.
Kasutajad, kasutajaliides ja andmevormingud Kasutaja autentimist tuleks hallata võrguteenuste praeguste parimate tavade kohaselt. KEP-is võivad olla kolm erinevat rolli: arst, kudede tüpiseerimise teadlane ja administraator. Iga doonori-retsipiendi paari saab hallata oma arst, kes peaks saama vaadata ja värskendada kõiki doonori või retsipiendi jaoks olulisi meditsiinilisi üksikasju. Arstil peaks olema ka võimalus vaadata retsipiendile määratud doonori omadusi. Kudede tüpiseerimisega tegelevatel teadlastel peaks olema privilegeeritud juurdepääs doonori ja retsipiendi veregrupi ja HLA andmete sisestamiseks ja värskendamiseks. Administraatorid, kes on programmi haldav keskasutus, peaksid suutma käitada ja hinnata sobivaid käitamisi. Muud võimalikud rollid hõlmavad süsteemi administraatori/arendaja rolle süsteemi või tarkvara hooldamiseks. Sellistele kasutajatele saab piirata juurdepääsu tegelikele andmetele, kuid selle asemel pääsevad nad juurde testandmete komplektile, et kontrollida kõigi komponentide funktsionaalsust. Enamik praeguseid KEP-e pakub kasutajatele veebiliidest. See esitab kasutajale praegused andmed ja pakub lihtsat meetodit uute andmete värskendamiseks või lisamiseks. Kasutajaliides võib sisaldada ka andmete terviklikkuse valikuid ja pakkuda administraatoritele võimalusi teatud parameetrite muutmiseks modelleerimis- ja lahendamisefaasis, näiteks maksimaalne tsükkel või ahela pikkus. Andmefailide ja levinud andmevormingute kasutamine võib hõlbustada koostööd erinevate KEP-ide vahel. Ühtset andmevormingut kasutades saaksid ühe KEP-i jaoks välja töötatud tarkvara vajaduse korral hõlpsamini üle võtta ka teised. Levinud andmevormingud pakuvad ka meetodeid andmete arhiveerimiseks KEP-i erinevates etappides tulevaseks valideerimiseks või analüüsiks. Enamik olemasolevaid KEP-e kasutab sellistel eesmärkidel kas XML-i või JSON-i.
Koostoimed teiste süsteemidegaKEP võib suhelda surnud doonorisüsteemidega, kuna siirdamise kandidaat võib olla samaaegselt kantud KEP-i ja surnud doonori ootenimekirja registrisse. Kõige sagedamini siis, kui retsipiendile määratakse doonorneerudelusdoonorluse süsteemi kaudu peatatakse nad ajutiselt surnud doonorsüsteemist. Surnud doonori ootenimekirjast eemaldamine on KEP-is ülioluline, et vältida mängujärgset ahela katkemist. Viimased edusammudneerudvahetus suurendab vajadust süsteemidevahelise suhtluse järele. Surnud doonorite 21,22 algatatud ahelad suurendavad surnud ja surnute vahelist suhtlustneerudvahetussüsteemid. Lisaks tuleks seoses kasvava rahvusvahelise koostööga KEP-ide vallas23,24 kaaluda ja käsitleda ka ülalmainitud probleeme. Teatud andmeid (nt HLA tüpiseerimine) on võimalik sisestada otse diagnostikaseadmetest ja kui sellised funktsioonid on saadaval, on oluline kontrollida, kas seadmed ja andmebaas suudavad suhelda.
Andmebaas ja alternatiivsed andmeallikadAndmed tuleb salvestada usaldusväärsesse andmebaasi ja varundada vastavalt. Juurdepääsu erinevat tüüpi teabele tuleks juhtida kasutajataseme juhtelementidega. Õigete andmete süsteemis salvestamise tagamiseks võib andmebaas nõuda andmete sisestamise kontrollimist, kui andmete käsitsi sisestamine on vajalik. Näiteks nõuavad mitmed KEP-id, et teatud andmete värskendusi peab kontrollima sõltumatu kasutaja. Sellised protseduurid vähendavad transkriptsioonivigade riski. Andmebaasile juurdepääsu ja muudatuste jälgimine võib samuti tagada andmete terviklikkuse. Suurt osa KEP-i jaoks nõutavatest andmetest nõuavad ka seotud programmid (nt surnud doonori programmid), nii et ressursikulude vähendamiseks ja väljajätmisvigade vältimiseks võib KEP jagada selliste programmide vahel ühist andmebaasi või sisestada süsteemid. tagamaks, et kõik sellised andmebaasid üksteist pidevalt uuendaksid. Enamik meie vastajatest teatas, et andmed on kopeeritud surnud doonoriprogrammist (nt Holland) või rohkem integreeritud süsteemidest, kus KEP kasutab sama andmebaasi (Scandiatransplant, Ühendkuningriik).
Modelleerimine ja lahendamineOptimeerimisprotsess hõlmab kolme etappi: andmete sõelumine, modelleerimine ja lahendamine. Esimeses etapis määratakse retsipientide ja doonorite esialgne ühilduvus virtuaalse ristsobitamise teel, et koostada ühilduvusgraafik. Modelleerimine on tihedalt seotud lahendusmeetodiga. Praegused KEP-id kasutavad ühte kolmest paradigmast: täielik loendamine, heuristika ja täisarvuline programmeerimine. Igal juhul sõnastatakse probleem ja leitakse lahendus.25,26 Modelleerimine võtab esmalt andmed andmebaasist ja arvutab ühilduvusinfo. Sageli esitatakse see tulemus ühilduvusgraafiku kujul: graafik, kus iga tipp tähistab retsipienti ja nende doonorit ning kaalutud servad näitavad doonori ja retsipiendi ühilduvust. Need kaalud arvutatakse doonorite ja retsipientide atribuutide põhjal ning võivad kajastada näiteks retsipiendi prioriteetsuse taset, mis põhinevad ooteajal ja sensibiliseerimise tasemel. Iga doonorit ja retsipienti saab esindada anonüümse identifikaatoriga, kusjuures igaühega on seotud vaid minimaalne nõutavate andmete kogum.25 Kui sobivuskäik on modelleeritud, tuleb see lahendada. See on protsess, mille käigus määratakse optimaalne lahendus, mis hõlmab vahetuste komplekti. Lahendaja sisend sisaldab (kuid mitte ainult) ühilduvusgraafikut. Mudeli lahendamise viise on palju ja mudeli tegelik rakendamine on sageli tugevalt seotud lahendaja valikuga. Lihtsaim meetod on ammendav otsing – otsing, mis leiab kõik võimalused ja loetleb need eelistuste kahanevas järjekorras. Selliseid meetodeid on sageli lihtne rakendada ega vaja väliseid teeke. Kuna kõik võimalikud lahendused on loetletud, siis kui hiljem avastatakse positiivne ristsobivus, on lihtne alustada järgmise parima lahenduse testimist. Suuremates KEP-ides on sellised meetodid aga hädas. Suuremad KEP-id kasutavad üldiselt spetsiaalseid lahendajapakette – kolmanda osapoole tarkvarapakette, mis kasutavad erinevaid spetsialiseeritud tehnikaid, et leida garanteeritud parim lahendus. Selliseid lahendajaid on nii tasuta kui ka kommertsvariantidena.27–30 Kaasaegsel riistvaral saab kuni 200 sobivalt modelleeritud doonor-retsipiendi paariga sobitamise lahendada vähem kui minutiga, kasutades tasuta lahendajaid (vt Mak-Hau26 ja Dickerson et al.31). Kaubanduslikud lahendajad pakuvad suurepärast jõudlust rahalise kuluga, kui seda vajatakse suuremate programmide jaoks.

CISTANCHE PARANDAB NEERU/NEERU FUNKTSIOONI
Lõplik ristmäng ja siirdamisedÜhilduvuse graafik põhineb üldiselt immunoloogilise ühilduvuse esialgsel hinnangul. Kui aga lahendus on välja pakutud, tehakse siirdamiseks valitud paaride puhul tavaliselt laboratoorsed ristsobitused. See võib paljastada ootamatud sobimatused ja takistada tuvastatud paaridega seotud siirdamist. Positiivsete ristsobivuste riski saab vähendada näiteks DQA ja DPA antikehade testimisega,17 kuid ükski süsteem ei saa garanteerida positiivsete ristvastavuste nulli. Erinevatel KEP-idel võivad olla erinevad meetodid nende positiivsete ristvastavuste lahendamiseks. Iga positiivne ristsobivus tühistab tsükli või ahela, kuhu see kuulub. Mõned KEP-id säilitavad ammendava loetelu kõigist lahendustest või võimaldavad lahendusi kiiresti ümber arvutada. Selle tulemusel saavad nad parimaid lahendusi iteratiivselt testida, kuni tuvastavad ühe ilma positiivsete ristvasteta. Sellist lähenemist on suuremates KEP-ides keeruline rakendada ristsobivuse testimise korralduslike väljakutsete tõttu. Enamik KEP-e ei püüa leida uuendatud ühilduvusgraafikult uut lahendust. Positiivsete ristmängude tagajärgede vähendamiseks võivad KEP-id kasutada mõningaid reegleid, mis näevad ette ebaõnnestumise võimalust.25
AruandlusMitmed aruanded võivad anda kasulikku teavet KEP-i pikaajalise tõhususe ja tõhususe kohta. Need peaksid hõlmama, kuid mitte ainult, tuvastatud vastete arvu ja ka siirdamisele minevaid vasteid; cPRA tasemed retsipientide kogumis ja neile eraldatud aneerud; adressaatide jagamise sobivuse tõenäosus aneerud; siirdamiste arv iga veregrupi sees ja iga veregrupi paari vahel ning dialüüsi ooteaeg ja iga retsipiendi KEP-programmi ooteaeg.neerud.32
Järeldused
ENCKEP COST-i meetmega seotud KEP-ide seas tehtud küsitluste põhjal leidsime andmenõuete osas piiratud konsensuse. Kõikidel riikidel on ühine tuum, sealhulgas doonori ja retsipientide identifitseerimine, veregrupp ja teatud HLA teave (A, B, DRB1, DQB1), kuigi küpsed KEP-id näitavad, et doonor-retsipiendi paaride laiendatud teise välja kõrge eraldusvõimega tüpiseerimine kõigis riikides. HLA lookused on olulised DSA õigeks hindamiseks. Lisaks sellele tuumikule põhjustavad erinevates KEP-ides kasutatavad erinevad meditsiinitavad erinevad andmevajadused. Mõned riigid teatavad, et nad suurendavad programmi küpsedes salvestatavaid andmeid. Lisaks nõuab täiendavate siirdamisviiside (ABOi, ühilduvad paarid jne) kaasamine täiendavaid andmeid. Sel põhjusel soovitame kaasata võimalikult palju andmeelemente, et tulla toime kasvava andmevajadusega, kui meditsiinipraktika programmis muutub. Lisaks võimaldab suurem andmete kättesaadavus lihtsamaks rahvusvaheliseks koostööks riikidega, kelle programmid seda teavet nõuavad. Infosüsteemide üldine struktuur on KEP-ide lõikes sarnane. Tavaliselt hõlmab see meditsiiniliselt oluliste andmete kogumist ja seejärel nende muutmist mudeliks, mille lahendust kasutatakse doonorite ja retsipientide sobitamiseks KEP-is, et tuvastada võimalikud siirdamised. Lisaks on neil süsteemidel sageli võimalused määratud vastete tõrgetega toimetulemiseks.
