Hüpoksiast indutseeritava faktori eristav jaotus-1 kultiveeritud neerutuubulirakkudes hüpoperfusiooniga, mida simuleeritakse katteklapi paigutusega
Mar 27, 2022
Kontakt: Audrey Hu Whatsapp/hp: 0086 13880143964 E-post:audrey.hu@wecistanche.com
Tomoko Honda1| Yosuke Hirakawa1 | Kiichi Mizukami2| Toshitada Yoshihara2| Tetsuhiro Tanaka1| Seiji Tobita2| Masaomi Nangaku
Abstraktne
Krooniline hüpoksia neerutuubulointerstitiumis mängib kroonilise haiguse progresseerumisel võtmerolli.neerudhaigus(CKD). Seetõttu on oluline uurida tubulaarset hüpoksiat ja hüpoksiaga indutseeritava faktori (HIF) -1 aktiivsust vastusena hüpoksiale. Peritubulaarse kapillaari harvem põhjustab kroonilise neeruhaiguse korral hüpoperfusiooni; hüpoperfusiooni mõju HIF-idele on siiski harva uuritud. Me kutsusime esile hüpoperfusiooni, mille põhjustas inimese katteklaasi asetamineneerud-2 rakku ja täheldas katteklaasi all hapnikugradienti. HIF-1 immunotsütokeemia näitas pimonidasool-positiivse piirkonna serval sõõrikukujulist moodustist, mille nimetasime "HIF-rõngaks". HIF-rõnga hapnikupinge oli hinnanguliselt vahemikus umbes 4 mmHg kuni 20 mmHg. See tulemus ei ühildunud varasemate uuringute tulemustega, mis näitasid HIF-1 akumuleerumist anoksilises vahemikus koos homogeense hapniku pingega. Lisaks täheldasime pH gradiendi olemasolu katteklaasi all, samuti HIF-i tsükli nihkumist söötme pH muutuste tõttu, mis viitab sellele, et HIF-tsükkel tekkis HIF-1-ga seotud pärssimisel. madalale pH-le. See uuring näitas, et HIF{10}} aktiveerimine jäljendab hüpoperfusiooniga kultiveeritud rakkude füsioloogilist seisundit.
MÄRKSÕNADhüpoperfusioon, hüpoksia, hüpoksiaga indutseeritav tegur, hapnikugradient, pH
Cistanche herbaennetab neeruhaigust, proovi saamiseks klõpsake siin
1|SISSEJUHATUS
Krooniliste haiguste esinemineneerudhaigus(CKD) suureneb kogu maailmas ühiskonna vananedes (Tonelli & Riella, 2014). Kroonilise neeruhaiguse progresseerumine on pöördumatu, kui neerukahjustus saavutab teatud taseme ja põhjustab lõpuks lõppstaadiumis neeruhaigust (ESRD), sõltumata põhihaigusest. See tulemus viitab "lõpliku ühise tee" olemasolule. Varasemate patoloogiliste analüüside kohaselt on neerufunktsiooni langus tugevamini korrelatsioonis tubulointerstitsiaalse kahjustusega kui glomerulaarkahjustusega. On olnud mitmeid teateid, mis näitavad, et neerufibroos kutsub esile kroonilise hüpoksia tubulointerstitiumis ja see tubulointerstitsiaalne hüpoksia süvendab kroonilist neeruhaigust ja viib ESRD-ni. Need tõendid näitavad, et tubulointerstitsiaalne hüpoksia mängib osa kroonilise neeruhaiguse lõplikus ühises rajas (Mimura & Nangaku, 2010; Nangaku, 2006). Theneerudon väga vastuvõtlik hüpoksiale, kuna tal on suur hapnikuvajadus ning intrarenaalsete arterite ja veenide vahel on hapniku šunt (Nangaku, 2006; Welch et al., 2001; Zhang et al., 2014). Seetõttu leiame, et neeru tubulointerstitiumi hüpoksia ja hüpoksia vastust on oluline uurida.
Esmane bioloogiline reaktsioon hüpoksiale elusorganismides toimub hüpoksiaga indutseeritava faktori (HIF) raja kaudu (Hypoxia, 2011; Semenza & Wang, 1992; Zhou et al., 2003). Haigekassa koosneb - ja -allüksustest. Kuigi -subühik on konstitutiivselt aktiivne, laguneb -subühik hapniku juuresolekul. Normoksilistes tingimustes hüdroksüülitakse HIF- prolüülhüdroksülaasi domeen (Ph.D.), mis muudab selle äratuntavaks von Hippel-Lindau kasvaja supressori (VHL) järgi. Selle äratundmise tulemuseks on hüdroksüülitud HIF-i ubikvitineerimine ja lagunemine proteasoomis. Hüpoksilistes tingimustes akumuleerub HIF tsütosoolis, kuna hüdroksüülimata HIF pääseb lagunemisest. Kogunenud HIF- siirdub tsütosoolist tuuma, kus see dimeriseerub HIF-ga ja toimib transkriptsioonifaktorina, soodustades allavoolu geenide ekspressiooni. HIF-subühikute kolmest tuvastatud isovormist – HIF-1, HIF-2 ja HIF-3 – ekspresseerivad teadaolevalt neerutuubulaarsed epiteelirakud HIF-1 (Tanaka et al. ., 2016). Varasemad uuringud on näidanud haigekassa ajutist või piirkondlikku kuhjumistneerudCKD-ga (Goldfarb et al., 2006; Yu et al., 2012) ja see HIF aktiveeritakse CKD keskkonnas vähenenud hapniku pinge korral. Kroonilise neeruhaiguse hüpoksiaga kohanemishäire võib olla põhjustatud HIF-i rada pärssivate tegurite olemasolust (Asai et al., 2016; Tanaka jt, 2013; Thangarajah jt, 2009). HIF-i aktiveerimise kaitsvatest mõjudest on teatatud mitmetes loommudelites, sealhulgas streptozototsiini indutseeritud diabeetilistel rottidel ja 5/6 nefrektoomiaga rottidel (Deng et al., 2010; Nordquist et al., 2015). Ph.D. inhibiitorid on hiljuti pälvinud tähelepanu uudsete ravimeetoditena neeruaneemia raviks kroonilise neeruhaigusega patsientidel (Akizawa et al., 2019; Chen jt, 2017, 2019; Coyne jt, 2017; Miyata jt, 2011; Pergola jt. ., 2016; Provenzano et al., 2016). Siiski on üksikasjad neeru hüpoksia progresseerumise ja HIF-i akumuleerumise kohtaneerudkroonilise neeruhaigusega, jäävad ebaselgeks. HIF-i hapnikust sõltuv hüdroksüülimine toimub tsütosoolis ja seetõttu on oluline mõõta rakusisest ja rakuvälist hapniku pinget. Hapniku pinge mõõtmiseks kasutatakse mitmeid meetodeid, sealhulgas mikroelektroodide või vere hapnikutasemest sõltuva magnetresonantstomograafia (BOLD-MRI) kasutamist. Intratsellulaarse hapniku seisundi kvantitatiivseks mõõtmiseks kasutasime fosforestsentsi eluaegset pildimikroskoopiat (PLIM) (Hirakawa et al., 2017; Yoshihara jt, 2015). BTPDM1 on fosforestseeruv värvaine, mis põhineb iriidiumi (III) kompleksil BTP, (bp)2Ir(acc) (bp=bensoaatpüridiin, aac=atsetüülatsetoon) katioonse dimetüülaminorühmaga, mis on passiivselt jaotunud rakusisestes lüsosoomides. See sünteesiti hiljutise fosfosondina rakusisese hapnikurõhu mõõtmiseks (Yoshihara et al., 2015). PLIM koos BTPDM1-ga võimaldas normaalsete hiirte neerupinnal saada kõrge eraldusvõimega pilte hapniku osarõhust neerutuubulirakkudes, andes andmeid hapnikugradiendi olemasolu kohta isegi normaalsetes neerudes (Hirakawa et al., 2018). ).
Elusorganites on hapnikugradientid, sealhulgasneerud, isegi tavatingimustes (Hirakawa et al., 2018; Kietzmann, 2017; Zhdanov et al., 2015) ja seetõttu võib selliseid gradiente oodata ka kroonilise neeruhaiguse korral. Hüpoperfusioon on põhjustatud kroonilise neeruhaiguse mikroveresoonkonna vähenemisest, mille korral progresseeruv glomerulaarkahjustus põhjustab peritubulaarse kapillaaride verevoolu vähenemist, mis süvendab interstitsiaalset fibroosi. Interstitsiaalne fibroos kahjustab tubulaarsete rakkude difusiooni ja hapnikuga varustamist ning viib mikroveresoonkonna vähenemiseni, süvendades veelgi tubulointerstitsiaalset hüpoksiat (Mimura & Nangaku, 2010; Nangaku, 2006). Hüpoperfusiooni bioloogilised mõjud jäävad aga ebaselgeks, kuna enamik uuringuid on uurinud hüpoksia ja HIF-1 mõju kultiveeritud rakkudele homogeense perfusiooni ja hapniku pinge tingimustes (Rexius-Hall et al., 2017). Varasemad uuringud on näidanud, et katteklaasiga kaetud ühekihilised kultiveeritud rakud pakuvad head hüpoperfusiooni mudelit, mille indutseerib söötmes difusioonitõke. Modelleeritud hüpoperfusioon on seotud hapnikugradiendiga, kuna katteklaas takistab hapniku difusiooni söötme ülaosast rakkudesse (Pitts & Toombs, 2004; Takahashi & Sato, 2010; Yoshihara et al., 2015). Katteklaasiga kaetud kultiveeritud rakkude monokihis langeb rakusisene hapniku pinge katteklaasi servast kaugenedes, kuna hapniku difusioon kultiveeritud rakkudesse on piiratud. Selle tulemusena moodustub katteklaasi servast keskkohani hapnikugradient ja rakusisene hapniku pinge võib langeda katteklaasi keskel anoksilise vahemikuni (Takahashi & Sato, 2010; Yoshihara et al., 2015) . Käesolevas uuringus keskendusime HIF-i aktiveerimisele ja uurisime, kas hapnikugradiendiga hüpoperfusiooni korral on HIF-ekspressioonis hapnikust sõltumatu muutus. Kuna hüpoperfusioon hapnikugradiendiga eksisteerib neerutuubulites in vivo, võib hapnikust sõltumatute mõjude jälgimine HIF-i ekspressioonile katteklaasi mudelis anda ülevaate mehhanismist, mis on aluseks HIF-i akumulatsiooni puudulikkusele kroonilise neeruhaiguse korral.

cistanche ekstraktneerude jaoks
2|MATERJALID JA MEETODID
2.1|Rakukultuur
Kultiveeritud rakke inkubeeriti niisutatud inkubaatoris 5% CO2-ga. Hüpoksiline inkubatsioon viidi läbi isiklikus CO2/mitmegaasilises inkubaatoris APM-30D (Astec). Anoksia kutsuti esile anoksiakotti, AnaeroPacki ja anaeroobsete kultiveerimiskomplektidega #A-13 (Mitsubishi Gas Chemical).
HK-2 rakud (Homo sapiens, inimeneneerud, isane, CRL- 2190, ATCC, RRID: CVCL_0302), immortaliseeritud proksimaalse tuubuli epiteeli rakuliin normaalsest täiskasvanud inimese neerust, kultiveeriti Dulbecco modifitseeritud Eagle'i söötmes/toitainete segus F{{2} } Sink (DMEM/F12) (D8062, Sigma Aldrich), mis sisaldab 10 protsenti veiseloote seerumit (FBS) (F7524, Sigma Aldrich) ja penitsilliini-streptomütsiini lahust (15070063, Thermo Fisher Scientific) 10 cm kultiveerimisnõus. Passaažiks eraldati HK-2 rakud trüpsiiniga (204-16935, Wako Pure Chemical Industries, Ltd.) ja tsentrifuugiti 300 g juures 5 minutit.
HeLa emakakaelavähi rakud ja inimese embrüoneerudrakke 293 (HEK293) kultiveeriti DMEM-is madala (1000 mg/l) glükoosiga (D6046, Sigma Aldrich), mis sisaldas 5 protsenti FBS-i, 10 cm kultiveerimisnõus. Need rakud passeeriti HK-2 rakkudena.
Neeru proksimaalsete tuubulite epiteelirakke (RPTEC) (CC- 2553, Cambrex) hooldati RenaLifeTM Compi komplektidega (LRC-LL0025, Lonza Ltd.). Passaažiks eraldati RPTEC-d trüpsiini abil, neutraliseeriti trüpsiini neutraliseeriva lahusega (CC-5002, Lonza Ltd.) ja tsentrifuugiti 200 g juures 5 minutit.
2.2|Hüpoperfusioonimudeli loomine katteklaasi paigutusega
Ümmargused 15 mm läbimõõduga katteklaasid (C015001, Matsunami) puhastati ultraheliga ja säilitati enne kasutamist 99,5 protsendilises etanoolis. Kasutati kahte meetodit, mis põhinesid katteklaasist väljaspool olevate rakkude vaatlemisel.
Ühekihilised kultiveeritud rakud asetati katteklaasi ja tassi põhja vahele (joonis S1a, b) või alternatiivse meetodi (joonis S1c), nagu allpool kirjeldatud. Meie katteklaasi mudeli loomiseks reaalajas pildistamiseks valiti kas traditsiooniline või alternatiivne meetod, olgu see siis hapniku- või PH-pildistamine. Immunotsütokeemia (ICC) jaoks valiti alternatiivne meetod, kuna traditsioonilise meetodi kasutamisel eraldus enamik rakke rakkude fikseerimiseks katteklaasi eemaldamise ajal sageli tassi põhjast (joonis S2a).
2.2.1|Traditsiooniline meetod
Esimesel päeval asetati rakud 27 mm klaasaluse (3910-035, Iwaki) põhjale 100% * (ligikaudu 5,0 × 105 tassi kohta) liitumiskohas. Neid kultiveeriti üle öö DMEM/F12-s, mis sisaldas 10% FBS-i ilma antibiootikumilahuseta. 2. päeval kanti kultiveeritud rakkudele näidatud perioodiks katteklaas (joonis S1b).
2.2.2|Alternatiivne meetod
Rakud külvati päeval 35 mm kultiveerimisnõus katteklaasile 100% konfluentsusel (ligikaudu 5,0 × 105 tassi kohta).
1. Neid kultiveeriti DMEM/F12-s, mis sisaldas 10% FBS-i ilma antibiootikumilahuseta üleöö. Teisel päeval pöörati katteklaas ümber, et kinnitada selle rakkude pind kindlaksmääratud ajaks uue 27 mm klaasaluse põhja külge (joonis S1c).
Samuti lõime katteklaasi mudeli, kasutades ümaraid 10 mm läbimõõduga katteklaase (CS01005, Matsunami) (joonis S2b).
2,3|Reaalajas hapniku pildistamine BTPDM1-ga
Kultiveeritud rakud valmistati 1. päeval, nagu eespool kirjeldatud. 2. päeval loputati rakke kaks korda Hanksi tasakaalustatud soolalahusega (HBSS) (H8264, Sigma Aldrich) ja inkubeeriti 500 nM BTPDM1-ga, iriidiumipõhise katioonse lipofiilse värvainega, mida kasutatakse intratsellulaarse fosforestseeruva sondina (Yoshihara et al., Yoshihara. 2015), DMEM/F12-s ilma fenoolpunaseta (21041-025, Thermo Fisher Scientific) 30 minutit. Pärast seda, kui rakke pesti kaks korda HBSS-iga, asetati need katteklaasi ja nõude põhja vahele, nagu ülalpool kirjeldatud. BTPDM1 fosforestsentsi intensiivsust katteklaasiga kaetud kultiveeritud rakkudes jälgiti ergastus- ja emissioonifiltri abil ning BTPDM1 fosforestsentsi (Hirakawa et al., 2015) tuvastamiseks kasutati fluorestsentsmikroskoobi BZ-X710 (Keyence Corporation). Pööratud fluorestsentsmikroskoobist saadud pilte reguleeriti BZ-X analüüsitarkvara abil heleduse ja kontrastsuse jaoks.
2.4|Immunotsütokeemia
Katteklaasil olevaid rakke kultiveeriti 200 µM pimonidasool-HCl-ga (HP3-100, Hypoxyprobe, Inc.) DMEM/F12-s ilma fenoolpunaseta 1 tund, misjärel katteklaas pöörati ja kinnitati katteklaasile. eelnevalt kirjeldatud. Seejärel kultiveeriti rakke kindlaksmääratud aja jooksul DMEM/F12-s ilma fenoolpunaseta. Kui pimonidasooli vastuvärvimist ei kasutatud, jäeti pimonidasooliga eeltöötlus ära.
Pärast kultiveerimisperioodi lõppu koguti iga katteklaas ja rakud fikseeriti kohe metanooli/atsetooniga (1:1) jääl, kuhu need jäid 30 minutiks. Pärast kahekordset pesemist Dulbecco fosfaatpuhverdatud soolalahusega (PBS) (D5652, Sigma Aldrich) muudeti rakumembraani läbilaskvus 30 minutiks, inkubeeriti 5% veise seerumi albumiiniga (BSA) (A3059, Sigma Aldrich) 30 minutit ja seejärel seerumivaba valgublokiga (X0909, DAKO) 10 min. Rakud värviti esimese antikehaga ja seejärel teise fluorestseeruva antikehaga. Esimeste antikehade loetelu on toodud tabelis S1. Kui peremees oli küülik, kasutati esimese antikehana FITC-sigade polüklonaalset küülikuvastast immunoglobuliini (F0205, lahjendus 1:20, DAKO). Kui peremeesorganism oli hiir, kasutati esimese antikehana fluorestseeruvat antikeha Alexa Fluor 594 streptavidiini (S11227, lahjendus 1:500, Thermo Fisher Scientific), millele järgnes biotinüülitud hiirevastane IgG (H plus L) (BA{{23} }, 1:1000 lahjendus, Vector Laboratories), teise antikehana. Tuumavärvimine viidi läbi, kasutades iga proovi jaoks bisbensimide H 33342 trivesinikkloriidi (B2261, Sigma Aldrich).
Fluorestsentssignaale vaadeldi ümberpööratud fluorestsentsmikroskoobiga BZ-X710 (Keyence Corporation) järgmiste filtritega: Texas Red ergastuslainepikkusega (Ex) 560/40 nm, emissiooni lainepikkus (Em) 630/75 nm, GFP ( Näide: 470/40 nm, Em: 525/50 nm ja DAPI (nt 360/40 nm, Em: 460/50 nm). Pilte reguleeriti heleduse ja kontrastsuse jaoks, kasutades BZ-X analüüsitarkvara.
2,5|Koobaltkloriidiga töödeldud HK-2 rakkude HIF-i ICC
Alternatiivset meetodit muudeti, et saada koobaltkloriidiga töödeldud HK-2 rakkude katteklaasi mudel. HK-2 rakud külvati 1. päeval poolkonfluentse tihedusega (2,5 × 105 tassi kohta) katteklaasile ja töödeldi 300 µM koobaltkloriidheksahüdraadiga (C 8661, Sigma Aldrich) 16 tundi. 2. päev. 3. päeval pöörati katteklaas tagurpidi, et kinnitada rakupinnad 3 tunniks uue 27 mm klaasaluse põhja külge, ja viidi läbi HIF-i ICC.
2,6|Western blotting
HIF{{0}} akumuleerumise uurimiseks erinevatel hapnikupingetel ja erinevatel pH tasemetel, 1.0 × 106 HK-2 rakku 10 cm kultiveerimisnõu kohta inkubeeriti kas normoksia, 2% hapniku, 1% hapniku või anoksia tingimustes 5 tundi või DMEM/F12-s pH 7,4, pH 6,0 või pH 5,0 juures 5 tundi.
Need rakud lüüsiti RIPA puhvris, mis sisaldas 50 mM Tris-puhvrit (pH 8.0), 150 mM NaCl, 0,5 w/v protsenti naatriumi. desoksükolaat, 0,1 massiprotsenti SDS ja 1,0 massiprotsenti NP40.
Western blot analüüsiks SDS proovipuhver, mis sisaldab {{0}},35 M Tris-HCl (pH 6,8), 10 protsenti SDS-i, 36 protsenti glütserooli, 0,012 protsenti bromofenoolsinist ja 0,1 M ditiotreitooli (DTT) lisati valkudele. SDS-i proovipuhvrit sisaldavad valgud elueeriti keetmisega 95 kraadi juures 5 minutit.
Valgud eraldati elektroforeesiga 10% SDS-polüakrüülamiidgeelidel. Seejärel kanti valgud AmershamTM HybondTM PVDF membraanile (10600023, GE Healthcare) ülekandepuhvris (48 mM Tris-aluse puhver, 39 mM glütsiin, 0,04 protsenti SDS ja 20 mahuprotsenti metanooli), kasutades Trans-Blot®. TurboTM ülekandesüsteem (Bio-Rad). Membraane inkubeeriti toatemperatuuril primaarsete antikehade, HIF1-vastase antikehaga (NB100-134, lahjendus 1:500, Novus Biologicals, RRID: AB_350071) ja anti-aktiini antikehaga (A2066) , 1:2000 lahjendus, Sigma Aldrich, RRID: AB_476693) ja seejärel sekundaarses antikehas polüklonaalne kitse küülikuvastane immunoglobuliin/HRP (P0448, lahjendus 1:10000, DAKO, RRID: AB{26) }}). Tuvastamiseks kasutati PierceTM ECL Plus Western Blotting Substrate (32132, ThermoFisher Scientific). Kemiluminestsentsi jälgiti seadmega Luminoimage Analyzer ImageQuantLAS4000mini (GE Healthcare). Reprodutseeritavus kinnitati vähemalt kolme sõltumatu katsega. Ribade intensiivsust kvantifitseeriti National Institutes of Health ImageJ tarkvara abil (Schneider et al., 2012).
2,7|Lutsiferaasi reporteri test
HIF1 akumulatsiooni mõõtmiseks homogeense hüpoksilise kultuuri inkubeerimisel viidi läbi lutsiferaasi reporteri test. Varem konstrueerisime märgistatud lutsiferaasi geeni, mida juhib hüpoksiale reageeriv element (HRE) ja töötasime välja hüpoksiale reageeriva reportervektori (Transgene Construction). See konstrueeriti roti vaskulaarse endoteeli kasvufaktori geeni HRE tandemkoopiatest, mis olid subkloonitud am CMV-promootor-lutsiferaasi transkriptsiooniüksuse (pre-Luc) 5'-piirkonda (Chiang et al., 2011; Tanaka et al. al., 2004).
HK{{0}} rakud kontsentratsiooniga 1,0 × 105 süvendi kohta valmistati 12-süvendiga kultiveerimisplaatidel (150628, Thermo Fisher Scientific). Rakud kotransfekteeriti 500 ng pGL3-Basic HRE-lutsiferaasi vektoritega ja 30 ng pRL-SV40 Renilla lutsiferaasi kontrollvektoritega (Promega), kasutades 2 µl FuGENE® HD transfektsioonireagenti (E2311, Promega) hästi. Negatiivse kontrollina kasutati HK-2 rakke, mis olid kotransfekteeritud 500 ng ofpGL3-Basic Firefly lutsiferaasi vektoritega ja 30 ng ofpRL-SV40 Renilla lutsiferaasi kontrollvektoritega (Promega).
Transfekteeritud rakke inkubeeriti normoksia, 2-protsendilise hüpoksia, 1-protsendilise hüpoksia või anoksiakotis 5 tundi. Seejärel koguti rakud kahekordse lutsiferaasi testi jaoks, kasutades 100 ui passiivset valgu lüüsipuhvrit. Mõõtmiseks kasutati luminomeetrit LB9507 (EG ja Berthold). Transfektsiooni efektiivsuse korrigeerimiseks jagati tulikärbse lutsiferaasi valgusühiku suhteline väärtus Renilla lutsiferaasi omaga.

cistanche toim
2,8|Apoptoosi analüüs
Kultiveeritud rakud kaeti katteklaasiga 0 minutiks, 15 minutiks, 30 minutiks, 1 tunniks, 3 tunniks, 6 tunniks ja 24 tunniks ning seejärel koguti trüpsiini abil. Rakud, mida töödeldi 3% vesinikperoksiidiga (081- 04215, Wako Pure Chemical Industries, Ltd.) 30 minutit, valmistati ette apoptootilise kontrollina. Apoptoosi kvantitatiivne analüüs viidi läbi Muse Annexin V ja Dead Cell Kits (MCH100105, Millipore) abil Muse™ Cell Analyzeris (Millipore) vastavalt tootja juhistele.
2,9|Kvantitatiivne reaalajas PCR (qRT-PCR)
RNA täielik ekstraheerimine ja cDNA süntees viidi läbi vastavalt tootja juhistele RNAiso Plus (9109, Takara) ja PrimeScript™ RT Master Mix (RR036B, Perfect Real Time) (Takara) jaoks. Reaalajas PCR viidi läbi, kasutades THUNDERBIRD SYBR qPCR Mixi (QPS- 201, Toyobo) CFX Connecti reaalajas PCR-tuvastussüsteemis (Bio-Rad). Transkripti tasemed normaliseeriti -aktiini mRNA ekspressiooni tasemele. qRT-PCR viidi läbi kolmes eksemplaris, kasutades geenispetsiifilisi praimereid. HIF-1 amplifitseeriti, kasutades päri-, 5'-CCATTAGAAAGCAGTTCCGC-3' ja tagurpidi, 5'-TGGGTAGGAGATGGAGATGC-3' praimereid. -aktiini amplifitseerimiseks kasutati päri-, 5'-TCCCCCAACTTGA GATGTATGAAG-3' ja pöördpraimereid 5'-AACTGGTCTCAAG TCAGTGTACAGG-3'.
2.10|Transfektsioon siRNA-ga
RNAi-indutseeritud HIF-1 knockdowni uurimiseks HK-2 rakkudes valmistati kuue süvendiga plaatidele 50 × 104 HK-2 rakku süvendi kohta. Lipofectamine RNAiMAX-iga kasutati kahte tüüpi RNAi-d – HIF-1 siRNA-d (siHIF-1 #1 [HSS104774, Thermo Fisher Scientific] ja siHIF-1 #2 [HSS104775, ThermoFisher Scientific]) Transfektsioonireagent (Thermo Fisher Scientific). Negatiivse kontrollina kasutati Stealth RNAi™ siRNA Negative Control Med GC Duplex #3 (12935-113); 1,5 µl iga siRNA ja 5 µl RNAiMAX segati. siRNA-ga transfekteeritud rakke inkubeeriti normoksilistes või hüpoksilistes (1% O2) tingimustes 48 tundi ja RNA ekstraheeriti. HIF-1 knockdowni efektiivsust uuriti qRT-PCR abil.
2.11|PH gradiendi mõjude reaalajas pildistamine
Visualiseerisime elusrakkude rakusisese pH gradiendi katteklaasi all. Rakke töödeldi enne katteklaasi mudeli rakendamist pHrodo Green AM intratsellulaarse pH indikaatoriga (p35373, ThermoFisher Scientific) vastavalt tootja juhistele. Fluorestsentsi intensiivsuse gradiendi ajalise ülemineku jälgimiseks katteklaasi all kasutati ümberpööratud fluorestsentsmikroskoopi BZ-X710 (Keyence Corporation) koos GFP filtriga.
2.12|HIF-i rõnga kvantitatiivne analüüs
2.12.1|Haigekassa ringi asukoht
Mõõtsime ImageJ abil HIF-rõngaste ja pimonidasooli-positiivsete alade kaugust katteklaasi servadest järgmiselt. Määrati HIF-i ringi ja pimonidasool-positiivse ringi välimise ja sisemise ringi pindalad ning arvutati iga ringi raadius. Iga väärtus lahutati 7,5 mm-st, mis on 15 mm katteklaasi raadius, et arvutada selle kaugus katteklaasi servast. Igas seisundis viidi läbi kolm sõltumatut HIF-i ICC katset.
2.12.2|Haigekassa rõnga määratlus
Kasutasime normoksia ja neutraalse pH all inkubeeritud katteklaasi mudelist saadud fluorestsentspilte. Määrasime HIF-i rõnga asukoha ja selle välis- ja siseküljena 2,5–3.0 skaala (0,22–0,45 mm), 0,5 –1.{11}} skaalal (1,12–1,35 mm) ja 5.0–5,5 skaalal (2,24–2,47 mm) katteklaasi servast, kasutades ImageJ-d. Mõõtsime proovi kohta viis HIF{24}} signaali saiti ja arvutasime keskmise. Viidi läbi kolm sõltumatut HIF-i ICC katset.

cistanche ekstrakti pulber
2,13|Hapniku rõhu mõõtmine PLIM-pildiga
2.13.1|Kalibreerimisliini ehitamine hapnikurõhu mõõtmiseks
HK{0}} rakkude kalibreerimiskõver koostati meie eelmises aruandes kirjeldatud meetodil (Yoshihara et al., 2015). HK-2 rakke, mis olid laetud 500 nM BTPDM1-ga 30 minutit, kultiveeriti muudetava hapniku kontsentratsiooniga mitme gaasiga inkubaatoris, mis oli varustatud ümberpööratud fluorestsentsmikroskoobiga, mis oli ühendatud eluea mõõtmise süsteemiga. Sterni-Volmeri analüüsidel põhinev kalibreerimisliin konstrueeriti, kasutades HK-2 rakkude fosforestsentsi eluiga (PL) mitme erineva hapniku pinge all, kasutades
Võrrand (1)
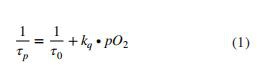
kus τp tähistab PL-d pO2-s, τ0 tähistab PL-i deoksügeenimisel, kq tähistab summutuskiiruse konstanti ja pO2 tähistab hapniku osarõhku. Seda kalibreerimisjoont kasutades saab hapniku rõhu arvutada PL-st.
2.13.2|PLIM-pilt katteklaasi mudelist
Valmistati ette HK-2 rakud, mis olid laaditud 30 minutiks 500 nM BTPDM1-ga. Katteklaasi mudel konstrueeriti ja kultiveeriti muudetava O2 kontsentratsiooniga mitme gaasi inkubaatoris, mis oli varustatud ümberpööratud fluorestsentsmikroskoobiga, mis oli ühendatud eluea mõõtmise süsteemiga.
Fosforestsentsi eluaegse kujutise mikroskoopia (PLIM) kujutised salvestati ümberpööratud fluorestsentsmikroskoobi abil, mis oli varustatud konfokaalse skaneerimissüsteemiga (Hirakawa et al., 2018). PLIM-kujutised saadi pärast 30-minutilist inkubeerimist 21% O2-s või 4% O2-s. Proovi kohta tehti neli PLIM-pilti katteklaasi serva lähedalt ülemisest, alt, vasakust ja paremast piirkonnast, et määrata keskmine PL, võttes arvesse PL-de varieerumist katteklaasis.
2.13.3|HIF-rõnga identifitseerimine PLIM-pildil
Pimonidasool oli positiivne hapnikurõhul alla 10 mmHg. 10 mmHg hapnikurõhu PL-ekvivalent oli kalibreerimisjoone järgi 4034,6 ns, nii et PLIM-pildil oli võimalik tuvastada pimonidasooli ringi välimine joon. Seejärel võis PLIM-pildi välimiste ja sisemiste HIF-rõngaste kohad leida kauguse kvantitatiivse analüüsi abil. Mõõtsime HIF-rõngaga võrdväärsete keskmiste PL-de vahemikku 21 protsendi O2 ja 4 protsendi O2 puhul.
2.13.4|HIF-rõnga hapnikurõhu mõõtmine
Arvutasime HIF-rõnga hapnikurõhu vahemiku PL-dest, kasutades kalibreerimisjoont. PLIM-pilte analüüsiti SPCImage 5 abil.0 (Becker & Hickl GmbH).
2,14|Statistiline analüüs
Katse- ja kontrollrühmade võrdlemiseks kasutati Dunnetti testi ning väärtusi < 0,05="" loeti="" statistiliselt="" olulistele="" erinevustele.="" kolme="" või="" enama="" rühma="" võrdlemiseks="" kasutati="" studenti="" t-teste="" ja="" rakendati="" bonferroni="" korrigeeritud="" p-väärtust.="" kõik="" statistilised="" analüüsid="" viidi="" läbi="" kasutades="" jmp="" pro="" ver13.2.1="" (sas).="" eeldati,="" et="" väärtused="" tuletati="" normaalselt="" jaotunud="" populatsioonist="" ja="" need="" on="" näidatud="" kui="" keskmine="" ±="" standardhälve="">

mis on cistanche
3|TULEMUSED
3.1|Hapniku gradiendi moodustumine hüpoperfusioonimudelis
Kinnitasime hapnikugradiendi olemasolu hüpoperfusioonimudelis, mis on põhjustatud katteklaasi paigutamisest, hinnates otseselt hapniku pinget, kasutades fosforestsentsi. Fosforestsentsi intensiivsuse mõõtmine võib ennustada ligikaudset hapnikurõhu trendi (Hirakawa et al., 2015; Yoshihara et al., 2015). Vaatlesime BTPDM1-ga töödeldud HK-2 rakkude kattekihi mudeli fosforestsentsi intensiivsust. Fosforestsentsi intensiivsuse kujutised näitasid hüpoksiat suuremas osas katteklaasi sees olevast piirkonnast, kuid hüpoksiat serva lähedal polnud. See tähelepanek viitas hapnikugradiendi olemasolule katteklaasi serva ümber HK-2 rakkudes, mis olid kaetud katteklaasiga. katteklaas (joonis 1a). Kuna fosforestsentsi intensiivsus sõltub sondi kontsentratsioonist ja ergutusajast, on fosforestsentsi eluea (PL) mõõtmine kasulik hapnikurõhu kvantitatiivseks analüüsiks (Yoshihara et al., 2015). Seega saime kultiveeritud rakkude hapnikupinge kvantitatiivseks mõõtmiseks katteklaasi serva ümber 30 minutiks katteklaasiga kaetud HK-2 rakkude PLIM-kujutised (joonis 1b). PL laienes, kui kaugus katteklaasi servast suurenes. Kinnitasime, et kalibreerimisjoone abil arvutatud hapniku pinge (joonis S3) vähenes, kui kaugus katteklaasi servast suurenes, pakkudes tõendeid hapniku gradiendi olemasolu kohta katteklaasi serva ümber (joonis 1c). Fosforestsentsi intensiivsuse ajalise profiili uurimine näitas, et hapnikugradient hakkas moodustuma 10 minutit pärast katteklaasi paigaldamist
(Joonis 1d).

3.2|Ainulaadne HIF-1 jaotus hüpoperfusioonimudelis "HIF ring"
Uurisime HIF-1 jaotust hüpoperfusioonimudelis hapnikugradiendiga. HIF-1 ICC HK-2 rakkudes näitas pimonidasool-positiivse ala serval sõõrikukujulist täiustust, mida me nimetasime "HIF-rõngaks" (joonis 2a). HIF-1 signaali intensiivsus oli HIF-rõngal oluliselt kõrgem kui selle sise- või välispiirkonnas (joonis 2b). Seda nähtust kinnitati ICC abil koos teise HIF-1 antikehaga (joonis S4a) või muude torukujuliste rakuliinidega (joonis S4b, c). Tegime ka HIF{11}} ICC-analüüsi teist tüüpi kultiveeritud rakkudes, näiteks HeLa emakakaelavähi rakkudes. Kuigi nende rakkude nõrk adhesioon katteklaasiga muutis HIF-1 jaotuse üksikasjaliku hindamise keeruliseks, täheldasime HeLa rakkudes HIF-1 sõõrikukujulist suurenemist (joonis S4d).
HIF-i rõngas ja pimonidasool-positiivne piirkond hakkasid moodustuma mitu tundi pärast katteklaasi asetamist ning HIF-i rõngas tundus staatiline 3 tunni pärast (joonis 2c). HIF-1 katkestamine põhjustas signaali HIF-1, sealhulgas HIF-i rõnga kadumise (joonis 2d, joonis S4e), mis näitab, et HIF-rõngas sõltus HIF-ist-1.
Uurimaks võimalust, et HIF-i rõnga moodustumine sõltub hapnikust, uurisime HIF-1 jaotust katteklaasi mudelis inkubeerimisel erinevate hapnikupingetega. Kohe pärast katteklaasi mudeli valmistamist asetasime nõude erinevate hapnikupingetega hüpoksikambritesse. Hüpoksilise inkubatsiooni ajal täheldasime, et nii HIF-i tsükkel kui ka pimonidasool-positiivne piirkond tundusid laienevat väljapoole (joonis 3a). Mõõtsime iga HIF-i rõnga ja pimonidasool-positiivse piirkonna kaugust katteklaasi servast normoksia, 4% O2 ja 1% O2 inkubatsiooni korral. Nii HIF-i tsükkel kui ka pimonidasool-positiivne ala laienesid ümbritseva hapniku pinge vähenemisel väljapoole (joonis 3b). Need tulemused näitasid, et HIF-i ring sõltus HIF{10}}-st ja hapniku pingest.
Kinnitamaks, et sõõrikukujuline akumuleerumine on HIF-i spetsiifiline nähtus, teostasime katteklaasi mudelis majapidamisgeenidega ICC. GAPDH ja aktiini signaale säilitati kogu katteklaasi piirkonnas ja need olid võrreldavad HIF-rõnga piirkonna ja teiste piirkondade vahel (joonis S5a, b).

3,3|HIF-rõnga hapnikurõhu vahemiku mõõtmine
Kinnitasime HIF-1 akumuleerumise rõngakujulist suurenemist katteklaasiga kaetud kultiveeritud rakkudes – nähtus, mis sõltub hapniku pingest. Kaasatud hapniku pinge ulatuse määramiseks analüüsisime HIF-i rõnga hapnikurõhku, kasutades fosforestsentsi eluea tehnikat. Saime PLIM-kujutised katteklaasi mudelist pärast 30-minutilist inkubeerimist 21% O2 või 4% O2 juures (joonis 4a). HIF-i rõngas tekkis HIF-i ICC-s pimonidasooli ringi servale (joonis 3b). Tuvastasime PLIM-pildil koha, mis oli samaväärne HIF-i ICC pimonidasool-positiivse piirkonnaga, ja seejärel tuvastasime HIF-i rõngale vastava saidi (joonis 4b), kasutades HIF-i rõnga ja kauguse andmete kvantitatiivset analüüsi. pimonidasool-positiivne piirkond (joonis 3b). Mõõtsime ka HIF-rõnga PL-de vahemikku ja seejärel kasutasime kalibreerimisjoont (joonis S3), et arvutada HIF-rõnga hapnikurõhk 21-protsendilises O2-s (4,20 [3,46–4,97] ~35,9 [28,5–44,9] mmHg). , ja 4 protsenti O2 (2,19 [0,21–4,32] ~20,4 [17,1–24,1] mmHg) (joonis 4c).

3,4|HIF-1 akumuleerumine homogeense hapniku pinge all
Kui HIF-i -1 nõrgad signaalid väljaspool HIF-rõngast katteklaasi mudelis võivad olla tingitud ebapiisavast hüpoksiast, siis rõnga sees olevad signaalid, kus HIF-1 oleks pidanud madalama hapnikupinge tõttu tugevamalt aktiveerima, peavad mida kontrollib hapnikust sõltumatu nähtus. Et uurida nähtusi, mis põhjustavad HIF-1 maksimaalse akumuleerumise puudumist anoksilises piirkonnas, mis esineb ainult hüpoperfusioonimudelis, uurisime, kas hapniku pinge ja HIF-1 akumuleerumise vahel inkubatsiooni ajal on pöördvõrdeline seos. homogeense hapnikupingega. Rakulüsaatide Western blot analüüs erinevate homogeensete hapniku pingete korral näitas HIF-1 akumulatsiooni suurenemist anoksilise inkubatsiooni ajal (joonis 5a). HRE-lutsiferaasi reporteranalüüs näitas ka, et homogeense hapniku pinge tingimustes suurenes HIF-1 akumulatsioon madalama hapnikupingega (joonis 5b). Need tulemused näitasid, et HIF-1 akumuleerumine sõltus hapniku pingest, kusjuures maksimaalne akumulatsioon täheldati anoksilises vahemikus. HIF-1 omadused peaksid hüpoperfusioonimudelil ja homogeense hapnikupingega mudelil erinema. Spekuleerisime, et selle hüpoperfusioonimudeli ainulaadse HIF{13}} kogunemise nähtuse võib määrata muu faktor peale hapniku pinge.

3,5|HIF-i rõnga moodustumine oli doktorikraadist sõltumatu
Uurisime, kas HIF{0}} lagunemine, HIF-i rõnga moodustumise võimalik mehhanism, oli HIF-i ringi sees ülesreguleeritud. See idee tundus olevat kehtetu, sest doktorikraadi hüdroksüülimine, HIF-i lagunemise kiirust piirav protsess, nõuab substraadina hapnikku. Koobaltkloriidi kasutatakse laialdaselt keemilise HIF stabilisaatorina. Koostasime koobaltkloriidiga töödeldud HK-2 rakkude katteklaasi mudeli ja teostasime HIF-i ICC analüüsi. HIF-1 signaal HIF-rõnga sees ei suurenenud, mis muutus ebaselgeks, kuna HIF-1 signaal suurenes väljaspool rõngast (joonis 6c). Sarnased tulemused andis HK-2 rakkude ICC koos PHD2, mis arvatakse olevat rakukultuurikatsetes esmane HIF prolüülhüdroksülaas (Strowitzki et al., 2019), knockdowniga (joonis S6). Need tulemused näitasid, et HIF-i lagunemise PHD-VHL telg ei olnud seotud HIF-i ringi moodustumisega.
3,6|PH mõju HIF-1 kogunemisele
Eelmises aruandes kirjeldati südame müotsüütide katteklaasi mudeli kasutamist, mille pH langes katteklaasi sees (Pitts & Toombs, 2004). Uurisime pH-d katteklaasi all ja selle mõju HIF-i rõnga moodustumisele. Töötlesime HK-2 rakke rakusisese pH indikaatoriga, mille fluorestsentsi intensiivsus võimaldab hinnata rakkude pH-d. Reaalajas pildistamine näitas, et pH langes suuremas osas sisepinnast, kuid mitte katteklaasi serva lähedal, mis viitab pH gradiendi olemasolule katteklaasi mudeli serva ümber (joonis 6a). Fluorestsentsi intensiivsuse ja katteklaasi servast kauguse vahelise korrelatsiooni kvantitatiivne analüüs näitas, et esimene oli kauguse suurenedes kõrgem – see tähelepanek toetas pH ja hapniku gradientide olemasolu katteklaasi serva ümber (joonis 6b). Rakulüsaatide Western blot analüüs homogeensete hapnikukontsentratsioonide juures leidis, et inkubeerimine pH 5,0 söötmega surus alla HIF-1 akumulatsiooni hüpoksilistes tingimustes (joonis S7a–d). Samuti kinnitasime, et HIF-1 akumuleerumine hüpoksia korral erinevates pH tingimustes langes alla pH 6,0 (joonis S8a–c).
Ühes aruandes rõhutati kergelt happeliste tingimuste tähtsust, mille pH on umbes 6.0. Selle uuringu kohaselt hapestas hüpoksiajärgne reoksüdatsioon söötme, mis põhjustas VHL-i nukleolaarse sekvestratsiooni. HIF-i lagunemist hoiti omakorda ära C2C12 müotorudes, PC12 neuronites ja 786-0 neeruvähirakkudes (Mekhail et al., 2004). Meie uuringus ei muutunud VHL-i jaotus torukujulistes rakkudes HIF-1 akumulatsiooniga piirkondade ja piirkondade vahel, kus see oli alla surutud, katteklaasi mudelis pH väärtustega 50 kuni 7,4. (Joonis S9a–c). Torukujulised rakud puutuvad kokku mitmesuguste pH-tingimustega (Burke et al., 1999; Pavuluri et al., 2019; Raghunand et al., 2003), seega uurisime HIF-i ringi varieerumist erineva pH-ga söötmes. väärtused vahemikus 5,0 kuni 8,5. HIF-tsüklit täheldati selgelt söötmes, mille pH oli 8,5 ja 7,4 (joonis 6c). HIF-tsükkel eksisteeris ka pH 6,5 juures, kuid oli varjatud (joonis 6c). HIF-1 signaal nõrgenes pH 5,0 juures kogu katteklaasi piirkonnas. (Joonis 6c). Tegime HIF-i rõnga ja pimonidasool-positiivse ala serva vahelise positsioonilise seose täiendava kvantitatiivse analüüsi (joonis 7a) ja avastasime, et rõnga asend varieerus sõltuvalt pH-st. Sisemine ring kippus pH väärtuse 6, 5 juures väljapoole laienema, võrreldes pH väärtusega 7, 4, samas kui välimine ring kahanes pH väärtusel 8, 5 märkimisväärselt sissepoole, tuginedes pimonidasool-positiivse ala servale (joonis 7b, c). Samuti kinnitasime, et majapidamisgeenide aktiivsust säilitati katteklaasi mudelis happelise inkubeerimise ajal (joonis S10). Seetõttu näib, et pH mängib HIF-i ringi moodustumise aluseks olevas mehhanismis olulist rolli.

4|ARUTELU
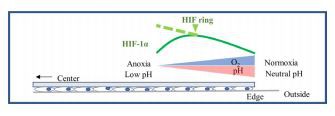
Selles uuringus tuvastasime HIF-1 ainulaadse jaotuse neerutuubulite rakkudes, kasutades katteklaasi paigaldamisega indutseeritud hüpoperfusiooni mudelit. Leidsime, et HIF-i rõnga moodustumist ja säilitamist reguleerisid hapniku rõhk ja pH, mis mõlemad eksisteerisid katteklaasi mudeli katteklaasi servas. Nende tulemuste põhjal pakume välja võimaliku HIF-i rõnga moodustumise mehhanismi, mis hõlmab HIF-1 akumuleerumist koos hapniku pinge vähenemisega ja akumuleerumist pärssitakse madala pH tõttu teatud kaugusel katteklaasi servast (joonis 8). ).
Hüpoperfusiooni põhjustab kroonilise neeruhaiguse mikroveresoonkonna vähenemine (Mimura & Nangaku, 2{{20}}10; Nangaku, 2006). Eelmises töös kasutasime in vivo pildistamist, et näidata hapnikugradiendi olemasolu normaalsete hiire neerude neerutuubulites (Hirakawa et al., 2018). Arvatakse, et CKD torukujulistes rakkudes on hapniku pinge heterogeenne. Siiski jääb ebaselgeks, kas hapnikugradiendiga hüpoperfusiooni olemasolu mõjutab kaitsesüsteemi hüpoksia vastu, HIF. Selles uuringus uurisime hüpoperfusioonimudeli alusel HIF-i jaotumist kultiveeritud proksimaalsetes tuubulite rakkudes ja avastasime, et kultiveeritud neerutuubulite rakkude hapnikugradienti modelleeriti edukalt ümmarguse klaasist katteklaasi abil. Homogeenset hapnikupinget kasutavate katsete tõendid näitasid, et HIF-1, mille hüdroksüülimine ja sellele järgnev lagunemine on peamiselt hapnikust sõltuv, kogunes. See tähendab, et HIF-1 hulk suureneb hapniku pinge vähenedes. Meie katteklaasi mudelis oli HIF-1 aga anoksilises piirkonnas alla surutud ja sellel oli suurim kogunemine teatud kaugusel katteklaasi servast. Seda sõõrikukujulist HIF-i kogunemist pole kunagi varem näidatud. Näitasime, et HIF-i rõnga moodustumist võis jälgida sõltumata inkubatsiooniatmosfääri hapniku pingest, kuid selle asukoht sõltus hapniku pingest. HIF-rõnga hapniku pinge vahemikku mõõdeti ligikaudu 4–20 mmHg, kasutades PLIM-i koos BTPDM1-ga. Enamik varasemaid uuringuid, mis keskendusid kultiveeritud rakkudele homogeense hapnikupingega atmosfääris, näitasid, et HIF-1 valgu kogus suurenes hüpoksilises või anoksilises vahemikus (Ameri et al., 2002; Carrera et al. , 2014). Seega pidi meie mudelis HIF-i rõnga moodustumist mõjutama mõni muu tegur peale hapniku pinge; see oli sõltumatu doktorikraadist, HIF-i lagunemise kiirust piiravast protsessist. Läbimurre HIF-i tsükli moodustumise mehhanismi selgitamisel oli meie avastus pH gradiendi ja ka hapniku gradiendi rolli kohta katte-huule mudelis, mis piiras in vivo hüpoperfusiooniga sarnaselt söötme sissevoolu. mudel. Selles hüpoperfusioonimudelis vähenes rakusisene pH, kui kaugus katteklaasi servast suurenes, ja katteklaasi serva ümber täheldati pH gradienti. Näitasime, et HIF-1 akumuleerumine pärssis madala pH juures, ligikaudu pH 5,0 juures, võrreldes inkubeerimisega ligikaudu neutraalse pH juures homogeense hapniku pinge all. HIF-i rõnga välisserv laienes väljapoole pH väärtusel 6,5 ja HIF-i rõnga siseserv kahanes sissepoole pH väärtusel 8,5, võttes aluseks pimonidasool-positiivse ala serva. HIF tsükkel oli happelistes tingimustes varjatud ja HIF-1 signaal kadus pH väärtusel 5,0. Seega selgitasime pH tähtsust HIF-i tsükli moodustumisel katteklaasi mudelis. Näitasime võimalust, et HIF-i tsükkel tekkis HIF-1-i kogunemise pärssimisel tsüklis madala pH-taseme tõttu.

Mitmed varasemad katteklaasi meetodit kasutanud uuringud on kasutanud vähirakke. Ühe aruande kohaselt, milles kasutati inimese hepatoomi rakuliini Hep3B, mis väljendab rohelise fluorestseeruva valgu (AcGFP1) hapnikust sõltuvat punanihet, näitas ristkülikukujulise katteklaasiga kaetud rakkude reaalajas pildistamine punanihet, kui kaugus katteklaasi servast suurenes (Takahashi & Sato, 2010). Hepatoomirakkude emissioonispekter nihkus hapniku pinge vähenedes rohelise fluorestseeruva valgu (GFP) fluorestsentsi lainepikkuselt punasele. Teises uuringus mõõdeti ümmarguse 15-mm katteklaasiga SCC-7 rakkude hapniku pinget, kasutades fosforestsentsi eluea tehnikat. Hapniku pinge oli 6,9 mmHg ja 166 mmHg, arvutatuna PL-st, mis oli vastavalt 3,89 µs ja 893 µs, katteklaasi servast vastavalt 0–2 mm sees ja 0–1 mm väljaspool (Yoshihara et al., 2015). Katteklaasi meetodit on kasutatud ka südame müotsüütidega – süsteemiga, mis on pälvinud tähelepanu paljutõotava in vivo isheemia-reperfusiooni mudelina. Kelly jt näitasid, et katteklaasiga kaetud müotsüüdid läbisid aja jooksul märkimisväärseid morfoloogilisi muutusi, millega kaasnesid muutused mitokondriaalse membraani potentsiaalis ja plasmamembraani dünaamikas, mille tulemuseks oli müotsüütide surm. Samuti näitasid nad, et katteklaasiga kaetud müotsüütide rakusisene pH langeb katteklaasi keskel kiiresti ligikaudu pH 4-ni (Pitts & Toombs, 2004). Katteklaasi mudel, mis pärsib hapniku või toitainete difusiooni kultiveeritud rakkudesse katteklaasi all, võib jäljendada isheemiliste, normaalsete ja marginaalsete tsoonide in vivo mudelit vastavalt katteklaasi keskel, väljaspool ja servas. Mitmetes uuringutes on seda mudelit kasutatud müotsüütide isheemia-reperfusioonimudelina in vitro (Chun et al., 2015; Pitts et al., 2008; Solhjoo & O'Rourke, 2015; Wang et al., 2012). Meie teadmiste kohaselt on meie uuring esimene, mis rakendab katteklaasi meetodit torukujulistele rakkudele. Meie süsteemis oli kaugus katteklaasi servast piirkonnani, mis vastab 10 mmHg hapniku pingele, kus pimonidasool peaks muutuma positiivseks, 1,22 mm ja hapniku pinge langes 2 mm kaugusel katteklaasi servast kuni nullini. . See tulemus võib ühilduda varasemate aruannetega, milles on kasutatud umbes 15 mm katteklaasi, mis näitab hapnikugradienti olemasolu vähemalt 2 mm kaugusel servast (Akiyama et al., 2018; Yoshihara et al., 2015). Uurisime katteklaaside all olevate rakkude apoptoosi kiirust (joonis S11) ja avastasime, et GAPDH ja aktiin säilisid isegi HIF-i ringi sees, mis näitab, et HIF-i tsüklit ei põhjustanud ainult raku apoptoos või surm HIF-i ringi sees.
Mitmed uuringud on mõõtnud erinevate meetoditega hapniku pinget neerudes. Mõned näited normaalsete neerude hapnikupinge mõõtmisest olid järgmised: 50 mmHg ja 30 mmHg ajukoores ja medullas, kasutades mikroelektroode; ja 49 mmHg ja 41 mmHg ajukoore torukujuliste rakkude S1 ja S2 segmentides, kasutades PLIM-i (Hirakawa et al., 2017, 2018; Zhang et al., 2014). Haigete neerude hapnikupinge oleks madalam. Eelmise aruande kohaselt, milles kasutati hapniku mikroelektroode, oli diabeetilistel rottidel madalam neeru parenhüümi hapniku pinge: ajukoores ja medullas vastavalt 36 mmHg ja 11 mmHg (Heyman et al., 2013; Palm et al., 2003). Kuna hapniku mikroelektroodid mõõdavad keskmist parenhüümi hapniku pinget, on haigete neerude puhul oodata laiemat vahemikku. Intratsellulaarne hapniku pinge langes nullini mmHg isheemilise neeru mudelis, mille külgne neeruarter ja -veen olid kinnitatud (Hirakawa et al., 2015). Arvestades neid leide, tundus hapniku pinge vahemik HIF-i ringis, ligikaudu 4–20 mmHg, olevat in vivo usutav.

Lisaks avastasime, et pH mõjutas nii HIF-i tsükli moodustumist kui ka hapniku pinget. Kuna neerude tubulaarsed epiteelirakud puutuvad pidevalt kokku uriinivedelikuga, peaks tubulaarsete rakkude pH-d mõjutama uriini pH. Arvestades uriini pH laia vahemikku, otsustasime uurida rakke, mida inkubeeriti pH vahemikus 5.0–8,5. Normaalsete neerude pH vahemikku on uuritud. Ühes uuringus leiti, et ajukoore pH oli 7,39 ± 0.{{10}}8 ja medulla pH 7,20 ± {{2{{39} }}}.09, mõõdetuna mikroelektroodidega (Burke et al., 1999). Teine uuring, milles kasutati MRI-põhist pH-kuvamist, näitas pH väärtusteks vastavalt 7,3 ± 0,13 ja 7.0 ± 0,29 (Raghunand et al., 2003). Teatati, et atsidoosiga kroonilise neeruhaiguse hiiremudelis langes neerude pH 6,5-lt 6,32-le ja raskel juhul 5,83-ni (Pavuluri et al., 2019). Need tähelepanekud on andnud tõendeid pH languse ja CKD varieerumise kohta. Kroonilise hüpoksiaga kroonilise hüpoksiaga indutseeritud pH mõju HIF{31}}-le ei ole siiski piisavalt põhjalikult uuritud. Käesolevas uuringus täheldati HIF-i tsükli nihet pH 6, 5 ja pH 7, 4 vahel, mis on CKD korral usutav pH vahemik. See tulemus toetas hüpoteesi, et pH kerge langus mõjutab HIF-1 akumuleerumist kroonilise neeruhaiguse korral. Tuginedes tõenditele pH languse kohta alla 6,0 raskete kroonilise neeruhaiguse juhtude korral, on vaja hinnata ka HIF{40}} füsioloogilist seisundit madalama pH korral. Kuigi on teatatud, et happeline keskkond, isegi normoksia korral, stabiliseerib HIF-1, on enamik neist teadetest uurinud kerge happesuse tingimusi, mille pH on üle 6,0 (Filatova et al., 2016; Mekhail et al., 2004). . Selles töös näitasime HIF-1 akumuleerumise pärssimist torukujulistes rakkudes pH 5,0 juures ja HIF-1 signaalide nõrgenemist katteklaasi mudelis, mida inkubeeriti pH väärtusel 5,0. Seetõttu võib neerude pH langus CKD-s in vivo olla korrelatsioonis ebapiisava HIF-i aktivatsiooniga, aga ka ureemiliste toksiinidega hüpoksilises neerus, mis raskendab CKD progresseerumist (Tanaka et al., 2013).
Meie uuringul on mitmeid piiranguid. Esiteks, hüpoperfusiooni piirkonnas peaks söötmes olema toitainete puudus, lisaks hapnikupuudus ja pH langus. Siiski on raske piiritleda pH, hapniku pinge ja muude hüpoperfusioonist põhjustatud tegurite mõju. Organismis esineb elundites ja rakkudes isheemia ehk vere patoloogiline hüpoperfusioon, mis on põhjustatud vähese hapniku ja toitainete puudumisest. Oluline on mõista hüpoksia tuvastamise ja isheemia tuvastamise erinevusi. Vaatamata raskustele iga teguri bioloogilise mõju selgitamisel, on meie hüpoperfusioonimudel füsioloogiliselt usutav, imiteerides patoloogilist seisundit in vivo. Teiseks nõuab katteklaasi mudeli valmistamine oskusi ja praktikat, kuna enamik rakke eraldus aeg-ajalt katteklaasi eemaldamise ajal, eriti traditsioonilise meetodi kasutamisel (joonis S2a). See probleem sõltus kasutatud rakuliinist. Näiteks oli meil raske kanda HEK 293 rakkudele katteklaasi mudelit, kuna nende nake katteklaasiga oli suhteliselt nõrk. Kolmandaks oli soovitav minimeerida katteklaasi all kultiveeritud rakkude kahjustamist. Kahjustatud rakkude arv suurenes, kui periood, mille jooksul need olid kaetud, suurenes, nagu näitab apoptoosi analüüs. Otsustasime, et 3 tundi oli sobiv HIF-i ringi hindamiseks, kui see tundus olevat staatiline, ja umbes 10 protsenti rakkudest muutus apoptootiliseks (joonis S11). Neljas piirang oli raskus kultiveeritud rakkude kinnitamisel katteklaasile ühtlaselt igas proovis (joonis S2b, c). Uuringut võis mõjutada ka erinevus traditsioonilise ja alternatiivse katte-huulemudeli valmistamise meetodi vahel. Mõõtsime HIF-rõngaga samaväärse hapnikupinge vahemikku fosforestsentsi eluea tehnikaga, mille käigus lõime traditsioonilisel meetodil katteklaasi mudeli. Kuna HIF-i ring immunotsütokeemia ajal visualiseeriti alternatiivse meetodi abil, võib tegelik hapniku pinge olla erinev. Minimeerisime need vead, kasutades tõendeid selle kohta, et pimonidasool oli positiivne hapniku pinge juures 10 mmHg või vähem. Viies piirang on see, et rakusisene pH ei pruugi olla sama, mis söötme pH. Mitmed varasemad aruanded on näidanud, et rakusisene pH on kultiveeritud rakkudes teatud määral kooskõlas söötme pH-ga (Michl et al., 2019), me saame hinnata ainult rakusisese pH suundumust, muutes söötme pH-d. In vivo on intratsellulaarsete ja rakuväliste piirkondade, nagu uriin või kehavedelik, pH seos keerulisem kui kultiveeritud rakkudes. Seega on tulevikus vaja täiendavaid uuringuid selle kohta, kuidas pH nihe reguleerib HIF-1 valgu akumuleerumist in vivo.

Cistanche kasu: paranda neerudfunktsiooni
Teine piirang on see, et pH peaks mõjutama hüpoksia markerit pimonidasooli. Võrdlesime pimonidasool-positiivse ala serva kaugust katteklaasi keskpunktist erinevates pH tingimustes meie katteklaasi mudelis. Pimonidasool-positiivse ala serv oli võrreldav pH 6, 5, 7, 4 ja 8, 5 vahel (joonis S12a, b). Eelnev uuring näitas ka pimonidasooli sidumise säilimist erinevate pH väärtuste juures (Kleiter et al., 2006). Nende tõendite põhjal järeldasime, et pimonidasool on meie katteklaasi katsete jaoks sobiv hüpoksia marker. Lõplik piirang on see, et arvestades HIF-tsükli hapniku pingevahemikku ligikaudu 4 mmHg kuni 20 mmHg (0,52 protsenti O2 kuni 2,6 protsenti O2), on Pt(II)- ja Pd(II)-porfüriinid, mida kasutatakse laialdaselt bioloogilistena. hapnikusondidel on eelised väga madalate hapnikukontsentratsioonide mõõtmiseks, kuna nende fosforestsentsi eluiga on oluliselt pikem, võrreldes nendega, mis kasutavad Ir (III) komplekse (Yoshihara et al., 2017). Kuid üldiselt on fosforestsentsil põhineval kvantitatiivsel hapniku mõõtmisel, mis arvutatakse Sterni-Volmeri võrrandi abil, parem tulemus madalates O2 vahemikes (Papkovsky & Zhdanov, 2016). Mitmed varasemad uuringud on näidanud Ir(III) kompleksipõhist hapniku pingete mõõtmist nii madalal kui umbes 10 mmHg (Akiyama et al., 2018; Yoshihara et al., 2015). Seetõttu usume, et HIF-i rõnga hapnikupinge vahemik peaks olema täpne tulemus.
5|JÄRELDUSED
Kokkuvõttes leidsime, et nii hapniku kui ka pH rollide mõistmine on oluline HIF-1 füsioloogilise seisundi mõistmiseks kroonilise neeruhaiguse korral ja seda saab saavutada hüpoperfusiooniga torukujuliste rakkude uurimisel. Katteklaasi mudel oma piirangutega söötme sissevoolule oli hea hüpoperfusiooni mudel in vivo, eriti kroonilise neeruhaiguse tuubulites, kuna peritubulaarsete kapillaaride hõrenemine on kroonilise neeruhaiguse peamine tunnus (Mimura & Nangaku, 2010; Nangaku, 2006). See hüpoperfusioonimudel võib jäljendada ka hapniku ja pH gradiente in vivo, nagu kasvajad ja isheemilised kahjustused. Mudel pakub paljutõotavat lähenemisviisi nende bioloogiliste mehhanismide selgitamiseks.
HUVIDE KONFLIKT
Kõigil autoritel pole huvide konflikte deklareerida.
AUTORIDE KAASUSED
Kõik autorid aitasid kaasa üldise kontseptsiooni kujunemisele. TH viis läbi üldised katsed. TH ja YH analüüsisid tulemusi ja tegid arvud. TH kirjutas originaalkäsikirja. KM, TY ja ST viisid katse läbi fosforestsentsi eluea tehnikat kasutades ja redigeerisid käsikirja osa. YH, TT ja MN redigeerisid üldist käsikirja. Kõik autorid on lõpliku käsikirja läbi lugenud ja heaks kiitnud.
VIIDE
Akiyama, H., Takahashi, I., Shimoda, Y., Mukai, R., Yoshihara, T. ja Tobita, S. (2018). Ir (iii) elusrakkude ja silmapõhja kompleksipõhine hapnikupildistamine ICCD kaameraga. Photochemical and Photobiological Sciences, 17(6), 846–853.
Akizawa, T., Nangaku, M., Yamaguchi, T., Arai, M., Koretomo, R., Maeda, K., Miyazawa, Y., & Hirakata, H. (2019). Enarodustaat, aneemia konversiooni- ja säilitusravi hemodialüüsi saavatel patsientidel: randomiseeritud platseebokontrolliga 2.b faasi uuring, millele järgneb pikaajaline uuring. Nephron, 143 (2), 77–85.
Ameri, K., Burke, B., Lewis, CE ja Harris, AL (2002). Roti VL30 elemendi reguleerimine inimese rinnavähirakkudes hüpoksia ja anoksia korral: HIF-1 roll. British Journal of Cancer, 87(10), 1173–1181.
Asai, H., Hirata, J., Hirano, A., Hirai, K., Seki, S., & Watanabe- Akanuma, M. (2016). Arüülsüsivesinike retseptori aktiveerimine vahendab hüpoksiast indutseeritava faktorist sõltuva erütropoetiini ekspressiooni pärssimist indoksüülsulfaadi poolt. American Journal of Physiology. Cell Physiology, 310(2), C142–C150.
Burke, TJ, Malhotra, D. ja Shapiro, JI (1999). Neerude pH-gradienti säilitavad tegurid: veresoonte arhitektuuri roll. Kidney International, 56(5), 1826–1837.
Carrera, S., Senra, J., Acosta, MI, Althubiti, M., Hammond, EM, de Verdier, PJ ja Macip, S. (2014). HIF-1alfa transkriptsioonifaktori roll rakkude suurenenud jagunemisel füsioloogilise hapniku pinge korral. PLoS One, 9 (5), e97938.
Chen, N., Hao, C., Peng, X., Lin, H., Yin, A., Hao, L., Tao, Y., Liang, X., Liu, Z., Xing, C., Chen, J., Luo, L., Zuo, L., Liao, Y., Liu, BC, Leong, R., Wang, C., Liu, C., Neff, T., … Yu, KHP (2019) ).
Roxadustat aneemia raviks neeruhaigusega patsientidel, kes ei saa dialüüsi. New England Journal of Medicine, 381 (11), 1001–1010.
Chen, N., Qian, J., Chen, J., Yu, X., Mei, C., Hao, C., Jiang, G., Lin, H., Zhang, X., Zuo, L., He, Q., Fu, P., Li, X., Ni, D., Hemmerich, S., Liu, C., Szczech, L., Besarab, A., Neff, TB, … Valone, F.
H. (2017). Suukaudse hüpoksiaga indutseeritava faktori prolüülhüdroksülaasi inhibiitori FG-4592 2. faasi uuringud aneemia raviks Hiinas. Nephrology, Dialysis, Transplantation, 32(8), 1373–1386.
Chiang, CK, Tanaka, T., Inagi, R., Fujita, T. ja Nangaku, M. (2011). Indoksüülsulfaat, tüüpiline ureemiline toksiin, pärsib erütropoetiini tootmist HIF-sõltuval viisil. Laboratory Investigation, 91(11), 1564–1571.
Chun, WJ, Nah, DY, Bae, JH, Chung, JW, Lee, H. ja Moon, IS (2015). Glükoosi-insuliini-kaaliumi lahus kaitseb vastsündinute rottide ventrikulaarseid müotsüüte in vitro katteklaasi isheemia/reperfusiooni mudelis. Korean Circulation Journal, 45(3), 234–241.
Coyne, DW, Goldsmith, D. ja Macdougall, IC (2017). Uued võimalused kroonilise neeruhaiguse aneemia raviks. Kidney International Supplement, 7(3), 157–163. suudlus.2017.09.002
Deng, A., Arndt, MA, Satriano, J., Singh, P., Rieg, T., Thomson, S. jt (2010). Neerude kaitse kroonilise neeruhaiguse korral: hüpoksiaga indutseeritud faktori aktiveerimine vs angiotensiin II blokaad. American Journal of Physiology. Neerufüsioloogia, 299(6), F1365–F1373.
Filatova, A., Seidel, S., Bogurcu, N., Graf, S., Garvalov, BK, & Acker, T. (2016). Atsidoos toimib HSP90 kaudu doktorikraadist/VHL-st sõltumatul viisil, et soodustada HIF funktsiooni ja tüvirakkude säilimist glioomi korral. Cancer Research, 76(19), 5845–5856. SAAB-15-2630
Goldfarb, M., Rosenberger, C., Abassi, Z., Shina, A., Zilbersat, F., Eckardt, KU, Rosen, S. ja Heyman, SN (2006). Äge ja krooniline neerupuudulikkus rottidel: funktsionaalne kompensatsioon ja hüpoksiataluvus. American Journal of Nephrology, 26(1), 22–33.
Heyman, SN, Rosenberger, C., Rosen, S. ja Khamaisi, M. (2013). Miks on suhkurtõbi kontrastainest põhjustatud nefropaatia riskitegur? BioMed Research International, 2013, 123589.
Hirakawa, Y., Mizukami, K., Yoshihara, T., Takahashi, I., Khulan, P., Honda, T., Mimura, I., Tanaka, T., Tobita, S., & Nangaku, M. (2018). Neerukoore eluaegne intravitaalne fosforestsentskujutis mõõdab täpselt neeru hüpoksiat. Kidney International, 93(6), 1483–1489.
Hirakawa, Y., Tanaka, T., & Nangaku, M. (2017). Neeru hüpoksia kroonilise neeruhaiguse korral; Patofüsioloogia ja avastamismeetodid. Piirid füsioloogias, 8, 99.
