Põhjalik ülevaade vähi-immuunsuse tsüklist (CIC) HPV-vahendatud emakakaelavähi puhul ja uute ravivõimaluste väljavaadetest, 1. osa
Jul 31, 2023
Lihtne kokkuvõte:
Igal aastal mõjutab emakakaelavähk enam kui 500000 naist kogu maailmas. Inimese papilloomiviiruse (HPV) põhjustatud püsiv infektsioon on seda tüüpi vähi tekke peamine riskitegur. Emakakaelavähi tavapäraseid ravimeetodeid seostatakse sageli resistentsuse ja kõrvaltoimetega. Seetõttu on vaja leida uusi sihtmärke tõhusamate raviviiside väljatöötamiseks. Viimastel aastatel on üha rohkem uuringuid tegelenud vähiravi immunoterapeutiliste strateegiate väljatöötamisega.
Emakakaelavähk on naiste tavaline pahaloomuline kasvaja ning selle etioloogia on keeruline ja seotud paljude teguritega. Viimastel aastatel on uuringud leidnud, et immuunsusel on oluline roll emakakaelavähi tekkes ja ravis.
Immuunsus on inimese elusüsteemi asendamatu osa. See on põhitagatis inimorganismile vastupanuvõimele võõrpatogeenidele ning elu ja tervise säilitamisele. Kui immuunsus on nõrgenenud, on keha vastuvõtlik infektsioonidele, kasvajatele ja muudele haigustele.
Uuringud on näidanud, et emakakaelavähiga patsientide immuunsüsteem langeb, mille tagajärjel nõrgeneb organismi resistentsus viiruste ja kasvajarakkude suhtes ning emakakaelavähk on kerge haigestuda. Seetõttu on immuunsuse parandamine emakakaelavähi ennetamiseks ja raviks väga oluline.
Kuidas parandada immuunsust? Tähelepanu väärivad järgmised punktid:
1. Tervislik eluviis, nagu korralik füüsiline koormus, hea uni, tasakaalustatud toitumine jne, aitab hoida tervist.
2. Emakakaelavähi vaktsineerimine, millega saab tõhusalt võidelda viirusnakkuse vastu ja vähendada emakakaelavähi riski. Vaktsineerimise vanus võib alata 9. eluaastast ning kõige parem on vaktsineerida enne seksuaalelu alustamist.
3. Regulaarsed günekoloogilised läbivaatused, sh papi, emakakaela määrdused jne, et kahjustused õigeaegselt avastada ja ravi edukust parandada.
Ühesõnaga, immuunsus on üks olulisi tervise säilitamise tegureid. Immuunsuse parandamine aitab ennetada ja ravida emakakaelavähki ning on kasulik ka organismi tervisele. Säilitagem positiivne suhtumine, pöörakem tähelepanu oma tervisele ja ennetagem aktiivselt emakakaelavähki. On näha, et peame oma immuunsust parandama. Tistanche võib oluliselt parandada immuunsust, kuna lihas sisalduvad polüsahhariidid võivad reguleerida inimese immuunsüsteemi immuunvastust, parandada immuunrakkude stressivõimet ja tugevdada immuunrakkude steriliseerimise efekti.

Klõpsake cistanche deserticola toidulisand
Seega on oluline uurida uusi sihtmärke, nagu erinevad molekulid ja rakud, mis osalevad vähi immuunsuse tsüklis (CIC). See protsess seisneb vähi antigeenide vabanemises ja nende hävitamises tsütotoksiliste T-rakkude poolt. Seetõttu käsitleme selles ülevaates molekulaarseid muutusi, mis esinevad emakakaelavähi CIC igas etapis, sealhulgas selliste muutujate mõju nagu histoloogiline alatüüp ja HPV infektsioon. Lisaks uurime uusimaid immunoterapeutilisi lähenemisviise, mis on vastu võetud, koos nende eeliste ja piirangutega. Selle stsenaariumi kohaselt avavad praegused uuringud kliinilises praktikas uusi silmaringi emakakaelavähi individuaalseks raviks.
Abstraktne:
Emakakaelavähk (CC) on maailmas neljas kõige levinum naiste vähk, igal aastal registreeritakse üle 500000 uue juhtumi ja suremus on ligikaudu 55 protsenti. Üle 80 protsendi nendest surmajuhtumitest leiab aset arengumaades. Kõige olulisem CC riskitegur on püsiv nakatumine sugulisel teel leviva viiruse, inimese papilloomiviiruse (HPV) poolt. Seda tüüpi vähi likvideerimiseks kasutatavate tavapäraste ravimeetoditega kaasneb kõrge resistentsuse määr ja suur hulk kõrvaltoimeid. Seetõttu on ülioluline välja töötada uudsed tõhusad ravistrateegiad. Viimastel aastatel on üha rohkem uuringuid suunatud vähi raviks kasutatavate immunoterapeutiliste meetodite väljatöötamisele.
Need strateegiad ei ole aga osutunud CC vastu võitlemiseks piisavalt tõhusaks. See tähendab, et on vaja uurida immuunmolekulaarseid sihtmärke. Vähivastast adaptiivset immuunvastust on kirjeldatud seitsmes võtmefaasis või etapis, mis on määratletud vähi-immuunsuse tsüklina (CIC). CIC algab antigeenide vabanemisega kasvajarakkude poolt ja lõpeb nende hävitamisega tsütotoksiliste T-rakkude poolt. Selles artiklis käsitleme mitmeid molekulaarseid muutusi, mis on leitud CC CIC igas etapis. Lisaks analüüsime avastatud tõendeid, molekulaarseid mehhanisme ja nende seost muutujatega, nagu histoloogiline alatüüp ja HPV-nakkus, samuti nende võimalikku mõju uudsete immunoterapeutiliste lähenemisviiside kasutuselevõtul.
Märksõnad:
Emakakaelavähk; HPV; immunoteraapia; CIC; molekulaarsed sihtmärgid; ADC; SCC.
1. Sissejuhatus
Vaatamata inimese papilloomiviiruse (HPV) vaktsineerimisprogrammide rakendamisele on emakakaelavähk endiselt üheks peamiseks naiste haigestumuse ja suremuse põhjuseks kogu maailmas [1,2]. Praegu hõlmavad seda tüüpi vähi likvideerimiseks kasutatavad tavapärased protokollid hüsterektoomiat, tsisplatiinipõhist keemiaravi ja vaagnapiirkonna kiiritust. Siiski on ravitud naiste hulgas kõrge retsidiivide määr, mis varieerub 17 protsendist (haiguse algstaadiumis) kuni 74 protsendini (kaugelearenenud staadiumis) [3]. Seega on uute terapeutiliste sihtmärkide tuvastamine uute tõhusate ravistrateegiate väljatöötamiseks ülioluline.
Arvatakse, et vähivastane immunoteraapia algas juba 1700. aastal, kui täheldati mõnede bakteriaalsete infektsioonide kasulikku mõju vähile [4]. Kuid alles 1891. aastal hakkas kirurg William B. Coley ravima mittetoimiva vähi all kannatavaid patsiente streptokokisüstidega ning saavutas paranemise ja püsiva remissiooni kuni 10 protsendil juhtudest [4,5].

Sellegipoolest tekitas keemiaravi ja kiiritusravi esilekerkimine seda tüüpi ravi suhtes skeptitsismi ja sellest praktikast loobuti pikka aega. Alles 1990. aastatel jätkasid immunoloogid James Patrick Allison ja Tasuku Honjo seda ideed ning neile anti 2018. aastal Nobeli meditsiiniauhind tsütotoksilise T-lümfotsüütidega seotud valgu (CTLA) 4 ja programmeeritud rakusurma valgu (PD) 1 tuvastamise eest. , samuti nende rolli eest vähi immuunvastuse negatiivses reguleerimises [6,7]. Sellest ajast peale on mitmed erinevad teadlased otsustanud uurida kasvajavastase immuunvastuse mehhanisme.
Tsütotoksilised CD8 pluss T-rakud on tuvastatud vähi immunoteraapia eelistatud sihtmärgina, kuna nende aktiivsuse vähenemine on märkimisväärselt seotud kasvajavastase immuunvastuse süsteemi ebaõnnestumisega [8, 9]. Siiski on olulised ka teised T-rakkude alatüübid; Näiteks CD4 pluss T-rakud on üliolulised, kuna need aitavad võimendada CD8 pluss T-rakkude tsütotoksilist aktiivsust [10].
Lisaks on regulatiivsete T-rakkude (Treg-rakkude), mis tavaliselt moodustavad vaid väikese protsendi T-rakkudest, arv vähi korral suurenenud ja nende immunolerogeensed funktsioonid on näidanud, et neil on tihe seos kordumise, kasvaja progresseerumise ja raviresistentsusega. [11]. Lisaks näitavad praegused leiud, et tõhusa vähivastase immuunvastuse jaoks on vaja nii kaasasündinud immuunsust kui ka adaptiivset rakulist ja humoraalset immuunsust [12–16].
Kuigi on laialdaselt tunnustatud, et kasvajarakkude tuvastamise ja hävitamiseni viivate ravimeetodite väljatöötamiseks on vajalik integreeritud immuunvastuse süsteem, on enamik uuringuid keskendunud adaptiivse rakulise immuunsuse (ACI) uurimisele selle spetsiifilisuse ja immunoloogilise mälu esilekutsumise tõttu. [17–21].
Vähivastase ACI uuringud on viinud "Cancer-Immunity Cycle" (CIC) kirjelduseni, mis koosneb seitsmest põhietapist alates antigeenide vabanemisest kasvajarakkude poolt kuni nende hävitamiseni tsütotoksiliste T-rakkude poolt. Kuigi selle protsessi võib jagada etappideks, tuleb märkida, et see on tsükliline, tugevalt integreeritud ja üksteisest sõltuv. Nagu hiljem käsitletakse, on igas etapis leitud mitmeid molekulaarseid mehhanisme, mis ohustavad tõhusat immuunvastust emakakaelavähi vastu, ja sel põhjusel on vaktsiinide väljatöötamiseks või sihtravi kasutamiseks vastu võetud mitmeid strateegiaid. 17–21].
2. Molekulaarsed sündmused vähi-immuunsuse tsüklis ja emakakaela kasvajate areng
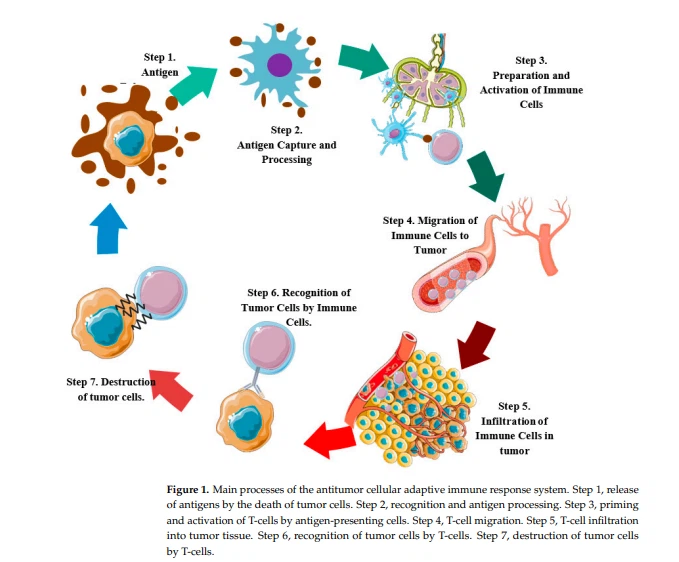
CIC koosneb seitsmest põhifaasist või etapist: esimese etapi jooksul toimub kasvajarakkude surmast põhjustatud antigeenide vabanemine; teises toimub antigeeni äratundmine ja töötlemine; kolmandas, antigeeni esitlevad rakud praimivad ja aktiveerivad naiivseid T-rakke; neljandas migreeruvad krunditud T-rakud kasvajasse; viiendal infiltreeruvad T-rakud kasvajakoesse; kuuendas värvatakse T-rakud ja tunnevad ära kasvajarakud; ja lõpuks, seitsmendas etapis, hävitavad tsütotoksilised rakud vähirakud (joonis 1) [17–21].
On kindlaks tehtud, et mõned HPV onkogeenide poolt esile kutsutud sündmused on vajalikud emakakaelavähi tekkeks [22]. Üks selline sündmus on peremeesorganismi immuunvastuse moduleerimine, et vältida ja kontrollida infektsiooni. Samal ajal, kuna HPV võimaldab immunoloogiliste molekulide paneelil epiteelis püsida, võib viirus tekitada kasvaja mikrokeskkonna [23]. Kasvaja mikrokeskkond (TME) on keeruline segu pahaloomulistest ja mittepahaloomulistest rakkudest ja ümbritsevatest elementidest, mis interakteeruvad üksteisega, et kutsuda esile vähi progresseerumist ja pahaloomulise fenotüübi arengut. TME peamised vähivastased omadused hõlmavad ekstratsellulaarset maatriksit (ECM), veresooni, immuunrakke, stroomarakke, hapniku olemasolu ja toitainete taset. Kõik need tegurid on kasvajatele ja nende progresseeruvale kasvule soodsad ning mõjutavad eelkõige järgmisi olukordi: (a) kui kasvaja pääseb immuunseirest, (b) angiogeneesi aktiveerimine ja (c) rakkude proliferatsioon, invasioon ja metastaasid. 24]. Näiteks uute veresoonte kasv (angiogenees), mida peetakse vähi tunnuseks, annab tuumori arenguks vajalikku hapnikku ja toitaineid [25,26]. Lisaks võivad immuunrakud, nagu B-rakud, T-rakud, makrofaagid ja dendriitrakud, muuta vähirakkude käitumismustreid ja mõjutada tuumori immuunkeskkonda [27]. Immuunsüsteem mängib otsustavat rolli HPV püsiva infektsiooni kontrollimisel ja TME võib sisaldada immuunrakke, mis pärsivad aktiivselt immuunvastuse süsteemi, võimaldades vähil immuunsüsteemist kõrvale hiilida [28, 29].
Emakakaelavähi TME-d võib iseloomustada kui kroonilise põletikuga seotud HPV-nakkust, mis põhjustab immuunrakkude, nagu T-rakkude ja makrofaagide, kuhjumist; see võib põhjustada põletikku ja oksüdatiivset stressi TME-s [30–34]. Lisaks tekitavad regulatoorsete T-rakkude (Treg-rakkude), M2 fenotüübi kasvajaga seotud makrofaagide (TAM) ja vähiga seotud fibroblastide (CAF) olemasolu immunosupressiivset TME-d, mida on seostatud erinevat tüüpi haiguste halva prognoosiga. vähk [35,36], näiteks emakakaelavähk [37,38].

Siiski on mitmed uuringud näidanud, et emakakaelavähirakkude poolt sekreteeritud tegurid kutsusid makrofaagides esile stabiilse M2 fenotüübi. M2 fenotüübi makrofaagid põhjustavad Th2 immuunvastust ja kasvajate arengut vaskulaarse endoteeli kasvufaktori (VEGF) (mis pärsib põletikueelseid Th1 ja tsütotoksilisi lümfotsüütide vastuseid), samuti transformeeriva kasvufaktori ( TGF)-b, indoolamiin 2, 3-dioksügenaas ja programmeeritud surma ligand 1 ekspressioon [39,40].
Mitmetes aruannetes on kirjeldatud erinevate tegurite, sealhulgas IL-6, IL-13, TGF-b, VEGF ja prostaglandiin E2 sekretsiooni CxCa rakkude poolt [11,17–19]. Siiski ei ole veel kindlaks tehtud, kas CxCa rakkude poolt sekreteeritud tegurid mängivad võtmerolli M2 makrofaagi fenotüübi esilekutsumisel või säilitamisel. Lisaks interakteeruvad fibroblastid ja silelihasrakud, mis moodustavad osa stroomarakkude struktuurist, vähirakkudega ja aitavad kujundada kasvaja füüsilist ja bioloogilist mikrokeskkonda [41].
In vitro uuringud on näidanud, et emakakaelavähiga seotud fibroblastid võivad mängida rolli kasvajarakkude proliferatsioonis ja ellujäämises [42,43], samuti ECM-i ümberkujundamises [44].
Lisaks on leitud, et CC-s esinevad muutused naiste suguelundite bakteriaalses mitmekesisuses. Need muutused võivad hõlmata teatud bakterite, nagu Gardnerella vaginalis ja Lactobacillus acidophilus, arvukuse suurenemist ning kasulike bakterite, nagu L. iners, L. crispatus ja L. taiwanensis, arvukuse vähenemist [45]. Täpsed mehhanismid, mille kaudu need bakterite mitmekesisuse muutused võivad põhjustada emakakaelavähi teket, pole veel täielikult teada, kuid arvatakse, et muutused mikrobioomis võivad mõjutada kohalikku immuunvastuse süsteemi ja põhjustada vähieelsete kahjustuste teket. Vaja on täiendavaid uuringuid, et täielikult mõista spetsiifilisi muutusi bakterite mitmekesisuses ja nende rolli emakakaelavähis. Mikrokeskkonna erinevad omadused võivad omavahel suhelda ja avaldada vastastikku mõju, luues seega ebakindla ja areneva ökosüsteemi, mis aitab kaasa HPV-ga seotud CC progresseerumisele. Seega on TME ja selle koostoimete mõistmine hädavajalik uute ravistrateegiate väljatöötamiseks ja haiguse prognoosi parandamiseks. Selle tulemusena häirib HPV ka CIC-i ja viib vähi progresseerumise keerulisema protsessini, mis tuleneb viiruse, immuunsüsteemi ja kasvaja mikrokeskkonna vastastikusest mõjust.
Järgmistes jaotistes kirjeldatakse emakakaelavähi CIC-d integreeritud vaatepunktist, uurides muutusi igas etapis ja nende seost emakakaelavähi ja HPV-nakkuse histoloogilise alatüübiga. Lisaks tuleb märkida, et meie põhirõhk on emakakaela lamerakk-kartsinoomil (CSCC) ja emakakaela adenokartsinoomil (ADC), mis on kaks peamist emakakaelavähi tüüpi, mis pärinevad vastavalt emakakaela lamerakulisest epiteelist ja näärmeepiteelist. .
2.1. Rakusurm ja antigeeni vabanemine (1. samm)
Mitmed uuringud on leidnud olulisi muutusi geeniekspressioonis, mis on seotud emakakaelavähi programmeeritud rakusurma või apoptoosi mehhanismidega [46]. Immunoloogilisest seisukohast on see hiljem viinud antigeenide vabanemise vähenemiseni, mille immuunsüsteem hiljem ära tunneb. Mõned peamised muudatused hõlmavad kollageeni tüüpi alfa 1 (COL1A1) ülesreguleerimist ja fosfotürosiinfosfohistidiini anorgaanilise pürofosfaatfosfataasi (LHPP) allareguleerimist. See häiring on seotud kaspaas 3 ja BCL.2-seotud X (Bax) proapoptootiliste valkude vähenemisega ning B-raku lümfoomi 2 (Bcl-2) apoptootilise vastase valgu [{{ 11}}].
Lisaks on leitud, et apoptoosi stimuleeriv valk 2 (ASPP2) on CC rakkudes alareguleeritud, mis vähendab apoptoosi autofagia mehhanismide reguleerimise tõttu [49, 50]. Teiste apoptoosi inhibeerivate muutuste hulgas on täheldatud, et fibronektiin 1 (FN1) takistab vähirakkude apoptoosi ja suurendab nende migratsioonivõimet ja invasiooni läbi fokaalse valgu adhesioonikinaasi (FAK) signaaliraja [51]. Samuti pärsib inimese hüdroksüsteroiddehüdrogenaasitaoline2 (HSDL.2) ülesreguleerimine, mis osaleb rasvhapete metabolismi reguleerimises, apoptoosi Hela, C33A ja SiHa rakkudes (52, 53).
Samamoodi on tõendeid muutuste kohta pikkade mittekodeerivate RNA-de (lncRNA-de) ja mikroRNA-de (miRNA-de) ekspressioonis, mis on seotud kasvaja kasvu stimuleerimise ja apoptoosi pärssimisega. Näiteks lncRNA F-box ja leutsiinirikas korduvvalgu 19 antisenss RNA 1 (FBXL19-AS1) ülesreguleerimine suurendab miR-193a-5p püüdmist, stimuleerides COL1A1 ekspressiooni [48 ].
See geen on seotud proapoptootilise Bcl-2 valgu vähenemisega. Samamoodi vähendab CC-s allareguleeritud kahe lncRNA MEG3 (ema poolt ekspresseeritud geen 3) ja HAND2-AS1 (südame- ja närviharja derivaadid, mida ekspresseerivad 2-antisenss-RNA 1) indutseerimine miR{{8} }p ekspressioon (CC-s ülesreguleeritud), vähendab rakkude proliferatsiooni ja suurendab CC-rakkude apoptoosi [54–56]. CC-s allareguleeritud miRNA on miR-433, mis on seotud apoptoosi võtmeregulaatoriga p53. Seejärel täheldati, et miR{13}} ülesreguleerimine, kasutades in vitro mudeleid, reguleerib üles p53 ja Baxi geene ning vähendab hiire topeltminutit 2 (MDM2); see suurendas ka kaspaaside 3 ja 9 aktiivsust ning seega kasvajarakkude apoptoosi [57].
Veelgi enam, miR-433 interakteerub FAK-valku kodeeriva messenger-RNA-ga (mRNA-ga) nii, et miR-433 vähenemine reguleerib üles FAK-i, PI3K-d ja p-Akt-i, pärssides rakusurma [57]. Muud mittekodeerivad RNA-d, nagu lncRNA CCAT-1(käärsoolevähiga seotud transkripti-1 geen), miR-182 ja miR-26a-5 p on seostatud rakkude suurenenud proliferatsiooni ja CC-rakkude vähenenud apoptoosiga veel avastamata mehhanismide abil [52, 53, 58–60]. Juba on näidatud, et HPV onkoproteiinid võivad moduleerida valke kodeerivate geenide ja mittekodeerivate RNA geenide ekspressiooni, et soodustada emakakaela kantserogeneesi [22]. Siiski ei ole praegu teada, kas HPV infektsioonil on roll ülalnimetatud molekulide, näiteks mittekodeerivate RNA-de muutustes. Kaasatud molekulaarsete mehhanismide selgitamiseks on vaja rohkem uuringuid.

Teisest küljest on hästi teada, et HPV onkoproteiinid E6 ja E7 kahjustavad apoptoosiprotsessi ja seega ka antigeenide vabanemist, suunates sihikule rakulised faktorid ja teatud molekulid, mis osalevad apoptoosi aktiveerimises, näiteks: p53 kasvaja supressorvalk. 61], tuumori nekroosifaktor (TNF) ja TNF-iga seotud apoptoosi indutseeriv ligand (TRAIL) [62]; miR-21 ja miR-27b, mis on suunatud vastavalt TNF-alfa- ja polo-sarnasele kinaasile 2 (PLK2), et pärssida apoptoosi [63,64]; ja lncRNA CRNDE, mis on seotud rakkude ellujäämisega p53 raja kaudu [65, 66].
Vaatamata sellele, et defektset apoptoosi seostatakse immuunvastuse nõrgenemisega, kuna immuunrakkudele esitatavate antigeenide kogus on väiksem, tuleb seda väidet hoolikalt analüüsida. Praegu näitavad tõendid, et apoptoos võib toimida immunosupressiivse või immunostimuleeriva signaalina. Seetõttu tuleks arvesse võtta selliseid muutujaid nagu etapid ja apoptoosi aktiveerimise ja mikrokeskkonna stiimulitega seotud mehhanismid [67].
For more information:1950477648nn@gmail.com
