2. Suhkur või rasv? Neerutuubulite ainevahetus, mida käsitletakse ajakirjas Tervis ja haigused
Apr 17, 2023
Vigastatud neeru ainevahetus
Nagu eelnevalt mainitud, on proksimaalne tuubul lahustunud aine reabsorptsiooni alustala ja rohked mitokondrid on vajalikud lahustunud aine koormuse taaskasutamiseks vajalike transporterite toetamiseks vajaliku ATP tootmiseks. ATP tootmine mitokondriaalsete ETC-de poolt nõuab hapnikku. Seetõttu on torukujulistel segmentidel, eriti proksimaalsetel tuubulitel, suur hapnikuvajadus, mistõttu need rakud on vastuvõtlikud neerukahjustusele. Proksimaalse tuubuli S3 segment on vigastuste suhtes eriti vastuvõtlik, kuna see asub sügaval neerus ning sellel on madal verevool ja hapnikupinge. Hemodünaamiliste häirete (nt sepsis ja kehaväline vereringe) põhjustatud hapnikuvarustuse halvenemine on paljude neerukahjustuste põhitunnus ning see põhjustab tubulaarset hüpoksiat ja funktsiooni halvenemist. Transportervalkude kõrge ekspressioon proksimaalses tuubulis muudab selle torukujulise segmendi haavatavaks ka toksiinide (nt elavhõbe, plii ja aristolochhape) või ravimite (nt aminoglükosiidid) põhjustatud vigastuste suhtes. Vigastus võib tekkida ägeda neerukahjustusena (AKI) või kroonilise neeruhaigusena (CKD), kui vigastus on tekkinud, näiteks hüpertensiooni või diabeedi korral. Kliinilises praktikas on AKI-ga patsientidel palju suurem risk kroonilise neeruhaiguse tekkeks ja kroonilise neeruhaigusega patsientidel on suurem tõenäosus AKI tekkeks, mis viitab sellele, et need kaks protsessi on omavahel seotud. Siiski võib AKI-st taastumise ajal esineda olulisi erinevusi neerude toiteväärtuses võrreldes kroonilise neeruhaigusega. Seetõttu vaadatakse AKI ja CKD metabolismi käsitlev kirjandus eraldi üle.
Neerutuubulite ainevahetus AKI-s
Ägedalt vigastatud neerutuubulid võivad läbida apoptootilise või nekrootilise surma või võivad muutuda integriini ekspressioonist tingitud vähenenud adhesioonide tõttu. Ümbritsevad epiteelirakud dediferentseeruvad, migreeruvad ja vohavad, et parandada kahjustatud torukujulist epiteeli. Kuidas need ellujäänud epiteelirakud reageerivad, võib määrata, kas neer paraneb edukalt või progresseerub tubulointerstitsiaalseks fibroosiks.
AKI ja anaeroobne glükolüüs
On kindlaid tõendeid selle kohta, et FAO, eelistatud metaboolne rada energia tootmiseks proksimaalses tuubulis, on AKI-s inhibeeritud, soodustades glükoosi metabolismi laktaadiks (joonis 3). Glükolüüs viitab tehniliselt glükoosi metabolismile püruvaadiks ja terminit "anaeroobne glükolüüs" kasutatakse siin selleks, et tähistada glükoosi metabolismi püruvaadiks, millele järgneb laktaadi, erinevalt glükoosi oksüdatsioonist (glükoos metaboliseerub püruvaadiks ja siseneb seejärel TCA tsüklisse ). Elavhõbekloriidist põhjustatud AKI rottidel on kirjeldatud ka suurenenud glükoosi omastamist ja anaeroobset glükolüüsi. Isheemia-reperfusioonikahjustus (IRI) suurendab laktaadi ja püruvaadi taset vigastatud neerus ning suurendab glükolüütiliste ensüümide, nagu heksokinaas 2, ekspressiooni. Need muutused ilmnevad dediferentseerunud tuubulis varakult, kuid hüpoksia tunnused jäävad atroofiliste tuubulite hilises staadiumis. Seega esineb glükolüütiline metabolism püsivalt vigastatud dediferentseerunud tuubulites. Siiski on ebaselge, kas glükolüüs on mehhanism, mis vastutab tuubulite taastumise ebaõnnestumise eest või peegeldab see lihtsalt püsivat vigastust.
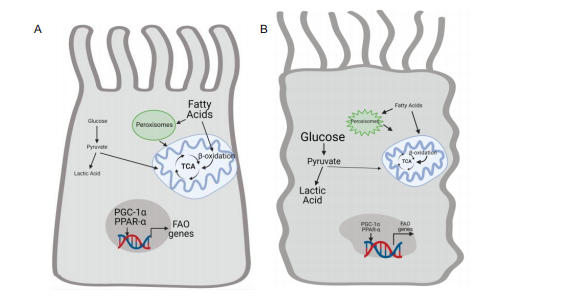
Joonis 3. Neerukahjustus muudab proksimaalsete tuubulite rakkude metabolismi, pärssides rasvhapete oksüdatsiooni ja suurendades anaeroobset glükolüüsi. (A) Terved proksimaalsed tuubulite (PT) rakud sõltuvad ATP tekitamiseks rasvhapete oksüdatsiooni kasutamisest peroksisoomide ja mitokondrite poolt. Transkriptsioonifaktorid, nagu PCG-1 ja PPAR-a, suurendavad mitokondriaalset biogeneesi ja rasvhapete oksüdatsiooniga seotud geenide ekspressiooni. Vastupidi, glükolüüs ei ole vigastamata proksimaalses tuubulis suur energiaallikas. Neerukahjustus kahjustab mitokondriaalset funktsiooni ja vähendab PGC-a ja PPAR-a (B) ekspressiooni. Seetõttu rasvhapete oksüdatsioon väheneb ja vigastatud PT-rakud sõltuvad energiavajaduste rahuldamiseks glükolüüsist. Anaeroobne glükolüüs põhjustab piimhappe taseme tõusu. Loonud BioRender.com.
AKI jaGlükoosi oksüdatsioon
On kindlaid tõendeid selle kohta, et neerutuubulite glükoosi oksüdatsiooni rolli AkI-s ei ole uuritud nii palju kui glükolüüsi proksimaalsetes tuubulites, mis toodavad neerutuubuleid. Glükoosi oksüdatsiooni soodustab püruvaadi dehüdrogenaas (PDH), mis muudab püruvaadi atsetüülkoensüümiks a, mis siseneb TCA tsüklisse, moodustades tsitraadi. pDH-d saab inhibeerida püruvaatdehüdrogenaasi kinaaside (PDK) fosforüülimisega S232, S293 ja S300 saitidel. Hüpoksia blokeeris PDH, indutseerides PDK-sid. 7 päeva pärast IRI-d suurenes neerutuubulites PDH Ela subühikute inhibeeriv fosforüülimine, mis püsis kuni 14 päeva ja millega kaasnes tubulaarne atroofia, suurenenud glükolüütilise ensüümi ekspressioon ja laktaadi akumuleerumine. See viitab sellele, et hüpoksiaga kahjustatud tuubulites glükoosi metabolismist põhjustatud kõrgenenud püruvaat toodab laktaati ilma TCA tsüklisse sisenemata. Plaatina (kemoterapeutiline aine, mida sageli piiratakse nefrotoksilisuse tõttu) suurendab ka PDH fosforüülimist, vähendades samal ajal neerufunktsiooni. PDK inhibiitor dikloroatsetaat (DCA) leevendab tsisplatiinist põhjustatud neerukahjustust, vähendab tubulaarset apoptoosi ja takistab inhibeerivat PDH fosforüülimist. Seega võivad jõupingutused suurendada püruvaadi sisenemist TCA tsüklisse või glükoosi oksüdatsiooni olla neerude jaoks kaitsvad.
Kuid DCA suurendas ka peroksisoomi proliferaatoriga aktiveeritud retseptorit (PPAR-), mis on FAO regulaator, nii et kasulikud mõjud võivad olla tingitud ka nendest metaboolsetest muutustest.

Selle kohta lisateabe saamiseks klõpsake siinCistanche mõju neerudele
AKI, mitokondriaalne vigastus ja rasvhapete oksüdatsioon
Mitokondriaalne kahjustus on AKI oluline tunnus ja on tihedalt seotud ainevahetusega. Rasvhapetest energia tootmise viimane etapp hõlmab mitokondriaalset ETC-d ja NAD pluss regenereerimist selle redutseeritud vormist NADH. Seega vähendab kahjustatud mitokondrites kahjustatud ETC funktsioon NAD pluss , mis on vajalik glükolüüsiks ja rasvhapete või glükoosi oksüdatsioonist tingitud püsivaks ATP tootmiseks. AKI loommudelid näitavad mitokondrite struktuurseid ja funktsionaalseid kahjustusi, mida tõendavad turse ja killustumine, samuti ETC valgu kadu ja vähenenud ATP tootmine. AKI-indutseeritud mitokondriaalset düsfunktsiooni soodustavad mitmed tegurid. Hüpoksia, AKI tavaline tunnus, põhjustab reaktiivsete hapnikuliikide (ROS) suurenenud akumuleerumist, mis võib inhibeerida ETC ensüüme. AKI-s on mitokondriaalse fusiooni ja lõhustumise tasakaal häiritud, mis viib mitokondriaalse killustumiseni, mis muudab rakud sensibiliseerivaks apoptoosi suhtes. Lisaks näitavad AKI sepsisemudelid mitokondriaalse biogeneesi indutseerija PPAR koaktivaatori-1 (PGC-1) vähenenud ekspressiooni. PGC-1 inhibeerimist seostatakse sarnasel määral vähenenud neerufunktsiooniga. ja suurenenud mitokondriaalne kahjustus. PGC-1 geneetiline deletsioon neerutuubulites süvendas endotoksiini poolt indutseeritud AKI-d, samas kui PGC-1 üleekspressioon kaitses isheemilise neerukahjustuse eest. Kokkuvõtteks võib öelda, et AKI hüpoksiline keskkond ja raku reaktsioon nendele vigastustele põhjustavad mitokondriaalse funktsiooni halvenemist. Lisaks võib mitokondriaalse biogeneesi taastamine PGC-1 abil parandada vastust AKI-le.
Mitokondrid on vajalikud ATP tekkeks rasvhapete metabolismi kaudu, seega aitab AKI-indutseeritud mitokondriaalne düsfunktsioon kaasa FAO halvenemisele. pGC-1 aktiivsus võib suurendada rakuhingamist, kuna PGC-1 üleekspresseerivad proksimaalsed tuubulid in vitro katsetes nõrgendasid TNF- --indutseeritud basaalhingamise pärssimist. Nagu eespool mainitud, vähendatakse AKI-s NAD pluss tasemeid, mis on FAO jaoks olulised. Suurenenud NAD pluss ammendumine torukujuliste PARP-ide kaudu aitab vähendada NAD pluss:NADH näriliste isheemilise vigastuse ajal. lisaks näitasid vikerkesta vigastatud hiirte uriiniga läbiviidud metaboolsed uuringud ekspressiooni ja NAD pluss NAD pluss biosünteesiga seotud ensüümide taseme halvenemist. Kuid PGC-1 üleekspressioon indutseeris NAD pluss biosünteesi ja päästis NAD plussi tasemed, mis viitab sellele, et PGC-1 kahjustus AKI-s võib NAD plussi tasemeid vähendades soodustada edasisi vigastusi. Lisaks seostati rasvhapete metabolismi halvenemist pärast IRI-d FAO kiirust piirava ensüümi CPT1 aktiivsuse vähenemisega. CPT1 suurendamine sünteetilise ühendiga C75, rasvhapete süntaasi inhibiitor, leevendab näriliste neerukahjustusi. Andmed inhibiitorite kohta tuleb kinnitada geneetiliste meetoditega, kuid need andmed viitavad sellele, et FAO kahjustus võib põhjustada, mitte ainult peegeldada neerukahjustust.
Hiljutised uuringud näitavad, et peroksisoom võib samuti mängida rolli neeruvastuses AKI-le, eriti isheemilisele AKI-le. Peroksisoom oksüdeerib eelistatavalt VLCFA-d, protsessi, mis tekitab vesinikperoksiidi (H2O2) ja vajab H2O2 metabolismiks suures koguses katalaasi. Seega võivad peroksisoomid olla olulised mitokondriaalse FAO toetamisel ja reaktiivsete hapnikuliikide (ROS) eemaldamisel, mis mõlemad on AKI-s reguleerimata. Peroksisomaalset FAO-d mõõdeti VLCFA lignokaiini oksüdatsiooniga ja selle vähenemine oli proportsionaalne isheemia kestusega. Isheemilise ja tsisplatiini poolt indutseeritud AKI korral oli peroksisoomi lokaliseeritud deatsetülaasi sirtuiini 5 deletsioon kaitsev, vähendades mitokondreid, kuid suurendades peroksisomaalset FAO-d. Tsisplatiini kahjustuse mudelis nõrgendas ravi PPAR-ligand betaiiniga neerukahjustusi ja suurendas peroksisomaalse valgu ekspressiooni. Kuigi need andmed toetavad peroksisoomide kaitsvat rolli AKI-s, on vaja täiendavaid uuringuid, mis mõjutavad otsesemalt peroksisoomi funktsiooni, et paremini teha kindlaks, kas peroksisoomi suurenemine FAO kaitseb AKI eest.
Kokkuvõttes näitavad need andmed, et äge neerukahjustus pärsib rasvhapete ja glükoosi oksüdatsiooni, vähendab mitokondriaalset funktsiooni ja suurendab glükolüüsi, mis viib laktaadi tekkeni (joonis 3). Püüdlused suurendada mitokondriaalset biogeneesi ja funktsiooni või soodustada rasvhapete ja glükoosi oksüdatsiooni neerutuubulites võivad parandada tubulite vigastusi ja neerufunktsiooni.

Standardiseeritud Cistanche
Neerutuubulite ainevahetus kroonilise neeruhaiguse korral
CKD ja rasvhapete oksüdatsioon
Neerude metabolism on kroonilise neeruhaigusega patsientidel oluliselt reguleerimata. Diabeedi ja hüpertensiivse kroonilise neeruhaigusega patsientide mikrodissekteeritud torukujuliste interstitsiaalsete proovide erapooletu transkriptoomika näitas rasvhapete, glükoosi ja aminohapete metabolismiga seotud geenide ekspressiooni vähenemist. Kuigi kõik metaboolsed teed olid mõjutatud, oli rasvhapete metabolismiga seotud ensüümide ekspressioon eriti alareguleeritud. Täpsemalt vähenes peamiste FAO regulaatorite Cpt1a ja Ppara geeniekspressioon nii inimese kui ka hiire CKD mudelites. Teises uuringus vähenes CPT1A tase inimese tuubulites glomerulaarfiltratsiooni kiiruse (eGFR) (neerufunktsiooni näitaja) languse ja fibroosisageduse suurenemisega. Teisel CKD-ga patsientide rühmal oli suurenenud lühikese ja keskmise ahelaga atsüülkarnitiinide kogunemine ja vähenenud eGFR, kuid CPT1a poolt transporditud pika ahelaga atsüülkarnitiinide hulk ei muutunud. FAO blokeerimine neerutuubulites in vitro, kasutades etomoksiiri või ranolasiini, põhjustas rakusurma ja dediferentseerumise kõrgema taseme. Dediferentseerunud neerutuubulaarrakud aitavad kaasa tubulointerstitsiaalse fibroosi progresseerumisele. mehhanism, mille abil vähendatud FAO põhjustab tubulaarset dediferentseerumist, ei ole täielikult teada, kuid Cpt1a pärssimine kultiveeritud endoteelirakkudes viib dediferentseerumiseni Smad7/TGF{8}}sõltuva raja kaudu.
AKI põhjustab mitokondriaalseid kahjustusi ja vähendab FAO-d ning püüded vähendada mitokondriaalseid kahjustusi või optimeerida rasvhapete metabolismi on parandanud reageerimist AKI-le, nagu eelnevalt kirjeldatud. Üha enam on tõendeid selle kohta, et tõhustatud mitokondriaalne biogenees ja/või FAO võivad olla kasulikud ka kroonilise neeruhaiguse kontekstis. ppargc1a on Cpt1a tugev indutseerija ja selle geeni üleekspressioon neerutuubulites vähendab folaadi poolt indutseeritud tubulaarset apoptoosi. Farmakoloogiline sekkumine fenofibraadi ja etomoksiiriga, et aktiveerida vastavalt PPAR või blokeerida CPT1, viidi läbi ühepoolse ureetra obstruktsiooni (UUO) mudelis, kus kusejuha ligeerimine põhjustas vasturõhust ja põletikust tingitud neerufibroosi kiire arengu 5-7 päeva jooksul . Kuigi hiljuti on teatatud etomoksiiri kõrvalmõjudest, viitavad need andmed sellele, et FAO suurendamine neerutuubulites Cpt1a või Ppara abil võib parandada vastust neerukahjustusele.
Hiljuti takistas Cpt1a geeni üleekspressioon neerutuubulites kolme kroonilise neeruhaiguse hiire mudelit: foolhappe nefropaatiat, UUO ja adeniinist põhjustatud nefrotoksilisust. Foolhappe nefropaatia koosneb foolhappe ühekordsest süstimisest, mis viib torukujulise kristalliseerumiseni, mille tulemuseks on tubulaarne interstitsiaalne fibroos. Mitu nädalat dieediga manustatud adeniin kutsus esile ka tubulaarsete kristallide ladestumise ja fibroosi. cpt1a üleekspressioon parandas mitokondriaalset morfoloogiat ja ATP tootmist pärast folaadi nefropaatiat lisaks FAO päästmisele isoleeritud kudedes, mõõdetuna [14C] palmitaadi uuringutega. Need elegantsed uuringud viitavad kindlalt sellele, et inhibeeritud FAO mängib tubulointerstitsiaalse fibroosi progresseerumisel patogeenset rolli.
CKD mudelid ja rasvhapete oksüdatsioon
Ükski näriliste kroonilise neeruhaiguse mudel ei suuda täiuslikult reprodutseerida inimese kroonilist neeruhaigust. paljudel sageli kasutatavatel kroonilise neeruhaiguse mudelitel on esialgne AKI komponent (nt IRI, folaatnefropaatia ja aristolochic acid nefropaatia) ning FAO mõju AKI-le võib määrata kroonilise neeruhaiguse progresseerumise. Paljudes FAO ja kroonilise neeruhaigusega seotud uuringutes on kasutatud foolhappemudeleid, mis tõstatab küsimuse: mil määral on FAO kaitsev toime tingitud tema rollist vigastuse ägedas faasis? Üks uuring näitas, et Cpt1a üleekspressiooni kaitsev toime püsis isegi pärast vigastusest põhjustatud rekombinatsiooni, mis viitab sellele, et FAO võib toimida pärast ägedat vigastust. Kuid üks päev pärast foolhappe süstimist manustati doksütsükliini indutseeritavatele Cpt1a üleekspresseerivatele hiirtele, mis tõstatas küsimuse, kas Cpt1a reguleerib vigastuse ägedat faasi. UUO mudel on klassikaline tubulointerstitsiaalse fibroosi mudel, mis sobib paremini kiiresti progresseeruva fibroosi esilekutsumiseks kui epiteeli vigastuse ja paranemise hindamiseks. Avaldatud uuringud viitavad julgustavalt sellele, et suurenenud FAO võib kaitsta kroonilise neeruhaiguse eest, kuid tulevased uuringud peaksid uurima ka FAO rolli progressiivsemates mudelites, mis kajastavad hüpertensiivset nefroskleroosi ja/või diabeetilist nefropaatiat, mis on kaks peamist lõppstaadiumis neeruhaiguse põhjust.

Cistanche Tubulosa
Rasvhapete oksüdatsioon ja tubulointerstitsiaalne fibroos
Mitmed mehhanismid viitavad sellele, et FAO suurendamine võib vähendada tubulointerstitsiaalset fibroosi. Inimese kroonilise neeruhaiguse tunnuseks on lipiidide akumuleerumine neerudes kas metabolismi vähenemise, suurenenud omastamise või sünteesi suurenemise kaudu. Lisaks lipiidide metabolismi alareguleerimisele on CKD-s ülesreguleeritud rasvhapperetseptori CD36 ekspressioon. CD36 geen või farmakoloogiline inhibeerimine hiirtel kaitseb hüpertensiivsete CKD mudelite eest. Mitmed uurimisrühmad on teinud ettepaneku, et liigsed lipiidid neerudes soodustavad kroonilise neeruhaiguse progresseerumist põletiku, oksüdatiivse stressi ja endoplasmaatilise retikulumi (ER) stressi kaudu. Kooskõlas sellega olid kõrge rasvasisaldusega dieedil CD36 puudulikkusega hiired kaitstud ka UUO-indutseeritud neerukahjustuse eest, kuna põletikku (nt NF-κB) ja oksüdatiivset stressi vahendavad pärsitud teed. Hiirtel, kellel puudus proksimaalne tubulaarne karnitiini atsetüültransferaas, ensüüm, mis ekspordib mitokondritest liigseid atsüülkoensüümi tooteid, tekkis spontaanselt apoptoos, fibroos ja suurenenud oksüdatiivne stress. Neid leide kiirendas kõrge rasvasisaldusega dieet ja need olid seotud mitokondrite funktsiooni halvenemisega. Kuid CD36 üleekspressioon, suurendades samal ajal neerutuubulite rasvhapete akumuleerumist, ei avaldanud olulist mõju streptozototsiini põhjustatud vigastusele, I tüüpi diabeedi mudelile ega foolhappe nefropaatiast põhjustatud fibroosile. On kindlaid tõendeid, mis toetavad CD36 ja lipotoksilisuse rolli kroonilise neeruhaiguse progresseerumisel, kuid täpne panus võib sõltuda vigastusmudelist ja muudest modifitseerivatest teguritest (nt dieet).
Teine oletatav mehhanism, mille abil CPT1a ja FAO võivad fibroosi vähendada, on läbi TGF-i signaaliülekanderaja. Nagu eespool mainitud, on endoteelirakkudel, millel puudub Cpt1a, suurenenud diferentseerumine TGF- / Smad7 raja kaudu. Sarnaselt näitasid Cpt1a üleekspresseerivate hiirte primaarsed neerutuubulakud vastusena TGF-le - 1 nõrgenenud dediferentseerumist. Need in vitro andmed tuleb in vivo valideerida ja küsimus, kas need CPT1a mõjud sõltuvad FAO-st, jääb alles.
Vähendatud FAO võib samuti soodustada tubulaarset atroofiat ATP tootmise halvenemise tõttu, mis on tubulaarse interstitsiaalse fibroosi komponent. Etomoksiirist sõltuv FAO inhibeerimine tuubulite rakkudes in vitro pärsib ATP tootmist ja suurendab apoptoosi. See viitab sellele, et FAO vähenemine võib ATP tootmise halvenemise tõttu põhjustada rakusurma. Neerutuubulites parandas Cpt1a suurendamine EM-i kaudu mitokondriaalset morfoloogiat, mis viitab sellele, et FAO suurendamine võib samuti avaldada kaitsvat toimet, parandades mitokondriaalset funktsiooni. Seega võib FAO vähendada tubulaarseid vigastusi ja tubulointerstitsiaalset progresseerumist, vähendades lipotoksilisusest põhjustatud oksüdatiivset stressi ja põletikku, vähendades tubulaarset TGF-i signaaliülekannet ja parandades tubulaarset ellujäämist paranenud ATP tootmise ja mitokondriaalse funktsiooni kaudu. Kuid seos FAO ja tubulointerstitsiaalse fibroosi vahel kroonilise neeruhaiguse korral nõuab täiendavaid uuringuid nende võimalike mehhanismide kinnitamiseks.
CKD ja anaeroobne glükolüüs
Anaeroobse glükolüüsiga seotud ensüümide hulk suureneb nii kroonilise neeruhaiguse inim- kui ka loomamudelites. See pole üllatav, kuna mitokondriaalsed kahjustused on kroonilise neeruhaiguse lahutamatu osa ja laktaadi tootmist põhjustav glükolüüs võib toota ATP-d, ilma et oleks vaja toimivaid mitokondreid. Glükolüüsi roll kroonilise neeruhaiguse progresseerumisel on ebaselge. UUO mudelis vähendab glükolüüsi inhibeerimine 2-desoksüglükoosiga ja lentiviiruse PKM2 RNAi süstimine või sümosaanravi nii fibroosi kui ka müofibroblastide aktivatsiooni. Arvatakse, et seda mehhanismi vahendavad neerufibroblastid (NRK-49F), suurenenud laktaadisisaldus neerufibroblastides ja müofibroblastide aktivatsioon (suurenenud fibronektiini ekspressioon, -SMA ja proliferatsioonimarker PCNA) pärast PKM2-ravi. Teine rühm kasutas UUO-ga vigastatud hiirtel ka purpurset ja teatas vähenenud fibroosist ja tubulaarsest apoptoosist, kuigi in vitro mõju strooma tootmisele ilmnes ainult fibroblastides, mitte epiteelirakkudes. Need uuringud viitavad sellele, et glükolüüsi blokeerimine takistab UUO mudelis fibroosi, kuigi kasulik mõju näib olevat vahendatud peamiselt fibroblastide, mitte tuubulirakkude kaudu.

Herba CistanchejaCistanche ekstrakt
Teised uuringud näitavad, et anaeroobne glükolüüs võib kroonilise neeruhaiguse korral olla kahjutu. Vastupidiselt PKM-i blokeerimise kaitsvale toimele AKI-le vähendas PKM-i aktivaator TEPP-46 streptozototsiiniga ravitud hiirte tuubulites fibronektiini ja teiste maatriksiga seotud geenide ekspressiooni. TEPP-46 parandas ka podotsüütide vigastusi ja basaalmembraani paksust, nii et torukeste kaitse võib olla tingitud glomerulaarsete vigastuste ja proteinuuria vähenemisest, mitte otseselt tubulaarsest glükolüüsist. Teises uuringus kasutati uudset geneetilist lähenemisviisi, et uurida glükolüüsi rolli neerukahjustuses. Transgeensetel hiirtel, kelle glükolüütilise võtmeensüümi 6-fosfoglükoosi-2 kinaasi/fruktoosi-2, 6-bisfosfataasi (PFKFB2) inaktiveerimisel olid punktmutatsioonid, oli glükolüütiline võime vähenenud. Need vähendatud glükolüüsiga transgeensed hiired ei olnud kaitstud UUO või folaadi poolt indutseeritud fibroosi eest, mis süvenes UUO vigastusega transgeensetel hiirtel. UUO mudel on suunatud distaalsetele tuubulitele ja kuigi mitte ainult, on distaalsed tuubulid kalduvamad metabolismi glükolüüsile, nii et proksimaalsem tuubulispetsiifilisem vigastus võib anda teistsuguse tulemuse. Teine võimalus on see, et teatud glükolüütilised võimed võivad olla vigastusreaktsiooni jaoks olulised. Kui vigastus on piisavalt tõsine, võib vaja minna glükolüüsi, et ajutiselt toota energiat kuni paranemiseni. Tulevased uuringud peaksid uurima, kas glükolüütilise võime blokeerimine pärast esialgset neerukahjustust võib vähendada tubulointerstitsiaalse fibroosi progresseerumist.
Viited
1. Coca, SG; Singanamala, S.; Parikh, CR Krooniline neeruhaigus pärast ägedat neerukahjustust: süstemaatiline ülevaade ja metaanalüüs. Kidney Int. 2012, 81, 442–448.
2. Bonventre, JV Isheemilise ägeda neerupuudulikkuse mehhanismid. Kidney Int. 1993, 43, 1160–1178.
3. Ash, SR; Cuppage, FE Nihe anaeroobse glükolüüsi poole regenereeruvas roti neerus. Olen. J. Pathol. 1970, 60, 385–402.
4. Lan, R.; Geng, H.; Singha, PK; Saikumar, P.; Bottinger, EP; Weinberg, JM; Venkatachalam, MA Mitokondriaalne patoloogia ja glükolüütiline nihe proksimaalse tuubuli atroofia ajal pärast isheemilist AKI-d. J. Am. Soc. Nephrol. 2016, 27, 3356–3367.
5. Eklund, T.; Wahlberg, J.; Ungerstedt, U.; Hillered, L. Interstitsiaalne laktaat, inosiin ja hüpoksantiin roti neerudes normotermilise isheemia ja retsirkulatsiooni ajal. Acta Physiol. Scand. 1991, 143, 279–286.
6. Zhou, HL; Zhang, R.; Anand, P.; Stomberski, CT; Qian, Z.; Hausladen, A.; Wang, L.; Rhee, EP; Parikh, SM; Karumanchi, SA; et al. Metaboolne ümberprogrammeerimine S-nitroso-CoA reduktaasi süsteemi poolt kaitseb neerukahjustuste eest. Loodus 2019, 565, 96–100.
7. Devalaradža-Narašimha, K.; Padanilam, BJ PARP-1 Inhibeerib glükolüüsi isheemilistes neerudes. J. Am. Soc. Nephrol. 2008, 20, 95–103.
8. Kim, J.; Devalaraja-Narashimha, K.; Padanilam, BJ TIGAR reguleerib glükolüüsi isheemilistes neerude proksimaalsetes tuubulites. Olen. J. Physiol. Physiol. 2015, 308, F298–F308.
9. Kim, JW; Tšernõšjov, I.; Semenza, GL; Dang, CV HIF-1-vahendatud püruvaatdehüdrogenaasi kinaasi ekspressioon: metaboolne lüliti, mis on vajalik raku hüpoksiaga kohanemiseks. Lahtri metab. 2006, 3, 177–185.
10. Lu, C.-W.; Lin, S.-C.; Chen, K.-F.; Lai, Y.-Y.; Tsai, S.-J. Püruvaatdehüdrogenaasi kinaasi-3 indutseerimine hüpoksiaga indutseeritava faktoriga-1 soodustab ainevahetust ja ravimiresistentsust. J. Biol. Chem. 2008, 283, 28106–28114.
11. Galgamuwa, R.; Hardy, K.; Dahlstrom, JE; Blackburn, AC; Wium, E.; Rooke, M.; Cappello, JY; Tummala, P.; Patel, HR; Chuah, A.; et al. Dikloroatsetaat hoiab ära tsisplatiinist põhjustatud nefrotoksilisuse, kahjustamata tsisplatiini vähivastaseid omadusi. J. Am. Soc. Nephrol. 2016, 27, 3331–3344.
12. Funk, JA; Schnellmann, RG Mitokondriaalse homöostaasi püsiv häire pärast ägedat neerukahjustust. Olen. J. Physiol. Physiol. 2012, 302, F853–F864.
13. Emma, F.; Montini, G.; Parikh, SM; Salviati, L. Mitokondriaalne düsfunktsioon päriliku neeruhaiguse ja ägeda neerukahjustuse korral. Nat. Rev. Nephrol. 2016, 12, 267–280.
14. Che, R.; Yuan, Y.; Huang, S.; Zhang, A. Mitokondriaalne düsfunktsioon neeruhaiguste patofüsioloogias. Olen. J. Physiol. Neerud. Physiol. 2014, 306, F367–F378.
15. Brooks, C.; Wei, Q.; Cho, SG; Dong, Z. Mitokondriaalse dünaamika reguleerimine ägeda neerukahjustuse korral rakukultuuris ja näriliste mudelites. J. Clin. Uurige. 2009, 119, 1275–1285.
16. Tran, M.; Tam, D.; Bardia, A.; Bhasin, M.; Rowe, GC; Kher, A.; Zsengeller, ZK; Akhavan-Sharif, MR; Hankin, EV; Saintgeniez, M.; et al. PGC-1 soodustab taastumist pärast ägedat neerukahjustust hiirte süsteemse põletiku ajal. J. Clin. Uurige. 2011, 121, 4003–4014.
17. Tran, MT; Zsengeller, ZK; Berg, ZKZAH; Hankin, EV; Bhasin, MK; Kim, W.; Clish, CB; Stillman, AHBIE; Karumanchi, SA; Rhee, CBCEP; et al. PGC1 juhib NAD biosünteesi, ühendades oksüdatiivse metabolismi neerude kaitsega. Nat. Cell Biol. 2016, 531, 528–532.
18. Martin, DR; Lewington, AJ; Hammerman, MR; Padanilam, BJ Polü(ADP-riboosi) polümeraasi inhibeerimine nõrgendab rottidel keemilist neerukahjustust. Olen. J. Physiol. Regul. Integr. Comp. Physiol. 2000, 279, R1834–1840.
19. Idrovo, JP; Yang, WL; Nicastro, J.; Coppa, GF; Wang, P. Karnitiini palmitoüültransferaasi 1 stimuleerimine parandab neerufunktsiooni ja nõrgendab koekahjustusi pärast isheemiat/reperfusiooni. J. Surg. Res. 2012, 177, 157–164.
20. Gulati, S.; Singh, AK; Irazu, C.; Orak, J.; Rajagopalan, PR; Fitts, CT; Singh, I. Isheemia-reperfusioonikahjustus: biokeemilised muutused roti neeru peroksisoomides. Arch. Biochem. Biophys. 1992, 295, 90–100.
21. Chiba, T.; Peasley, KD; Cargill, KR; Maringer, KV; Bharathi, SS; Mukherjee, E.; Zhang, Y.; Holtz, A.; Basisty, N.; Yagobian, SD; et al. Sirtuin 5 reguleerib proksimaalse tuubuli rasvhapete oksüdatsiooni, et kaitsta AKI eest. J. Am. Soc. Nephrol. 2019, 30, 2384–2398.
22. Negishi, K.; Noiri, E.; Sugaya, T.; Li, S.; Megyesi, J.; Nagothu, K.; Portilla, D. Maksa rasvhappeid siduva valgu roll tsisplatiin-tina-indutseeritud ägeda neerupuudulikkuse korral. Kidney Int. 2007, 72, 348–358.
23. Kang, HM; Ahn, SH; Choi, P.; Ko, Y.-A.; Han, SH; Chinga, F.; Park, ASD; Tao, J.; Sharma, K.; Pullman, J.; et al. Defektsel rasvhapete oksüdatsioonil neerutuubulite epiteelirakkudes on neerufibroosi arengus võtmeroll. Nat. Med. 2015, 21, 37–46.
24. Miguel, V.; Tituana, J.; Herrero, JI; Herrero, L.; Serra, D.; Cuevas-Delgado, P.; Barbas, C.; Rodriguez-Puyol, D.; Marquez Exposito, L.; Ruiz-Ortega, M.; et al. Neerutuubulite Cpt1a üleekspressioon kaitseb neerufibroosi eest, taastades mitokondriaalse homöostaasi. J. Clin. Uurige. 2021. aasta.
25. Lovisa, S.; LeBleu, VS; Tampe, B.; Sugimoto, H.; Vadnagara, K.; Carstens, JL; Wu, C.-C.; Hagos, Y.; Burckhardt, eKr; Pentcheva Hoang, T.; et al. Epiteel-mesenhümaalne üleminek kutsub esile rakutsükli seiskumise ja parenhüümi kahjustuse neerufibroosi korral. Nat. Med. 2015, 21, 998–1009.
26. Grande, MT; Sanchez-Laorden, B.; Lopez-Blau, C.; De Frutos, CA; Boutet, A.; Arevalo, M.; Rowe, RG; Weiss, SJ; Lopez-Novoa, JM; Nieto, MA Snail1-indutseeritud osaline epiteeli-mesenhümaalne üleminek põhjustab hiirtel neerufibroosi ja võib olla suunatud väljakujunenud haiguse tagasipööramisele. Nat. Med. 2015, 21, 989–997.
27. Xiong, J.; Kawagishi, H.; Yan, Y.; Liu, J.; Wells, QS; Edmunds, LR; Fergusson, MM; Yu, Z.-X.; Rovira, II; Brittain, EL; et al. Endoteeli-mesenhümaalseks ülemineku metaboolne alus. Mol. Cell 2018, 69, 689–698.e7.
28. O'Connor, RS; Guo, L.; Ghassemi, S.; Snyder, NW; Worth, AJ; Weng, L.; Kam, Y.; Philipson, B.; Trefely, S.; Nunez-Cruz, S.; et al. CPT1a inhibiitor etomoksiir kutsub tavaliselt kasutatavates kontsentratsioonides esile tõsise oksüdatiivse stressi. Sci. Vabariik 2018, 8, 6289.
29. Hua, W.; Huang, H.-Z.; Tan, L.-T.; Wan, J.-M.; Gui, H.-B.; Zhao, L.; Ruan, X.-Z.; Chen, X.-M.; Du, X.-G. CD36 vahendatud rasvhapete poolt indutseeritud podotsüütide apoptoos oksüdatiivse stressi kaudu. PLoS ONE 2015, 10, e0127507.
30. Herman-Edelstein, M.; Scherzer, P.; Tobar, A.; Levi, M.; Gafter, U. Muutunud neerulipiidide metabolism ja neerulipiidide akumulatsioon inimese diabeetilise nefropaatia korral. J. Lipid Res. 2014, 55, 561–572.
31. Yang, X.; Okamura, DM; Lu, X.; Chen, Y.; Moorhead, J.; Varghese, Z.; Ruan, XZ CD36 kroonilise neeruhaiguse korral: uudsed teadmised ja ravivõimalused. Nat. Rev. Nephrol. 2017, 13, 769–781.
32. Souza, AKV; Botšarov, AV; Baranova, IN; Višnjakova, TG; Huang, YG; Wilkins, KJ; Hu, X.; tänav, JM; Alvarez-Prats, A.; Mullick, AE; et al. Püüdja retseptori CD36 antagonism 5A peptiidi poolt hoiab ära kroonilise neeruhaiguse progresseerumise hiirtel, sõltumata vererõhu reguleerimisest. Kidney Int. 2016, 89, 809–822.
33. Moorhead, JF; Chan, MK; El-Nahas, M.; Varghese, Z. Lipiidide nefrotoksilisus kroonilise progresseeruva glomerulaar- ja tubulointerstitsiaalse haiguse korral. Lancet 1982, 2, 1309–1311.
34. Ruan, XZ; Varghese, Z.; Moorhead, JF Lipiidide nefrotoksilisuse hüpoteesi värskendus. Nat. Rev. Nephrol. 2009, 5, 713–721.
35. Okamura, DM; Pennathur, S.; Pasichnyk, K.; López-Guisa, JM; Collins, S.; Febbraio, M.; Heinecke, J.; Eddy, AA CD36 reguleerib oksüdatiivset stressi ja põletikku hüperkolesteroleemilise kroonilise neeruhaiguse korral. J. Am. Soc. Nephrol. 2009, 20, 495–505.
36. Kruger, C.; Nguyen, T.-T.; Breaux, C.; Guillory, A.; Mangelli, M.; Fridianto, KT; Kovalik, J.-P.; Burk, DH; Noland, RC; Mynatt, R.; et al. Karnitiini atsetüültransferaasi proksimaalne torurakk-spetsiifiline ablatsioon põhjustab tubulaarset haigust ja sekundaarset glomeruloskleroosi. Diabeet 2019, 68, 819–831.
37. Ding, H.; Jiang, L.; Xu, J.; Bai, F.; Zhou, Y.; Yuan, Q.; Luo, J.; Zen, K.; Yang, J. Aeroobse glükolüüsi inhibeerimine pärsib neerude interstitsiaalsete fibroblastide aktivatsiooni ja neerufibroosi. Olen. J. Physiol. Neerude füsiool. 2017, 313, F561–F575.
38. Wei, Q.; Su, J.; Dong, G.; Zhang, M.; Huo, Y.; Dong, Z. Glükolüüsi inhibiitorid pärsivad neerude interstitsiaalset fibroosi fibroblastidele ja tubulaarsetele rakkudele avalduva lahkneva toime kaudu. Olen. J. Physiol. Neerude füsiool. 2019, 316, F1162–F1172.
39. Qi, W.; Keenan, HA; Li, Q.; Ishikado, A.; Kannt, A.; Sadowski, T.; York, MA; Wu, IH; Lockhart, S.; Coppey, LJ; et al. Püruvaatkinaasi M2 aktiveerimine võib kaitsta diabeetilise glomerulaarpatoloogia ja mitokondriaalse düsfunktsiooni progresseerumise eest. Nat. Med. 2017, 23, 753–762.
40. Lee, M.; Harley, G.; Katerelos, M.; Gleich, K.; Sullivan, MA; Laskowski, A.; Coughlan, M.; Fraser, SA; Mount, PF; Võimsus, DA PFKFB2 regulatiivsete fosforüülimissaitide mutatsioon halvendab neerufibroosi. Sci. Vabariik 2020, 10, 14531.
Leslie S. Gewin 1,2,3
