Theaflaviiniga reguleeritud imd-kondensaadid kontrollivad Drosophila soolestiku homöostaasi ja vananemist
Jul 01, 2022
Palun võtke ühendustoscar.xiao@wecistanche.comrohkem informatsiooni
KOKKUVÕTE
Must tee on maailmas enim tarbitav teejook ja sellel on järjepidevalt teatatud vananemisvastaseid omadusi. Siiski on suures osas teadmata, kas teaflaviinid, üks musta tee ekstraktide iseloomulikest fütokemikaalidest, on seotud tarbijate vananemise ja eluea reguleerimisega. Selles uuringus näitame, et teaflaviinid mängivad kasulikku rolli vanusega tekkiva soolelekke ja düsbioosi ennetamisel, lükates seega edasi Drosophila vananemist. Mehhaaniliselt reguleerivad teaflaviinid Imd kondensaadi koostu, et negatiivselt reguleerida Imd-signaalide üleaktiveerimist äädikakärbse sooltes. Lisaks takistavad teaflaviinid hiirtel DSS-indutseeritud koliiti, mis viitab sellele, et teaflaviinid mängivad rolli soolestiku terviklikkuse moduleerimisel. Üldiselt näitab meie uuring molekulaarset mehhanismi, mille abil teaflaviinid reguleerivad soolestiku homöostaasi tõenäoliselt Imd koalestsentsi kontrollimise kaudu.

Lisateabe saamiseks klõpsake siin
SISSEJUHATUS
Vananemine, mida iseloomustab üksikute organsüsteemide füsioloogiliste funktsioonide langus ning kasvav haiguste ja surma oht, hõlmab molekulide, rakkude ja kudede kahjustuste kuhjumist (Alavez et al., 2011; Bartke et al., 2019; Engeet al., 2017). Funktsionaalsete materjalide või kemikaalide tuvastamine, mis takistavad bioloogilist riknemist, et aeglustada vananemisprotsessi ja pikendada eluiga, on kahtlemata otsustava tähtsusega (Bar-ardo et al., 2017; Kapahi et al., 2017). Varasemad uuringud on teatanud, et must tee, maailmas enim tarbitav tee, omab olulisi vananemist aeglustavaid toimeid (Cameron et al., 2008; Fei jt, 2017; Kumar ja Rizvi, 2017; Naumovski jt, 2019). Peng et al., 2009; Xiao jt, 2020). Musta tee ekstraktidega toidulisandid pikendavad tõhusalt katseloomade, nagu ussid (Feet al., 2017), puuviljakärbsed (Peng et al., 2009; Site al., 2011), hiired (Site al., 2011) eluiga. Xiao et al., 2020) ja rotid (Kumar ja Rizvi, 2017).
On hästi teada, et musta tee ekstraktid sisaldavad peamiselt kahte tüüpi fütokemikaale, nimelt katehhiine ja teaflaviine (TF) (Cameron et al., 2008; Kondo et al., 2019; Li jt, 2013), millest viimane toodetakse katehhiinidest endogeense polüfenooloksüdaasi ja peroksidaasi toimel musta tee tootmise oksüdatsiooniprotsessi käigus (Li et al., 2013). Mitmetes uuringutes on tuvastatud katehhiinide vananemisvastane roll oksüdatiivse stressi ja vanusega seotud põletiku parandamise ning koekahjustuste vähendamise kaudu (Cameron et al., 2008; Niu jt, 2013; Peng jt, 2009; Si et al. .2011; Waaner et al., 2015). Funktsionaalsed uuringud TF-ide panuse kohta vananemisse on aga suuresti maha jäänud katehhiinide omadest, kuna musta tee lehtedest on meditsiiniliste uuringute jaoks raske eraldada piisavas koguses TF-e (Takemoto ja Takemoto, 2018). Hiljuti on TF-ide masstootmiseks välja töötatud mitu biosünteesimeetodit (Takemoto ja Takemoto, 2018), mis võimaldavad uurida TF-de täpseid bioloogilisi mõjusid ja nende aluseks olevaid regulatiivseid mehhanisme.
Hiljuti on üha suurenevad andmekogumid toonud esile soolte pöördelise rolli vananemises ja eluea moduleerimises (Guo et al., 2014; Jji jt, 2019; Maynard ja Weinkove, 2018; Rothenberg ja Zhang, 2019; Salazar jt. ,2018). Sooleepiteel, mis toimib selektiivse barjäärina, võimaldab toitainete, ioonide ja vee imendumist ning piirab peremeesorganismi kokkupuudet kahjulike üksustega, sealhulgas mikroorganismide, toiduantigeenide ja keskkonnatoksiinidega (Capo et al., 2019; Nicholson et al. , 2012; Ryu et al., 2010). Inimeste suure ringlusega koena pakub soolestik sümbiootiliste mikroorganismide jaoks parimat elukeskkonda, sealhulgas looduslikke anaeroobseid tingimusi, rikkalikult toitaineid ning sobivat temperatuuri ja pH-d.

Joonis 1. Theaflaviinid pikendavad Drosophila eluiga ja suurendavad ronimisvõimet
(A ja B) Emasloomakärbseid kasvatati standardse toiduga, millele lisati 1 mg/ml või 2,5 mg/ml teaflaviine (TF) või ilma TF-ideta. Kärbsed viidi ülepäeviti värsketesse viaalidesse, mis sisaldasid uut söödet, ja surnud kärbseid on kogu täiskasvanu eluea jooksul hinnatud, analüüsiti ja näidati emaste kärbeste ellujäämiskõveraid (A) ja keskmist pikaealisust (B).
(Cand D) Emaslooma w18 toideti standardsete Drosophila toiduainetega (viidatud Basal) või toiduga, millele oli lisatud vastavalt 1 mg/ml või 2,5 mg/ETF-i. Kuuele sõltumatule kärbeste rühmale näidatud vanuses (vastavalt 10 päeva, 30 päeva, 40 päeva ja 50 päeva) viidi läbi kohviku (C) ja fluorestseiini söötmise (D) testid. väärtust, moodustades kehas nišše, mis on hõivatud konkreetsete bakteriliikidega (Bonfini et al., 2016; Buchon et al., 2013; Nicholson jt, 2012). Samal ajal mõjutavad need sümbiootilised mikroorganismid ja nende metaboliidid otseselt või kaudselt ka toitainete töötlemist; seedimine ja imendumine; energiabilanss; immuunfunktsioon; seedetrakti areng ja küpsemine; ja paljud teised olulised füsioloogilised tegevused (Bonfini et al., 2016; Broderick, 2016; Maynard ja VVeinkove, 2018; Nicholson jt, 2012). Kahe sümbionti vastastikku kasulik suhe võib säilitada soolestiku mikroökosüsteemi stabiilsust ja dünaamilist tasakaalu (Bonfini et al., 2016; Brodeerick, 2016; Broderick et al., 2014; Guo jt, 2014; May-nard ja Weinkove, 2018; Nicholson et al., 2012).

cistanche võib vananemisvastane
Mitmed uuringud on näidanud, et kaasasündinud immuunvastus on soolestiku mikrobiota homöostaasi säilitamiseks kriitilise tähtsusega ja see säilib selgrootutest selgroogseteni (Guillouet al., 2016; Guo et al., 2014; Ryu jt, 2006, 2010; Vijay- Kumar et al., 2010). Drosophilas on kaasasündinud immuunvastustes kaasatud kaks peamist signalisatsiooniteed, nimelt Toll ja immuunpuudulikkuse (Imd) rada (Lu et al., 2020; Myllymakiet al., 2014; Valanne et al., 2011). Drosophila Toll rajal on sarnasusi imetajate interleukiini-1 retseptori (IL-1R) ja MyD88-sõltuva Toll-sarnase retseptori (TLR) radadega, samas kui Imd rada on sarnane. kasvaja nekroosifaktori retseptori (TNFR) rajale ja TRIF-sõltuvale TLR rajale imetajatel (Imler, 2014; Myllymaki et al., 2014; Valanne et al., 2011). Need kaks rada kontrollivad antimikroobsete peptiidide (AMP) ekspressiooni NF-KB transkriptsioonifaktorite aktiveerimise kaudu (Imler, 2014; Myllymaki et al., 2014; Valanne jt, 2011).bioflavonoididImd signaalirada aktiveerib tavaliselt gramnegatiivne bakteriaalne infektsioon ja selle tulemuseks on teise AMP-de komplekti, nagu Attacin, Cecropin ja Diptericin, ekspressioon (Kleino ja Silverman, 2014; Myllymaki et al., 2014). Nende AMP-de ekspresseerimiseks on vaja peptidoglükaani äratundmisvalgu (PGRP)-LC retseptorit Imd rajas ning Relishi, NF-kB perekonna transkriptsioonifaktori signaalist sõltuvat lõhustamist ja tuuma translokatsiooni (Kleino ja Silverman, 2014; Myllymaki et al., 2014). Hiljutine uuring näitas, et bakteriaalsete peptidoglükaanide äratundmisel on Drosophila Imd raja aktiveerimiseks vajalik amüloidi moodustumine (Kleino et al., 2017). Siiski jääb suuresti teadmata, kas see Imd-kondensaat on seotud muude bioloogiliste protsessidega, nagu soolestiku homöostaasi säilitamine ja vananemise reguleerimine.
Käesolevas uuringus kasutasime loommudelitena puuviljakärbseid ja hiiri, et uurida TF-de rolli soolestiku terviklikkuse ja vananemise kontrollimisel. Näitasime, et TF-id lükkavad edasi soolestiku tüvirakkude vanusest tingitud üleproliferatsiooni, kaitsevad soolestiku mikrobioomi düsbioosi eest ja takistavad Imd signaaliraja aktiveerumist, pikendades seega Drosophila eluiga. Täiendavad mehhaanilised uuringud näitasid, et TF-id võivad Imd signaaliülekandele negatiivselt kaasa aidata, blokeerides pigem Imd kondenseerumist kui selle ubikvitinatsiooni. Lisaks leidsime, et TF-id on DSS-i poolt indutseeritud koliidi ennetamisel hiirtel väga tõhusad. Kokkuvõttes näitavad meie leiud TF-ide potentsiaalset rolli Imd käitumise moduleerimisel, mis võib olla võtmetegur nende positiivses panuses soolestiku homöostaasi ja eluea pikenemisse.
TULEMUSED
Theaflaviinide toidulisand pikendab Drosophila eluiga
Et uurida, kas teaflaviinid (TF-id) mõjutavad Drosophilas vananemist ja eluiga, kasvatasime emaseid w'118 kärbseid standardse kasvatustoiduga, millele lisati 1 mg/ml või 2,5 mg/ml TF-d, ja teostasime eluea analüüsid, nagu eelnevalt kirjeldatud (Ji et al. .,2019). Kontrollideks peeti kärbseid, kellele toideti toitu, millele oli lisatud võrdne kogus TF-i lahustit (H2O). Nagu on näidatud joonisel fig 1A, pikendas suhteliselt madala kontsentratsiooniga TF-ide (1 mg / ml) toiduga lisamine äädikakärbse eluiga veidi ja TF-ide kõrge kontsentratsioon (2, 5 mg / ml) avaldas eluea pikenemisele oluliselt positiivset mõju. Eelkõige põhjustas kõrgete TF-ide (2, 5 mg / ml) pikaajaline omastamine emaste kärbeste keskmise eluea pikenemist ligikaudu 8 päeva võrra (joonis 1B), mis viitab TFsini kasulikule rollile Drosophila pikaealisuse reguleerimisel. Sarnased tulemused saadi, kui testisime täiendavate TF-ide võimalikku mõju isaste w'*'''8 kärbeste elueale (joonised S1A ja S1B).

Joonis 2. Theaflaviinid hoiavad ära vanusega tekkiva soolestiku düsfunktsiooni ja mikrobiota düsbioosi Drosophilas
(A ja B) Soolestiku terviklikkuse kaotust testiti Smurftestiga 10-päevaste, 30-päevaste, 40-päevaste ja 50-päevaste naiste vanuses w18. Mitte-Smurfi ja Smurfi näited on näidatud punktis (A). Smurfi protsentides erinevates näidatud rühmades analüüsiti ja näidati (B).
(C) Analüüsiti ja näidati erinevatest näidatud rühmadest pärit 16S rRNA geeni qPCR-ga salvestatud bakterite arvukust naiste w18-failides.
(DF) Viidi läbi kommensaalse bakteriaalse 16S rRNA geeni sekveneerimine. Analüüsiti ja esitati bakteritaksonite (D) proportsioone, peamiste mikroobitaksonite (F) soojuskaarti ja gammaproteobakterite (F) suhtelist arvukust.
Joonis 2. Jätkub

(G ja H) Soolestikud lõigati näidatud emaskärbestel, keda toideti kontrollina 2,5 mg/ml TF-ga või ilma TF-deta, 10 päeva ja 40 päeva vanuselt. Kesksoole slaidide kujutised jäädvustati fluorestsentsmikroskoopia abil GFP signaalide jaoks (G). Statistiline analüüs, mis näitab GFP-positiivsete rakkude protsenti, on näidatud (H).
(I) Näidatud emaste kärbeste sooled koguti ja neile viidi läbi immunovärvimise testid, kasutades fosforüülitud histooni 3(pH3) vastaseid antikehi. Analüüsiti ja näidati statistilisi tulemusi, mis kvantifitseerisid pH3--positiivsete rakkude sisalduse soolestiku kohta. B, C, H ja, andmeid analüüsitakse kahepoolse Studenti testiga ja need on näidatud keskmistena ± SEM.NS, mitteoluline,*p<><0.001. see="" also="" figure="">
ETF-idel on teadaolevalt mõru maitse ja nii tarbijad, sealhulgas äädikakärbsed kui ka imetajad, väldivad tavaliselt kibedaid toite (Yamazaki et al., 2014; Yang et al., 2018). Seejärel püüdsime selgitada, kas TF-id võivad mõjutada Drosophila toidutarbimist, sest varasemad uuringud on tõestanud, et toitumispiirangud pikendavad nii selgroogsete kui ka selgrootute eluiga (Hudry et al., 2019; Kapahi jt, 2017; Moger-Reischer et al. ., 2020). Selleks viisime esmalt läbi kohviku testi, mis on laialdaselt kasutatav lähenemisviis söötmiskiiruse otseseks ja täpseks mõõtmiseks, kasutades vedelat söödet sisaldavat kapillaarsööturit, nagu eelnevalt kirjeldatud (Ja et al., 2007). Nagu on näidatud joonistel 1C ja S1C, muutis TF-ide toidulisand (vastavalt 1 mg / ml ja 2, 5 mg / ml) testitud kärbeste toidutarbimist peaaegu mitte. Selle täiendavaks kinnitamiseks kasutasime seejärel fluorestseiini toidu jälgijana (Rera et al., 2012; Wang jt, 2005) ja teostasime loomuliku toitumise analüüsi (Danilov et al., 2015). Nagu on näidatud joonistel 1D ja S1D, ei täheldanud me korrelatsioone TF-i lisamise ja toidutarbimise taseme vahel. Kokkuvõttes näitasid meie tulemused, et TF-de kasulik roll eluea pikendamisel ei pruugi olla tingitud Drosophila toitumispiirangutest.
Täiendavad TF-id on Drosophila energia homöostaasi mõjutamiseks asendamatud
On oletatud, et musta tee polüfenoolid avaldavad positiivset mõju rasvumise ennetamisele, pärssides lipiidide ja sahhariidide seedimist, imendumist ja omastamist, vähendades seega kalorite tarbimist (Cameron et al., 2008). Seejärel püüdsime selgitada, kas TF-idega reguleeritud LDrosophila eluea pikenemine on tingitud toitainete imendumise ja energia salvestamise muutustest. Selleks uurisime kõigepealt triatsüülglütseriidi (TAG), ühe kõige sagedamini tuvastatava lipiidide metaboliidi (Tennessen et al., 2014), taset emaskärbestel kogu nende elu jooksul, nagu eelnevalt kirjeldatud (Fan et al., 2017).osta cistancheNagu on näidatud joonisel 1E, ei mõjutanud TF-ide ravi TAG-i üldist arvukust erinevates vanusepunktides. Kui tuvastasime glükogeenisisalduse ja kvantifitseerisime tsirkuleerivaid süsivesikuid (glükoos ja trehaloos) Hexokinase komplekti abil (Li et al., 2018; Ten-nessen et al., 2014), näitasid tulemused, et ega proovide vahel ei ilmnenud ilmseid muutusi. ilma TF-ideta (joonised 1F-1H). Pange tähele, et järjekindlad tulemused saadi metaboolsete fenotüüpide uurimisel, kasutades loommudelitena isast w118 (joonised S1E-S1H). Need andmed viitasid ühiselt sellele, et TF-ide toidulisandid on süsivesikute ja energia homöostaasi reguleerimiseks kogu Drosophila eluea jooksul hädavajalikud.

Lisaks uurisime Drosophila loomuliku vananemise kineetikat dieedi TF-i sekkumise korral, viies läbi kiire iteratiivse negatiivse geotaksise (RING) testid, nagu eelnevalt kirjeldatud (Dilliane et al., 2017; Staats et al., 2018). Nagu on näidatud joonistel 1l, 1J, S1l ja S1J, paranesid vanuse (40 päeva) w1118 (nii naised kui ka mehed) tõusuindeksid TF-i toidulisandite rühmas märkimisväärselt (naistel peaaegu 12% ja meestel peaaegu 18% tõus). ) võrreldes kontrollrühmadega, mis viitab sellele, et TF-id võivad parandada Drosophila ronimist ja liikumisaktiivsust.
Theaflaviinid hoiavad ära vanusega tekkiva soolestiku lekke ja mikrobiota düsbioosi
Varasemad uuringud on näidanud, et äädikakärbse liikumisaktiivsus ja eluiga on tugevalt seotud peremehe tervisliku seisundiga, nagu sugu, toitumine, vanus ja genotüüp (Caruso et al., 2013; Heintz ja Mair, 2014). Hiljuti on mitmed tõendid tõestanud, et soole Imd signaaliülekande homöostaasi säilitamine parandab soolestiku terviklikkust, vältides ISC ja prekursorrakkude üleproliferatsiooni ning lükates edasi vanusega tekkivat sooleepiteeli düsfunktsiooni, mis omakorda aitab positiivselt kaasa organismi tervisele (Clark et al. , 2015; Guo jt, 2014). Drosophilas on lühenenud eluiga tihedalt seotud sooleepiteeli barjääri düsfunktsiooniga ja selle barjääri terviklikkuse areng vananemise ajal pikendab eluiga (Clark et al., 2015; Guoet al., 2014; Jet al., 2019). Seega püüdsime kindlaks teha, kas TF-id muudavad soolestiku terviklikkust, viies läbi Smurfi testi, meetodi, mida on varem kirjeldatud (Clark et al., 2015; Rera et al., 2011). Nagu on näidatud joonisel 2A, viidati testitud äädikakärbsetele, mille sinised värvained piirdusid seedetraktiga, mitte-smurfideks (vasakpoolne paneel joonisel 2A). Kui täheldati siniseid värvaineid

Joonis 3. Jätkub
(EG) Soolestikud isoleeriti emaste w1118-failidest, mida toideti 2,5 mg/ml TF-idega või ilma TF-ideta, vastavalt 10 päeva, 30 päeva, 40 päeva ja 50 päeva vanuselt. Kogu RNA ekstraheeriti ja sellele tehti aRT-PCR analüüs. Analüüsiti ja näidati dipteritsiini (F), attatsiini (F) ja tsekropiin A1 (G) mRNA ekspressioonitasemeid. EG-s analüüsitakse andmeid kahepoolse Studenti t-testiga ja näidatakse keskmisena ± SEM.NS, mitteoluline, *p<><><0.001. see="" also="" figure="">
soolestikust kõhtu lekkides loeti peremehed smurfideks (parem paneel joonisel 2A). Kooskõlas varasemate leidudega (Clark et al.,2015) suurenes smurfi osakaal vananemise ajal järk-järgult (joonis 2B). Huvitav on see, et täiskasvanud smurfide osakaal vähenes TF-iga toidetud rühmades võrreldes vastava vanusega kontrollidega mõlemal naisel (8,2 protsendilt 3,7 protsendile, 19,4 protsendilt 15,6 protsendile ja rühmades 35,4 protsendilt 27,1 protsendile). vanuses vastavalt 30 päeva, 40 päeva ja 50 päeva, joonis 2B) ja meessoost täiskasvanud (2,7 protsendilt 0,9 protsendile, 6,9 protsendilt 0,9 protsendile ja 8,3 protsendilt 2,7 protsendile 30-aastaselt päeva, 40 päeva ja 50 päeva vastavalt, joonis S2A), mis näitab, et TF-id võivad ära hoida soolebarjääri düsfunktsiooni vanuses puuviljakärbestel. Märkimist väärib see, et meestel täheldati smurfide osakaalu suuremat vähenemist (vähenes peaaegu 65,8 protsenti , 86,9 protsenti ja 67,4 protsenti vastavalt 30 päeva, 40 päeva ja 50 päeva vanuselt) kui vanus. -sobivad emased (vähenenud peaaegu 54,1%, 19,5% ja 23,3% vastavalt 30-, 40- ja 50-päevastele vanustele), mis tähendab, et TF-id võivad mängida paremat rolli isaste kärbeste soolelekke vähendamisel.
Varasemad uuringud on näidanud, et vanusega tekkiv soolebarjääri düsfunktsioon on sageli korrelatsioonis soolestiku mikrobiota düsbioosiga (Clark et al., 2015; Guo jt, 2014). Seega uurisime pärast TF-ide lisamist soolestiku kommensaalset bakterikoostist. Esmalt kasutasime universaalseid praimereid ja teostasime kvantitatiivseid PCR katseid, et kvantifitseerida bakteriaalse 16S rRNA geeni tase. Nagu on näidatud joonisel 2C, vähenes vananenud jaotustükkide puhul TF-i sekkumisrühmade bakterite kogupopulatsioon kontrollrühmaga võrreldes silmatorkavalt (peaaegu 45 protsenti -55 protsenti), mis viitab sellele, et TF-ide lisamine takistab tõenäoliselt mikrobiota laienemist vananemise ajal. . Seejärel teostasime metagenoomika, et uurida üksikasjalikult TF-idega toidulisanditest põhjustatud muutusi soolestiku mikroobide kogukonnas. Nagu on näidatud joonistel 2D-2F, vähenes gammaproteobakterite osakaal, mille laienemine leiti olevat tihedalt seotud soolebarjääri puudulikkusega (Clark et al., 2015), ilmselgelt vähenenud TF-ide lisamine vananenud sooltes ( peaaegu 7 protsenti vähenemist), mis tähendab, et TF-id aitavad Drosophilas vananemise ajal positiivselt kaasa soolestiku mikrobiota homöostaasile.
Theaflaviinid parandavad soolestiku proliferatiivset homöostaasi Drosophilas
We further examined the intestinal integrity of flies that were treated with or without TFs. First, we employed the widely-used P{Esg-Gal4}/P{Uasp-GFP};{Tub-Gal80*s}strain(referred to as esgts>GFP), milles soolestiku tüvirakud (ISC-d) ja eellasrakud märgistati GFP-ga. Nagu on näidatud joonistel 2G ja 2H, oli GFP-positiivsete rakkude arv TF-i sekkumisrühmades 40 päeva vanuses (loendati 20 soolestikku) palju väiksem (ligi 29,7 protsenti) kui vanusega sobivates kontrollides (peaaegu 47,6 protsenti ja Loendati 19 soolestikku), mis viitab sellele, et TF-id võivad pärssida ISC-de vanusest tulenevat üleproliferatsiooni. Lisaks teostasime immunovärvimise katseid, kasutades fosfohistooni 3 (pH3) vastaseid antikehi, mis on soole kudede mitootiliste rakkude spetsiifiline marker. Täheldasime ealiste TF-i saanud täiskasvanute soolestikus vähem pH{15}}positiivseid rakke (keskmine arv oli 20,6) kui kontrollrühma omades (keskmine arv oli 39,5, joonis 2). Kokkuvõttes näitavad meie tulemused, et toidulisandid TF-idega parandavad soole proliferatiivset homöostaasi ja takistavad vanusega tekkivat mikrobiota düsplaasiat, lükates seega edasi Drosophila vananemist.
Theaflaviinid moduleerivad negatiivselt soolestiku Imd signaale
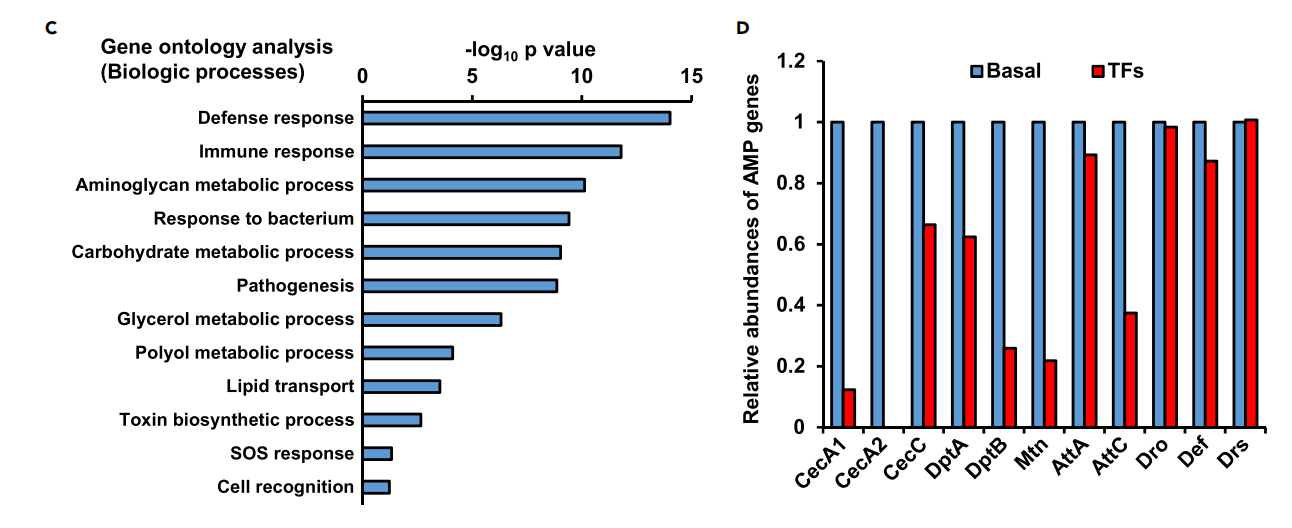
Et uurida aluseks olevaid molekulaarseid mehhanisme, mille abil TF-id positiivselt aitavad kaasa Drosophila soolestiku homöostaasile, teostasime RNA-seq analüüsi, kasutades vanusega sobivaid sooleproove naiste w1118 täiskasvanutelt, keda raviti TF-idega või ilma. Fragmentide kilobaasi kohta miljoni kohta (FPKM) analüüsid näitasid, et üldised geeniekspressiooni mustrid olid kahe katserühma vahel sarnased (joonis 3A). Edasine diferentsiaalekspressioonianalüüs tuvastas aga kokku 229 erinevalt ekspresseeritud geeni, millest 99 olid ülesreguleeritud ja 126 allareguleeritud (joonis 3B). Huvitaval kombel näitas nende geenide geeniontoloogia analüüs, et TF-idega toidulisandid muutsid immuunvastuse rada tugevalt (joonis 3C).
Drosophilas on tõestatud, et kaasasündinud immuunsignalisatsioonirajad mängivad domineerivat rolli vanusega algava soolestiku homöostaasi ja pikaealisuse reguleerimisel (Clark et al, 2015; Guo jt, 2014). Seejärel keskendusime antimikroobsete peptiidide (AMP) ekspressioonimustrite uurimisele kaasasündinud immuunsignaalidest allavoolu. Nagu näidatud

Joonis 4. Jätkub
(D) Puhastatud Imd valke inkubeeriti erinevate kontsentratsioonidega TF-idega (vastavalt 50 uM, 100 uM ja 200 uM) toatemperatuuril 5 minutit. Seejärel viidi proovidega läbi fluorestsentsi emissioonispektri analüüs, kasutades näidatud lainepikkusi (ergastus 430 nm juures, emissioon 450 nm kuni 550 nm pilu laiusega 5 nm). Algtaseme kontrollina kasutati ilma TF-deta proovi.
(E and F)Lysates of guts from NP11>Valmistati ette Myc-Imd kärbsed ja inkubeeriti TF-idega (100 μM) toatemperatuuril 30 minutit. Imd valgu agregaatide analüüsimiseks viidi läbi SDD-AGE (ülemine paneel E-s) ja SDS-PAGE (alumine paneel E-s) analüüsid. Laadimiskontrollina kasutati tubuliini.tsisantšImd-kondensaatide kvantifitseerimiseks erinevates proovides viidi läbi densitomeetria analüüs ja tulemused on näidatud (F). (G) TF-i proovi tüüpiline kromatogramm.
(H ja I) Puhastatud Flag-Imd valke inkubeeriti TF-de, TF1, TF2a, TF2b või TF3-ga (iga proovi jaoks 100 μM) või võrdse mahu puhvriga (kontroll) toatemperatuuril 30 minutit, nagu näidatud. Seejärel viidi proovidega läbi SDD-AGE (ülemine paneel H-s) ja SDS-PAGE (alumine paneel H-s), et määrata Imd agregatsioonimustrid. Viidi läbi densitomeetria analüüs Imd-kondensaatide kvantifitseerimiseks erinevates proovides ja see on näidatud punktis (). C, F ja I puhul analüüsitakse andmeid kahepoolse Studenti testiga ja näidatakse keskmisena ± SEM.***p< 0.001.="" see="" also="" figure="">
joonisel fig 3D on AMP geenid, mida juhib immuunpuudulikkuse (Imd) rada, sealhulgas dipteritsiin A (DptA), dipteritsiin B (DptB), attatsiin A (AttA), tsekropiin A1 (CecA1), tsekropiin A2 (CecA2) ja tsekropiin C (Cece), vähenesid TF-idega ravitud rühmades kontrollrühmadega võrreldes oluliselt (vastavalt 39,4 protsenti, 72,3 protsenti, 10,5 protsenti, 86,5 protsenti, 99,8 protsenti ja 36,1 protsenti). RNA-seq analüüsist saadud tulemuste täiendavaks kinnitamiseks viisime läbi kvantitatiivse pöördtranskriptsiooni-polümeraasi ahelreaktsiooni (gRT-PCR), et kvantifitseerida Imd-ga seotud AMP geenide suhtelised ekspressioonitasemed neljas erinevas vanusepunktis saadud Drosophila sooleproovides. sealhulgas 10 päeva, 30 päeva, 40 päeva ja 50 päeva. Nagu on näidatud joonistel 3E-3G, vähenesid teatud geenide, sealhulgas dipteritsiini, attatsiini ja tsekropiin A1 mRNA ekspressioonitasemed oluliselt (peaaegu 35,9 protsenti -66,6 protsenti) TF-idega töödeldud korral. vananenud sisikond. Kokkuvõttes näitasid meie andmed, et TF-id potentsiaalselt antagoniseerisid Imd signaaliraja aktiveerimist Drosophila soolestiku rakkudes vananemise ajal.
Theaflaviinid on asendamatud Imd raja transkriptsiooni reguleerimiseks või Imd ubikvitineerimiseks
Püüdsime uurida seost TF-de ja Imd vahel ning viisime läbi pinnaplasmonresonantsi (SPR) testi, nagu eelnevalt kirjeldatud (Lan et al., 2020). Nagu on näidatud joonisel 4A. TF-idel oli mõõdukas seondumisafiinsus puhastatud Imd-valguga hinnangulise Kp konstandi juures 8,078 uM. Seejärel kipume kindlaks tegema, kuidas TF-id kontrollivad soole Imd signaalirada. RNA-seq andmete transkriptoomianalüüsi tulemuste põhjal leidsime, et Imd signaaliraja peamiste regulatoorsete tegurite, nagu PGRP-LC, Imd ja Relish, ekspressioonitasemeid TF-idega töötlemine peaaegu ei muutnud (joonis S3A). ). Lisaks kogusime sooleproove kärbestelt, kellele lisati erinevas vanuses TF-idega või ilma, ja viisime läbi qRT-PCR katsed, et tuvastada nende geenide ekspressioonimustrid. Nagu on näidatud joonisel S3B, olid teatud geenide, sealhulgas effete, faded, tak1, pgrp-Ica, uev1a, bendless, relish, imd, pgrp-sc2, tab2, ird5 Kenny ja diap2 mRNA tasemed kontrollrühmade vahel sarnased. ja TF-ide sekkumisrühmad, mis viitab sellele, et TF-id ei osale Imd-signaalide reguleerimises transkriptsiooni tasemel.
Järgmisena uurisime Imd ubikvitinatsiooni profiile, kuna varasemad uuringud on näidanud, et Imd ubiguitineerimine on Imd raja allavoolu signaaliülekande jaoks hädavajalik (Myllymaki et al., 2014; Zhou et al., 2005). Esmalt teostasime in vitro E1 nihketesti ja leidsime, et TF-idega töötlemisel ei ole nähtavat mõju E1 ja ubikvitiini ensümaatilistele reaktsioonidele, et moodustada konjugeeritud E1 / Ub (joonis S4A). Veelgi enam, me transfekteerisime Drosophila S2 rakud plasmiididega, mis ekspresseerisid Flag-märgistatud Imd koos HA-märgistatud Ub-ga ja seejärel töödeldi rakke TF-idega või ilma. Täiendavad ubikvitinatsiooni testid näitasid, et TF-ide lisamine mõjutas vaevu ubikvitineeritud Imd taset kultiveeritud rakkudes (joonised S4B ja S4C). TF-ide ja Imd ubikvitinatsiooni vaheliste seoste määramiseks in vivo kasutasime transgeenset kärbest P {NP1-Gal4}/P{Uasp-Myc-Imd};P{Tub-Gal80*} (viidatud kui NP1* s > Myc-Imd), milles Myc-märgistatud Imd-valk ekspresseeriti soolerakkudes tugevalt (joonis S4D). Meie ubikvitineerimise katsed näitasid, et TF-idega toidulisand oli vajalik Imd ubikvitineerimise moduleerimiseks soolestiku kudedes (joonised S4D ja S4E). Kokkuvõttes näitasid meie tulemused, et TF-id reguleerivad negatiivselt Drosophila Imd signaale, kuna ei mõjuta Imd ubikvitinatsioonimustrit.
Theaflaviinid takistavad Imd kondensaadi kogunemist
Hiljutine uuring näitas, et Imd agregatsioon on Imd raja allavoolu geenide aktiveerimiseks hädavajalik (Kleino et al., 2017). Seejärel püüdsime uurida, kas TF-id reguleerivad protsessi

Joonis 5. Jätkub
(F ja G)Emaslooma w18 (mida nimetatakse imd pluss / pluss), imd' heterosügootsed ja homosügootsed mutandid (nimetatud vastavalt kui imd plus /- ja imd-/-) kasvatati standardse Drosophila toiduna (viidatud kui Basal) või toidulisandina 2,5 mg/ml (nimetatakse TF-deks) ja seejärel viidi läbi eluea test. Elulemuskõverat (F) ja keskmist eluiga (G) analüüsiti ja näidati.
In ja F kasutati statistilise analüüsi jaoks Log Rank testi. BE ja, ja, statistilise analüüsi jaoks kasutati kahepoolset Studenti t-testi ja andmed on sh keskmised ± SEM. NS, mitteoluline, *lk<0.05, **p="" <="" 0.01,=""><0.001. see="" also="" figure="">
Imd agregaadi moodustumine. Esiteks puhastasime kultiveeritud S2 rakkudest Myc-märgistatud Imd valgud ja inkubeerisime valke erinevate TF-ide kontsentratsioonidega (joonis 4B). Huvitaval kombel avastasime, et TF-id takistasid märkimisväärselt Imd agregatsiooni (vähendasid 81,7 protsenti -89,7 protsenti, joonised 4B ja 4C), nagu näitasid meie poolidenatureeriva detergendi agaroosgeelelektroforeesi (SDD-AGE) testid. Selle leiu kinnitamiseks teostasime täiendavalt tioflaviin-T sidumisanalüüse ja saime järjekindlad tulemused (joonis 4D). Viimasena kasvatasime NP1ts > Myc-Imd transgeenseid kärbseid, kellele lisati toidulisandit TF-idega või ilma, ja kogusime sooleproove eakatelt täiskasvanutelt. SDD-AGE katsed näitasid, et TF-id vähendasid soolerakkudes Imd agregatsiooni oluliselt (vähenesid 16,7 protsenti -22 protsenti, joonised 4E ja 4F).
Et teha kindlaks, kuidas TF-id aitavad kaasa Imd kondensaadi kogunemise kontrollimisele, viidi TF-idele läbi HPLC-analüüs ja leidsime, et need sisaldasid peamiselt nelja tüüpi monomeere (joonis 4G), nimelt teaflaviini (TF1), teaflaviini 3-O-gallaati ( TF2a), teaflaviini 3'-O-gallaat (TF2b) ja teaflaviin 3,3'-di-O-gallaat (TF3), mis olid kooskõlas varasemate aruannetega (Li et al., 2013; Takemoto ja Takemoto, 2018) . Seejärel inkubeerisime kõiki neid kemikaale puhastatud Imdproteiiniga ja teostasime SDD-AGE katsed. Nagu on näidatud joonistel 4H ja 4l, põhjustas kõigi nende TF-monomeeride töötlemine märgatava vähenemise (vastavalt 59,5%, 60,9%, 58,4%, 58,2% ja 55,8% TF-ide, TF1, TF2a, TF2b ja TF3 puhul) Imd koondtasemed. Kokkuvõttes näitasid meie tulemused, et TF-id reguleerivad negatiivselt Drosophila Imd signaalirada, tõenäoliselt kontrollides Imd kondensaatide käitumist.
Theaflaviinid pikendavad Drosophila eluiga Imd-sõltuval viisil
To examine whether TFs prolong Drosophila lifespan depending on their regulatory role in Imd, we specifically knocked down Imd in gut tissues using the transgenic flies P{NP1-gal4)PITub-gal80*}/P{Uasp-imd-IR(KK)} (referred to as Imd RNAi). As shown in Figures 5A and 5B, dietary supplementation of TFs extended the lifespan of controls (elevation of nearly 7.2 days in the mean lifespan), whereas prevention of Imd expression in guts apparently reversed the lifespan extension caused by TFs. Consistent results were obtained when we utilized male Imd RNAi and control flies to perform lifespan assays (Figures S5A and S5B). Further qRT-PCR assays showed that the mRNA expression levels of AMP genes at ages of 10 days, 30 days, 40 days, and 50 days, including diptericin, attacin, and cecropin A1.hardly changed in the gut tissues of Imd RNAi flies(Figures 5C-5E), whereas additional TFs caused reductions of 31%-72.3% in mRNA abundances of these genes in samples from control groups. To confirm these results from Imd RNAi flies, we first performed lifespan assays using w18(control, referred to as imd+/+), imd' heterozygous (referred to as imd+/-), and homozygous(referred as imd-/-)mutant flies. We found that TFs addition extended lifespan and increased mean life longevity of imd+/-flies (elevation of nearly 6.2 days, Figures 5F and 5G). However, this lifespan extension effect by TFs was almost abolished in imd-/-flies (Figures 5F and 5G). Next, we performed lifespan assays utilizing Relish RNAi(NP1's>Relish RNAi and control(NP1ts>pluss )kärbsed. sest Relish on peamine transkriptsioonifaktor, mis vastutab Imd-allavoolu AMP geeniekspressioonide eest (Myllymaki et al., 2014). Nagu on näidatud Fiqures S5C ja S5D. TF-ide lisamine toiduga pikendas märkimisväärselt kontrollkärbeste pikaealisust ja seda eluea pikenemist välditi oluliselt Relishi RNAi kärbeste puhul. Meie andmed näitasid ühiselt, et TF-ide toidulisandid aitavad positiivselt kaasa Drosophila elueale, mis sõltub tõenäoliselt soole Imd-signaalidest.
Et näha, kas TFstill pikendab eluiga akseenilisel taustal, teostasime eluea analüüsid w1118 emasloomadega akseenilistes tingimustes. Nagu on näidatud joonistel S5E ja S5F, ei mõjutanud erinevate kontsentratsioonidega TF-ide (1 mg / ml ja 2, 5 mg / ml) lisamine w18 täiskasvanute suremuse ja keskmise eluea suhet. Kuna akseenilised kasvatustingimused võivad suures osas ära hoida rikkalikku mikrobiootat, piirates seega Imd-signaale kärbete korral (Clarke al., 2015), näitavad meie andmed, et TF-id pikendavad Drosophila eluiga, võivad olla tingitud soolestiku mikrobiota reguleeritud kaasasündinud immuunsignaalide moduleerimisest.
Joonis 6. Theaflaviinid leevendavad DSS-i põhjustatud koliiti CD-1 hiirtel
(A) TF-i ravi ei mõjutanud veetarbimist erinevates CD{0}} hiirte rühmades.
(BD) Erinevate TF-ide (vastavalt 1 mg/mL, 2,5 mg/ml ja 5 mg/ml) manustamine sondiga parandas DSS-i põhjustatud käärsoole lühenemist ja põrna suurenemist CD-1 hiirtel. Näidati käärsoole (C) ja põrna (D) tüüpilisi pilte (B) ja statistilisi analüüse. (E) TF-ide erinevate kontsentratsioonide (vastavalt 1 mg/ml, 2,5 mg/ml ja 5 mg/ml) manustamine hoidis ära DSS-i põhjustatud soolestiku lekke CD{10}} hiirtel. (F ja G) Käärsooled koguti näidatud hiirte rühmadest. Kogu RNA ekstraheeriti ja allutati qRT-PCR analüüsidele, et tuvastada TNFa(F) ja IL-6(G) mRNA ekspressioonitasemed.
(HL) Erinevate hiirte rühmade käärsooled koguti pikisuunas ja allutati HE värvimistestidele. Proove uuriti mikroskoobiga ning näidatud proovidest (HL) saadi ja näidati representatiivseid kujutisi. Skaalavardad, 40 μm. (M-Q') SEM-pildid, mis näitavad käärsoole mikrotrihhoome erinevatest näidatud proovidest. Skaalavardad, 50 um (MQ) ja 4 um (M'-Q').
CG-s analüüsitakse andmeid kahepoolse Studenti testiga ja näidatakse keskmisena ± SEM.NS, mitteoluline, *p<><><0.001. see="" also="" figure="">
Theaflaviinid leevendavad CD{1}} hiirtel DSS-i põhjustatud koliiti
Et täiendavalt uurida TF-de võimalikku rolli soolestiku homöostaasi säilitamisel imetajatel, kasutati CD{0}} hiiri koliidi esilekutsumiseks naatriumdekstraansulfaadiga (DSS). Hiirtele manustati nelja nädala jooksul intragastraalselt erinevas kontsentratsioonis TF-e (1 g/l, 2,5 g/l või 5 a/l) või vett kontrollina nelja nädala jooksul, millele järgnes ravi 2-protsendilise DSS-iga joogivees 7 päeva. Et näha, kas TF-id mõjutavad DSS-i joomise kogust erinevates hiirte rühmades, jälgisime hiirte joomist iga päev. Nagu on näidatud Fiqure6A-s, ei ole TF-ravi DSS-i indutseeritud koliidi hiirtel joogitarbimise mõjutamiseks vajalik, DSS-ga ravitud hiirtel esines koliidi sündroom koos kõhulahtisuse ja/või hematoheesiaga, mida hoidis ära annusest sõltuv TF-ravi (joonised S6A-S6E).cistanche AustraaliaLisaks päästis sekkumine TF-idega DSS-i põhjustatud käärsoole pikkuse vähenemise ja leevendas põrna suurenemist (joonised 6B-6D).
Seejärel kasutasime dekstraan{0}}FITC-d (FITC-DX), et uurida nende hiirte soolebarjääri funktsiooni. Nagu on näidatud joonisel fig 6E, näitas DSS-ga töödeldud rühmade hiirtel vereproovides kõrge FITC-DX kontsentratsioon, mis viitab nende loomade soolestiku lekkele. Kuid sekkumine TF-idega takistas oluliselt FITC-DX transporti seedeorganitest vereringesüsteemi (vähenenud 56,1 protsenti -77,5 protsenti, joonis 6E). Eelkõige ei muutnud TF-ide manustamine normaalsetes tingimustes hiirte soolestiku läbilaskvust (joonis S6F). Kuna põletik mängib hiiremudeli koliidi arengus keskset rolli, teostasime täiendavalt qRT-PCR katseid, mis näitasid, et ravi TF-idega vähendas oluliselt IL-6 ja TNF ekspressiooni DSS-ga töödeldud hiirte soolestikus (joonised 6F ja 6G).
Käärsoole patoloogiliste muutuste edasiseks analüüsimiseks viisime läbi hematoksüliini-eosiini (HE) värvimise testid. Nagu on näidatud joonistel 6H-6L ja S6G-S6J, leevendas DSS-i põhjustatud tõsist epiteeli kahjustust TF-idega ravi annusest sõltuval viisil. Nende sooleproovide skaneerimine elektronmikroskoopiaga andis veelgi järjekindlaid tulemusi (joonised 6M-6Q' ja S6K-S6N'). Kokkuvõttes näitasid meie leiud, et TF-idel on kasulik roll soolebarjääri funktsiooni kaitsmisel nii putukatel kui ka imetajatel.
ARUTELU
Selles uuringus uurisime TF-de füsioloogilisi funktsioone soolestiku homöostaasi ja pikaealisuse moduleerimisel ning selle aluseks olevaid molekulaarseid mehhanisme. Näitasime, et TF-idega toidulisandid aitavad positiivselt kaasa soolestiku mikrobiota vanusest tingitud düsbioosi ennetamisele ja soole epiteeli düsfunktsiooni edasilükkamisele, pikendades seega Drosophila eluiga. Meie in vitro ja in vivo mehaanilised uuringud näitasid, et TF-id mängivad tõenäoliselt negatiivset rolli Imd signaaliraja kontrollimisel, blokeerides Imd ühinemise. Lisaks avastasime, et DSS-indutseeritud koliiti saab CD-1 hiirtel tõhusalt leevendada TF-ide lisamisega. Meie tulemused toetavad arvamust, et TF-id aitavad soodsalt kaasa soolestiku homöostaasile nii selgrootutel kui ka selgroogsetel.
Toidulisand teaflaviinidega pikendab Drosophila eluiga
Tee tarbimine on kogu maailmas populaarne ja on veetarbimise järel teisel kohal (Rothenberg ja Zhang, 2019). Paljud uuringud on keskendunud füsioloogilistele funktsioonidele sageli nii eksperimentaalsete kui ka kliiniliste lähenemisviiside kaudu (Cameron et al., 2008; Niu jt, 2013; Peng jt, 2009; Rothenberg ja Zhang. 2019; Spindleret al., 2013; Takemoto ja Takemoto, 2018; Unno et al., 2020; Zhou jt, 2020. On laialdaselt tõestatud, et tee on tervisele kasulik, kuna alandab lipiidide taset ja vähendab rasvumist, ning tee peamised funktsionaalsed ühendid on katehhiinid, eriti epigallokatehhiingallaat (EGCG) (Abbas ja Wink, 2009; Modernelli et al., 2015; Niu jt, 2013; Wagner jt, 2015; Xiong jt, 2018). Varasemad uuringud on samuti näidanud, et roheline tee ja must tee võib pikendada puuviljakärbeste (Site al., 2011; Wagner jt, 2015), usside (Fei et al., 2017; Xiong jt, 2018) ja rottide (Imran et al.) tervist ja eluiga. .,2018; Niu etal.2013). ja peamine regulatiivne mehhanism on EGCG oksüdatiivse stressi tõhus ennetamine ROS-signaalide moduleerimise kaudu.cistanche eelised,Siiski on suuresti teadmata, kas TF-id kui musta tee iseloomulikud "kuldsed" ühendid mängivad vananemise ja eluea reguleerimisel rolli. See uuring annab veenvaid tõendeid, mis näitavad, et TF-ide sekkumine on toidutarbimise mõjutamiseks hädavajalik ja TF-ide pikaajaline omastamine dieedi kaudu pikendab oluliselt nii isaste kui ka emaste äädikakärbeste eluiga. Need leiud annavad juhiseid edasisteks uuringuteks TF-de funktsioonide kohta imetajate pikaealisuses.
Theaflaviinid parandavad vanusega tekkivat mikrobiota düsbioosi ja soodustavad soolestiku homöostaasi Proliferatiivse homöostaasi ja taastumisvõime järkjärguline tasakaalustamatus on vananemise ja vanusega tekkivate haiguste tunnus (Clark et al., 2015; Heintz ja Mair, 2014; Maynard ja Weinkove, Rera 2018). jt 2012). Kroonilist põletikku seostatakse homöostaasi kadumise ja vähi esinemissageduse suurenemisega vananevates organismides (Bartke et al., 2019; Kapahi et al., 2017; Xiao et al., 2020). See on eriti oluline barjääri epiteeli, näiteks sooleepiteeli puhul (Guo et al., 2014; Maynard ja Weinkove, 2018). Vananeva soolestiku vanusega seotud düsplaasia arengu mudeliga näitasime, et peremees-kommensaalse interaktsiooni parandamine vananeva barjääri epiteelis võib edendada tervist ja eluiga. Vananemise ajal kasutasime soolefunktsiooni ja mikrobiota dünaamika analüüsimiseks mitmeid mitteinvasiivseid lähenemisviise. Esiteks näitas Smurfi test TF-de positiivset rolli epiteeli barjääri düsfunktsiooni reguleerimisel vananemise ajal. Seejärel näitas mitut transgeenset kärbest kasutav immunovärvimise test, et TF-id lükkasid edasi ISC-de üleproliferatsiooni ja diferentseerunud rakkude käivet. Lõpuks näitas mikrobioomi järjestamine, et TF-id vähendavad soolestiku kommensaalse mikrofloora vanusest tingitud laienemist. Need tulemused näitasid tugevalt, et TF-id mängivad võtmerolli peremeesorganismi vananemisprotsessi edasilükkamisel, säilitades soolestiku homöostaasi.
Theaflaviinid leevendavad liigset immuunvastust soolestikus, reguleerides negatiivselt Imd signaaliülekannet
On tehtud ettepanek, et barjääri epiteeli pikaajalise homöostaasi tagamiseks tuleb säilitada õrn tasakaal soolestiku immuunfunktsiooni ja mikrobiota vahel (Guo et al., 2014; Maynard ja Weinkove, 2018). Varasemad uuringud on samuti näidanud, et krooniline liigne põletik soolestikus on seotud vanusega seotud düsfunktsiooniga barjääri epiteelis ja on vananemise tunnus (Clark et al., 2015; Guo jt, 2014; Ji et al., 2019). . Seega on terve kommensaalse populatsiooni säilitamine kaasasündinud immuunhomöostaasi säilitamise kaudu sellises epiteelis paljutõotav lähenemisviis tervise ja pikaealisuse edendamiseks (Bonfini jt, 2016; Broderick, 2016; Clark jt, 2015). Molekulaarsete mehhanismide uurimiseks mis TF-id aeglustavad vananemist, teostasime RNA-seq analüüsi, kasutades tükeldatud soolestikku koos TF-idega või ilma. Meie andmed näitasid, et kontroll-äädikakärbeste soolestikus tugevalt ekspresseeritud geenide rühm võrreldes TF-ga ravitud loomade omaga oli rikastatud geenidega, mis on klassifitseeritud "immuunvastuse" geenideks. Täiendav bioinformaatiline analüüs ja get-PCR testid näitasid, et TF-ide toidulisandiga toidulisandiga pärssis järsult Imd-ga seotud AMP geenide ekspressiooni. CD-1 hiirekatsete tulemused, milles kasutati DSS-i, et kutsuda esile ebanormaalseid immuunvastuseid sooltes, kinnitasid veelgi arusaama, et TF-id toimivad soolepõletiku eest kaitsjatena.
Theaflaviinid pärsivad signaale, määrates Imd amüloidi koostise
Kuidas TF-id negatiivselt reguleerivad Imd signaalirada? Transkriptoomianalüüsi tulemuste põhjal leidsime, et TF-id on Imd signaaliraja võtmetegurite transkriptsioonilise reguleerimise jaoks hädavajalikud. Huvitaval kombel täheldasime SPR-testiga TF-de ilmset seondumisafiinsust puhastatud Imd-valguga, mis viitas tõenäosusele, et TF-id võivad mängida rolli Imd-valgu käitumise või selle translatsioonijärgse modifitseerimisprotsessi kontrollimisel. Varasemad uuringud on toonud esile ubikvitinatsiooni keskset rolli Imd-signaali ülekandes (Kleino ja Silverman, 2014; Myllymaki et al., 2014) ning Imd ubikvitinatsiooni vältimine põhjustab Imd-signalisatsiooni põhjaliku sulgemise (Myllymaki et al., 2014; Thevenon). et al., 2009). Kuid meie in vitro ja in vivoubikvitinatsiooni testid näitasid, et TF-id ei mõjuta peaaegu Imd ubikvitinatsiooni mustrit. Hiljutine uuring on näidanud, et bakteriaalsete peptidoglükaanide äratundmisel on Drosophila Imd raja aktiveerimiseks vajalik amüloidi moodustumine (Kleino et al., 2017). Huvitaval kombel näitasid meie SDD-AGE ja ThTbinding testid, et TF-id takistavad Imd ühinemist. Imd agregatsiooni vältimine Imd mahalöömise või mutatsiooni teel soolerakkudes muutis ilmselt TF-de kasuliku mõju eluea pikendamisele. Meie järelduse täiendavaks kinnitamiseks oleks huvitav uurida, kas TF-id ei ole enam funktsionaalsed puuviljalendajate eluea pikendamiseks, kui Imd konserveeritud krüptiline RHIM (cRHIM, aminohapped 118. kuni 121. h) motiiv on konkreetselt välja tõrjutud. põhineb järeldusel, et Imd-s toimuv kuritegu on selle agregeerumise ja amüloidi moodustumise jaoks hädavajalik (Kleino et al., 2017). Sellegipoolest tõstab meie uuring esile TF-de keskset rolli soolestiku homöostaasi ja vananemisprotsessi kontrollimisel, võib-olla Imd koalestsentsi moduleerimise kaudu. Tulevased uuringud peaksid keskenduma sellele, et uurida, millised Imd jäägid või piirkonnad on TF-idega seotud ja kuidas see sidumine aitab vältida Imd kondenseerumist. Veelgi enam, meie leiud imetajate süsteemis näitasid, et TF-id võivad käärsoole tõhusalt kaitsta eksogeense mürgise kemikaali DSS põhjustatud põletiku eest, mis viitab TF-de konservatiivsele regulatiivsele rollile soolestiku homöostaasi säilitamisel. Tasub uurida, kas TF-id mängivad rolli valgu kogunemise reguleerimisel imetajate kudedes.
See artikkel on välja võetud saidilt zhongwenxie@ahau.edu.cn
