Kvertsetiini mitsellkoostis hoiab ära tsisplatiini nefrotoksilisuse
Mar 16, 2022
lisateabe saamiseks:ali.ma@wecistanche.com
Alfredo G. Casanova, Marta Prieto, Clara I. Colino jt.
Antioksüdantne flavonoidkvertsetiinon näidatud, et see takistabnefrotoksilisusloommudelites ja kliinilises uuringus ning on seega väga paljulubav profülaktiline kandidaat väljatöötamisel.kvertsetiinlahustuvus on väga madal, mis takistab kliinilist kasutamist. Selle töö eesmärk oli uurida rottidel Pluronic F{0}}kapseldatud mitsellaarse koostise biosaadavust ja nefroprotektiivset efektiivsust.kvertsetiin(P-kvertsetiin), parema vees lahustuvusega. P-i intraperitoneaalne manustaminekvertsetiinpõhjustab plasmakontsentratsiooni ja biosaadavuse suurenemistkvertsetiinvõrreldes looduslike ekvimolaarse manustamisegakvertsetiin. Veelgi enam, P-kvertsetiinsäilitab üldised nefroprotektiivsed omadused ja isegi veidi parandab mõningaid neerufunktsiooni parameetreid võrreldes loomulikekvertsetiin. Täpsemalt P-kvertsetiinvähendas plasma kreatiniini (3,4±0,5-lt 1,2±0,3 mg/dL-le) ja uureasisaldust (490,9±43,8-lt 184,1±-le) 50,1 mg/dl) ja kreatiniini kliirensi vähenemine ({{20}},08±0,02 kuni 0,58±0,19 ml/min), mis on põhjustatud nefrotoksilisest kemoterapeutilisest ravimist tsisplatiin, ja see parandas torukujulise kahjustuse histoloogilisi tõendeid. See uus täiustatud kineetiliste ja biofarmatseutiliste omadustega koostis võimaldab edasist uurimistkvertsetiinNefroprotektiivse kandidaatainena väiksemates annustes ja manustamisviiside kaudu, mis on orienteeritud selle kliinilisele kasutamisele.
Märksõnad:tsisplatiin;nefrotoksilisus; flavonoid;kvertsetiin; nefroprotektsioon; biosaadavus;neerud;mitsellid; lahustuvus; formuleering

Ennetaminenefrotoksilisus
Klõpsake Cistanche para que sirve neeruhaiguse kohta
1. Sissejuhatus
Ravimnefrotoksilisuson tõsine meditsiiniline ja majanduslik probleem [1,2], sest 25 protsenti 100 intensiivraviosakondades enimkasutatavast ravimist on nefrotoksilised [3] janefrotoksilisuson ka kandidaatide languse oluline põhjus ravimite avastamise protsessis 4]. Tsisplatiin on plaatinapõhine kasvajavastane aine, mida kasutatakse sageli mitmesuguste tahkete pahaloomuliste kasvajate raviks [5, 6]. Peaaegu 30 protsenti patsientidest näitavadnefrotoksilisusesimese kümne päeva jooksul pärast tsisplatiini manustamist, mis piirab oluliselt selle annust ja terapeutilist efektiivsust [5-8]. Äge tsisplatiinnefrotoksilisuspõhjustab tubulopaatiat, mis tuleneb 5-kordsest kuhjumisest proksimaalse tuubuli epiteelirakkudes, võrreldes selle plasmakontsentratsiooniga [9-1l], ja vähemal määral distaalses tuubulis [12,13 ].
Tsisplatiini tubulopaatiaga kaasnevad elektrolüütilised häired (peamiselt hüpomagneseemia ja hüpokaleemia) jaägeneerudvigastus(AKI). AKI on tavaline sündroom, mida iseloomustab glomerulaarfiltratsiooni kiiruse (GFR) järsk langus, raske asoteemia ja sageli oliguuria või anuuria [7,14]. Lisaks aitab tsisplatiini poolt indutseeritud AKI-le kaasa ka endoteeli düsfunktsioon, mis suurendab neerude veresoonte resistentsust ja kahjustab autoregulatsiooni [9]. Tavaliselt on AKI pöörduv seisund, millel on siiski oluline mõju patsientide tulemustele, sealhulgas kõrgenenud haiglasuremus (üle 50 protsendi juhtudest kriitiliselt haigete seas), pikaajaline haiglaravi, täiendavad tervishoiukulud ja keskmised ja pikaajalised stsenaariumid, suurenenud risk haigestudakrooniline neeruhaigusning üldise ja kardiovaskulaarse suremuse kohta [7,14]. Subtsellulaarsel ja molekulaarsel tasemel põhjustab tsisplatiini tubulaarset tsütotoksilisust mitokondriaalne kahjustus, mis piirab hingamist, tekitab oksüdatiivset stressi ning kutsub esile apoptootilise ja nekrootilise rakusurma ning kahjuliku põletikureaktsiooni [13, 15, 16]. Oksüdatiivset stressi peetakse tsisplatiini tsütotoksilisuse keskseks mehhanismiks janefrotoksilisus[12,13,15-17], mis tuleneb reaktiivsete hapnikuliikide suurenenud tootmisest ja endogeense antioksüdantse ensüümi barjääri nõrgenemisest [5,7,18].
Tsisplatiini tõhusad profülaktilised meetmednefrotoksilisuson rahuldamata kliiniline vajadus selle farmakotoksikoloogilise profiili parandamiseks ja selle kasulikkuse maksimeerimiseks. Olemasolevad ennetusstrateegiad, sealhulgas intensiivne hüdratsioon, on näidanud vaid piiratud kaitset [6, 19]. Väljatöötamisel on uued strateegiad, mis põhinevad nefroprotektiivsete ravimite koosmanustamisel. Nefroprotektiivsete ainete kandidaatide hulka kuuluvad magneesiumipreparaadid |6,9 ja kõige silmatorkavamalt mitmesugused antioksüdandid [6,20,21]. Flavonoidid on nefroprotektiivsete polüfenooltoodete perekond, mis on saadud köögiviljadest, puuviljadest, pähklitest ja veinist ning millel on tugevad antioksüdantsed omadused [22].kvertsetiinon flavonoid, millel on palju kasulikke toimeid [23, 24], sealhulgas reaktiivsete hapnikuliikide eemaldamine, trombotsüütide aktivatsiooni pärssimine, endoteeli kaitse, põletiku moduleerimine, apoptoosi pärssimine, kasvaja supressioon ja nefroprotektsioon. Kaasmanustaminekvertsetiinkoos tsisplatiinraviga loomkasvaja mudelis tagab nefrokaitse ilma kasvajavastast toimet häirimata |25,26]. Tegelikult tuvastati ajakohastatud metaanalüüskvertsetiinväga paljulubava kandidaadina neuroprotektorina edasiseks kliiniliseks arendamiseks [21]. Järjekindlalt teatas hiljutine kliiniline uuring selle kaitsvast toimestkvertsetiinkontrastainest põhjustatud nefropaatia (CIN) kohta [27].
Tugev piirang võimalikule rakendamiselekvertsetiin(mida jagavad üldiselt flavonoidid) on selle madal vees lahustuvus, mis tuleneb selle keemilisest struktuurist ja osadest, mis vähendavad selle imendumist peensooles ning seega ka selle biosaadavust ja efektiivsust [23,24,28]. Huvitav on see, et lipofoobne glükooskvertsetiinkonjugaadid (glükosiidid) on oluliselt paremini biosaadavad kui lipofiilsed aglükoonid, kuna viimased lahustuvad soolestiku luumenis vähem [24]. Tegelikult,kvertsetiinsibulast pärit glükosiidid näitavad kõrgeimat imendumiskiirust ja toidurasv suurenebkvertsetiinaglükooni imendumine peensooles [29]. Väga madal vees lahustuvuskvertsetiinmitte ainult ei takista selle kliinilist kasutamist praktilistel manustamisviisidel (st suukaudselt, intravaskulaarselt), vaid piirab ka prekliinilisi uuringuid. Sellegipoolest saab loommudelites kontseptsiooni tõestamise eesmärgil kasutada alternatiivseid manustamisviise (st intraperitoneaalselt) koos ravimisuspensioonidega [25, 26].
kvertsetiinon välja töötatud uute kandematerjalidega preparaadid, millel on parem vees lahustuvus ja mille biomeditsiinilised omadused vajavad testimist. Pluronic poloksameerid on kandematerjalide klass, mis majutavad vees lahustumatuid ühendeid ja suurendavad nende imendumist tänu nende võimele moodustada vesikeskkonnas mitselle [30]. Siin püstitasime hüpoteesi, et mitsellaarne preparaatkvertsetiineelnevalt kirjeldatud Pluronic F127-ga kapseldatud [31, säilitaks looduslike nefroprotektiivsed omadused.kvertsetiinpakkudes samal ajal täiustatud biofarmatseutilisi omadusi käsitsemiseks, formuleerimiseks ja manustamiseks.

Ennetadanefrotoksilisus:kvertsetiin
2. Tulemused
Biosaadavuse ja nefroprotektsiooni uuring viidi läbi uue mi-cellar preparaadigakvertsetiinkapseldatud Pluronic F127[31-ga ja meie traditsioonilise loodusliku koostisegakvertsetiin|25,26|(vt allpool Materjalid ja meetodid). Kui viimane oli tensoaktiivset ainet sisaldav suspensioon, siis esimene oli soolalahus ilma täiendavate lisanditeta. Meie traditsiooniline loodusliku koostiskvertsetiinsobis ainult eksperimenteerimiseks, paigal jätmisel sadenes välja ning seda oli raskem käsitseda ja süstida. Seevastu mitsellkoostis käitus lahusena ega näidanud kasutamisega mingeid ebamugavusi.
2.1. Biosaadavuse uuring
Võrdleva biosaadavuse meetodina evolutsioonikvertsetiin(Q) plasmakontsentratsiooni uuriti pärast ühekordset intraperitoneaalset loodusliku ja P-boolust.kvertsetiin(PQ). Joonis 1 näitab keskmistkvertsetiinplasmataseme kõverad, mis on saadud pärast annuse manustamistkvertsetiinvõi P-kvertsetiin. Maksimaalsed ravimikontsentratsioonid (Cmax), mida täheldati rühmades Q ja PQ, olid vastavalt 1,14 ± 1,28 ug/mL ja 8,90 ± 4,62 ug/mL, st P- 78-kordne kasv.kvertsetiin, mis näitab, et mitsellaarne preparaat suurendas ravimi imendumist.
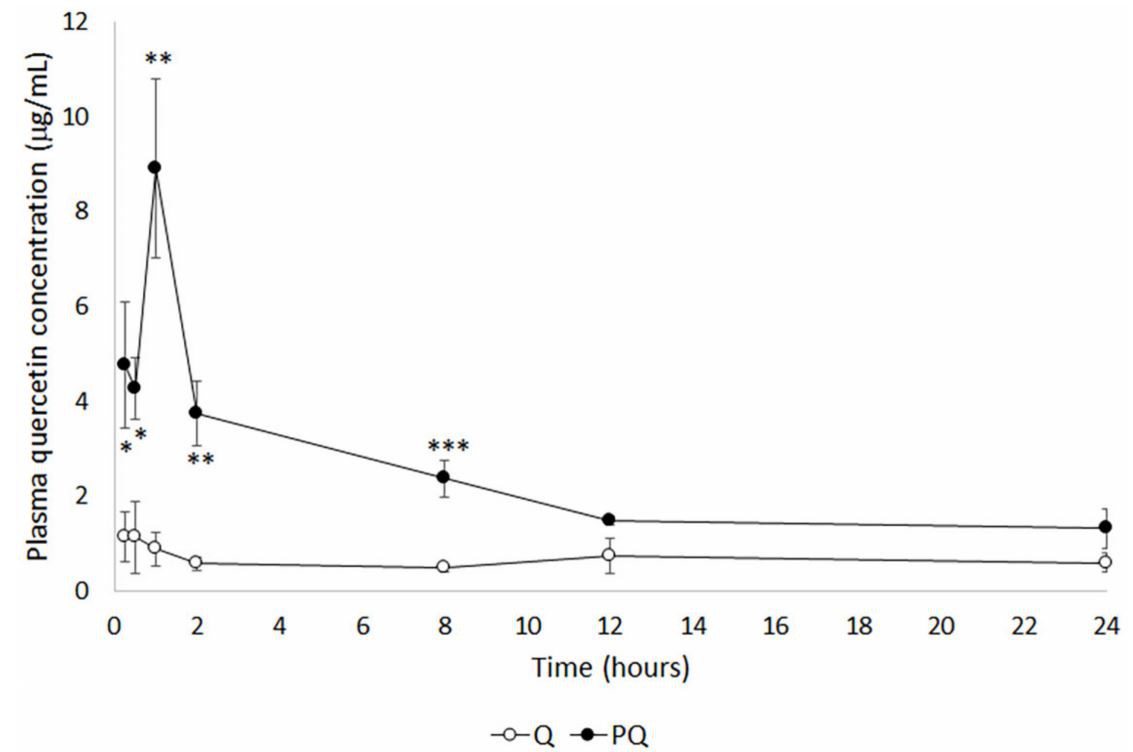
Joonis 1. Kvertsetiini plasmakontsentratsiooni areng pärast ekvimolaarse P-kvertsetiini ja loodusliku kvertsetiini ühekordset intraperitoneaalset manustamist.
Väärtused on väljendatud keskmise ± keskmise standardveana (SEM) (n=5 rühma kohta). *lk<0.05;><0.01;><0.001 vs.qgroup.="">kvertsetiin(50mg/kg, ip.);PQ:100mg/kg.pP-kvertsetiin(sisaldab 50 mg/kgkvertsetiin).
Tabel 1. Farmakokineetilised parameetrid pärast P-kvertsetiini ja loodusliku kvertsetiini intraperitoneaalset manustamist (n=5 rühma kohta).
K: kvertsetiin(50 mg/kg, ip; PQ: P-kvertsetiin(100 mg/kg, ip).AUCo24: osakõvera alune pindala; AUCo: kogukõvera alune pindala; MRT: keskmine viibimisaeg; t1/2: eliminatsiooni poolväärtusaeg; X: lõppfaasi kalle.
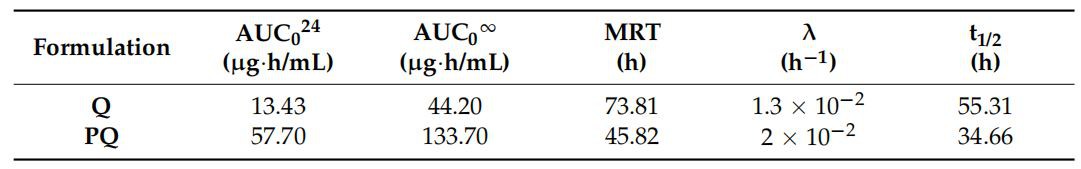
Tabelis 1 on näidatud mudelist sõltumatud farmakokineetilised parameetridkvertsetiinrottidel pärast ühekordse loodusliku boolusannuse manustamistkvertsetiinvõi P-kvertsetiin. Cmax-i saavutamise aega suurendati 15 minutilt (looduslikukvertsetiin) kuni 1 h (P kvertsetiini puhul). See viivitus võib olla tingitud rakenduse pidevast vabastamisestkvertsetiinmitsellaarsest koostisest. Rottide üldine kokkupuude flavonoididega oli oluliselt suurem P-kvertsetiin, mida näitab suurem kõveraalune pindala (AUC), mis tähendab 302,5 protsenti kõrgemat biosaadavust. Need tulemused viitavad sellele, et mitsellkoostise suurem lahustuvus suurendab selle imendumist.
2.2. Nephroprotectioe efektiivsuse uuring 2.2.1. Füsioloogiline seisund
Nagu näitab kehakaalu areng (joonis 2a), halvenes üldine tervis pärast tsisplatiiniga ravi võrreldes kontrollloomadega. Kumbki mitte loomulikkvertsetiinega P-kvertsetiinmuutis oluliselt tsisplatiini toimet. Samas mõlemadkvertsetiinravid hoidsid peaaegu täielikult äraneerudtsisplatiini poolt indutseeritud kehamassi suhe (joonis 2b) – parameeter, mis teadaolevalt korreleerub hõõrdumise ulatusega.nefrotoksilisus[32].
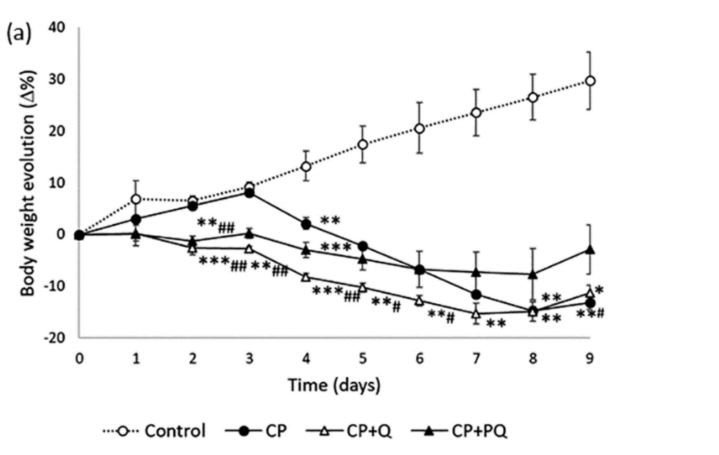
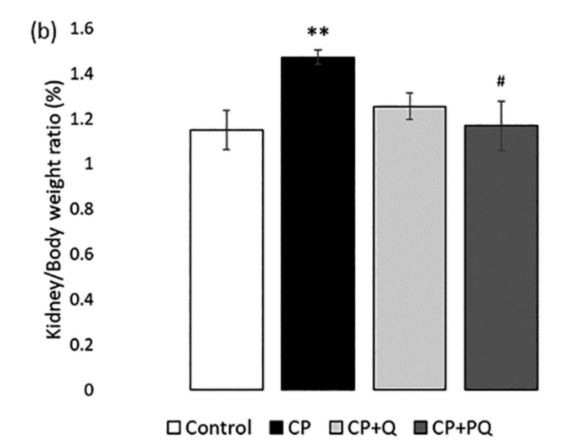
Joonis 2. Üldise tervisliku seisundi areng. a) Kehakaalu protsentuaalne kõikumine katse jooksul; b) Neerude ja kehamassi suhe 9. päeval.
Väärtused on väljendatud keskmisena ± SEM (n=3-5 rühma kohta). *lk<><0.01;><0.001vs.controlgroup.><0.05;><0.01 vs.="" cp="" group.cp:cisplatin(6.5="" mg/kg,="" i.p.)on="" day="">
CP pluss Q:kvertsetiin(50 mg/kg, ip) 9 päeva ja tsisplatiin (6,5 mg/kg, ip) 3. päeval; CP pluss PQ:P-kvertsetiin(100 mg/kg, ip) 9 päeva ja tsisplatiin (6,5 mg/kg, ip) 3. päeval.
2.2.2.Neerufunktsiooni ja neerukudede hindamine
Rahvusvaheliste kriteeriumide kohaselt määratakse ja diagnoositakse AKI plasma kreatiniini kontsentratsiooni (Crp) [33-35], glomerulaarfiltratsiooni kiiruse (GFR) asendusmarkeri, tõusu järgi. Asoteemia indikaatoritena hinnatakse sageli ka muid parameetreid, nagu plasma uurea kontsentratsioon [36-38]. Crp ja plasma uurea suurenemine on märgid vähenenud GFR-ist ja AKI-st. Meie uuringus kahjustas tsisplatiin tõsiselt neerufunktsiooni ja seda toimet leevendas osaliseltkvertsetiin. P-kvertsetiinnäitas veidi julgemat tegevust kui loomulikkvertsetiin, mida näitavad kergemad kahjustused ja paranenud taastumisprofiil (joonis 3). Tsisplatiini (CP) rühma rottidel esines ilmne AKI, kuna nende plasma kreatiniini ja uurea tase tõusis progresseeruvalt ja märkimisväärselt võrreldes kontrollrühmadega (joonis 3a, b). Need parameetrid suurenesid ka CP pluss Q ja CP plus PQ rühmades, kuid oluliselt väiksemal määral. Erinevused CP pluss Q ja CP plus PQ rühmade vahel ei olnud statistiliselt olulised, kuid P-ga ravitud rotidkvertsetiinnäitasid veidi madalamat kreatiniini ja uurea taset kui looduslike preparaatidega ravitudkvertsetiin. Kreatiniini kliirens (ClCr) on GFR mõõtmise standardmeetod]39,40]. Kooskõlas Cr andmetega kutsus tsisplatiin esile sügava languse, mida osaliselt leevendaskvertsetiin(Joonis 3c). Sel juhul oli aga märgatav erinevus P-kvertsetiini ja loodusliku kvertsetiini vahel, kusjuures esimene oli paranemise parandamisel ja kiirendamisel oluliselt tõhusam. Pange tähele, et Clcr ja Crpl käituvad pöördvõrdeliselt, mis on ilmne ainult püsiolekus. AKI ajal muutub neerufunktsioon aga pidevalt ja kiiresti, mille tulemuseks on selle seose kerge lahtihaakimine.
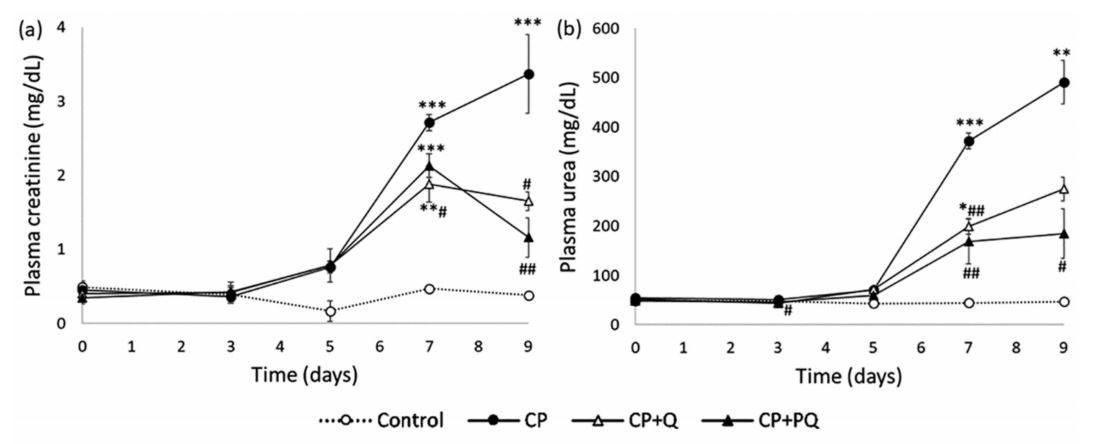
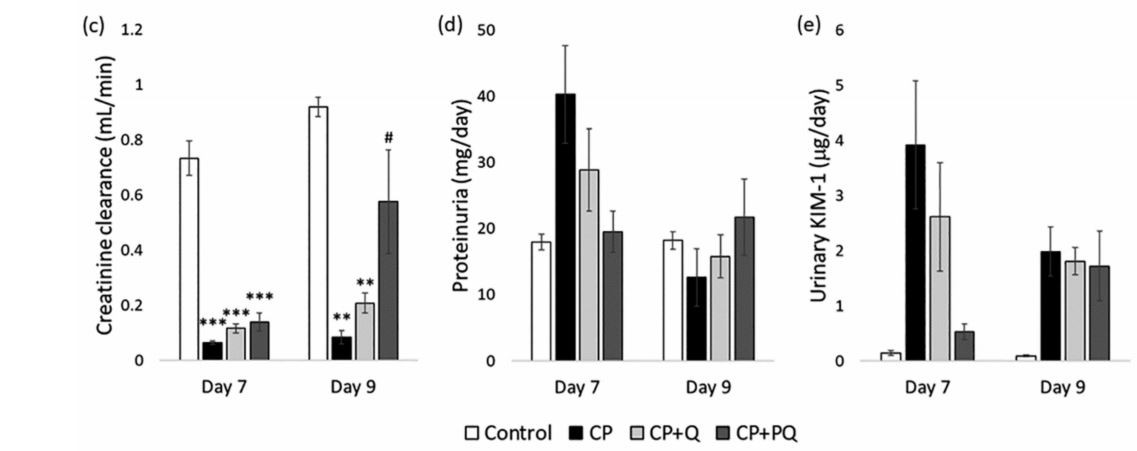
Joonis 3. Neeruparameetrite areng.
a) plasma kreatiniini kontsentratsioon; b) uurea kontsentratsioon plasmas; c) kreatiniini kliirens; d) proteinuuria; ja (e)KIM{0}} eritumine uriiniga.
Väärtused on väljendatud keskmisena ± SEM(n=3-5 rühma kohta). *lk<><><0.001 vs=""><0.05;><0.01vs.cp group.cp:cisplatin(6.5="" mg/kg,i.p.)on="" day="">
CP pluss Q:kvertsetiin(50 mg/kg, ip) 9 päeva ja tsisplatiin (6,5 mg/kg, ip) 3. päeval; CP pluss PQ:P-kvertsetiin(100 mg/kg, ip.) 9 päeva ja tsisplatiin (6,5 mg/kg, ip) 3. päeval.KIM-1:neerudvigastusmolekul 1.
Proteinuuriat mõõdetakse sageli ka neerupatoloogia kontekstis. Sõltuvalt kahjustuse algkujust võib proteinuuria olla glomerulaarse päritoluga (st glomerulaarfiltratsiooni barjääri suurenenud läbilaskvus) või, nagu tsisplatiini puhul.nefrotoksilisus[13], võib see tuleneda torukujulisest vigastusest tingitud defektsest tubulaarsest reabsorptsioonist. CP ja CP-Q rühmades tuvastati proteinuuria mitteoluline suurenemine (kuigi viimases vähem märgatav) 7. päeval, mis normaliseerus 9. päevaks. Samamoodi ilmnes tubulaarse kahjustuse biomarkeri (st.neerudvigastusmolekul 1; KIM-1)[41,42] suurendas tsisplatiin märkimisväärselt ja seda suurenemist vähendasid mõlemadkvertsetiin, kuigi P-kvertsetiinoli jälle veidi tõhusam.
Neerukoe histoloogiline uuring oli kooskõlas biokeemiliste leidudega. Tsisplatiiniga ravitud rottide proovidel ilmnes välimise medulla ülemises ribas massiivne torukujuline nekroos, millega kaasnes teatav kortikaalne kiindumus jakvertsetiinvähenenud kortikaalne vigastus (joonised 4 ja 5). Rottidel, kes said ainult nefrotoksilist ainet, tekkis torukujuline laienemine ja obstruktsioon (näha kogunenud hüaliinmaterjalina) ning tubulaarnekroos koos epiteeli eemaldamise ja rakkude hõrenemisega. Mõlemadkvertsetiinravi vähendas samamoodi tsisplatiini poolt põhjustatud kortikaalset kahjustust, kuid ei mõjutanud medullaarset kahjustust (joonised 4 ja 5).
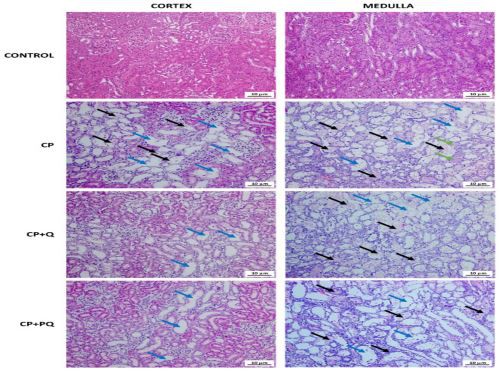
Joonis 4. Hematoksüliini ja eosiiniga värvitud neeruproovide esinduslikud kujutised.
Mustad nooled: torukujuline nekroos ja rakkude hõrenemine; sinised nooled: torukujulised laienemised; rohelised nooled: hüaliinse materjali tubulaarsed ladestused. CP: tsisplatiin (6,5 mg/kg, ip) 3. päeval;
CP pluss Q:kvertsetiin(50 mg/kg, ip) 9 päeva ja tsisplatiin (6,5 mg/kg, ip) 3. päeval; CP pluss PQ:P-kvertsetiin(100 mg/kg, ip) 9 päeva ja tsisplatiin (6,5 mg/kg, ip) 3. päeval.
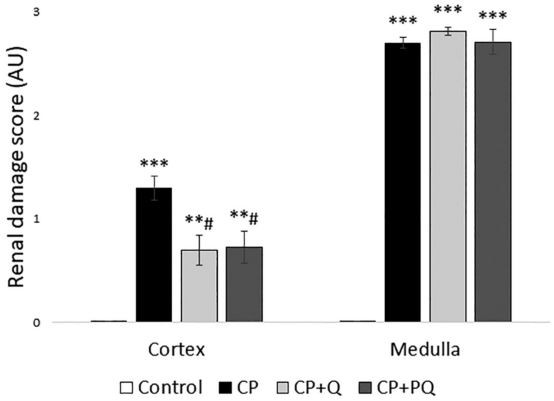
Joonis 5. Neerukahjustuse kvantifitseerimine.
Väärtused on väljendatud keskmisena ± SEM (n =5 kujutist × 3 rotti rühma kohta). * lk<><0.001 vs.=""><0.05 vs.cp="">
CP: tsisplatiin (6,5 mg/kg, ip.) 3. päeval; CP pluss Q:kvertsetiin(50 mg/kg, ip-9 päeva ja tsisplatiin (6,5 mg/kg, ip) päeval 3; CP pluss PQ:P-kvertsetiin(100 mg/kg, ip) 9 päeva ja tsisplatiin (6,5 mg/kg, ip) 3. päeval. AU: suvalised ühikud.
3. Arutelu
Meie tulemused näitavad, et mitsellaarne koostiskvertsetiinkoos Pluronic F127 (P-kvertsetiin), millel on täiustatud biofarmatseutilised omadused, suurendas selle antioksüdandi flavonoidi biosaadavust ja säilitas (või isegi veidi paranes) selle üldised nefroprotektiivsed omadused võrreldes looduslike omadustega.kvertsetiin.
kvertsetiinon peetud paljutõotavaks kandidaadiks, et kaitsta neerukahjustuste eest, mida põhjustavad mitmed ravimid ja toksiinid, sealhulgas tsisplatiin [25,26], metotreksaat [43.44], tsiprofloksatsiin [45], NaF [46], HgCl [47l ja kaadmium [48]. Kuigi need uuringud näitasid prekliinilist efektiivsust,kvertsetiinei ole koostise takistuste ja madala biosaadavuse tõttu sarnastes kliinilistes stsenaariumides testitud, välja arvatud kliiniline uuring, kuskvertsetiinandis teatud kaitse CIN-i eest [27]. Mõlemad piirangud tulenevad vees väga halvast lahustuvusest (ainult 0,01 mg/mL, 25 kraadi juures [49]).kvertsetiinja selle madal stabiilsus (mida mõjutavad temperatuur, pH, hüdroksüülimine, ensümaatiline aktiivsus ja metalliioonid)[28,29,50]. Suukaudselt manustatavkvertsetiinMao väga madala pH (st 1,5) tõttu esineb mao transiidi ajal ulatuslik lagunemine[50]. Peensooles, mis on keemiliselt kaitstud kõrgema pH-ga (7,5), ülejäänudkvertsetiinimendub minimaalselt. Seetõttu on selle biosaadavuse ja bioloogilise efektiivsuse suurendamiseks välja töötatud uued kvertsetiini koostised, mille eesmärk on parandada selle vees lahustuvust ning kaitsta selle aktiivseid osi lagunemise eest, sealhulgas liposoome, nanoosakesi, nanoemulsioone ja mitselle [28].
Meie mitsellkoostis Pluronic F127-ga suurendabkvertsetiinlahustuvus on kümnekordne ja in vitro uuringutes on see näidanud paremat lahustumiskäitumist simuleeritud mao- ja soolevedelikes, kuna sellega saavutatakse osakeste suuruse märkimisväärne vähenemine ja homogeensem dispersioon.kvertsetiinpolümeermaatriksis I3l. See koostis annab oluliselt suurema kogusekvertsetiinvereringesse, mille tulemuseks on 3-kordne biosaadavus, mis kummalisel kombel väljendub vaid veidi suuremas nefroprotektiivses toimes. Kokkuleppel ei täheldanud me täiendavat nefroprotektiivset toimet, kui kasutasime looduslikku suuremat annust (st 100 mg/kg).kvertsetiinvarasemates katsetes (meie avaldamata tähelepanekud)[25,26]. Nendes uuringutes oli meie tõlgendus, et tõenäoliselt suuremad annused ipkvertsetiin(i.e., >50 mg/kg) ei toonud kaasa vähenenud lahustuvuse tõttu suurenenud biosaadavust, mille tulemusena ei suurenenud netoabsorptsioon oluliselt. See langes kokku imendumata kollaste ladestustegakvertsetiinleitakse ohverdamisel kõhukelmeõõnest. Lisaks näitavad meie praegused tulemused, et isegi kõrgemad kvertsetiini plasmakontsentratsioonid (nagu need, mis saadi P-kvertsetiiniga) annavad vaid veidi suurema efekti. Sestkvertsetiinjaotust on lihtsustatud kujul selgitatud esimese järgu kahekambrilise mudeliga [51], ligipääs sihtrakkudele põhisektsioonist (st vereringest) ei tundu olevat piiranguks. Seega on põhjus, miks maksimaalne nefroprotektiivne toime saavutatakse loodusliku kvertsetiini madalamate plasmakontsentratsioonidega, endiselt tabamatu.
Sellel on praktiline mõju edasisele arengulekvertsetiinprofülaktilise nefroprotektorina. Esiteks avavad need tulemused võimaluse uurida, kas väiksemad annustamisrežiimid on sama tõhusad, kuna P- biosaadavus on liiga suur.kvertsetiinvõib ohverdada ilma ravitoimet kaotamata, kuid see suurendab turvaprofiili. Teiseks on nüüd avatud võimalus suukaudseks manustamiseks, mida tuleb siiski uue ravimvormi jaoks testida. Kõhuõõnest imendumine väldib suukaudsel manustamisel tekkivaid tõkkeid. Oletatakse, et suurem lahustuvus soolestiku luumenis võib põhjustada suurenenud ja settimistkvertsetiinbiosaadavus terapeutilises aknas. Kolmandaks, intravenoosne manustamisviis võib nüüd olla realistlik alternatiiv minimaalse toksilisusega, mis väldiks absorptsioonitõkkeid. Seni on eksperimentaalsed süstitavad ravimvormidkvertsetiinkasutas lahustina dimetüülsulfoksiidi (DMSO) [51].
On teada, et tsisplatiin akumuleerub proksimaalsetes ja distaalsetes tuubulites ja kahjustab neid ning kutsub esile tuubulite epiteelirakkude apoptoosi ja nekroosi, olenevalt kontsentratsioonist [16]. Proksimaalne S3 segment on kõige enam mõjutatud, kuigi ka S1 ja S2 on suuremate annuste tõttu üha enam kahjustatud. Kooskõlas selle teadaolevate antiapoptootiliste omadustega tuubulirakkudel [52,53],kvertsetiinvähenenud kortikaalne tubulaarne epitelisatsioon. Mõlema ravimvormi puhul täheldatud identne efekt tugevdab ideed, etkvertsetiinjaotuskineetikaneerudon meie uuringus küllastunud. Lisaks on seesneerud, kvertsetiinnäitab erinevat käitumist piki nefroni. Tegelikult,kvertsetiinei avaldanud mingit mõju välimisele medullale, kus leiti proksimaalsete tuubulite S3 segment.kvertsetiinnäib kogunevat S1, S2 või distaalsetesse tuubulitesse, mis asuvad ajukoore lähedal. Kuna pole teada, kuidas (st millised transporterid või difusiooniteed) ja kust (st luminaalne või basolateraalne külg)kvertsetiinjuurdepääsu torukujulistele rakkudele, on nende erinevuste selgitamiseks vaja rohkem uurida.
Mõõdukas kortikaalse koe säilimine võib seletada ainult osaliselt selle mõjukvertsetiinneerufunktsiooni (st GFR) suhtes. Täiendav kaitse võib tekkida vaskulaarsete mõjude tõttukvertsetiin. Endoteeli funktsioon osaleb neerude verevoolu (RBF) ja GFR reguleerimises, moduleerides aferentset ja eferentset arteriooli kontraktiilset tooni [54-57]. Tsisplatiin kutsub esile endoteeli düsfunktsiooni ja arvatakse, et see aitab oluliselt kaasa GFR langusele koos neeru aferentse vasokonstriktsiooniga, mille põhjustavad tubuloglomerulaarsed tagasiside mehhanismid (aktiveeritakse tubulaarsete kahjustuste tõttu) ja põletikulised tsütokiinid [13, 58]. Tõepoolest, endoteeli düsfunktsiooni pöördumine on laialdaselt tunnustatud mõjukvertsetiin(ja flavonoidide kohta üldiselt)[59-61l, mis võib selgitada, mikskvertsetiinparandab RBF-i (ja seega ka GFR-i), nagu varem teatatud [25]. Lisaks võivad need endoteeli-vaskulaarsed toimed aidata selgitada P- veidi suuremat efektiivsust.kvertsetiinneerufunktsiooni parandamiseks ja neerufunktsiooni taastumiseks. Tõenäoliselt ei ole põhjendatud oletada, et suurem biosaadavus võib avaldada julgemat mõju otseses kokkupuutes verega endoteeli pesasse.
Mõned pärast manustamist täheldatud toimedkvertsetiinseda võivad avaldada selle metaboliidid.kvertsetiinmetaboliseerub soole limaskestas ja maksas glükuronisatsiooni-, sulfaadimis- ja metüülimisreaktsioonide kaudu [62], kusjuures kõige levinumad metaboliidid on glükuroniidi metaboliidid vereringes [63]. TäpsemaltkvertsetiinOn näidatud, et -3-bO-glükuroniidil (Q3GA), mis on peamine plasmametaboliit, on põletikuvastane ja vaskulaarne toime nii vahetult kui ka pärast metaboliseerumist tagasi aglükooni vormiks [64]. Vaja on rohkem uuringuid, et mõista neuroprotektsiooni eest vastutavaid spetsiifilisi metaboliite ning nende erinevat tootmist ja muundumist erinevatest manustamiskohtadest nende lõppsihtmärkideks.
Kokkuvõttes näitab see esialgne uuring P- terapeutilist potentsiaali.kvertsetiintäiustatud ravimvormina, millel on täiustatud biofarmatseutilised ja farmakokineetilised omadused, mis on kasulik edasiseks arendamiseks ja tulevaseks kliiniliseks kasutamiseks haiguse profülaktikas.nefrotoksilisus.

Kvertsetiini eelised nefrotoksilisusele
4. Materjalid ja meetodid
Kõik kemikaalid ja reaktiivid osteti Merckist (Darmstadt, Saksamaa), välja arvatud juhul, kui on märgitud teisiti.
4.1.Mitsellpreparaadi valmistamine (P-kvertsetiin) ja loomulikkvertsetiinFormulatsioon
kvertsetiinhüdraat (minimaalne puhtusaste 95 protsenti) saadi firmalt Acros Organics (Madrid, Hispaania) ja etüleenoksiid-propüleenoksiidi plokk-kopolümeeri Pluronic F127 (keskmine molekulmass 12,6 kDa, hüdrofiilsus-lipofiilsuse tasakaal 22) hankis BASF (Lud R amwiin, Hafen Saksamaa). Mitsellkoostise valmistamiseks kasutati superkriitilist antisolventi sadestamise tehnikatkvertsetiin/Pluronic F127 osakesed (P-kvertsetiin) nagu eelnevalt kirjeldatud [31]. Saadud Pluronic-kvertsetiinpreparaadi suhteline koostis oli 50 protsenti /50 massiprotsenti Pluronic F127/kvertsetiin. Loomuliku jaokskvertsetiinkoostis,kvertsetiinsuspendeeriti 0,16 protsenti Tween 20 soolalahuses, nagu eelnevalt kirjeldatud [25,26].
4.2. Loomad ja bioeetika
Kõik protseduurid kiitsid heaks Sala-manca ülikooli bioeetikakomitee ning Kastiilia ja Leoni piirkondlik valitsus, põllumajandus- ja loomakasvatusministeerium (kood: 0000037, 27. juuli 2015). Loomi käideldi vastavalt Euroopa Ühenduse Nõukogu direktiivi 2010/63/UE juhistele ja Hispaania kehtivatele seadustele loomade katseloomade kasutamise ja hooldamise kohta (RD53/2013, 01. veebruar 2013). Isaseid Wis-tõrva rotte (200-250 g) peeti Salamanca ülikooli loomamajas kontrollitud keskkonnatingimustes ning neil oli tasuta juurdepääs veele ja tavalisele toidule.
4.3. Biosaadavuse uuring
Rotid jagati kahte katserühma: O (n=5), kus loomad said ühekordse annusekvertsetiin(50 mg/kg); ja PQ(n=5), mille puhul loomad said ühe ip ekvimolaarse annuse P-kvertsetiin(100 mg/kg (st sisaldab 50 mg/kgkvertsetiin). Seejärel võeti vereproovid etüleendiamiintetraäädikhappega (EDTA) kaetud katsutites väikesest sisselõikest sabaotsas järgmistel aegadel:0.25,0.5,1,2,8, 12 ja 24 tundi. Plasma saadi tsentrifuugimise ja 10 µl 10 mM askorbiinhappega (et vältidakvertsetiindegradatsioon) lisati 100 μL plasmale ja külmutati -80 kraadi juures kuni analüüsimiseni.kvertsetiinkontsentratsioonid määrati pöördfaasi kõrgsurvevedelikkromatograafia (HPLC) meetodil UV-detektoriga. Kasutati Prosper 3 um osakeste suurusega C18 kolonni, mille liikuv faas koosnes 28 protsendist atsetonitriilist ja 72 protsendist 0,2 protsendilisest ortofosforhappe vesilahusest voolukiirusel 1 ml/min. Tuvastamise lainepikkus oli 371 nm. Enne kromatograafiaseadmesse süstimist viidi proovid läbi glükuroniseerimise protsessi, et määrata kogusisaldus.kvertsetiin. Sel eesmärgil lisati 100 μL plasmale 1000 ühikut Helix pomatia -glükuronidaasi 0,1 M atsetaatpuhvris (pH 5) ja seda segu inkubeeriti 37 kraadi juures 1 tund. . Seejärel viidi läbi ekstraheerimine 100 µl 0,5 M80-20 atsetonitriili/äädikhappe seguga (kolm korda). Kui supernatant oli lämmastikuvoolus aurustunud, lahustati kuiv jääk uuesti 40 µl liikuvas faasis ja 20 µl süstiti HPLC süsteemi.
4.4. Nefroprotektsiooni uuring
Rotid jagati järgmistesse katserühmadesse (joonis 6): Kontroll- (n=3) loomad said 9 päeva jooksul intraperitoneaalselt (ip) kandjat (NaCl0,9 protsenti); CP(n=5) loomad said katse 3. päeval ühekordse nefrotoksilise annuse tsisplatiini (6,5 mg/kg, ip); CP pluss Q(n=5) loomad said päevase annusekvertsetiin(50 mg/kg, ip) 9 päeva jooksul ja ühekordne tsisplatiini annus (6,5 mg/kg, ip) 3. päeval; ja CP pluss PQ (n=5) loomad said päevase annuse P-kvertsetiin(100 mg/kg, ip (st sisaldab 50 mg/kgkvertsetiin)) 9 päeva ja tsisplatiini annus (6,5 mg/kg, ip) 3. päeval.
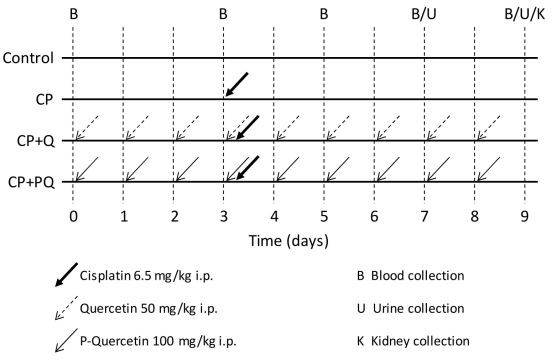
Joonis 6. Nefrotoksilisuse mudeli skeem.
CP: tsisplatiin (6,5 mg/kg, ip) 3. päeval; CP pluss Q:kvertsetiin(50 mg/kg, ip) 9 päeva ja tsisplatiin (6,5 mg/kg, ip) 3. päeval; CP pluss PQ:P-kvertsetiin(100 mg/kg, ip.) 9 päeva ja tsisplatiin (6,5 mg/kg, ip) 3. päeval.
Vereproovid (15{1}} μL) koguti päeval 0, 3, 5, 7 ja 9 hepariniseeritud kapillaaridesse väikesest sisselõikest sabaotsas. Plasma eraldati tsentrifuugimisega (11.000 p/min 3 minutit) ja hoiti temperatuuril -80C. 7. ja 9. päeval koguti 24 tundi uriin metaboolsetesse puuridesse, puhastati tsentrifuugimisega (2000 × g 9 minutit) ja säilitati -80 kraadi juures. Katse lõpus (9. päev) anesteseeriti rotid ja nendeneerudlõigati lahti, kaaluti ja fikseeriti histoloogiliste uuringute jaoks 3,7% paraformaldehüüdis.
Plasma ja uriini kreatiniini mõõdeti Jaffe meetodil [65] põhineva kaubandusliku komplekti abil (QuantiChrom Creatinine Assay Kit, BioAssay Systems, Hayward, CA, USA). Plasma uurea määramiseks kasutati kaubanduslikku komplekti, mis põhines Jungi meetodil [66] (Quan-tiChrom Urea Assay Kit, BioAssay Systems, Hayward, CA, USA). Kreatiniini kliirens (Clcr) arvutati järgmise valemi abil: Clcr=Crur × UF/ Crp); kus Crur vastab kreatiniini kontsentratsioonile uriinis, UF on uriinivool ja Crp on kreatiniini kontsentratsioon plasmas. Proteinuuriat mõõdeti Bradfordi testiga [67]. KIM-1 kvantifitseeriti roti abilNeervigastusmolekuli 1 (KIM-1)ELISA komplekt (Cusabio, Houston. TX, USA). järgides tootja juhiseid.
Histoloogiliste uuringute jaoks sisestati neeruproovid parafiini ja 5 um koelõigud värviti hematoksüliini ja eosiiniga. Fotod tehti Olympus BX51 mikroskoobi all, mis on ühendatud Olympus DP70 värvilise digitaalkaameraga (Olympus, Madrid, Hispaania). Kahjude kvantifitseerimine viidi läbi pimedal viisil, nagu eelnevalt kirjeldatud [68]. Lühidalt öeldes tehti viis juhuslikku fotot kortikaalsest piirkonnast ja viis fotot välisest medullaarsest piirkonnast (st tsisplatiini poolt kahjustatud piirkondadest), mis kaardistasid need piirkonnad ühtlaselt. Iga pilt jaotati 10 identseks osaks (kasutades Microsoft Office PowerPoint 2016 tarkvara), millest igaühele määrati skoor 0 (kahjustusteta), 1 (kahjustuste olemasolu vähem kui 1/3 alast), 2 (kahjustuste olemasolu). vahemikus 1/3-2/3 alast) või 3 (kahjustuste olemasolu rohkem kui 2/3 alast). Kahjustuste hindamisel võeti arvesse tubulaarset nekroosi ja rakkude hõrenemist, torukujulist laienemist, vakuoliseerumist, hüaliini ladestumist ja harja piiride kadumist.
4.5.Statistiline analüüs
Andmed on esitatud kui keskmine ± keskmise standardviga (SEM). Kõrvalekalded tuvastati Grubbsi testiga|69]. Andmete normaaljaotust hinnati Shapiro-Wilki testi abil. Biosaadavuse uuringus võrreldi kahte rühma, kasutades Studenti t-testi või Mann-Whitney U testi. Farmakokineetiline uuring viidi läbi keskmise plasmataseme mudelist sõltumatu analüüsi abilkvertsetiin. Hinnangulised parameetrid suhtelise biosaadavuse hindamisekskvertsetiinolid plasmatasemete osakõvera alune pindala (AUC)24, plasmatasemete kogukõvera alune pindala (AUC)0~, lõppfaasi kalle, eliminatsiooni poolväärtusaeg (ti/2) ja keskmine viibimisaeg (MRT). Farmakokineetiliste parameetrite hindamine viidi läbi, kombineerides trapetsikujulist meetodit osakõvera aluse pindala hindamiseks ja plasmataseme kõvera lõppfaasi mittelineaarset regressiooni. Nefroprotektsiooni uuringu jaoks viidi rühmadevaheliste võrdluste jaoks läbi dispersioonanalüüs (ANOVA) Scheffe testidega või Kruskal-Wallise test. Statistiline analüüs viidi läbi tarkvaraga IBM SPSS Statistics 20.0 (International Business Machines, Armonk, NY, USA). Kunstiteoste ja illustratsioonide loomisel kasutati Microsoft Office Exceli ja PowerPoint 2016 (Microsoft, Redmond, WA, USA).
Viited
1. Awdishu, L.; Mehta, ravimitest põhjustatud RLThe6RNefrotoksilisus. BMCNephrol.2017,18,124. [CrossRefl[PubMed]
2. Perazella, MADrugi kasutamine jaNefrotoksilisusintensiivravi osakonnas.NeerInt.2012,81,1172-1178. [CrossRef] [PubMed]
3. Taber, SS; Mueller, BADrugiga seotud neerufunktsiooni häired. Crit.Care Clin.2006,22,357-374, vi. [CrossRef] Huang, JX; Blaskovich, MA; Cooperi, MACelli ja biomarkeripõhised analüüsid ennustamiseksNefrotoksilisus.
Märge:ülaltoodud ei ole täielik viidete loend
