Metastaatilised doonorilt pärinevad pahaloomulised kasvajad pärast samaaegset kõhunäärme-neeru siirdamist: kolm juhtumiaruannet ja ravistrateegiad
Mar 06, 2022
Kontakt: emily.li@wecistanche.com
Metastaatilised doonorilt pärinevad pahaloomulised kasvajad pärast samaaegset kõhunäärme-neeru siirdamist: kolm juhtumiaruannet ja ravistrateegiad
Dominic Amara, BA,1et al
Taust.Immunosupressiooni peatamine siirdatud patsiendil, kellel on doonorilt saadud pahaloomuline kasvaja, annab teoreetilise kasu, et patsiendi immuunsüsteemi taastamine võimaldab pahaloomulist kasvajat "tõrjuda", kuna pahaloomuline kasvaja pärineb samuti allogeensest koest. See valik on siiski olemas hoiatusega, et tõenäoliselt lükatakse tagasi ka patsiendi allograft(id). Samaaegsel kõhunäärmes -neerud(SPK) retsipientide normaalset jätkuvat funktsioneerimist ja pahaloomuliste kasvajate võimalikku puudumist mõlemalneerudvõi pankreas muudab selle otsuse veelgi keerulisemaks. meetodid. 3 doonorilt pärinevate metastaatiliste pahaloomuliste kasvajatega patsiendi diagrammid pärast SPK-d vaadati retrospektiivselt üksikasjalikult läbi. Pakume ravi- ja juhtimissoovitusi edukate tulemuste ja olemasoleva kirjanduse ülevaate põhjal. Tulemused. Kooskõlas kirjanduse laiaulatusliku ülevaatega oli kõigil kolmel juhul edukas immunosupressiooni täielik lõpetamine, mõlema siiriku eemaldamine ja ühel juhul immuunvastuse suurendamiseks tehtud ravi immuunkontrollpunkti inhibiitoriga. Ühel patsiendil läheb hästi 1 aasta pärast edukat neerude retransplantatsiooni, samal ajal kui teine patsient on SPK retransplantatsiooni ootenimekirjas aktiivne pärast seda, kui 2 aasta jooksul ei esinenud metastaatilise haiguse tunnuseid. Järeldus. Metastaatilise doonorilt pärinevate pahaloomuliste kasvajate edukas ravi nõuab allografti eemaldamist, immunosupressiooni lõpetamist ja adjuvantravi, mis hõlmab aeg-ajalt kontrollpunkti inhibiitorite kasutamist immuunvastuse suurendamiseks.

Cistanche on hea neerufunktsioonile
SISSEJUHATUS
Pankrease-neeru (SPK) retsipiendid vajavad alloimmuunvastuse ja autoimmuunsuse kordumise aeglustamiseks agressiivset immunosupressiooni. SPK programmides kasutatakse üldiselt lümfotsüüte kahandavaid induktsioonirežiime, millele järgneb suhteliselt märkimisväärne immunosupressiooni säilitamise koormus võrreldes raviskeemidega, mida tavaliselt kasutatakse pärast üksinda viibimist.neerudsiirdamine.1 Järelikult on immuunsupressiooni muutmine, kui retsipientidel tekib uus pahaloomuline kasvaja, väljakutse. Doonorilt pärinevate pahaloomuliste kasvajate puhul on immunosupressiooni vähendamise või peatamise võimalus kasvaja "tõrjumiseks" ainulaadne ravivõimalus tingimusega, et allograft lükatakse tõenäoliselt tagasi.2 Selle lähenemisviisi teoreetiline alus on see, et peremeesorganismi immuunsüsteemi taastamine käivitab alloimmuunvastus pahaloomulise kasvaja vastu, kuna pahaloomuline kasvaja pärineb doonorkoest. Immunosupressiooni peatamise, allografti eemaldamise ja meditsiiniliste meetmete, nagu keemiaravi, rakendamise algoritm pole aga täpselt määratletud. Hästi toimiva keskkonna tingimustes võib otsustamine olla keerulineneerudvõi pankrease allotransplantaadiga, mis ei pruugi olla metastaatilise vähiga seotud, kuna immunosupressiooni ärajätmiseks tuleb tõsiselt kaaluda allografti eemaldamist. Arvestades selle teema ja kaasnevate otsuste vähest kirjandust, on selle uuringu eesmärk esitada 3 doonorilt pärinevate metastaatiliste pahaloomuliste kasvajate juhtumit pärast SPK-d ning anda ravisoovitusi, mis põhinevad edukatel tulemustel ja olemasoleva kirjanduse ülevaatel.
MATERJALID JA MEETODID
Tagasiulatuvalt vaadati üle kolm doonorist pärineva pahaloomulise kasvajaga SPK retsipientide diagrammi. Meie asutus ei nõua IRB läbivaatamist kliiniliste juhtumiuuringute aruannete jaoks, mis käsitlevad kuni kolme kliinilise hoolduse käigus tuvastatud kliinilist kogemust. Privaatsuse huvides on eemaldatud kõik ravikindlustuse kaasaskantavuse ja vastutuse seaduse tunnused. Kõigile kolmele patsiendile implanteeriti doonorkõhunääre paremasse niudesoole (süsteemne endokriinne drenaaž) koos enteraalse eksokriinse drenaažiga (doonor-kaksteistsõrmiksool retsipiendi niudesoole) ja doonor.neerudimplanteerimine vasakusse niudeveresoontesse ureteroneotsüstostoomiaga.
JUHTUMI KOKKUVÕTE
Juhtum nr 1: doonori kaudu ülekantav pankrease adenokartsinoom avastati 6 kuud pärast SPK-d
Kliiniline ajalugu
At the time of her SPK, patient 1 was a 42-year-old woman with a history of end-stage renal disease (ESRD) secondary to type 1 diabetes (DM1) with a calculated panel reactive antibodies (cPRA) of 91. She underwent thymoglobulin induction and transitioned to maintenance immunosuppression of tacrolimus (trough goal 5–15 µg/L), everolimus (trough goal 5–7 µg/L), mycophenolate 540mg BID, and prednisone 5mg daily. In the 6 months following transplant, she was seen >10 korda mitmes haiglas korduva kõhuvalu tõttu. Võimaliku äratõukereaktsiooni korral sai ta steroide ja tümoglobuliini. Kaks kuud pärast SPK-d näitas kõhu-vaagna kompuutertomograafia (CT) kõhunäärme allotransplantaadi ümber keerdumist, mis viitas võimalikule pankreatiidile, kuid normaalse lipaasiga. 6-kuu jooksul pärast siirdamist sai teatavaks, et patsiendi doonor oli edastanud adenokartsinoomi veel kolmele retsipiendile, kes said samalt doonorilt elundeid. Sel ajal näitas positronemissioontomograafia (PET) sõlme difuusne neeldumine vasakpoolses supraklavikulaarses, mediastiinumis, mesenteriaalses ja paremas välises niudesõlme piirkonnas.
Juhtimine ja tulemus
Kolm päeva pärast PET-skaneerimist, võttes arvesse muret doonorilt pärineva pahaloomulise kasvaja pärast, eemaldati patsiendilt mõlemad siirikud, millele järgnes immunosupressiooni katkestamine. Võttes arvesse muret metastaatilise haiguse pärast ja agressiivse pahaloomulise kasvaja kinnitatud ülekandumist teistele sama doonori elundite retsipientidele, ei tehtud operatsioonieelset biopsiat, kuna transplantaadid kavatseti eemaldada sõltumata biopsia leidudest. PET-i innukatest lümfisõlmedest ei võetud ka operatsiooni ajal biopsiat. Eksplantaadi patoloogia kinnitas kõhunäärmes laialt levinud adenokartsinoomi, mis on kõige paremini kooskõlas pankrease primaarse kahjustusega ulatusliku lümfovaskulaarse invasiooni ning periovaarsete ja munajuhade kaasamisega. Kasvaja genotüpiseerimine tuvastas mutatsioonid, mis potentsiaalselt võimaldaksid järjestikust jälgimist rakuvaba DNA (cf-DNA) testimise kaudu. Kuue kuu jooksul pärast siirdamise eemaldamist olid varem nähtud PET-i innukad kahjustused taandunud. Nii ristlõike pildistamise kui ka cf-DNA testimise põhjal ei olnud patsiendil vähi tõendeid järgmise pooleteise aasta jooksul. Kui kaalutakse kordamistneeru siirdamine, täheldati tal mitmeid uusi doonor-spetsiifilisi antikehi (DSA). Kaks aastat pärast siiriku eemaldamist, arvestades pikka aega ilma pahaloomuliste kasvajateta, tehti patsiendile teineneerude siirdaminetja taasalustanud immunosupressiooni. Patsiendil oli ka pankrease siirdamine, kuid talle tehti ainult neerude pakkumine, mis võeti vastu, arvestades madalamaid immunosupressiooninõudeid ja muret pikema viivituse pärast, mis tekkis ühilduva pankrease ootamisel, kuna tal oli sel ajal cPRA 100 protsenti. Kuus kuud hiljem raviti teda antikehade poolt vahendatud äratõukepisoodiga ja 11 kuud pärast teistneeru siirdaminetehti PET-uuring, mis ei leidnud vähile viitavaid tunnuseid. Patsiendil on nüüd 3,5 aastat oma esialgsest SPK-st, 3 aastat siiriku eemaldamisest ja 1 aasta temastneeru ümbersiirdamine. Talle on kaalutud pankrease siirdamist, kuid tema hiljutise äratõukereaktsiooni ja jätkuva 100-protsendilise cPRA tõttu ei arvata, et ta kandideerib.

Juhtum nr 2: doonorilt pärinev pankrease adenokartsinoom, mis avastati rohkem kui 10 aastat pärast SPK-d
Kliiniline ajalugu
SPK manustamise ajal oli patsient 2 28--aastane naine, kellel oli alates 12. eluaastast anamneesis DM1 ja ESRD ning kelle cPRA oli 0 protsenti. Talle tehti tümoglobuliini induktsioon ja ta viidi üle takroliimuse (minimaalne eesmärk 5–15 µg/l), mükofenolaadi 540 mg kaks korda päevas ja everoliimusele (minimaalne eesmärk 2–3 µg/l). Tal oli 10 aasta jooksul sündmustevaene kulg ja mõlema transplantaat toimis suurepäraselt, kui tal tekkis krooniline kõhuvalu. Esialgne pildistamine ja endoskoopiad ei tuvastanud valu etioloogiat. Kaksteist aastat pärast SPK-d raviti patsienti tümoglobuliiniga, kuna kahtlustati äratõukereaktsiooni kõrgenenud lipaasi tõttu, kuid biopsiat sel ajal ei tehtud. Lipaas normaliseerus, kuid pildistamine näitas doonori kaksteistsõrmiksoole seina täitumist. Järgnev peene nõela aspiratsioon näitas adenokartsinoomi (joonis 1). Patsiendile tehti PET-CT-uuring, mis näitas lisaks siirdatud pankrease pea ja kaksteistsõrmiksoole manseti märgatavale hüpermetabolismile ka mediastiinumi, vasaku supraklavikulaarset ja retroperitoneaalset lümfadenopaatiat.

Juhtimine ja tulemus
Patsiendi takroliimuse minimaalset eesmärki alandati 3–5 µg/l-ni, mükofenolaati 180 mg-ni kaks korda päevas ja everoliimust jätkati minimaalse tasemega 2–3 µg/l. Kavas oli immuunsupressioon täielikult katkestada, kui vähi tuvastati doonorilt. Kasvajaga viidi läbi lühike tandem-korduspõhine identiteedi kaardistamine, mis kinnitas doonorilt pärinevat pahaloomulist kasvajat. Pärast seda tulemust eemaldati patsiendilt mõlemad siirikud, nii et metastaatilise doonorilt pärineva pankrease adenokartsinoomi raviks võis immunosupressiooni katkestada. Lõplik patoloogia kinnitas 6{11}}cm halvasti diferentseerunud adenokartsinoomi, mis hõlmas pankrease pead koos invasiooniga kaksteistsõrmiksoole, ampulli ja peripankrease pehmetesse kudedesse ning metastaatilise adenokartsinoomiga 5 lümfisõlmes 16-st. Kolm kuud pärast siiriku eemaldamist ei näidanud korduv PET-skaneerimine hüpermetaboolseid kahjustusi, mis viitaksid pahaloomulisele kasvajale, ja tema CA 19-9 langes 85-st enne siiriku eemaldamist normaalsesse vahemikku. PET-skaneeringud 11 kuu jooksul pärast pankreatektoomiat ja nefrektoomiat ei näidanud vähi tunnuseid ja tema CA 19-9 on jäänud normaalseks. Tema cPRA on praegu 99 protsenti ja tal oli ka uus HLA 1. klassi DSA. Patsiendil on nüüd 14 aastat oma esialgsest SPK-st, 2 aastat siirdatud pankreatektoomiast ja nefrektoomiast ning nüüd on ta teise SPK loendis. Onkoloogiateenistus jätkab tema jälgimist ootenimekirjas PET-skaneeringute ja seerumi CA-ga-19-9.

Juhtum nr 3: doonorilt saadud neerurakk-kartsinoom, mis avastati 13 aastat pärast SPK-d
Kliiniline ajalugu
SPK manustamise ajal oli patsient 3 33-aastane naine, kellel oli anamneesis DM1 ja ESRD ning cPRA oli 24 protsenti. Talle tehti tümoglobuliini induktsioon ja ta läks üle immunosupressioonirežiimile, mis sisaldas takroliimust (minimaalne eesmärk 5–15 µg/l), mükofenolaati 360 mg kaks korda ööpäevas ja prednisooni 5 mg päevas. Tal oli suurepärane siirdamise funktsioon ja tal oli 7 aastat tüsistusteta kulg. Tal tekkis biopsiaga tõestatud krooniline allotransplantaadi nefropaatia 7 aastat pärast siirdamist ja ta naasis dialüüsile, kuid jäi insuliinist sõltumatuks. Kolmteist aastat pärast tema SPK-d näitas kirjeldamatu kõhuvalu hindamiseks tehtud CT-skaneerimine uut 3-cm massi.siirdatud neer. Kuus kuud hiljem tehtud ultraheliuuring kirjeldas seda kahjustust veresoonte kahjustusenaneeru siirdamine"s ülemine poolus, mis oli kasvanud 4,7 cm-ni. Kui varem oli anuuriline, tekkis järgmise kuu jooksul patsiendil hematuria koos suureneva kõhuvaluga. Tehtud PET/CT-skaneerimine näitas siirdatud neerus hüpermetaboolset kahjustust ilma metastaatilise haiguseta.
Juhtimine ja tulemus
Arvestades muret doonorilt pärineva pahaloomulise kasvaja pärastsiirdatud neer2 päeva pärast PET-skaneerimist tehti patsiendile siirdatud nefrektoomia. Lõplik patoloogia tuvastas klassifitseerimata alatüübi 58-cm staadiumi T1b neerurakulise kartsinoomi (RCC). Arvestades seda diagnoosi, vähendati patsiendi immunosupressioonirežiimi takroliimuseni eesmärgiga 3–5 µg/l, kuid säilitati muul viisil, et säilitada allotransplantaadi pankrease funktsioon. Järgneva 6 kuu jooksul ei näidanud jälgimis-CT-skaneeringud metastaatilise haiguse tunnuseid. Kuid 11 kuud pärast siirdatud nefrektoomiat tuvastas CT-skaneerimine vasakpoolses alumises kvadrandis 7- mm pehmete kudede sõlme, mida peeti RCC madalat staadiumi arvestades väikeseks kordumise tõenäosuseks. Seeriapildistamine tuvastas kahjustuse aeglase kasvu 1,6 cm-ni. Ta suunati onkoloogiale, kes otsustas ravida seda kahjustust lokaalse kordumisena stereotaktilise kiiritusraviga. Kahjustus näitas järgneva 9 kuu jooksul kerget intervallikasvu ilma metastaatilise levikuta, hoolimata kiiritusravist.
Kaks aastat pärast siirdatud nefrektoomiat avastati tal uued retroperitoneaalsed, kopsu- ja maksasõlmed, mis kahtlustasid metastaatilise haiguse suhtes. Ta oli endiselt insuliinist sõltumatu. Mitmete multidistsiplinaarsete arutelude käigus soovitati immunosupressiooni peatamist, nagu ka türosiinkinaasi inhibeerimist. Ta lükkas need soovitused edasi, kuna pankrease siirdamise tõttu elukvaliteet on dramaatiliselt paranenud ning probleeme pimedaks jäämise ja insuliini manustamisega. Kaks kuud hiljem viidi ta vastuvõtule tugevate valudega ning tal avastati pahaloomuline pleuraefusioon ja metastaasid maksas. Seejärel nõustus ta katkestama immunosupressiooni ja algatama kontrollpunkti inhibiitori nivolumabi. Ta oli endiselt resistentne siiriku pankreatektoomia suhtes, otsustades oodata, et näha, kas ta võib jääda insuliinist sõltumatuks. Neli nädalat pärast nivolumabi alustamist tekkis tal tugev parema alumise kvadrandi valu koos palavikuga. CT-skaneerimine näitas maksa- ja retroperitoneaalsete metastaatiliste haiguste koormuse dramaatilist paranemist, kuid tema siirdatud kõhunääre oli nekrootiline. Patsiendile tehti koheselt siirdatud pankreatektoomia, mis oli raske kohaliku põletiku tõttu. Niudeveeni rekonstrueerimiseks oli vaja veise perikardi plaastrit. Esimesel päeval pärast pankreatektoomiat tromboositi niudeveen, mistõttu oli vajalik trombektoomia ja metallist stendi paigaldamine üle ahenemise. Seejärel vabastati ta jätkuva CT-skaneerimise jälgimisega, mis näitas tema retroperitoneaalse lümfadenopaatia taandumist ja maksa metastaaside suuruse vähenemist (joonis 2). Patsiendil on nüüd 16 aastat oma esialgsest SPK-st, 2,5 aastat siirdatud nefrektoomiast ja 3 kuud siirdatud pankreatektoomiast. Doonorilt saadud RCC puhul jätkab ta igakuise nivolumabi manustamist 1 aasta ja jälgib regulaarselt onkoloogiat.


ARUTELU
See seeria kirjeldab 3 doonorilt pärinevate metastaatiliste pahaloomuliste kasvajatega SPK retsipiendi edukat esialgset ravi. Kirjandus metastaatilise doonorilt pärineva pahaloomulise kasvaja ravi kohta on üldiselt piiratud ja eriti piiratud SPK retsipientide puhul. Suuremasneeru siirdaminekirjanduses on mitmed süstemaatilised ülevaated uurinud doonori poolt ülekantud pahaloomuliste kasvajate juhtimist. Aastal 2013 tuvastasid Xiao jt 104 doonorilt ülekantud juhtumit ja näitasid, et 67 protsendile patsientidest tehti transplantaadi nefrektoomia ja immunosupressioon tühistati, mis on kõige levinum lähenemisviis. Adjuvantkemoteraapia, kiiritusravi ja immunoteraapia kasutamine oli väga erinev, ulatudes 0 kuni 80 protsendini, sõltuvalt kasvajakoest.3 2020. aastal esitasid Eccher jt sarnase analüüsi 234 doonoripäritolu vähiga retsipiendi kohta ja märkisid, et metastaatiline haigus oli isegi selles populatsioonis kõige olulisem surma ennustaja. Dialüüsi juurde naasmise võimaluse tõttu enamikneerudretsipiente raviti maksimaalselt immunosupressiooni katkestamisega, transplantaadi eemaldamisega, sõltumata kasvajakoest, mille päritolu oli, raskusaste või alatüüp. Siiski kasutati adjuvantravi ja individuaalseid ravimeetodeid lähtuti kasvajakoe päritolust, astmest ja alatüübist.4 Näiteks on kahes hiljutises juhtumiaruandes kirjeldatud metastaatilise melanoomi edukat ravineerud-ainult retsipiendid immunosupressiooni lõpetamise, allografti eksplantatsiooni ja üldise metastaatilise melanoomi suhtelise edukuse alusel adjuvant-immuunkontrollravi kaudu.5,6
Kirjandus ainult pankrease siirdamise kohta (PTA) piirdub üksikute juhtumite aruannetega. Perosa jt teatasid 2010. aastal esimesest doonorilt ülekantud pahaloomulisest kasvajast PTA-s. Pahaloomuline kasvaja piirdus kõhunäärmega ja seda raviti edukalt siirdatud pankreatektoomia ja immunosupressiooni lõpetamisega.7 Nagaraju jt teatasid pehmete kudede sarkoomi juhtumist, mis tekkis pankrease allograft, mida ei testitud doonori päritolu suhtes, kuid mida siiski edukalt raviti siiriku pankreatektoomiaga ja immunosupressiooni katkestamisega.

Keskendudes SPK patsientidele, teatasid Roza jt 2001. aastal esimesest doonorilt saadud pahaloomulisest kasvajast siirdatud kõhunäärmes SPK retsipiendil. See patsient suri aga pärast siirdatud pankreatektoomiat, immunosupressiooni katkestamist ja 2 keemiaravi kuuri pahaloomulise kasvaja tõttu.9 2020. aastal kirjutas Meier. jt teatasid laialdaselt metastaatilise BK viirusega seotud neerukartsinoomi edukast ravist SPK-ga patsiendil, kellel oli transplantaadi nefrektoomia ja IL-2 immunoteraapia. Nende puhul põhjustas pankrease äratõukereaktsioon pankrease arteriaalse anastomoosi pseudoaneurüsmi spontaanse rebenemise, mis nõudis erakorralist operatsiooni.10 Meile teadaolevalt puudub muu kirjandus metastaatilise doonorilt põhjustatud pahaloomulise kasvaja eduka ravi kohta SPK retsipientidel.
Meie seeria täiendab seda kirjandust, kirjeldades 3 doonorilt pärineva metastaatilise pahaloomulise kasvajaga SPK patsiendi edukat esialgset ravi. Patsiendil 1 oli doonorilt ülekantud pahaloomuline kasvaja, mis tähendab, et pahaloomuline kasvaja esines doonoril annetamise ajal, samas kui patsientidel 2 ja 3 oli pahaloomuline kasvaja, mis tõenäoliselt pärines doonorkoest aastaid pärast siirdamist. Kuigi nende doonorilt pärinevate pahaloomuliste kasvajate väljakujunemise ajastus oli erinev, suurenes pahaloomuline kasvaja kõigil kolmel juhul retsipiendi immuunsüsteemi järelevalve all, mis oli äratõukereaktsiooni vältimiseks alla surutud. Kõigil kolmel juhul kasutatav ühine strateegia on joonisel 3 kirjeldatud algoritmi aluseks. Strateegiad ja pakutud algoritm põhinevad meie kogemusel ja põhjalikul kirjanduse ülevaatel, mis näitavad, et siirdatud retsipientide metastaatiliste pahaloomuliste kasvajate edukas ravi sõltub varajasest ravist. allografti eemaldamine pärast doonorilt pärineva pahaloomulise kasvaja tuvastamist, mis võimaldab immuunsüsteemi taastamist immunosupressiooni lõpetamise kaudu. Need etapid võimaldavad ka täiendavat ravivõimalust kontrollpunkti inhibiitoriga, mis võib siirdatud organi korral põhjustada tugevat äratõukereaktsiooni. Ülaltoodud juhtudel hõlmasid meetodid doonori ja retsipiendi kasvaja päritolu eristamiseks mikrosatelliitide erinevuste analüüsi, st lühiajalist tandemit. kordused või spetsiifiliste geenimutatsioonide paneeli kontrollimine. Need genoomilised tehnikad esindavad vaid mõnda võimalust suuremas tehnikaarsenalis, mida saab kasutada doonor- ja retsipientkoe eristamiseks. Need lähenemisviisid hõlmavad ka HLA tüpiseerimist või fluorestsentsi in situ hübridisatsiooni kasutamist karüotüpiseerimiseks.{13}} Genoomitehnikate kasutamine võimaldas meil rakendada rakuvaba DNA testimist lisandina, et toetada kasvaja kordumise puudumist juhul 1. Rakk. -Pahaloomuliste kasvajate vaba DNA testimist on kirjeldatud kui potentsiaalselt kasulikku vähi kordumise määramisel. Siiski jääb see arenevaks, eksperimentaalseks diagnostikavahendiks.16
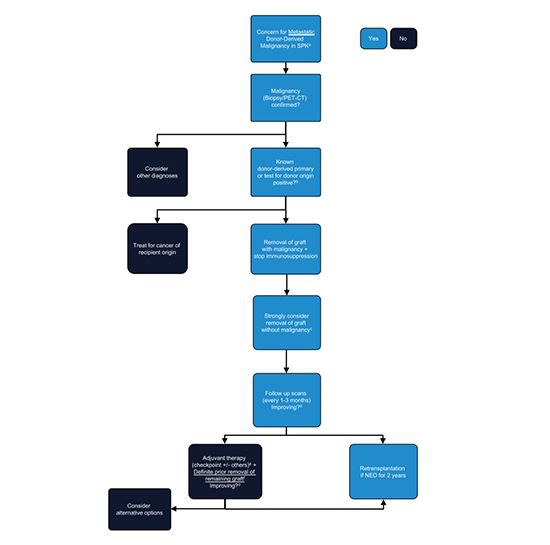

Keskendudes iga juhtumi puhul juhtimisviisile, oli juhtum 1 selgelt kasvaja, mis edastati doonorkõhunäärmega, kuna südame- ja maksaretsipientidel oli sarnase histopatoloogiaga metastaatiline pankrease adenokartsinoom. Erinevalt SPK juhtudest oleks immuunsupressiooni peatamine või transplantaatide eemaldamine südame- ja maksaretsipientide puhul olnud surmav. Selle tulemusena suri südame ja maksa retsipient lõpuks metastaatilise pankrease adenokartsinoomi tõttu. Meie puhul onneerudja pankrease saaks kohe eemaldada tänu dialüüsi ja insuliini võimalustele. Allotransplantaadi pankreatektoomia ja nefrektoomia ajal (6 kuud pärast siirdamist) oli kasvaja metastaseerunud külgnevasse munajuhasse. Kuigi eksplantaadil ei olnud tõendeid kasvaja kohtaneerud, näitas pankreatektoomia ja nefrektoomia ajal tehtud PET-skaneerimine difuusset sõlme neeldumist vasakpoolses supraklavikulaarses, mediastiinumis, mesenteriaalses ja paremas välises niudepiirkonnas. Hoolimata kasvaja lokaalselt agressiivsest olemusest koos lümfovaskulaarse invasiooniga, põhjustas kogu immunosupressiooni peatamine PET-skannimise normaliseerumise 6 kuu jooksul ja metastaatilise haiguse tunnuseid ei esinenud. Sel juhul võimaldas lihtsalt immuunvastuse taastamine doonorilt pärineva kasvaja tagasilükkamist. Raske on kindlaks teha, kui suur osa kasvaja kontrollist on seotud immuunvahendatud tuumori jälgimise taastamisega, peatades immunosupressiooni versus kasvajaga doonori HLA alloimmuunne äratõukereaktsioon. Asjaolu, et alloimmuunvastus andis tõenäoliselt olulise panuse kasvaja kõrvaldamisse, peegeldub anti-HLA antikehade dramaatilisest suurenemisest cPRA-le 100 protsenti. Vaatamata kõrgele paneelireaktiivsetele antikehadele siirdati talle 0-mittevastav neer ligikaudu 2 aastat pärast eksplantaati ja tal läheb jätkuvalt hästi, ilma kasvaja kordumiseta.
Juhtumi 2 pahaloomuline kasvaja tekkis SPK retsipiendi siirdatud kõhunäärmes 10 aastat pärast siirdamist. Kasvaja doonorpäritolu kinnituse järel on nii kõhunäärme kuineerudsiirdati välja ja immunosupressioon peatati. Sarnaselt juhtumiga 1 võimaldas mõlema organi eemaldamine immunosupressiooni täielikku lõpetamist ja põhjustas süsteemse lümfadenopaatia ja hüpermetabolismi lahenemise pankrease siirdamise kohas, mida täheldati järjestikuste PET-skaneeringutega. Otsus eemaldada normaalselt töötavneeru siirdaminehaiguse tunnuste puudumisel oli raske, kuid kuna kasvaja oli doonorilt pärit, tundsime muret varjatud haiguse pärast. Samuti tahtsime olla valmis kasutama kontrollpunkti inhibiitoreid immuunvastuse suurendamiseks, kui immunosupressiooni tühistamine ei olnud kasvajarakkude puhastamiseks piisav. Juhtumil 2, nagu juhtumil 1, seostati immunosupressiooni ärajätmist ka doonori-spetsiifiliste HLA antikehade ja cPRA suurenemisega peaaegu 100 protsenti, mis viitab sellele, et alloimmuunvastus aitas kaasa kasvaja kontrollile. 2 aastat pärast eksplantaate ei ole esinenud tõendeid kordumise kohta ja patsient on aktiivne nii neeru kui ka kõhunäärme siirdamiseks.
Juhtum 3 erineb teistest selle poolest, et doonorilt saadud pahaloomuline kasvaja tekkis mittetoimivas kohasneerudy allograft 13 aastat pärast SPK-d ja pankrease siirdamine toimis normaalselt. Nefrektoomia ajal puudusid metastaatilise haiguse tunnused, mistõttu immuunsupressioon langes, kuid seda ei peatatud, võttes aluseks kõhunäärme suurepärase funktsiooni. Transplantaadi pankreatektoomia oleks võimaldanud immunosupressiooni peatamist ja oleks olnud kooskõlas kirjandusega ühe organi siirdamise kohta, kus transplantaadi eemaldamine ja immunosupressiooni lõpetamine on standardsed lähenemisviisid. SPK patsientide ravi on siiski keerulisem kui nende ravineerudvõi PTA-transplantaadid kui pakkujad peavad kaaluma riske, mis kaasnevad normaalselt toimiva transplantaadi eemaldamisega, mis võib olla kasvajavaba. Seega hõlmas see otsus siirdamismeeskonna riski-kasu hindamist ja vestlust patsiendiga eelistuste üle. Retsipient ei tahtnud lõpuks immuunsupressioonist loobuda ja tundis, et toimivast kõhunäärmest saadav kasu kaalub üles haiguse kordumise riski. Kui ilmnes metastaatiline haigus (kopsuefusioon, maksakahjustused), lõpetati immunosupressioon. Tal oli jätkuvalt normaalne pankrease funktsioon, kuid tal tekkis tugev valu lokaalses kordumise kohas ja ta vajas pahaloomulise efusiooni ärajuhtimiseks rindkere toru. Sel hetkel käivitati kontrollpunkti inhibiitorid, kuid tema nõrga seisundi ja normaalse funktsiooni tõttu (sel ajal) pankrease allografti ei eemaldatud. Kuid mõne nädala jooksul pärast kontrollpunkti inhibiitorite kasutamise alustamist ajendas tema kasvav insuliinivajadus ja tugev valu kõhunäärme allotransplantaadi kohal pankreatektoomia siirdamist. Kontrollpunkti inhibiitorravi tugevus oli märkimisväärne ja esilekutsutud agressiivne tagasilükkamine oli peaaegu kohene. Tagantjärele oleks tulnud pankreatektoomia läbi viia enne kontrollpunkti inhibiitori alustamist, kuna märgatavalt põletikulise ja vaskulaarse allografti eemaldamine oli keeruline. Suurema verekaotuse ja eksplantatsioonijärgse süvaveenide tromboosi tüsistusi oleks võinud vältida. Seetõttu võib kõige ohutum olla pankrease eemaldamine enne, kui massiivse põletikulise reaktsiooni kontrollpunkti inhibiitorid võivad esile kutsuda. Vaatamata kontrollpunkti inhibiitorravi põhjustatud äratõukereaktsiooni negatiivsetele aspektidele seostati agressiivset immuunvastust ka tema metastaatilise haiguse kiire paranemisega. Kolme kuu jooksul pärast immunoteraapia alustamist on kopsu-, maksa- ja lümfikahjustused pildiuuringute põhjal oluliselt paranenud.

Otsustasime patsiendid uuesti aktiveeridaneerudüksi või SPK 1. ja 2. juhtudel pärast 2-aastast vähivaba olemist. Kuigi otsus jätkata siirdamist kõigi potentsiaalsete retsipientide puhul, kellel on anamneesis ravitud vähktõbe, sõltub iga pahaloomulise kasvaja haigusvaba elulemuse hinnangutest, ei ole need andmed siin kirjeldatud stsenaariumide kohta saadaval. Oleme optimistlikud, et doonori HLA immuunmälu suudab säilitada piisava kontrolli algse doonorilt pärineva kasvaja üle, kuid vajalik on range järelkontroll tagamaks, et immunosupressiooni taaskäivitamine ei ole kahjustanud kasvaja immuunvahendatud kontrolli. DSA pidev esinemine viitab jätkuvale kasvajavastasele toimele ja seda saab tulevaste uuringute jaoks jälgida.
Kokkuvõttes peaks metastaatilise doonorist pärineva pahaloomulise kasvaja leidmine pärast SPK-d viivitamatult eemaldama allografti koos primaarse kahjustusega, lõpetama immunosupressiooni ja kaaluma ka teise allografti eemaldamist. Kui immuunsupressiooni peatamisega seotud loomulik immuunseire ei suuda metastaatilist haigust kontrollida, võib kontrollpunkti pärssimine suurendada loomulikku immuunvastust ja edukalt kontrollida agressiivset metastaatilist haigust. See algoritm on võimalik ainultneerudy või SPK retsipientidele, kuna neil patsientidel on pärast allografti eemaldamist alternatiivsed meditsiinilised ravimeetodid, erinevalt südame-, kopsu- või maksaretsipientidest. See strateegia on kooskõlas laiaulatusliku kirjanduse ülevaatega, mis näitab, et metastaatiliste doonoritest pärinevate pahaloomuliste kasvajate edukaks raviks on vaja allografti eemaldamist, immunosupressiooni lõpetamist ja adjuvantravi, mis on tingitud kasvajakoest, mis võib hõlmata aeg-ajalt immunoteraapia kasutamist immuunvastuse suurendamiseks.
TUNNUSTUS
Sisu eest vastutavad ainult autorid ja see ei pruugi esindada riiklike tervishoiuinstituutide ametlikke seisukohti.
Alates 'Metastaatilised doonorilt pärinevad pahaloomulised kasvajad pärast samaaegset kõhunäärme-neeru siirdamist: kolm juhtumiaruannet ja ravistrateegiad
kõrvalDominic Amara, BA,1 et al
---© 2020 Autor(id). Väljaandja Wolters Kluwer Health, Inc. DOI 10.1097/txd.0000000000001090
VIITED
1. Redfield RR, Scalea JR, Odorico JS. Pankrease ja neeru samaaegne siirdamine: praegused suundumused ja tulevikusuunad. Curr Opin organisiirdamine. 2015;20:94–102.
2. Strauss DC, Thomas JM. Doonori melanoomi edasikandumine elundisiirdamise teel. Lancet Oncol. 2010;11:790–796.
3. Xiao D, Craig JC, Chapman JR jt. Doonorivähi ülekanne neerusiirdamisel: süstemaatiline ülevaade. Olen J siirdamine. 2013;13:2645–2652.
4. Eccher A, Girolami I, Motter JD jt. Doonori kaudu leviv vähkneeru siirdaminesaajad: süstemaatiline ülevaade. J Nephrol. 2020.
5. Boyle SM, Ali N, Olszanski AJ jt. Doonorilt saadud metastaatiline melanoom ja kontrollpunkti pärssimine. Transplant Proc. 2017;49:1551–1554.
6. Singh P, Pandey D, Rovin B jt. Edukas ravi ja viieaastane haigusvaba elulemus doonori ülekantud metastaatilise melanoomi puhul ipilimumabraviga. Cureus. 2019;11:e4658.
7. Perosa M, Crescentini F, Antunes I jt. Doonorilt saadud pahaloomuline kasvaja pankrease siirdamisel. Transpl Int. 2010;23:e5–e6.
8. Nagaraju S, Grethlein SJ, Vaishnav S jt. Juhtumi aruanne: primaarne de novo sarkoom siirdatud pankrease allograftis. Transplant Proc. 2017;49:2352–2354.
9. Roza AM, Johnson C, Juckett M jt. Adenokartsinoom, mis tekib siirdatud kõhunäärmes. Siirdamine. 2001;72:1156–1157.
10. Meier RPH, Müller YD, Dietrich PY jt. BK viirusega seotud metastaatilise neerutransplantaadi kartsinoomi immunoloogiline kliirens. Siirdamine. 2020.
11. Schmitt C, Ciré K, Schattenkirchner S jt. Väga tundlik DNA tüpiseerimine siirdamise teel levivate kasvajate tuvastamiseks. Transpl Int. 1998;11:382–386.
12. Robin AJ, Cohen EP, Chongkrairatanakul T jt. Ühe keskuse lähenemisviis neeru neoplaasia doonori ja peremeesorganismi päritolu eristamiseks allografti neerus. Ann Diagn Pathol. 2016;23:32–34.
13. Milton CA, Barbara J, Cooper J jt. Doonorilt pärineva pahaloomulise melanoomi ülekandumine neeru allotransplantaadi retsipiendile. Clini siirdamine. 2006;20:547–550.
14. Palanisamy A, Persad P, Koty PP jt. Doonorilt pärinev müeloidne sarkoom kahesneeru siirdamineretsipiendid ühelt doonorilt. Juhtum Rep Nephrol. 2015;2015:821346.
15. Kim JK, Carmody IC, Cohen AJ jt. Pahaloomulise melanoomi doonori ülekandumine maksatransplantaadi retsipiendile: juhtumiaruanne ja kirjanduse ülevaade. Clini siirdamine. 2009;23:571–574.
16. Corcoran RB, Chabner BA. Rakuvaba DNA analüüsi rakendamine vähiravis. N Engl J Med. 2018;379:1754–1765.
