Kokkupuute bioseire ja silikoosi varajane diagnoosimine: praeguse kirjanduse põhjalik ülevaade
Oct 23, 2023
Abstraktne: Silikoos on spetsiifiline kopsufibroosi vorm, mis on tingitud töökeskkonnas kokkupuutest kristallilise ränidioksiidiga. Tööalane kokkupuude kristallilise ränidioksiidiga suurendab ka kroonilise obstruktiivse kopsuhaiguse (KOK), vähi ja kopsuinfektsioonide, eriti kopsutuberkuloosi riski. Praegu diagnoositakse silikoosi varem kokku puutunud töötajatel tavalise rindkere röntgenuuringuga, kui kahjustused on nähtavad ja pöördumatud. Seetõttu oleks vaja leida spetsiifilised ja mitteinvasiivsed markerid, mis suudaksid tuvastada silikoosi varasemates staadiumides, enne röntgenikiirguse läbipaistmatuse tekkimist. Selles jutustavas ülevaates tutvustame mitmeid diagnostilisi, jälgivaid ja ennustavaid biomarkereid, millel on suur potentsiaal silikoosi ravis, nagu pro- ja põletikuvastased tsütokiinid (TNF (kasvajanekroosifaktor), IL-1 (interleukiin{). {7}}), IL-6, IL-10), CC16 (Clara rakk 16, epiteelirakkude hävimise kaudne marker), KL-6 (Krebs von den Lungen 6, an alveolaarse epiteeli kahjustuse kaudne marker), neopteriin (rakulise immuunsuse näitaja) ja MUC5B geen (Mucin 5B, geeli moodustav mutsiin limas). Uuringud on näidanud, et kõigil eelnimetatud markeritel on suur potentsiaal silikoosi varaseks diagnoosimiseks või progresseerumise hindamiseks ning need kujutavad endast paljulubavaid alternatiive radioloogiale. Leiame, et esitatud biomarkerite täpsuse paremaks hindamiseks on vaja multitsentrilist uuringut, et hinnata neid biomarkereid korrelatsioonis tööajaloo, histopatoloogilise uuringu, kuvamisnähtude ja kopsufunktsiooni testidega suurtes katsealuste rühmades.

cistanche tubulosa - parandab immuunsüsteemi
Märksõnad: silikoos; biomarkerid; varajane diagnoosimine; monitooring; ametiajalugu
1. Sissejuhatus
Silicosis is a collagenous pneumoconiosis caused by long-term exposure to crystalline silica-rich dust. More precisely, silicosis is a type of pulmonary fibrosis caused by inhaled silica particles [1]. For crystalline silica particles to be biologically active, they must be small enough ("respirable") to reach the distal airways and alveoli; [2] therefore, their diameter should be less than 5 µm [3]. In addition, the concentration of crystalline silica in inhaled particles must reach a certain threshold (usually >10%) ja kokkupuuteaeg peab olema vähemalt 5 aastat [1]. Silikoosi areng on krooniline ja progresseeruv protsess; seetõttu, kui see kord esineb, on see pöördumatu. Esinemisriski suurendavad mitmed individuaalsed tunnused ja käitumisviisid, näiteks olemasolevad hingamisteede patoloogiad (kopsutuberkuloos, krooniline riniit, bronhiit jne), geneetilised polümorfismid, alkoholi tarbimine, suitsetamine ja füüsiline aktiivsus [1 ,4].
2. Tööalane kokkupuude
Kristalne ränidioksiid on silikoosi tekkega seotud etioloogiline aine. See on maakoores leiduv mineraal, [5] kus seda esineb kahel erilisel kujul: kristalne (kvarts) ja amorfne (diatom) [1]. Nii kristalsed kui ka amorfsed vormid muutuvad kõrgel temperatuuril (800–1000 ◦C) tridümiidiks, mis omakorda muutub veelgi kõrgemate temperatuuride (1100–1400 ◦C) mõjul kristobaliidiks. . Need kolm vormi (kvarts, tridüümiit, kristobaliit) on peamised silikoosi etioloogilised tekitajad, mille fibrogeenne potentsiaal suureneb nimetatud järjekorras. Rumeenias on kvartsi kokkupuute piirväärtused 1 mg/m3, tridümiidi ja kristobaliidi puhul aga 0,5 mg/m3 [1,2,4]. Riiklik tööohutuse ja töötervishoiu instituut (NIOSH) soovitab mis tahes allomorfse kuju puhul kokkupuute piirnormiks olla alla 0,5 mg/m3 [6]. Riikliku rahvatervise instituudi andmetel vähenes Rumeenias 2019. aastal silikoosi uute juhtude arv märkimisväärselt: 87 juhtu võrreldes 2018. aasta 149-ga ja oli üldises haigestumuse struktuuris teisel kohal. Hiljem, 2021. aastal, täheldati juhtude üldarvu mõningast kasvu: 55 juhtu võrreldes 30-ga 2020. aastal. Aastatel 1998–2021 oli uute ränidioksiidi juhtude keskmine väärtus 294,3 juhtu aastas [7]. Epidemioloogilised uuringud on näidanud, et kristallilise ränidioksiidi kokkupuude on seotud suurenenud suremuse ja haigestumuse määraga [8], mis on tingitud silikoosist, kroonilisest obstruktiivsest kopsuhaigusest (KOK) ja kopsuvähist [9]. Kogu maailmas omistati 2019. aastal silikoosile 655,7 tuhat puude järgi kohandatud eluaastat [10]. 2017. aastal teatati kogu maailmas 23 695 silikoosi juhtumist. Aastatel 1990–2017 teatasid mõned geograafilised piirkonnad silikoosijuhtude arvu vähenemisest (peamiselt Euroopas), kuid teatud piirkondades, nagu Põhja- ja Lõuna-Aafrika, Hiina ja Sahara-taguse Aafrika, teatasid kasvutendentsid [11]. NIOSH määratleb ohustatud ametitena järgmised tegevused: (1) klaasi, keraamika, keraamika, telliste, betooni ja tehiskivide tootmine, (2) abrasiivpritsitööd, (3) valutööd, (4) hüdrauliline purustamine, (5) kiviraiumine ja kivide tööpinnad, (6) kivide puurimine, (7) karjääritööd, (8) tunnelitööd, (9) ehitus, (10) kaevandamine, (11) nafta ja gaasi kaevandamine ning (12) hambaravi [6]. Arvestades ühiskonna arengut ja tehnoloogilisi protsesse, peavad arstid pöörama erilist tähelepanu silikoosi diagnoosimisel nii endistes tööstusharudes varem kokku puutunud isikutel, isegi kui mõned neist on teatud riikides kadunud (nt kaevandused, valukojad) ja äsja paigutatud. esilekerkivad elukutsed (nt liivapritsiga teksapüksid, tehiskivist töölaud) [9,12].

cistanche taime suurendav immuunsüsteem
3. Materjalid ja meetodid
See artikkel on narratiivne ülevaade, mille eesmärk on hinnata ja esitleda mitmeid diagnostilisi, seire- ja ennustavaid biomarkereid, mida kasutatakse patsientidel, kellel on tööalane kokkupuude kristalse ränidioksiidiga. Selle ülevaate jaoks valiti olemasolev kirjandus erinevatest andmebaasidest, nagu Pubmed, Scopus, ScienceDirect ja Google Scholar. Pärast põhjalikku analüüsi, nagu on näidatud joonisel 1 (n=138 274 artiklit), valisime välja 33 tabelis 1 esitatud uuringut, mille eesmärk oli uurida markereid, et hinnata silikoosi varast diagnoosimist ja progresseerumist. Tsütokiinid (TNF- (kasvaja nekroosifaktor), IL-1 (interleukiin-1), IL-10, IL-6), CC16 (Clara rakk 16), KL -6 (Krebs von den Lungen 6), MUC5B (Mucin 5B) geen ja neopteriin valiti edasiseks otsinguks huvipunktideks. Kasutasime ülalnimetatud markerite nimetusi, millele järgnesid terminid "silikoos", "põletik", "põletikuvastane", "immuunsüsteemi düsregulatsioon", "füsiopatoloogia", "evolutsioon", "varajane diagnoos", "geneetilised polümorfismid" ja "ravi" erinevates permutatsioonides. Iga üksuse puhul oleme teinud kokkuvõtte bioloogilistest mehhanismidest, kasutades ülalkirjeldatud otsingumootoreid ja riiklikku kirjandust. Seejärel tutvustasime valikut kliinilistest ja eksperimentaalsetest uuringutest, milles hinnati mitmeid biomarkereid nende potentsiaalse väärtuse osas silikoosi varajases diagnoosimises ja arengus. Me ei piiranud ajavahemikku, kuigi eelistati värskemaid uuringuid.
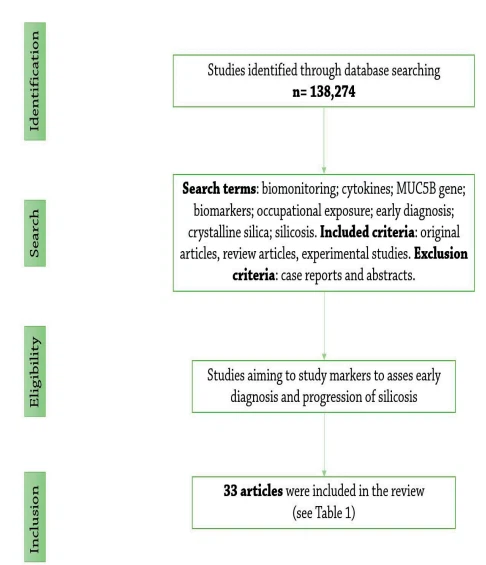
Joonis 1. Kirjanduse otsingu vooskeem. Kirjanduse otsingu vooskeem.
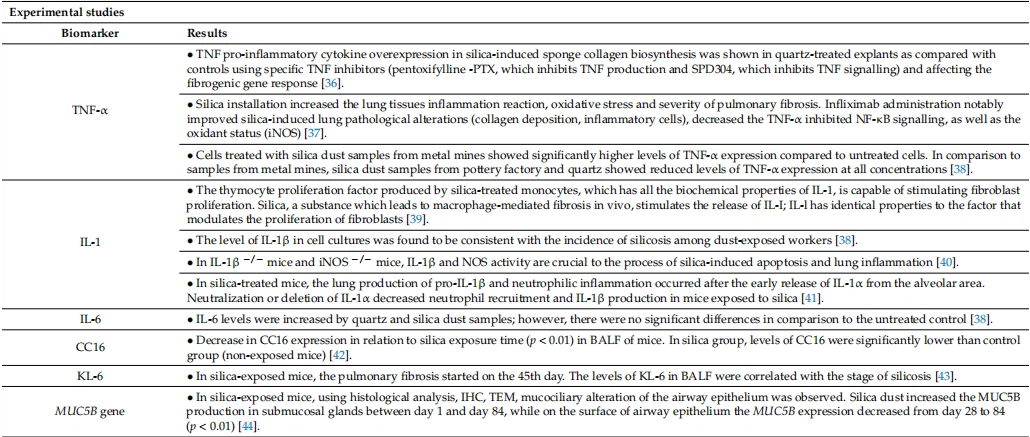
Tabel 1. Jutustavasse ülevaatesse kaasatud 33 artikli ekstraheerimise tabel (TNF – kasvaja nekroosifaktor, OR – tõenäosussuhe, CI – usaldusvahemik, IL – interleukiin, CC16 – Clara rakk 16, BALF – bronhoalveolaarne loputusvedelik, FEV1 — sunnitud väljahingamise maht 1 sekundiga, VC — elutähtsus, ELISA — ensüümseotud immunosorbentanalüüs, KL-6 — Krebs von den Lungen 6, SP-D — seerumi surfaktant valk D, MMP — maatriksi metalloproteinaas, MUC5B — mutsiin 5B, CWP – kivisöetöötajate pneumokonioos, NF-κB – tuumafaktor kappa B, iNOS – indutseeritav lämmastikoksiidi süntaas, IHC – immunohistokeemia, TEM – ülekandeelektronmikroskoopia).

Tabel 1. Jätk.

Tabel 1. Jätk.
4. Mõju tervisele
Silikoos on kõige levinum pneumokonioos ja see liigitatakse radioloogiliste leidude põhjal kahte kategooriasse: lihtne (<10 mm diameter opacities) and complicated (>10 mm läbimõõduga läbipaistmatus). Silikoosi patogenees põhineb kolmel teoorial: makrofaagide hävitamine, fibroosini viiv põletik ja immunoloogilised mehhanismid [4].
Makrofaagide hävitamine loob aluse põletiku, fibroosi ja immunoloogiliste protsesside tekkeks. Kristallilised ränidioksiidi osakesed fagotsüteeritakse makrofaagide poolt, mis viib sündmuste jadani, mis toimuvad kronoloogilises järjestuses järgmiselt: (1) fagosoomi seina purunemine lüsosoomide toimel, (2) sisu vabanemine makrofaagide tsütoplasmasse, (3) ) makrofaagi lagunemine, (4) osakeste ja ensüümide vabanemine rakuvälisesse vedelikku, (5) protsessi taasalustamine. Pärast sissehingatava suurusega ränidioksiidi aktiveerimist käivitavad makrofaagid põletikulise protsessi, kollageeni hüpersünteesi ja immunoloogilised protsessid (joonis 2) [1,4].
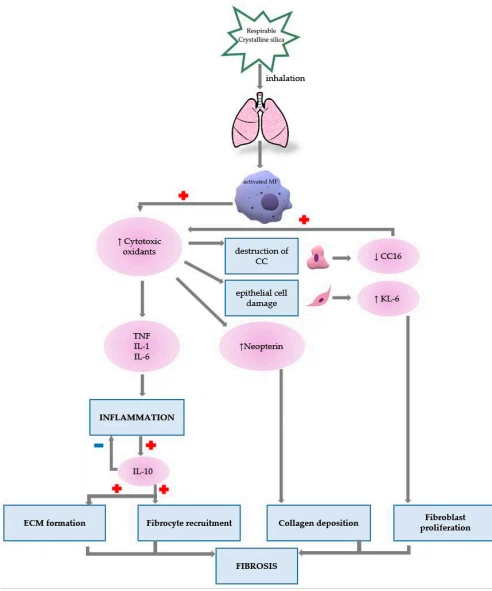
Joonis 2. Esitatud biomarkerite roll silikoosi patogeneesis
Arvestades, et haiguse histopatoloogilisel algusel puuduvad radioloogilised tunnused (histopatoloogilise alguse ja radioloogiliselt nähtavate kahjustuste vahel on viivitus) [1,3], on välja pakutud potentsiaalseid varajaseks diagnoosimiseks kasulikke biomarkereid. Oleme kokku võtnud kõige olulisemad eelnimetatud biomarkerid, nagu on seni erikirjanduses esile tõstetud.

cistanche tubulosa - parandab immuunsüsteemi
Cistanche Enhance Immunity toodete vaatamiseks klõpsake siin
【Küsi lisa】 E-post:cindy.xue@wecistanche.com / Whats App: 0086 18599088692 / Wechat: 18599088692
5. Biomarkerid
5.1. TNF
Alveolaarsed makrofaagid, esimene kaitseliin võõrainete vastu, neelavad sisse sissehingatud ränidioksiidi, põhjustades rakusurma ja ekstratsellulaarse ränidioksiidi vabanemise. Seejärel hõivavad ränidioksiidi teised makrofaagid, mis viib korduva tsüklini, mis säilitab põletikulise protsessi. Makrofaagid vabastavad mitmeid vahendajaid, nagu tsütotoksilised oksüdeerijad, arahhidoonhappe metaboliidid ja põletikulised tsütokiinid, sealhulgas TNF- ja IL-1. Need vahendajad käivitavad põletikuliste rakkude sissevoolu ja indutseerivad nende infiltratsiooni alveoolide seina, vabastades proteolüütilisi ensüüme ja toksilisi hapniku derivaate, mis põhjustab rakukahjustusi ja rakuvälise maatriksi hävimist [45]. TNF on glükoproteiin, mida toodavad peamiselt aktiveeritud makrofaagid, aga ka teised rakud: nuumrakud, lümfotsüüdid, fibroblastid, granulotsüüdid ja NK (looduslikud tapjarakud) [46]. TNF-i toimete hulka kuuluvad neutrofiilide, makrofaagide, B- ja T-lümfotsüütide aktiveerimine ning immunoglobuliinide sünteesi stimuleerimine. Samuti kutsub see esile kasvajarakkude surma nekroosi või apoptoosi tõttu ja stimuleerib teiste tsütokiinide sünteesi: IL-1, IL-6 ja IFN (interferoon). TNF-stimuleerib rakuvälise maatriksi sünteesi ja ladestumist ning kollageeni sünteesi, soodustades seega fibroosi teket [13]. Seetõttu on TNF-l oluline roll põletikulise protsessi säilitamisel, aktiveerides makrofaage, stimuleerides põletikuliste valkude (tsütokiinide) tootmist ja stimuleerides T-lümfotsüüte [4]. TNF-il on silikoosis mitu olulist rolli, sealhulgas põletikuliste rakkude sissevoolu vallandamine ja teiste tsütokiinide vabanemine [13]. Uuringud näitasid, et TNF-i tase on kõrgenenud enne silikoosiga seotud kliiniliste nähtude ilmnemist, mistõttu on TNF-i väärtus varajase diagnoosimise jaoks väärtuslik [14,47]. Andmed ühest uuringust, mis hõlmas 30 kontrollrühma (terved isikud), 28 ränidioksiidiga kokkupuutunud isikut (ilma kliiniliste haigusteta) ja 30 ränidioksiidiga isikut, näitasid, et TNF-i plasmatase oli kokkupuutel töötajatel kõrgem. (p < 0,05) ja oluliselt kõrgem silikoosipatsientidel kui tervete isikute rühmas (p < 0,01), mis tõestab, et TNF- on silikoosi patogeneesis kaasaaitaja [13]. Tõendid TNF-i puudulikkusega hiirtelt, kes on resistentsed ränidioksiidi põhjustatud fibroosi tekkele, toetavad ideed, et TNF-il on oluline roll kopsufibroosi tekkes [16]. On näidatud, et IL-1 ja TNF-i lokaalne vabanemine monotsüütide ja makrofaagide kultuurides inimestel on kooskõlas haiguse patogeneesiga [39]. Kasutades spetsiifilisi TNF-i inhibiitoreid, mis muudavad NF-kollageeni (mittefibrillaarne), F-kollageeni (fibrillaarne) ja P4H (prolüül4-hüdroksülaasi) geeni vastust (fibrogeense geeni ekspressioonitasemed), näidati, et kvarts- töödeldud eksplantaadikultuurides esines võrreldes kontrollidega TNF-i ja ränidioksiidiga indutseeritud käsna kollageeni tootmist üleekspressioon [36]. Anti-TNF võib vähendada ränidioksiidist põhjustatud kopsupõletikku, vähendades NF-κB (tuumafaktor kappa B), signaaliülekannet, oksüdatiivset stressi ja TNF-i, mis viitab sellele, et anti-TNF-i võib kasutada ränidioksiidist põhjustatud kopsukahjustuse raviks [37]. Varasemad uuringud asetavad TNF-i promootori polümorfismid põletikulistesse ja nakkusohtlikesse seisunditesse [4]. Praegu ei ole dokumenteeritud seost TNF polümorfismiga seotud vastuvõtlikkuse vahel infektsioonidele ja silikoosile [23, 48], kuid jääb lahtiseks, kas otsene seos on võimalik, arvestades silikoosiga patsientide vastuvõtlikkust kopsutuberkuloosile [4]. Metaanalüüs näitab, et TNF -308 (11 uuringut) ja -238 (8 uuringut) polümorfismid on seotud vastuvõtlikkusega silikoosile [17]. Meie leiud näitavad, et ka teised TNF-i polümorfismid on seotud silikoosiga. Corbett et al. tuvastas tugeva seose TNF-polümorfismide -238 ja -376 ning raske silikoosi vahel [18]. Tsemenditehases töötavate isikutega läbi viidud uuring näitas, et isikud, kellel oli TNF -308 geeni lookuste geneetiline varieeruvus, olid vastuvõtlikumad silikoosi tekkele. Neid leide kinnitas TNF -308 geenivariatsiooni subjektide poolt toodetud suurem kogus TNF-i (p=0,004) [19]. Üldiselt näitasid uuringud, et ränidioksiidiga kokkupuutunud töötajate suurenenud TNF-i tase ilma haiguse kliiniliste tunnusteta võib olla potentsiaalne biomarker varajase silikoosi diagnoosimisel. Nende tulemuste tõlgendamisel on veel kaks küsimust, mis vajavad täiendavat hindamist. Esiteks tuleks TNF-i polümorfismide genotüpiseerimist arvesse võtta kõigis uuringutes, mis viitavad TNF-ile kui silikoosi biomarkerile, kuna näidati, et TNF määrab vastuvõtlikkuse silikoosile ja keerulise vormi (progresseeruv massiivne fibroos) tekkele. Teiseks tuleks kasutada TNF/TNF-i ajakohastatud klassifikatsiooni. Algselt omistati TNF kahele molekulile, TNF-le, monotsüütidest pärinevale tuumori nekroosifaktorile ja TNF---le, lümfotsüütidest pärinevale kasvaja nekroosifaktorile [46]. Seejärel, seitsmendal rahvusvahelisel TNF-i kongressil (17.–21. mai 1998; Hyannis, Massachusetts), muudeti nimi "TNF-" nimeks "lümfotoksiin-". Samal ajal muutus "TNF-" tarbetuks terminiks, millel on sama tähendus kui algsel terminil "TNF", mis taastati ametliku tsütokiini nimetusena [49]. Kuigi see nimetati ümber rohkem kui 20 aastat tagasi, kasutatakse TNF-i jätkuvalt paljudes praegustes teadusuuringutes kui TNF-i, mis põhjustab teatud arusaamatust selle kohta, millistele molekulidele autorid viitavad. Ühes eksperimentaalses uuringus näitas anti-TNF-ravi paljulubavat potentsiaali ränidioksiidiga seotud põletiku vähendamisel. Siiski puuduvad kliinilised uuringud ja praegu ei saa me teha järeldusi silikoosi efektiivsuse kohta.
5.2. IL-1
Sissehingatava suurusega kristalse ränidioksiidi poolt aktiveeritud makrofaagid toodavad vahendajaid ja käivitavad põletikulise protsessi. IL-1 avaldab sünergistlikku toimet teiste põletikueelsete tsütokiinidega, nagu TNF- ja IL-6. Aktiveeritud makrofaagide poolt sekreteeritud tsütokiinid (IL-1, IL-6, IL-12, IL-18) tõmbavad omakorda ligi ja aktiveerivad T-lümfotsüüte, mis viib B-lümfotsüütide stimuleerimiseni viimane (IL-11 ja IL{{10}} kaudu) ja immunoloogilise vastuse algatamine. Ränidioksiidi osakeste püsimine kopsukoes kutsub esile kõigi nende rakkude kroonilise aktivatsiooni, tagades jätkuva põletikulise protsessi [4]. Loomkatsed ja kliinilised uuringud näitavad, et TNF- ja IL-1 on olulised fibrootiliste vahendajate reguleerimisel silikoosi korral. Indiviididevahelised erinevused IL-1 ja TNF-i tootmises toetavad ideed, et silikoos ja progresseerumine selle keeruliseks vormiks on seotud peremeesorganismi geneetilise eelsoodumusega neid valke toota, kuna põletikuliste haiguste puhul leiti, et mõned alleelsed variandid olla üleekspresseeritud. Näiteks IL-1 geeni polümorfismil (IL-1RA +2018) on sõltumatud ja korrelatsioonis toimed silikoosi tundlikkuse ja raskusastmega kokkupuutunud isikutel, seega ei sõltu silikoosi esinemine ainult kokkupuute intensiivsust, kestust ja aega, aga ka tsütokiini polümorfismi [24,39]. Need tulemused on kooskõlas Yucesoy B jt järeldustega, kus IL-1RA +2018 suurenes märkimisväärselt mõõduka ja raske silikoosiga patsientidel, mis viitab sellele, et see variant mõjutab peamiselt vastuvõtlikkust haigustele [39] . Türgi keraamikatehases kristallilise ränidioksiidiga kokkupuutunud 99 isikust koosneva rühmaga läbiviidud uuring näitas 81-st isikust koosneva kontrollrühmaga võrreldes oluliselt suurenenud uuritud interleukiinide taset seerumis, sealhulgas IL-1. Lisaks olid vanematel isikutel seerumi IL-1 väärtused kõrgemad kui noorematel uuritavatel [20]. Uuringud, milles hinnati seost vere IL-1 taseme ja kristallilise ränidioksiidiga kokkupuute vahel, näitasid olulist korrelatsiooni läbipaistmatuse rohkuse vahel ränidioksiidi rühmas võrreldes tervete isikutega (p < 0,05) [21,38]. Kuigi IL-1 ja IL-1 homoloogia on 27%, [50] seonduvad nad sama retseptoriga, IL-1R1 (IL-1 tüüpi 1 retseptor), ja kutsuvad esile samu bioloogilisi funktsioone [50,51]. Seega on silikoosi korral IL-1 seotud kollageeni ladestumisega ja PDGF (trombotsüütidest pärineva kasvufaktori) aktiivsuse moduleerimisega [40]. Lisaks näitas näriliste kopsukoest võetud rakukultuuridega läbiviidud uuring, et pärast kokkupuudet kristallilise ränidioksiidiga vabanevad alveolaarsed makrofaagid kiiresti IL-1, stimuleerides IL-1 tootmist, soodustades seega kopsupõletikku. [41]. Lisaks TNF-ile näitasid tulemused, et IL-1 polümorfismide genotüpiseerimine, eriti IL-1RA +2018, võib olla seotud silikoosi tundlikkuse ja raskusastmega. Korrelatsioonist IL-1 taseme ja ränidioksiidiga patsientide radioloogilise läbipaistmatuse tiheduse vahel teatati ainult ühes uuringus ja see tuleb kinnitada teistes kohortides. Seetõttu on vaja täiendavaid uuringuid suuremate katsealuste rühmadega, et lõpuks rakendada IL-1 haiguse jälgimisel ja IL-1 kokku puutunud isikute sõeluuringuprotokollis ning määrata konkreetne IL-1 silikoosi tekkega seotud polümorfismid.

cistanche tubulosa - parandab immuunsüsteemi
5.3. IL-10
Põletikuvastased tsütokiinid on immunoregulatoorsete molekulide rühm, mis reguleerib põletikueelset tsütokiini vastust. Immuunvastuse kontrollimiseks toimivad tsütokiinid koos teatud spetsiifiliste tsütokiini inhibiitorite ja lahustuvate tsütokiini retseptoritega. Üks tähtsamaid põletikuvastaseid tsütokiine on IL-10. IL-10 on erinevate immuunrakkude diferentseerumise ja proliferatsiooni oluline kontroller ning põletikureaktsioonide aeglustav ja isegi mahasurumine [52]. Silikoosi korral on IL-10 kõrgenenud, kuid sellel on kahekordne toime: ühelt poolt piirab IL-10 põletikulise vastuse amplituudi, pärssides IL-1, IL{{9 tootmist. }} ja TNF- monotsüütides ja makrofaagides [53]. Teisest küljest aitab IL-10 fibrootilist protsessi esile kutsudes kaasa pneumokonioosi kahjustuste laienemisele. Kurniawidjaja LM lähtus hüpoteesist, et põletikuline protsess stimuleerib IL-10 tootmist, millel on põletikuvastane roll. Hinnati TNF-i ja IL{16}} suhet ja tulemused näitasid, et suhe, mis on väiksem kui 1, avaldas silikoosi tekkele kaitsvat toimet. Kõige tõenäolisem seletus oli, et IL-10 põletikuvastane toime kaalub üles TNF- põletikuvastase toime. Kui TNF- /IL-10 suhe on üleühtne, ei suuda IL-10 pärssida TNF- põletikueelset toimet, mis viitab sellele, et silikoosi riskifaktor tuleks tuletada sellest suhtest, mitte aga mitte. sõltumatutest TNF- ja IL väärtustest-10. Oluline erinevus TNF-/IL-10 suhte väärtuste vahel ei sõltunud TNF-i geneetilisest variatsioonist [49].
5.4. IL-6
IL{{0}} on multifunktsionaalne tsütokiin ja mängib olulist rolli põletikes ja immuunsuses. Kopsuhaiguste korral leitakse kõrgenenud IL-6 tase bronhoalveolaarses loputusvedelikus, kopsukoes ja veres. IL-6 hõlbustab kopsude infiltratsiooni põletikuliste rakkudega, indutseerides põletikulistel rakkudel adhesioonimolekulide ekspressiooni, ja mängib rolli fibroosi reguleerimises, moduleerides Th2 tsütokiinide ekspressiooni [54]. IL-6 kontrollib IL-1 ja TNF-i tootmist ning on tuntud kui akuutse faasi vastuse esmane vahendaja ning sellel on ka põletikuvastane toime. TGF- (transformeeriv kasvufaktor-) juuresolekul inhibeerib IL-6 regulatoorsete T-rakkude arengut ja soodustab Th17 diferentseerumist, mis toodab IL-17 [16]. Braz NFT et al. ja Blanco-Pérez JJ et al. uuris erinevaid tsütokiine; Mõlema uuringu üks peamisi leide oli see, et silikoosiga patsientidel ja kristalse ränidioksiidiga kokkupuutunud patsientidel leiti kõrgem IL-6 sisaldus seerumis kui tervetel inimestel, kes ei olnud kokku puutunud [15,16]. Hiljutises kliinilises uuringus jagati silikoosiga patsientide rühm kahte kategooriasse, et hinnata silikoosi võimalikku ravi (atsetüültsüsteiin + tetrandriin) ja selle mõju seerumi IL-6 ja TNF-tasemetele. Tetrandriini koos N-atsetüültsüsteiiniga kasutati rutiinselt vaatlusrühma patsientide raviks, samas kui kontrollrühm sai standardset sümptomaatilist ravi. Enne ravi ei täheldatud kahe rühma IL-6 ja TNF- (p > 0,05) veres märgatavat erinevust. Pärast ravi langes eelnimetatud tsütokiinide tase mõlemas rühmas, kuid vaatlusrühmas oli vähenemine tunduvalt väiksem (p < 0,05). Tetrandriin koos atsetüültsüsteiiniga võivad koos hästi kaasa aidata, et tugevdada silikoosi kliinilist terapeutilist toimet ja vähendada põletiku raskust. Kliinilist terapeutilist toimet hinnati FVC (forsseeritud eluvõime), FEV1 (sunnitud väljahingamise maht 1 sekundi jooksul) ja RR (hingamissagedus) määramisega. FVC, FEV1 ja RR näitasid pärast ravi paranemist, kuid rindkere röntgeni või kompuutertomograafiaga korrelatsiooni ei leitud. Nende tulemuste põhjal jõudsid autorid järeldusele, et perifeerse vere IL-6 ja TNF-i tasemed on silikoosi ravis olulised ning nende tuvastamine võib järelkontrollina vähendada röntgenikiirte arvu [22]. Koos TNF- ja IL-1-ga on IL-6-d pikka aega peetud lipopolüsahhariidi poolt toodetud põletikueelseks tsütokiiniks. IL-6 kasutatakse sageli süsteemse põletikueelse tsütokiini aktiivsuse märgina. IL-6-l on põletikuvastased ja põletikuvastased omadused, nagu ka paljudel teistel tsütokiinidel, kusjuures IL-6 indutseerib tugevalt ägeda faasi valguvastust. IL-6 vähendab põletikuvastaste tsütokiinide (nt IL-10 ja TGF-) tootmist ning vähendab põletikueelsete tsütokiinide sekretsiooni. Lisaks IL-1Ra (IL-1 retseptori antagonisti) tootmise ja lahustuva TNF-i retseptori vabanemise suurendamisele suurendab IL-6 glükokortikoidide sünteesi. IL-6 takistab ka põletikueelsete tsütokiinide, nagu GM-CSF (granulotsüütide-makrofaagide kolooniaid stimuleeriv faktor), IFN- ja MIP-2 (makrofaagide põletikuline valk-2) sünteesi. [55]. IL-6 näitas paljulubavaid tulemusi silikoosi diagnoosimisel, sealhulgas selle algstaadiumis, kui hägusus ei ole radioloogiliselt nähtav. Siiski on IL-6 tsütokiin, mida sekreteeritakse vastusena paljudele teistele põletikulistele reaktsioonidele (infektsioonid, kokkupuude teiste osakestega jne) ja need asjaolud tuleb selle biomarkeri olulisuse individuaalsel hinnangul välistada. Juba diagnoositud silikoosiga patsientidel võib IL-6 dünaamika vähendada rindkere röntgenülesvõtete arvu ja seda saaks kasutada haiguse ravi jälgimisel.
5.5. CC16
Clara raku valk (CC16) on Clara rakkude poolt sekreteeritud valk, mille nimi tuleneb selle molekulmassist 16 kD. Seda leidub peamiselt distaalsetes hingamisteedes, täpsemalt terminaalsetes bronhioolides [25,42,56]. Sellel valgul on põletikuvastane, antioksüdant, antifibrootiline ja immunosupressiivne roll [25,57]. Hingamisteede põletik võib põhjustada Clara rakkude arvu vähenemist ja vähenemise määr võib kajastada epiteelirakkude kahjustusi aja jooksul [58]. Mitmed uuringud on isegi näidanud, et CC16 on kopsuepiteeli hävimise perifeerne biomarker [25–28]. Clara rakkude kahjustuse erinevad tasemed võivad põhjustada funktsiooni, eriti nende põletikuvastase võime vähenemist. Võimalik põhjus võib olla ränidioksiidi tolmu võime põhjustada kopsude põletikulisi kahjustusi; kuna see põletik suureneb järk-järgult pikaajalise kokkupuute korral, põhjustab see rakukahjustuse kaudu Clara rakkude sekretsiooni vähenemist. Sellele hävitamisele aitavad kaasa ka aktiveeritud fagotsüütide ja vabade radikaalide poolt vabanevad toksiinid [26]. Üks uuring näitas CC16 taseme langust BALF-is (bronhoalveolaarne loputusvedelik) silikoosirühmas, kus esines väike hägusus (<10 mm) compared to the control group [3,26]. Moreover, the authors reported lower CC16 levels in patients with simple silicosis compared to the group with complicated silicosis (progressive massive fibrosis) (p < 0.05) [3,26]. This result was attributed by the authors to a possible self-repair process of epithelial cells [26] but, to the best of our knowledge, without experimental evidence, such as a lung biopsy, to support the assumption. Another study comparing three groups (silicosis, exposed, and control group) showed that the serum levels of CC16 were lower in the silicosis group, followed by the exposed group, and the highest levels were in the control group (p < 0.001) [25]. A 2020 study suggests that a CC16 serum value below 7.0 ng/mL in workers with an occupational history of crystalline silica exposure could represent a potential marker for the detection of silicosis in the early stage [27]. Sarkar K et al. investigated the CC16 in the serum of 117 silicosis subjects and 32 nonexposed individuals. The results of the study showed an inversely proportional relationship between the degree of lung damage on chest X-rays and CC16 serum values. The study also suggests that a cut-off value of 9 ng/mL can be correlated with early silicosis [28]. Although the cut-off values of the two studies differ, it is a promising start in recruiting peripheral biomarkers for the diagnosis of early-stage silicosis. Considering the limitations discussed, more studies are needed to accurately determine the cut-off value of CC16, preferably on larger groups of subjects with different radiological stages. A study conducted on 106 subjects (68 silica-exposed and 38 healthy individuals) measured serum CC16 levels by two methods: ELISA (enzyme-linked immunosorbent assay), the standard reference method, and semi-quantitative lateral flow assay (immunochromatography). By ELISA, all subjects radiologically confirmed with silicosis had CC16 levels below 9 ng/mL, while healthy subjects showed CC16 > 9 ng/mL. In the semi-quantitative lateral flow assay, CC16 values were represented by ranges (<6 ng/mL, 6.1–9 ng/mL, >9 ng/mL) ja selle meetodi tulemused näitasid ELISA tulemustega võrreldes 100% tundlikkust ja 95% spetsiifilisust [29]. Need leiud pakuvad uut lähenemisviisi CC16 tuvastamisele, mis on palju taskukohasem ja reprodutseeritavam meetod, mida saab hõlpsasti rakendada sõelumismeetodina kõigi ränidioksiidiga seotud tööalaste kokkupuute korral, isegi vähem arenenud geograafilistes piirkondades. Kõik leiud näitasid, et seerumi ja BALF CC16 tasemed ränidioksiidiga patsientidel olid oluliselt madalamad kui mitte-eksponeeritud rühmades. Lisaks teatati, et seerumi CC16 tasemed langesid vastavalt silikoosi staadiumile ja korreleerusid FEV1 / VC suhtega. CC16 tuvastamist poolkvantitatiivse külgvoolu testiga tuleks rakendada suuremate katsealuste rühmade puhul, et paremini hinnata tundlikkust ja spetsiifilisust ELISA-ga võrreldes ränidioksiidiga kokku puutunud isikutel.
5.6. KL-6
KL-6, tuntud ka kui MUC-1 (Mucin 1), on suure molekulmassiga mutsiinilaadne glükoproteiin, mis ekspresseerub 2. tüüpi pneumotsüütidel (enamasti tsütoplasmas ja membraanis). [59,60], Clara rakud ja bronhiaalnäärmed [61]. Tänapäeval on teada, et KL-6 suurenenud sisaldus seerumis peegeldab aktiivset alveolaarse epiteeli kahjustust [62]. KL-6 võib soodustada fibroblastide migratsiooni ja proliferatsiooni ning pärssida programmeeritud rakusurma (apoptoosi). Seega võib KL-6 põhjustada kopsufibroosi [63]. KL-6, mis vabaneb 2. tüüpi pneumotsüütide proliferatsioonist kopsufibroosi korral, mis on seotud tööalase kokkupuutega tolmu või kiududega (pneumokonioosidena), põhjustab KL-6 kontsentratsiooni suurenemist seerumis. Seega võib see stimuleerida fibrootilisi protsesse interstitsiaalse kopsuhaigusega patsientidel ja suurendada KL-6-vastaste antikehade ravi vajaduse [64]. Uuring hiirtega näitas, et pärast 45-päevast kristallilise ränidioksiidiga kokkupuudet muutus kopsufibroos märgatavaks ja KL-6 tase seerumis oli positiivses korrelatsioonis fibrootiliste kahjustuste raskusastmega [43]. Inimeste kohta käivad andmed näitasid, et seerumi KL-6 kontsentratsioon on pneumokonioosi korral kõrgem kui tervetel kontrollrühmadel või kokkupuutega isikutel [30]. Seega on konkreetselt ränidioksiidile viitavaid tulemusi napilt. KL-6 on potentsiaalne biomarker kutsetegevusest põhjustatud fibroosi ja üldiselt kopsufibroosi jaoks. Silikoosi diagnoosimise roll pole veel määratletud.
5.7. MUC5B geen
MUC5B geen kodeerib MUC5B valku, mis on peamine geeli moodustav mutsiin inimestel ja hiirtel. Seega aitab MUC5B kaasa kopsude, sülje ja emakakaela lima määrimisele ja viskoelastsusele [65]. Uuringud näitasid, et MUC5B üleekspressioon distaalsetes hingamisteedes häirib tõhusa mukotsiliaarse transpordi toetamiseks vajalikku tasakaalu, mõjutades seeläbi lima funktsiooni. MUC5B mõju kopsufibroosi arengule pakub välja kaks hüpoteesi. Esiteks võib kokkupuude sissehingatava tolmu ja mikroosakestega ning seejärel nende kopsudes kinnipidamine põhjustada mukotsiliaarse düsfunktsiooni. Teiseks võib säilinud ainete põhjustatud põletik kujutada endast fibrootiliste mikrokahjustuste kaudu kollageeni ladestumise algust. Teine teooria MUC5B üleekspressiooniga seotud kopsufibroosi esinemise kohta toetab kopsude kliirensi vähenemist ja lima viskoossuse suurenemist [66]. Hiirtega läbiviidud uuring näitas, et ränidioksiidi osakesed võivad põhjustada mitte ainult MUC5B ekspressiooni muutusi, vaid ka ripsmete talitlushäireid ja liigset lima sekretsiooni. Vaja on rohkem uuringuid, et paremini mõista, kas need leiud on otseselt seotud silikoosiga, ja need peaksid sisaldama ka andmeid MUC5B polümorfismide ja nende mõju kohta ränidioksiidiga seotud fibroosi tundlikkusele [44]. Hiina populatsiooniga läbi viidud uuring näitab, et MUC5B rs2672794 geeni polümorfism on otseses seoses söekaevurite pneumokonioosiga, seega võib MUC5B rs2672794 CC genotüüp suurendada pneumokonioosi tekke riski [31]. Kuna MUC5B on geen, mida on selle rolli osas põhjalikult uuritudkopsufibroosi korral tuleks tulevastes uuringutes kaaluda geeniekspressiooni muutmist inimestel ränidioksiidiga kokkupuute tõttu.
5.8. Neopteriin
Neopteriin, pteridiinide klassi kuuluv pürasinopürimidiini molekul, lahustub plasmas või seerumis ning on rakulise immuunsuse oluline ja varajane näitaja. IFN-i poolt stimuleeritud dendriitrakud, makrofaagid ja monotsüüdid toodavad neopteriini. Neopteriin on kasulik prognostiline biomarker immunoloogilise stimulatsiooni, püsiva infektsiooni, rakuvahendatud immuunsuse ja oksüdatiivse stressi jaoks [67]. IFN-i indutseeritud neopteriini sekretsioon on seotud tsütotoksiliste oksüdeerijate tootmisega, muutes neopteriini kandidaadiks oksüdatiivse stressi, mitte ainult rakulise immuunsuse jälgimiseks [32]. Seerumi neopteriini taset võiks kasutada ränidioksiidiga kokkupuutest tingitud mõju ja muude kutsehäirete indikaatorina. Kõrgenenud neopteriini tase silikoosihaigete seerumis suurendab võimalust, et see mõjutab rakulist immuunsust ja makrofaagide pidevat aktivatsiooni haiguse patogeneesis [34]. Neopteriini võib pidada potentsiaalseks biomarkeriks kristallilise ränidioksiidi kõige varasemate tervisemõjude tuvastamiseks [32]. Siiski on kliinilises praktikas rakendamiseks vaja täiendavaid uuringuid, et uurida lisaks neopteriinile ka oksüdatiivse stressi parameetreid [32]. Kristallilise ränidioksiidiga kokkupuutuvate töötajatega läbiviidud uuringus leiti oluliselt kõrgemaid tasemeid kokkupuutel isikutel võrreldes tervete inimestega (p < 0,05). Tulemused näitasid ka, et eksponeeritud isikute suurenenud neopteriini väärtusi mõjutab peamiselt kristalse ränidioksiidi sisaldus sissehingatavas fraktsioonis ja neid ei mõjuta individuaalsed omadused ega kokkupuuteaeg [35]. Sellegipoolest algab uuringu analüüs meetodi mittetäielikust kirjeldusest, võtmata arvesse katsealuste keskmist kokkupuudet kristalse ränidioksiidiga. Uuring annab piiratud teavet kokkupuute, eriti pikaajalise kokkupuute kohta. Andmed põhinevad ainult teatud ajahetkel mõõdetud sissehingatavale fraktsioonile, kuigi katsealuste kokkupuude oli mõnel juhul üle 20 aasta. Teises uuringus leiti olulisi statistilisi erinevusi seerumi ja uriini neopteriini tasemetes eksponeeritud isikute ja tervete isikute vahel. Ränidioksiidiga kokkupuutunud töötajatel on neopteriini tase uriinis ja seerumis märgatavalt tõusnud. Neopteriini taseme tõus veres, uriinis ja muudes kehavedelikes võib näidata rakulise immuunsüsteemi aktivatsiooni taset ja hinnata oksüdatiivse stressi suurust [33]. Üldised uuringud näitasid, et neopteriinil on suur potentsiaal silikoosi varajase avastamise biomarkerina, kuid parema täpsuse huvides tuleks mõõta ka oksüdatiivse stressi parameetreid.

cistanche tubulosa - parandab immuunsüsteemi
6. Järeldused
Silikoos on endiselt üks peamisi tööstustervise probleeme kogu maailmas. Arvestades praegust olukorda, kus silikoosi diagnoos pannakse paika ainult hiliste ja pöördumatute radioloogiliste muutuste põhjal, muutub ränidioksiidiga kokkupuutunud patsientide sõeluuringu protokollis spetsiifiliste biomarkerite puudumine üha vajalikumaks.
Esitatud tulemuste integreerimiseks kliinilisse praktikasse ja varajase silikoosi diagnostikaprotokolli on vaja täiendavaid uuringuid tsütokiiniprofiili ja funktsionaalsete polümorfismide uurimiseks silikoosiga patsientidel. Need tulemused peaksid olema korrelatsioonis tööalase ajalooga (ekspositsiooniaeg, retentsiooniaeg, kokkupuute kestus ja intensiivsus), histopatoloogilise uuringu, kujutise leidude ja kopsufunktsiooni testi tulemustega. Lisaks tuleks neid tulemusi tõlgendada kliinilises kontekstis ja need peaksid välistama ränidioksiidiga seotud hingamisteede haigused, nagu tööstuslik bronhiit ja võimalikud ägenemised. Kuigi kõik leiud näitavad tohutut potentsiaali silikoosi varajaseks diagnoosimiseks, näib CC16 tuvastamine immunokromatograafia abil kõige lootustandvam ja seda tuleks rakendada suuremate katsealuste rühmade puhul, et näidata palju laiemalt meetodi tundlikkust ja spetsiifilisust edaspidiseks kliinilises praktikas kasutuselevõtuks. ja sõelumisprotokollid.
Viited
1. Rascu, A.; Naghi, E. Boli Profesionale ale Respiraator; Silicoza; Ghid Pentru Studenti ja Medici; Universitara Carol Davila: Bukarest, Rumeenia, 2019; lk 76–99, ISBN 978-606-011-103-0.
2. Hoy, RF; Chambers, DC ränidioksiidiga seotud haigused tänapäeva maailmas. Allergia 2020, 75, 2785–2797. [CrossRef] [PubMed]
3. Rahvusvaheline Tööorganisatsioon. ILO pneumokoniooside radiograafiate rahvusvahelise klassifikatsiooni kasutamise juhised, muudetud väljaanne 2011, Genf. Saadaval võrgus: https://www.ilo.org/wcmsp5/groups/public/---ed_protect/---protrav/ ---safework/documents/publication/ wcms_168260.pdf (vaadatud 20. novembril 2022).
4. Cocarla, A. Medicina Ocupat, ională; Silicoza; Universitara Iuliu Hatieganu: Cluj-Napoca, Rumeenia, 2008; 1. köide, lk 590–630, ISBN 978-973-693-298-4.
5. Mohamed, AMO; Paleologos, EK Geokeskkonnatehnika alused; Saasteainete säilimine ja mõju maakeskkonnale; Elsevier Butterworth-Heinemann: Oxford, Suurbritannia, 2018; lk 239–281, ISBN 978-012-805-145-0.
6. Haiguste tõrje ja ennetamise keskused. Riiklik tööohutuse ja töötervishoiu instituut (NIOSH). Tööohutuse ja töötervishoiu teemad. Kristalliline ränidioksiid. Saadaval võrgus: https://www.cdc.gov/niosh/topics/silica/jobs.html (kasutatud 20. novembril 2022).
7. Rahvatervise Instituut. Kutsehaigestumine Rumeenias. Saadaval võrgus: https://insp.gov.ro/centrul-nationalde-monitorizare-a-riscurilor-din-mediul-comunitar-cnmrmc/rapoarte/ (juurdepääs 22. novembril 2022).
8. Laney, AS; Weissman, DN Söekaevanduse tolmust põhjustatud hingamisteede haigused. J. Occup. Keskkond. Med. 2014, 56 (lisa S10), S18–S22. [CrossRef] [PubMed] 9. Smărăndescu, RA; Călut,u, IM; Ras, cu, A.; Buss,natu, S, .S. Radioloogilise läbipaistmatuse diagnostilised väljakutsed silikoosi korral – juhtumiaruanded. hõivata. Med. 2022, 72, 424–427. [CrossRef] [PubMed]
10. Chen, S.; Liu, M.; Xie, F. Silikoosi suremuse ja puude järgi kohandatud eluaastate ülemaailmne ja riiklik koormus ja trendid aastatel 1990–2019: 2019. aasta ülemaailmse haiguskoormuse uuringu tulemused. BMC Pulm. Med. 2022, 22, 240. [CrossRef]
11. Shi, P.; Xing, X.; Xi, S.; Jing, H.; Yuan, J.; Fu, Z.; Zhao, H. Erinevate etioloogiate põhjustatud pneumokonioosi globaalse, piirkondliku ja riikliku esinemissageduse suundumused: 2017. aasta ülemaailmse haiguskoormuse uuringu analüüs. Occup. Keskkond. Med. 2020, 77, 407–414. [CrossRef]
12. Klaas, alalisvoolu; Dimitriadis, C.; Hansen, J.; Tere, RF; Hore-Lacy, F.; Sim, MR ränidioksiidi kokkupuute hinnangud tehiskivist lauaplaadi valmistamisel ja kahjulikud hingamisteede tagajärjed. Ann. Töö. Expo. Tervis 2022, 66, 5–13. [CrossRef]
13. Jiang, PR; Cao, Z.; Qiu, ZL; Pan, JW; Zhang, N.; Wu, YF TNF- ja MMP tase plasmas-9 silikoosiga patsientidel. Eur. Rev. Med. Pharmacol. Sci. 2015, 19, 1716–1720.
14. Blanco-Pérez, JJ; Blanco-Dorado, S.; Rodríguez-García, J.; Gonzalez-Bello, ME; Salgado-Barreira, Á.; Caldera-Díaz, AC; Pallarés-Sanmartín, A.; Fernandez-Villar, A.; González-Barcala, FJ Põletikuliste vahendajate seerumitasemed kui prognostiline biomarker ränidioksiidiga kokkupuutunud töötajatel. Sci. Rep. 2021, 11, 13348. [CrossRef]
15. Braz, NF; Carneiro, AP; Avelar, NC; Miranda, AS; Lacerda, AC; Teixeira, MM; Teixeira, AL; Mendonça, VA Tsütokiinide ja lahustuvate retseptorite mõju ränidioksiidiga kokkupuutuvate töötajate elukvaliteedile ja funktsionaalsele võimekusele. hõivata. Keskkond. Med. 2016, 58, 272–276. [CrossRef]
16. Yucesoy, B.; Vallyathan, V.; Landsittel, DP; Simeonova, P.; Läige, MI Tsütokiini polümorfismid silikoosi ja teiste pneumokoniooside korral. Mol. Cell Biochem. 2002, 234, 219–224. [CrossRef]
17. Zhang, M.; Peng, LL; Ji, XL; Yang, HB; Zha, RS; Gui, GP Kasvajanekroosifaktori geeni polümorfismid on seotud silikoosiga: süsteemne ülevaade ja metaanalüüs. Biosci. Vabariik 2019, 39, BSR20181896. [CrossRef] [PubMed]
18. Corbett, EL; Mozzato-Chamay, N.; Butterworth, AE; De Cock, KM; Williams, BG; kirikuaed, GJ; Conway, DJ Kasvaja nekroosifaktori alfa-geeni promootori polümorfismid võivad mustanahaliste Lõuna-Aafrika kaevurite puhul soodustada rasket silikoosi. Olen. J. Respir. Crit. Care Med. 2002, 165, 690–693. [CrossRef] [PubMed]
19. Kurniawidjaja, LM Indoneesia tsemenditehase töötajate TNF-alfa lookuse-308, TNF-alfa ja IL-10 tsütokiini geneetilisest variatsioonist tingitud silikoos ja selle edenemine. Pak. J. Biol. Sci. 2014, 17, 419–423. [CrossRef] [PubMed]
20. Anlar, HG; Bacanli, M.; ˙Irita¸s, S.; Bal, C.; Kurt, T.; Tutkun, E.; Hinc Yilmaz, O.; Basaran, N. Tööalase ränidioksiidiga kokkupuute mõju oksüdatiivsele stressile ja immuunsüsteemi parameetritele Türgi keraamikatöötajatel. J. Toxicol. Keskkond. Tervis A 2017, 80, 688–696. [CrossRef]
21. Lee, JS; Shin, JH; Lee, JO; Lee, WJ; Hwang, JH; Kim, JH; Choi, BS IL-I, IL-6, IL-8, TNF- ja MCP-1 tase anorgaanilise tolmuga kokkupuutunud pneumokonioosipatsientidel. Toksikool. Res. 2009, 25, 217–224. [CrossRef] [PubMed]
22. Sun, J.; Laul, P.; Wang, Y.; Chen, Y. Atsetüültsüsteiini ja tetrandriini tablettidega kombineeritud kliiniline efektiivsus silikoosi ravis ning mõju seerumi IL-6 ja TNF-. Exp. Seal. Med. 2019, 18, 3383–3388. [CrossRef]
23. Salum, KCR; de Castro, MCS; Moreira, VB; Nani, ASF; Kohlrausch, FB Interleukiini 1 ja 1 geenivariatsioonid on seotud ränidioksiidiga kokkupuutunud isikute tuberkuloosiga. Olen. J. Ind. Med. 2020, 63, 74–84. [CrossRef]
24. Zhou, Y.; Kang, Y.; Zhang, Z.; Liu, J. IL-1RA polümorfism ja vastuvõtlikkus ülemine pneumokonioos: metaanalüüs. Int. J. Clin. Exp. Med. 2014, 7, 2204–2208.
25. Liu, J.; Laul, HY; Zhu, BL; Pan, LP; Qian, XL Ränidioksiidi tolmu mõju seerumi Clara rakuvalgu 16 tasemele Hiina töötajatel. Biomed. Keskkond. Sci. 2019, 32, 47–50. [CrossRef]
26. Zhang, S.; Jia, Q.; Song, J.; Tan, Q.; Yu, G.; Guo, X.; Zhang, H. CC16 ja IL-12 kliiniline tähtsus silikoosi eri staadiumide bronhoalveolaarses loputusvedelikus. Ann. Palliat. Med. 2020, 9, 3848–3856. [CrossRef]
27. Naha, N.; Muhamed, JCJ; Pagdhune, A.; Sarkar, B.; Sarkar, K. Clubi rakuvalk 16 kui biomarker silikoosi varajaseks avastamiseks. India J. Med. Res. 2020, 151, 319–325. [CrossRef]
28. Sarkar, K.; Dhatrak, S.; Sarkar, B.; Ojha, UC; Raghav, P.; Pagdhune, A. Silikoosi ja räni-tuberkuloosi sekundaarne ennetamine ränidioksiidi tolmuga kokkupuutuvate töötajate perioodilise skriinimise teel, kasutades proksimarkerina seerumiklubi rakuproteiini 16. Health Sci. Vabariik 2021, 4, e373. [CrossRef] [PubMed]
29. Nandi, SS; Lambe, UP; Sarkar, K.; Sawant, S.; Deshpande, J. Kiirabikomplekt CC16 töökeskkonna ränidioksiidi tolmuga kokkupuutuvate töötajate skriinimiseks silikoosi/ränituberkuloosi varaseks avastamiseks. Sci. Rep. 2021, 11, 23485. [CrossRef] [PubMed]
30. Xue, C.; Wu, N.; Li, X.; Qiu, M.; Du, X.; Jah, Q. Krebs von den Lungen-6, pindaktiivse aine valgu D ja maatriksi metalloproteinaasi-2 kontsentratsioonid seerumis kui diagnostilised biomarkerid asbestoosi ja silikoosiga patsientidel: juhtumi-kontrolli uuring. BMC Pulm. Med. 2017, 17, 144. [CrossRef] [PubMed]
31. Ji, X.; Wu, B.; Jin, K.; Luo, C.; Han, R.; Chen, M.; Hou, Z.; Fan, J.; Ni, C. MUC5B promootori polümorfismid ja kivisöetöötajate pneumokonioosi risk Hiina populatsioonis. Mol. Biol. Vabariik 2014, 41, 4171–4176. [CrossRef] [PubMed]
32. Mohammadi, H.; Dehghan, SF; Golbabaei, F.; Ansari, M.; Yaseri, M.; Roshani, S.; Divani, R. Seerumi ja uriini neopteriini taseme hindamine kristallilise ränidioksiidiga kokkupuute biomarkerina. Ann. Med. Health Sci. Res. 2016, 6, 274–279. [CrossRef] [PubMed]
33. Altindag, ZZ; Baydar, T.; Isimer, A.; Sahin, G. Neopterin kui uus biomarker töökeskkonna ränidioksiidiga kokkupuute hindamiseks. Int. Arch. hõivata. Keskkond. Tervis 2003, 76, 318–322. [CrossRef]
34. Prakova, G.; Gidikova, P.; Slavov, E.; Sandeva, G.; Stanilova, S. Neopteriini potentsiaalne roll silikoosi biomarkerina. Trakia J. Sci. 2005, 3, 37–41.
35. Prakova, G.; Gidikova, P.; Slavov, E.; Sandeva, G.; Stanilova, S. Seerumi neopteriin töötajatel, kes puutuvad kokku vaba kristallilist ränidioksiidi sisaldava anorgaanilise tolmuga. Cent. Eur. J. Med. 2009, 4, 104–109. [CrossRef]
36. Pozzolini, M.; Scarfì, S.; Gallus, L.; Ferrando, S.; Cerrano, C.; Giovine, M. Ränidioksiid-indutseeritud fibroos: iidne vastus varajastelt metazoanidelt. J. Exp. Biol. 2017, 220, 4007–4015. [CrossRef]
37. Zhang, H.; Sui, JN; Gao, L.; Guo, J. Infliksimabiga nõrgestatud ränidioksiidist põhjustatud kopsufibroosi subkutaanne manustamine. Int. J. Occup. Med. Keskkond. Tervis 2018, 31, 503–515. [CrossRef] [PubMed]
38. Zhou, T.; Rong, Y.; Liu, Y.; Zhou, Y.; Guo, J.; Cheng, W.; Wang, H.; Chen, W. Seos sissehingatava ränidioksiidi tolmu põletikueelsete reaktsioonide ja tolmuga kokkupuutuvate töötajate tervisele kahjulike mõjude vahel. J. Occup. Keskkond. Med. 2012, 54, 459–465. [CrossRef]
39. Schmidt, JA; Oliver, CN; Lepe-Zuniga, JL; Green, I.; Gery, I. Ränidioksiidiga stimuleeritud monotsüüdid vabastavad fibroblastide proliferatsioonifaktoreid, mis on identsed interleukiin 1-ga. Interleukiin 1 potentsiaalne roll silikoosi patogeneesis. J. Clin. Investeeri. 1984, 73, 1462–1472. [CrossRef] [PubMed]
40. Srivastava, KD; Rom, WN; Jagirdar, J.; Yie, TA; Gordon, T.; Tchou-Wong, KM Interleukiin-1beeta ja lämmastikoksiidi süntaasi otsustav roll ränidioksiidist põhjustatud põletiku ja apoptoosi korral hiirtel. Olen. J. Respir. Crit. Care Med. 2002, 165, 527–533. [CrossRef] [PubMed]
41. Rabolli, V.; Badissi, AA; Devosse, R.; Uwambayinema, F.; Yakoub, Y.; Palmai-Pallag, M.; Lebrun, A.; De Gussem, V.; Couillin, I.; Ryffel, B.; et al. Alarmiini IL-1 on ränidioksiidi mikro- ja nanoosakeste poolt indutseeritud ägeda kopsupõletiku peamine tsütokiin. Osa Fiber Toxicol. 2014, 11, 69. [CrossRef] [PubMed]
42. Zhang, H.; Wang, R.; Wang, H.; Zhang, W. Clara rakuvalgu ja pindaktiivse valgu-D ekspressiooni dünaamilised muutused ränidioksiidiga töödeldud rottide kopsukudedes ja bronhoalveolaarses loputusvedelikus. Zhonghua Lao Dong Wei Sheng Zhi Ye Bing Za Zhi 2014, 32, 168–172. [PubMed]
43. Xu, B.; Zhang, H.; Xu, J.; Zhang, T.; Hu, C.; Zhou, H.; Shao, S. Korrelatsioon kopsufibroosi ja KL-6 taseme vahel ränidioksiidiga töödeldud hiirtel. Lõug. J. Rahvatervis 2014, 30, 1536–1538. [CrossRef]
44. Yu, Q.; Fu, G.; Lin, H.; Zhao, Q.; Liu, Y.; Zhou, Y.; Shi, Y.; Zhang, L.; Wang, Z.; Zhang, Z.; et al. Ränidioksiidi osakeste mõju mukotsiliaarsele struktuurile ja MUC5B ekspressioonile C57BL / 6 hiirte hingamisteedes. Exp. Lung Res. 2020, 46, 217–225. [CrossRef]
45. Rimal, B.; Greenberg, AK; Rom, WN Silikoosi peamised patogeneetilised mehhanismid: praegune arusaam. Curr. Arvamus. Pulm. Med. 2005, 11, 169–173. [CrossRef]
46. Turner, MD; Nedjai, B.; Hurst, T.; Pennington, DJ Tsütokiinid ja kemokiinid: raku signaalimise ja põletikuliste haiguste ristteel. Biochim. Biophys. Acta 2014, 1843, 2563–2582. [CrossRef]
47. Slavov, E.; Miteva, L.; Prakova, G.; Gidikova, P.; Stanilova, S. Korrelatsioon TNF-alfa ja IL{2}}p40-sisaldavate tsütokiinide vahel silikoosi korral. Toksikool. Ind Tervis 2010, 26, 479–486. [CrossRef] [PubMed]
48. Qu, Y.; Tang, Y.; Cao, D.; Wu, F.; Liu, J.; Lu, G.; Zhang, Z.; Xia, Z. Alveolaarsete makrofaagide vastusega seotud geenide geneetilised polümorfismid ning Hiina rauakaevurite silikoosi ja kopsutuberkuloosi risk. Int. J. Hyg. Keskkond. Tervis 2007, 210, 679–689. [CrossRef] [PubMed]
49. Grimstad, Ø. Kasvaja nekroosifaktor ja vastupidavus. JAMA Dermatol. 2016, 152, 557. [CrossRef] [PubMed]
50. Kaneko, N.; Kurata, M.; Yamamoto, T.; Morikawa, S.; Masumoto, J. Interleukiini-1 roll üldises patoloogias. Põletik. Regener. 2019, 39, 12. [CrossRef] [PubMed]
51. Voronov, E.; Dotan, S.; Krelin, Y.; Laul, X.; Elkabets, M.; Carmi, Y.; Rider, P.; Cohen, I.; Romzova, M.; Kaplanov, I.; et al. IL-1 ja IL-1 unikaalsed versus üleliigsed funktsioonid kasvajate mikrokeskkonnas. Esiosa. Immunol. 2013, 4, 177. [CrossRef]
52. Zhang, JM; An, J. Tsütokiinid, põletik ja valu. Int. Anestesiool. Clin. 2007, 45, 27–37. [CrossRef]
53. Chen, Y.; Li, C.; Lu, Y.; Zhuang, H.; Gu, W.; Liu, B.; Liu, F.; Sun, J.; Yan, B.; Weng, D.; et al. IL-10-CD1dhiCD5+ regulatiivsete B-rakkude tootmine võib mängida olulist rolli immuunhomöostaasi moduleerimisel silikoosiga patsientidel. Esiosa. Immunol. 2017, 8, 110. [CrossRef]
54. Tripathi, SS; Haushila, PP; Bholanath, P. Ülevaade silikoosi tsütokiinidest ja retseptoritest. J. Appl. Pharm. Sci. 2011, 1, 1–5.
55. Opaal, SM; DePalo, VA Põletikuvastased tsütokiinid. Rind 2000, 117, 1162–1172. [CrossRef]
56. Manning, CM; Johnston, CJ; Hernady, E.; Miller, JN; pilliroog, CK; Lawrence, BP; Williams, JP; Finkelstein, JN Kopsu kiirguskahjustuse ägenemine viirusnakkuse tõttu: Clara rakkude ja Clara raku sekretoorse valgu roll. Kiirgus. Res. 2013, 179, 617–629. [CrossRef]
57. Briana, DD; Gourgiotis, D.; Boutsikou, M.; Baka, S.; Marmarinos, A.; Liosi, S.; Hassiakos, D.; Malamitsi-Puchner, A. Clara rakuvalk täisaegses raseduses: Emakasisese kasvupiirangu mõju. Pediatr. Pulmonool. 2010, 45, 1186–1191. [CrossRef] [PubMed]
58. Song, Y.; Xiaoguang, L.; Chen, L.; Fan, Z.; Kang, X.; Bai, L.; Wang, Y.; Liu, J. AQP5 ja CC16 valgu ekspressioon ja olulisus kopsukahjustuses pärast hemorraagilise šoki taaselustamist rottidel. Lõug. J. Emerg. Med. 2017, 26, 1397–1401. [CrossRef]
59. Kohno, N.; Inoue, Y.; Hamada, H.; Fujioka, S.; Fujino, S.; Yokoyama, A.; Hiwada, K.; Ueda, N.; Akiyama, M. Serodiagnostiliste väärtuste erinevus KL-6--ga seotud mutsiinide vahel, mis on klassifitseeritud 9. klastris. Int. J. Cancer 1994, 8 (Suppl. S8), 81–83. [CrossRef]
60. Kobayashi, J.; Kitamura, S. KL-6: interstitsiaalse kopsupõletiku seerumimarker. Rind 1995, 108, 311–315. [CrossRef] [PubMed]
61. Ohnishi, H.; Yokoyama, A.; Kondo, K.; Hamada, H.; Abe, M.; Nishimura, K.; Hiwada, K.; Kohno, N. KL-6, pindaktiivse valgu-A, pindaktiivse valgu-D ja monotsüütide kemoatraktandi valgu-1 kui interstitsiaalsete kopsuhaiguste seerumimarkerite võrdlev uuring. Olen. J. Respir. Crit. Care Med. 2002, 165, 378–381. [CrossRef] [PubMed]
62. Kohno, N.; Awaya, Y.; Oyama, T.; Yamakido, M.; Akiyama, M.; Inoue, Y.; Yokoyama, A.; Hamada, H.; Fujioka, S.; Hiwada, K. KL-6, mutsiinilaadne glükoproteiin interstitsiaalse kopsuhaigusega patsientide bronhoalveolaarses loputusvedelikus. Olen. Respir. Dis. 1993, 148, 637–642. [CrossRef]
63. Ohshimo, S.; Yokoyama, A.; Hattori, N.; Ishikawa, N.; Hirasawa, Y.; Kohno, N. KL-6, inimese MUC1 mutsiin, soodustab kopsufibroblastide proliferatsiooni ja ellujäämist. Biochem. Biophys. Res. Commun. 2005, 338, 1845–1852. [CrossRef]
64. Wakamatsu, K.; Nagata, N.; Kumazoe, H.; Oda, K.; Ishimoto, H.; Yoshimi, M.; Takata, S.; Hamada, M.; Koreeda, Y.; Takakura, K.; et al. Seerumi KL-6 järjestikuste mõõtmiste prognostiline väärtus idiopaatilise kopsufibroosiga patsientidel. Hingake. Uurige. 2017, 55, 16–23. [CrossRef]
65. Riiklik Biotehnoloogia Teabekeskus. MUC5B Mucin 5B, oligomeerne lima/geeli moodustav [Homo Sapiens (inimene)] – geen. Saadaval Internetis: https://www.ncbi.nlm.nih.gov/gene/727897 (kasutatud 20. novembril 2022).
